В этой статье спецпроекта о вакцинации мы поговорим о самых «тихих» вирусах, против которых делают прививки. Они могут годами существовать в организме, не вызывая симптомов; чаще всего на этом инфекция и заканчивается. Но иногда коварный захватчик изменяет зараженные клетки настолько, что они становятся злокачественными. В отличие от возбудителей кори или ветрянки, подобных агрессивным налетчикам, сразу начинающим «жечь деревню», вирусы папилломы человека (ВПЧ) часто действуют как незаметные диверсанты. Самые коварные из них убивают хозяина — но лишь спустя много лет, и оттого угроза долгое время остается неочевидной.
Вакцинация
Изобретение вакцин кардинально изменило жизнь человечества. Многие болезни, уносившие тысячи, а то и миллионы жизней ежегодно, теперь практически не встречаются. В этом спецпроекте мы не только рассказываем об истории возникновения вакцин, общих принципах их разработки и роли вакцинопрофилактики в современном здравоохранении (этому посвящены первые три статьи), но и подробно говорим о каждой вакцине, включенной в Национальный календарь прививок, а также вакцинах против гриппа и вируса папилломы человека. Вы узнаете о том, что собой представляет каждый из возбудителей болезней, какие существуют варианты вакцин и чем они различаются между собой, затронем тему поствакцинальных осложнений и эффективности вакцин.
Пандемия COVID-19, разгоревшаяся весной 2020 года, в очередной раз напомнила человечеству, что ему практически нечего противопоставить вездесущим вирусам . Эффективных противовирусных препаратов в арсенале современной медицины — раз два и обчелся . На данный момент самым действенным инструментом в борьбе с опасными вирусными инфекциями является вакцинация. И тут ученым есть, чем похвастать: например, вакцины против нового коронавируса создали и зарегистрировали в рекордно короткие сроки .
На «Биомолекуле» можно найти не одну статью о болезни COVID-19 и вирусе SARS-CoV-2, который ее вызывает. Среди таких публикаций: «Хроника распространения SARS-CoV-2» [1], «Как вылечить COVID-19? (Спойлер: пока точно не знаем, но догадываемся)» [2], «COVID-19: отвечаем на вопросы» [3], «Животные как объект для проведения испытаний вакцин против COVID-19: необходимость или излишество» [4] и др.
О современных медикаментах против вирусных инфекций читайте в статьях «Иллюзия уверенности» [5], «Пилюля от гриппа: современные противовирусные средства» [6] и «Гепатит С: решенная проблема?» [7]. Ну а достаточно полную сводку по коронавирусным вакцинам дадут публикация «“Спутник V”, “ЭпиВакКорону”, “Модерну” делать будем? Ликбез по вакцинам против коронавируса» [8] и инфографика «Гонки вакцин 2020» [9].
Но не все вирусы получили всемирную известность благодаря тому, что вызывают яркие эпидемии с множеством случаев тяжелого течения и смертей за относительно короткое время. В то время как SARS-CoV-2 или грипп действуют в открытую, другие вирусные агенты успешно скрываются.
О прививках против гриппа, которые положено делать каждую осень, мы рассказывали в статье «Неуловимый грипп» [10]. А об исторических бесчинствах гриппа читайте тут: «Объяснена различная вирулентность вирусов гриппа — возбудителей “испанки”» [11].
Иногда нужно приложить немало усилий, чтобы распознать врага и доказать, что именно он вызывает болезнь. Именно так произошло с вирусами папилломы человека (ВПЧ). Некоторые из них способны приводить к онкологическим заболеваниям, и ученым потребовалось немало времени, чтобы разобраться в причинно-следственных связях (кстати, ВПЧ — не единственные вирусы, вызывающие рак, но об этом позже). Когда все точки над i были расставлены, вакцины против ВПЧ появились довольно быстро; сейчас многие страны уже включили их в свои прививочные календари. В недалеком будущем это, надеемся, случится и в России.
История изучения вирусов папилломы человека
О том, что у людей могут возникать бородавки, было известно очень давно. Первые письменные источники, в которых были описаны эти новообразования, датируются еще временами Гиппократа. Древнеримский ученый и врач Цельс, живший в начале нашей эры, создал первую классификацию, в которой поделил все кожные бородавки на три группы: акрохордоны (встречаются только у детей и исчезают самостоятельно), тимионы (бугристые, с обильным кровоснабжением) и мирмеции (в настоящее время известны как подошвенные бородавки) [12], [13].
Со времен этих первых описаний в изучении папилломавирусной инфекции не происходило ничего интересного почти до XX столетия. Средневековье породило много теорий, не имеющих отношения к действительности: считалось, что бородавки возникают от прикосновения к жабам, цыплятам, коровам и другими животным; от мытья рук в воде, в которой были сварены яйца; и даже от мастурбации [13].
Тем не менее наука не стояла на месте. В 1842 году итальянский врач Ригони-Штерн решил проанализировать заболеваемость раком шейки матки (РШМ) среди жительниц Италии. Он обнаружил, что у девственниц и монахинь это онкологическое заболевание встречалось намного реже, чем среди замужних женщин и вдов. Таким образом, Ригони-Штерну впервые удалось связать заболеваемость раком шейки матки с половыми контактами. Впоследствии ученые неоднократно успешно заражали подопытных и даже себя бородавками, втирая в кожу ткани патологических образований, полученные от больных людей [12], [14]. Так было доказано, что бородавки вызывает некий инфекционный агент.
В 1907 году стало понятно, что кожные и половые бородавки — это вирусное заболевание. Итальянский доктор Джузеппе Чуффо получил экстракт из остроконечных кондилом и пропустил его через фильтр, который задерживал бактерии и грибки. После того, как полученный фильтрат втирали в кожу, на ней возникали бородавки. А значит, их появление было связано не с бактериями или грибами, а с самыми мелкими патогенами — вирусами. Поначалу считалось, что все кожные и половые бородавки вызывает один и тот же вирус. Но впоследствии оказалось, что это не так. Ученые открывают новые типы ВПЧ до сих пор.
В 1949 году удалось наконец рассмотреть кристаллические вирусоподобные частицы в ткани папилломы кожи — ученые впервые увидели ВПЧ собственными глазами [12], [14], [15]. Получить подробное изображение вирусов папилломы человека с помощью электронной микроскопии [14] удалось гораздо позднее, в 1960-е годы, а в 1982 году были секвенированы геномы вирусов папилломы крупного рогатого скота 1 типа и папилломы человека типа 1a [16–18].
Роль вирусов в развитии онкологических заболеваний изучали многие специалисты, в том числе и российские. В 30-е годы прошлого столетия советский иммунолог и вирусолог Лев Александрович Зильбер , опираясь на серию экспериментов, в которых он пропускал образцы опухолевых тканей через фильтр и прививал животным, предположил, что вирусы могут запускать процесс превращения нормальных клеток в раковые [19].
С именем Зильбера связывают также открытие клещевого энцефалита: «Клещевой энцефалит: крошечный укус — серьезные последствия» [20].
Огромное значение в ранней диагностике онкологических заболеваний, связанных с папилломавирусной инфекцией, сыграли работы греческого врача Георгиоса Николау Папаниколау. В 1920 году он начал изучать патологические изменения в клетках органов женской репродуктивной системы. В 1928 году Папаниколау переехал в США и опубликовал работу, в которой утверждал, что можно выявлять злокачественные клетки в шейке матки с помощью цитологических мазков. В научном сообществе к новой методике поначалу отнеслись скептически: в то время считалось, что диагностировать рак шейки матки можно только путем биопсии после операции. Но спустя некоторое время многие врачи убедились, что цитологический мазок — весьма эффективный метод обнаружения атипичных клеток. Эта простая и недорогая процедура быстро нашла широкое применение, стала золотым стандартом в ранней диагностике РШМ и сегодня известна как мазок Папаниколау, или ПАП-тест, который применяется в виде стандартного скрининга [21].
В 1976 году произошло событие, которое помогло окончательно связать вирусы папилломы человека с онкологическими заболеваниями и стало первым шагом к созданию вакцин против ВПЧ. Немецкий ученый Харальд цур Хаузен опубликовал гипотезу о том, что вирусы папилломы человека способствуют развитию рака шейки матки. В 1983 году он идентифицировал онкогенные ВПЧ 16 и 18 типов (рис. 2). В 2008 году ученый получил за свои работы Нобелевскую премию по физиологии и медицине [14] .
О жизни и работе Харальда цур Хаузена можно почитать в нашей статье «Увидевший вирусы в раке. Харальд цур Хаузен» [22]. Интересно, что Нобелевскую премию он получил только спустя 25 лет после своего открытия. О том, как это было, читайте в статье «Нобелевскую премию 2008 года по физиологии и медицине вручили за вирусологические исследования» [23].
Со времен открытий цур Хаузена прошло много лет, но вирусы папилломы человека продолжают находиться под пристальным вниманием ученых. И это не удивительно, ведь ВПЧ — один из немногих видов вирусов, способных вызывать онкологические заболевания, а рак шейки матки по-прежнему остается глобальной проблемой здравоохранения. Чтобы понимать, как бороться с таким опасным врагом, его нужно хорошо знать в лицо.
Рисунок 2. История борьбы с ВПЧ. В Древней Греции «отец медицины» Гиппократ начал изучение ВПЧ-инфекции, а первая классификация бородавок, вызванных ВПЧ, обязана своим появлением древнеримскому ученому Авлу Корнелию Цельсу. Тем не менее вплоть до 19 века в обществе бытовало мнение, что бородавки — признак греха или плод черной магии. Только в 1842 году, когда Ригони-Штерн в Италии обнаружил, что раку шейки матки замужние женщины и вдовы подвержены больше, чем девственницы и монахини, изучение ВПЧ получило новый толчок. В 1907 году другой итальянец, Джузеппе Чуффо, доказал вирусное происхождение кондилом, а в 1949 году в ткани папилломы кожи впервые были обнаружены кристаллические вирусоподобные частицы. Затем, в 1928 году, всемирно известный врач Георгиос Николау Папаниколау предложил метод ранней диагностики РШМ с помощью взятия цитологического мазка из цервикального канала (ПАП-тест). В 1930-е годы свою лепту в исследование ВПЧ как причины развития рака внес отечественный ученый Лев Александрович Зильбер, а в 1976 году Харальд цур Хаузен окончательно связал РМШ с вирусами папилломы человека. Позднее, в 1983 году, именно он описал онкогенные ВПЧ 16 и 18 типов. В 1990-е годы в Университете Квинсленда Яном Гектором Фрейзером и Цзянь Чжоу была разработана первая вакцина против ВПЧ. В 2006 году в США получила одобрение вакцина «Гардасил», в 2007 году вакцина «Церварикс» появилась в Австралии. Самая молодая вакцина против ВПЧ — «Гардасил-9», была зарегистрирована в 2014 году и защищает от девяти генотипов ВПЧ высокого онкогенного риска.
Кто вы, мистер ВПЧ?
Вирусы папилломы — большая группа, которая включает более 200 разных типов, из них более 150 заражают человека (это и есть ВПЧ). Животные познакомились с этими вирусами, видимо, около 350 миллионов лет назад, когда появились первые рептилии. Сейчас эти возбудители встречаются у рептилий, птиц и млекопитающих, включая человека. У земноводных и рыб папилломавирусных инфекций не бывает. Вирусы папилломы — одни из тех вирусов, которые медленно эволюционируют вместе со своими хозяевами и вызывают хронические, зачастую бессимптомные инфекции.
По меркам вирусов ВПЧ относятся к карликам. Диаметр их частиц составляет 30 нм, что примерно в четыре раза меньше, чем у ВИЧ и вируса гриппа . Кстати, в отличие них, ВПЧ «голые», у них нет мембраны, заимствованной у клеток-хозяев. Отсюда и разница в размерах.
О вирусах гриппа и вакцинах против них мы уже писали в статье «Неуловимый грипп» [10].
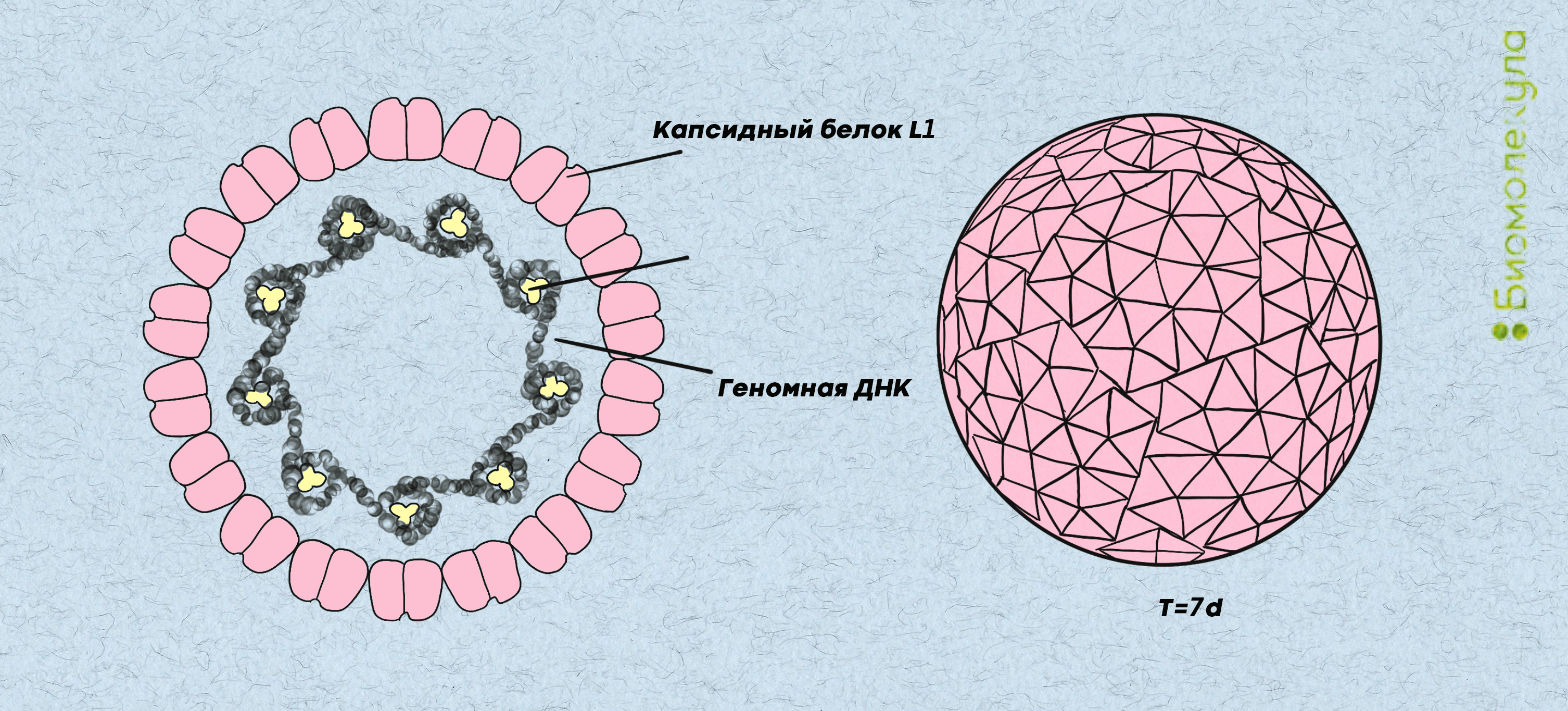
Вирусная частица ВПЧ имеет форму икосаэдра, но внешне больше напоминает сферу (рис. 3). Внутри находится ДНК, которая кодирует два типа белков:
- Ранние белки (early proteins, E-proteins) отвечают за размножение вируса и регулируют экспрессию (активность) его генов. Они способны привести к злокачественному перерождению клеток, особенно это касается белков E6 и E7. Например, ранний белок E6 связывается с белком человека p53 — «стражем генома», убивающим клетки с поврежденной ДНК, и способствует его разрушению.
- Поздние белки (late proteins, L-proteins) — это строительный материал для оболочки (капсида) вирусной частицы. Среди них нужно особо отметить белок L1 — именно он используется в современных вакцинах в качестве антигена, вызывающего иммунную реакцию.
Рисунок 3. Строение вирусов папилломы человека. Внутри находится генетический материал. Розовым цветом обозначена белковая оболочка, на которую реагирует иммунная система, когда происходит заражение.
Заражение вирусом происходит половым путем, а также во время тесного контакта «кожа к коже». Причем человек заразен, даже если у него нет симптомов. Папилломавирусную инфекцию нельзя «подцепить» в бассейне и общественном туалете, а также просто при прикосновении к другому человеку, например, во время рукопожатия.
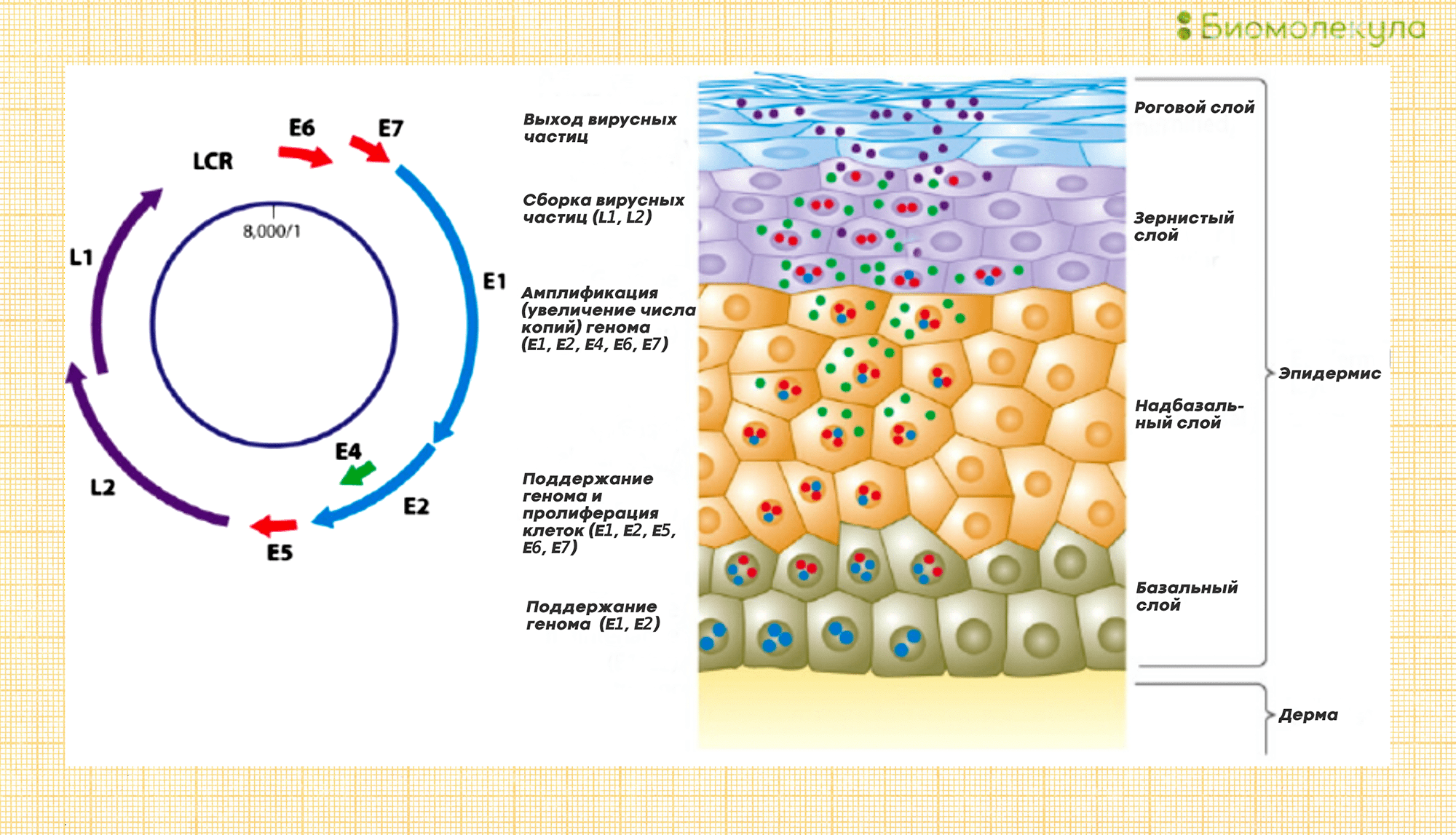
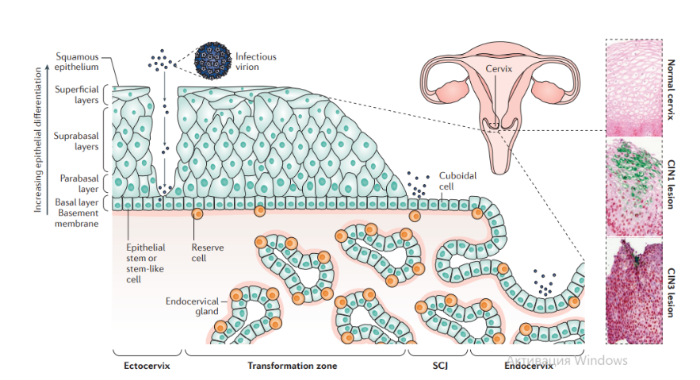
После попадания в организм ВПЧ поражает кератиноциты — клетки, из которых состоят кожа и слизистые оболочки. Молодые зараженные клетки, которые находятся в самых нижних слоях (обычно вирус проникает в кожу через повреждения — ссадины, царапины и пр.), постепенно созревают, продвигаются в верхние слои, и тут новые вирусные частицы выходят наружу (рис. 4). За счет такой связи с жизненным циклом клеток-хозяев ВПЧ сложно культивировать в лаборатории [16], [24].
Рисунок 4. Жизненный цикл ВПЧ. Слева разными цветами показана последовательность синтеза вирусных белков. Справа — схема продвижения вируса в слоях эпидермиса.
От бородавки до злокачественной опухоли
Типичное проявление инфекции, вызванной ВПЧ, — папилломы, или, обычным языком, вирусные бородавки. Собственно, за это вирусы и получили свое название. Несмотря на то, что ВПЧ широко распространены (в какой-то момент заражается примерно половина людей, ведущих половую жизнь [25]), они вызывают симптомы далеко не у всех зараженных, и далеко не всегда опасны. Чаще всего инфекция протекает латентно — нет ни симптомов, ни клинических проявлений; человек даже не подозревает, что заражен. Иногда встречается субклиническое течение, при котором ярких, заметных симптомов нет, но заболевание может быть обнаружено во время обследования. Например, вирусные кондиломы шейки матки или влагалища зачастую не доставляют женщине никаких проблем, и их обнаруживают врачи-гинекологи во время профилактических осмотров [26].
Клинические формы с ярко выраженными симптомами встречаются редко. Например, по данным американских исследователей, распространенное проявление папилломавирусной инфекции — остроконечные кондиломы («половые бородавки») — встречаются только у 1% людей, активно ведущих половую жизнь [26].
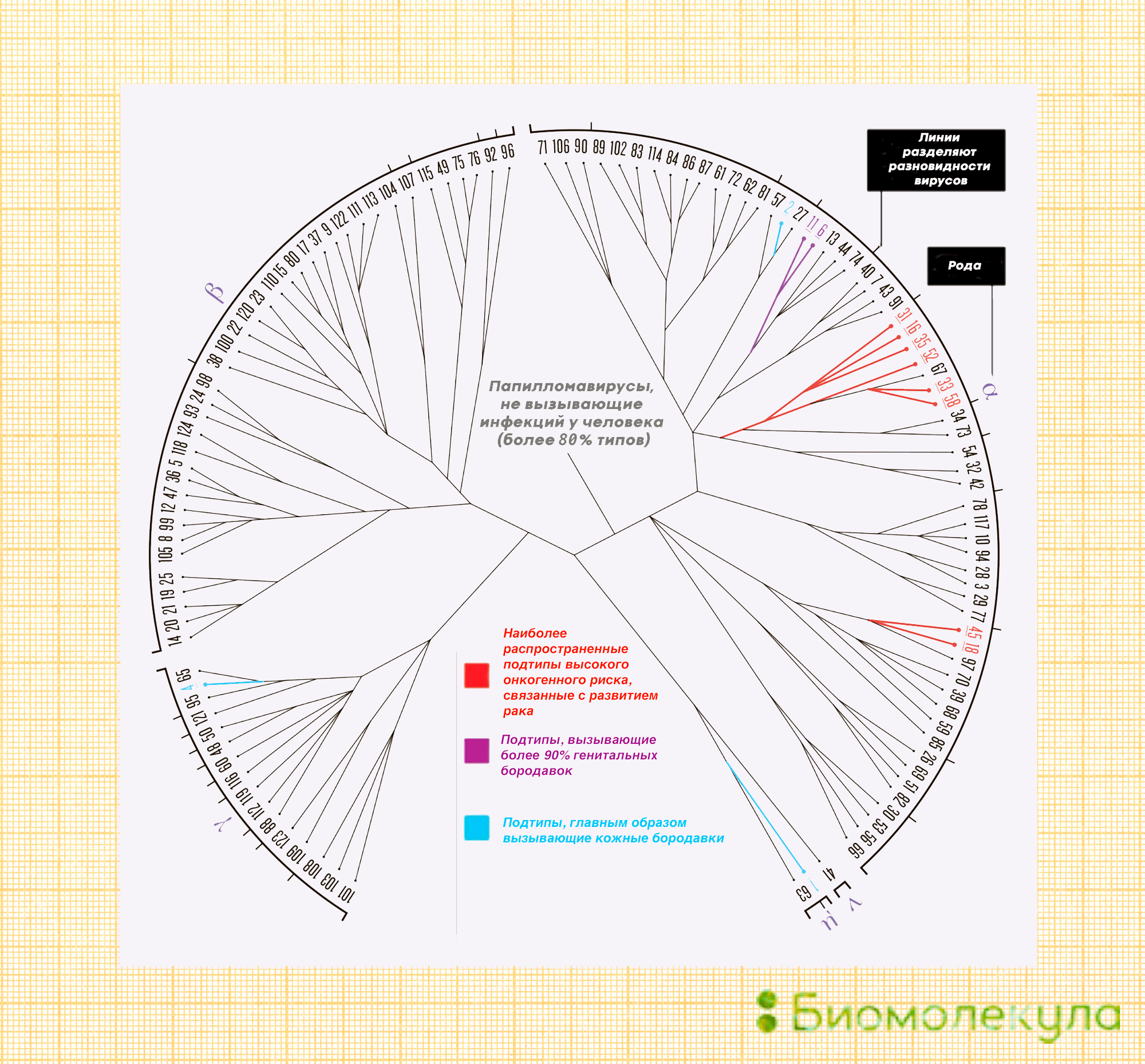
Но, конечно, основной интерес медицинского сообщества к ВПЧ вызван не их связью с бородавками, а тем, что некоторые вирусы папилломы, присутствуя в организме в форме хронической инфекции, могут приводить к злокачественному перерождению клеток. В зависимости от способности вызывать рак, все ВПЧ делятся на вирусы высокого и низкого риска. Большинство относится ко второй группе, многих из них ученые даже предлагают рассматривать как комменсалов — «квартирантов», которые не приносят ни вреда, ни пользы. Вирусов высокого риска, способных вызывать онкологические заболевания, не так много — всего 15 генотипов (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73 и 82) [27], [28]. На рисунке 5 можно видеть, какие типы ВПЧ связаны с различными доброкачественными заболеваниями и злокачественными опухолями.
Рисунок 5. Родословное дерево вирусов папилломы. Разными цветами отмечены типы, которые вызывают злокачественные опухоли, кожные и генитальные бородавки у человека. На рисунке видно, что эти заболевания связаны с разными типами вирусов.
Итак, проявления болезни во многом зависят от того, каким именно типом вируса был заражен человек (табл. 1). Однако то, станет ли болезнь хронической и приведет ли к серьезным проблемам, также зависит и от других факторов, например, иммунного статуса больного, наличия у него сопутствующих инфекций (герпеса, хламидиоза и др.), вредных привычек и так далее.
| Название заболевания | Описание | Типы ВПЧ |
|---|---|---|
| Инфекции слизистых оболочек | ||
| Остроконечные кондиломы (рис. 6а) | Чаще всего возникают в области половых органов. Кондилома выглядит как узелок, может иметь вид цветной капусты, быть плоской. Она может располагаться на ножке или широком основании, иметь розовый цвет. Размеры бывают разными: некоторые образования едва можно рассмотреть, и их выявляет только врач во время осмотра, а другие достигают очень больших размеров. У мужчин остроконечные кондиломы чаще всего возникают на половом члене, у женщин — в области наружных половых органов, на слизистой оболочке шейки матки. «Половые бородавки» постоянно трутся о белье, это вызывает боль, кровотечения, способствует раздражению кожи и воспалению. У людей с остроконечными кондиломами повышен риск развития рака в области половых органов и ануса [29], [30] | В 90% случаев — 6 и 11. Также в остроконечных кондиломах обнаруживаются ВПЧ 2, 16, 18, 30–33, 35, 39, 41–45, 51–56 и 59 типов |
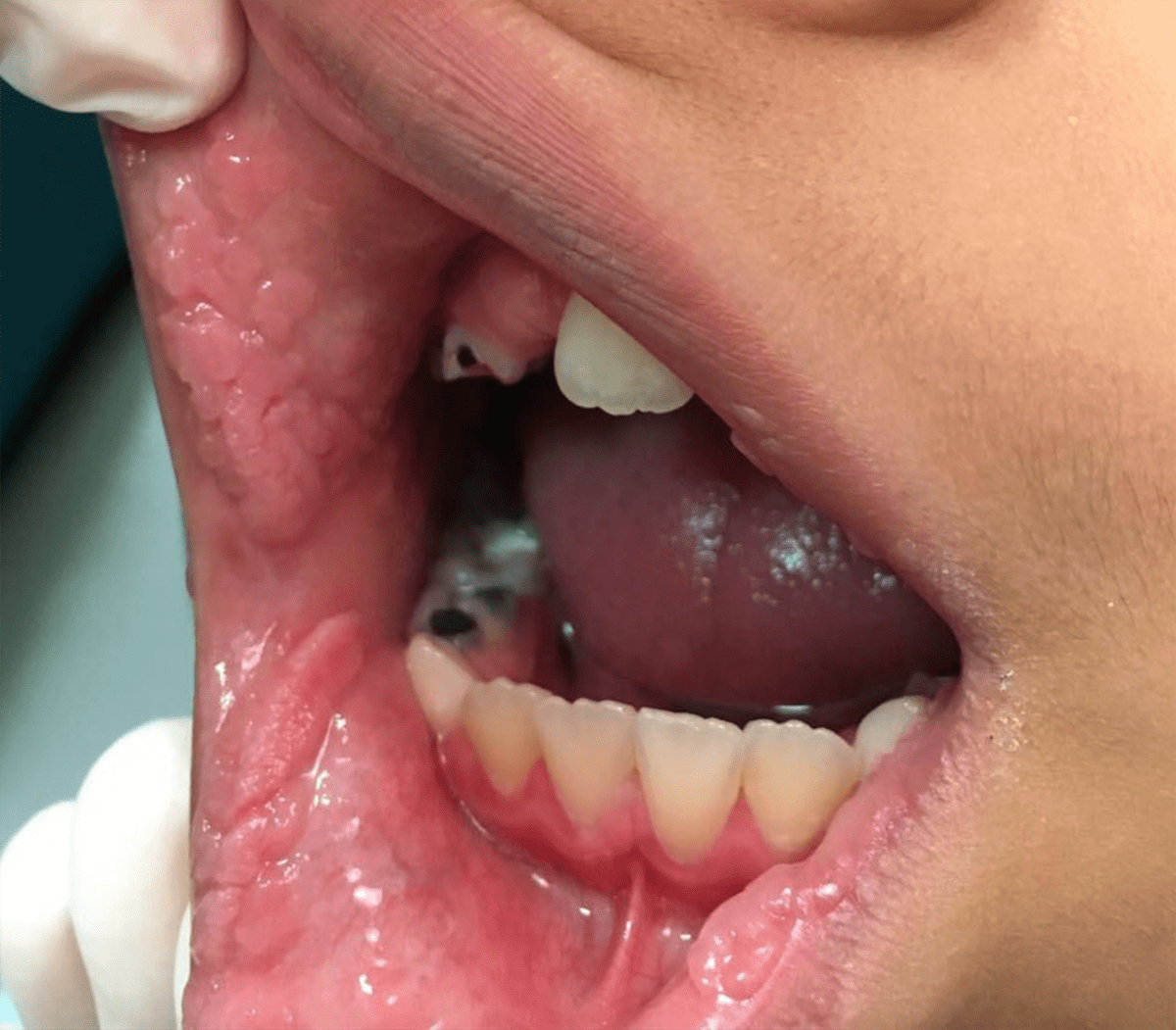
| Очаговая эпителиальная гиперплазия (болезнь Хека, рис. 6б) | Редкое доброкачественное поражение слизистой оболочки рта, чаще встречается у детей и женщин. Проявляется в виде узелков, чаще всего на слизистой оболочке нижней губы, реже — в области верхней губы, языка, дна ротовой полости, неба, ротоглотки | Чаще всего 13 и 32 типы |
| Дисплазия и рак шейки матки | Вирусы папилломы человека обнаруживаются в большинстве случаев при предраковых изменениях и злокачественных опухолях шейки матки | В 70% случаев к раку шейки матки приводят ВПЧ 16 и 18 типов [31] |
| Рак в области половых органов и ануса | ВПЧ обнаруживаются у многих пациентов с раком вульвы, влагалища, полового члена, заднего прохода | Чаще всего 18 тип. Реже 21, 31, 33 и 34 типы |
| Рак головы и шеи | ВПЧ считаются основным фактором риска развития плоскоклеточного рака головы и шеи. Чаще всего вирусы обнаруживаются при раке ротоглотки и миндалин. Пациенты со злокачественными опухолями, ассоциированными с ВПЧ, имеют более благоприятный прогноз за счет более высокой чувствительности раковых клеток к химиопрепаратам | Чаще всего 16 тип. Реже 18, 31, 33 и 35 типы |
| Респираторный папилломатоз | В группе риска дети в возрасте 3–4 лет и взрослые старше 40 лет. Папилломы возникают на слизистой оболочке гортани, что может приводить к грубому, «лающему» кашлю, ощущению кома в горле, боли в ушах, изменению голоса, охриплости. Большие папилломы приводят к нарушению дыхания | 6, 11 и 16 типы |
| Инфекции кожи | ||
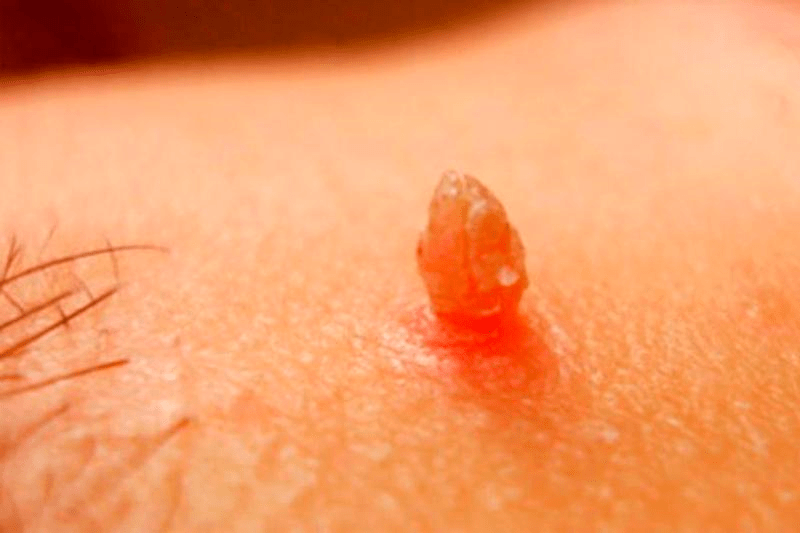
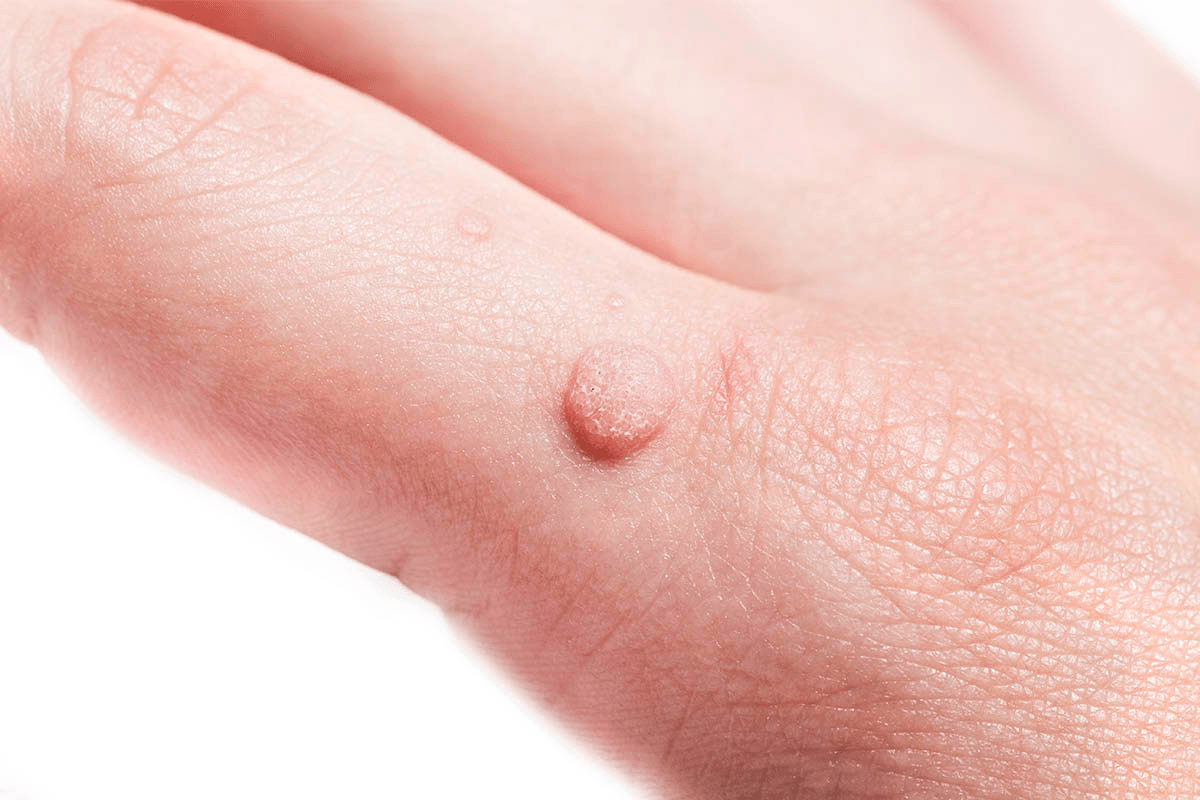
| Обыкновенные (вульгарные) бородавки (рис. 6 в) | Бывают единичными и множественными, разных размеров. При ослабленном иммунитете становятся многочисленными, и от них сложнее избавиться. Как правило, возникают на тыльной поверхности кистей рук, у детей — на коленях | Обычно 1, 2, 4, 27 и 57 типы. У людей, руки которых часто переохлаждаются и подвергаются действию влаги, в бородавках обнаруживается ВПЧ 7 типа |
| Подошвенные бородавки | Болезненные бляшки из уплотненной огрубевшей кожи желтого цвета. Если сковырнуть такую бляшку, на ее месте появляется кровоточивость или черные точки — это тромбированные капилляры. Обычно встречаются у детей | Чаще всего 1 и 4 типы. Также встречаются ВПЧ 57, 60, 63, 65 и 66 типов |
| Плоские бородавки | Слегка приподнятые участки кожи обычного цвета или пигментированные. Могут иметь гладкую или слегка шероховатую поверхность. Чаще всего возникают на лице, тыльной поверхности рук | Чаще всего 3 и 10 типы |
| Нитевидные бородавки | Образования на ножке, которые растут перпендикулярно или под некоторым углом к коже. Обычно возникают на лице и шее | Те же, что и при обыкновенных бородавках, особенно часто 2 тип |
| Пигментные бородавки | Могут быть разного цвета, от серого до черно-коричневого. Появляются на ладонях, подошвах, боковых поверхностях кистей, стоп, пальцев | Чаще всего 4, 60 и 65 типы |
| Эпидермоидные кисты | Доброкачественные образования в виде полости, стенки которой образованы клетками сальной железы или волосяного фолликула. Внутри находится белок кератин, кожное сало и продукты его разрушения | 57 и 60 типы |
| Рак кожи | Болезнь Боуэна — поверхностный плоскоклеточный рак кожи in situ («на месте»). Злокачественная опухоль, клетки которой пока еще не распространяются в окружающие ткани. В 3–5% случаев трансформируется в инвазивный рак и начинает метастазировать. Также доказана роль ВПЧ в развитии злокачественных опухолей кожи у людей с ослабленным иммунитетом (например, при ВИЧ-инфекции, приеме иммунодепрессантов) | Те же типы, что вызывают поражения слизистых оболочек. Иногда 2, 6, 11, 54, 58, 61, 62 и 73 типы |
Рисунок 6а. Проявления папилломовирусной инфекции. Остроконечные кондиломы. Они же половые, или аногенитальные, бородавки. Выглядит жутко, но это не злокачественная опухоль, и она не всегда бывает вызвана папилломавирусами высокого онкогенного риска.
Рисунок 6б. Очаговая эпителиальная гиперплазия (болезнь Хека). Так в редких случаях может протекать папилломавирусная инфекция слизистой оболочки рта.
Рисунок 6в. Обычная бородавка — типичное проявление ВПЧ-инфекции на коже
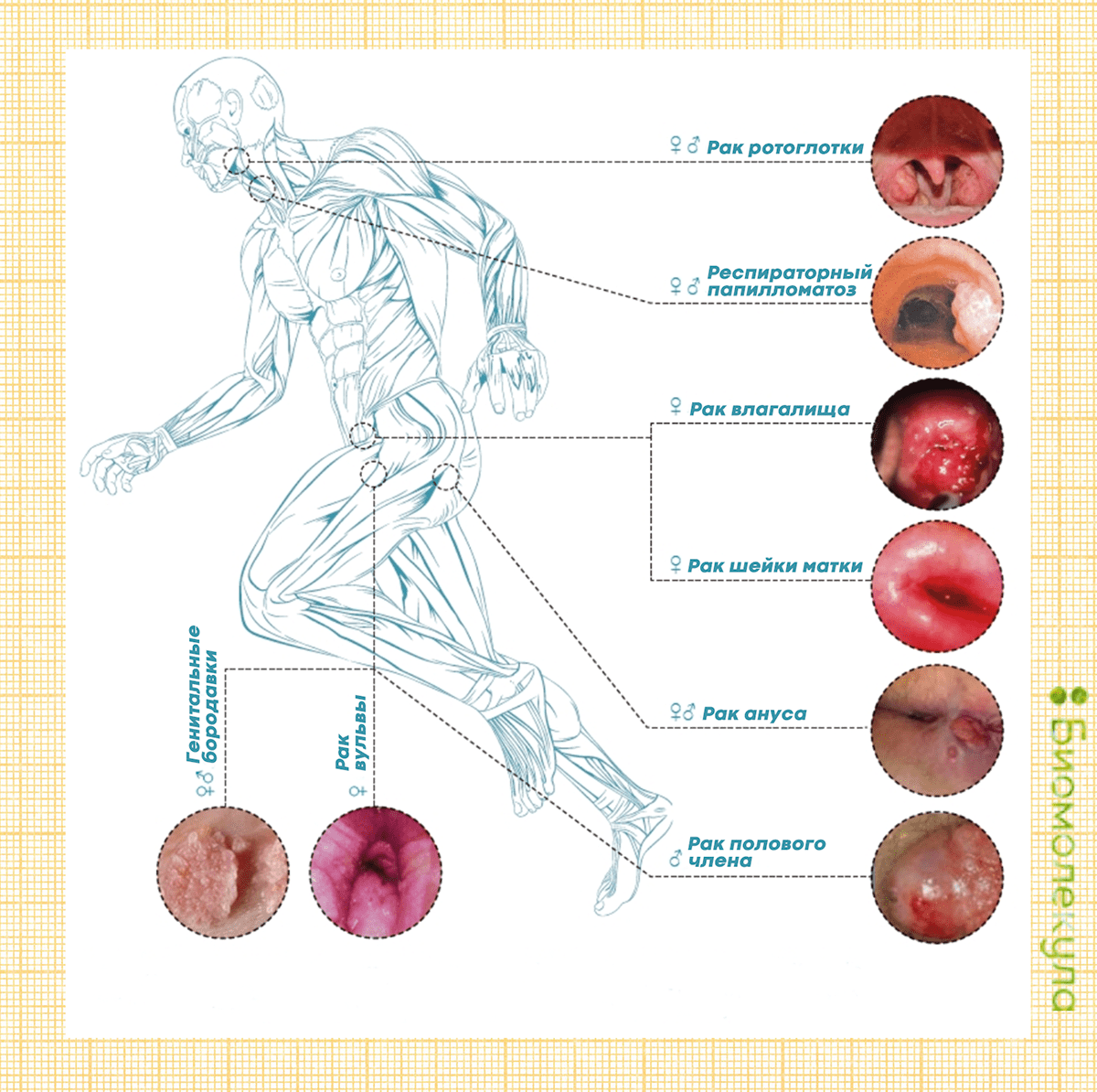
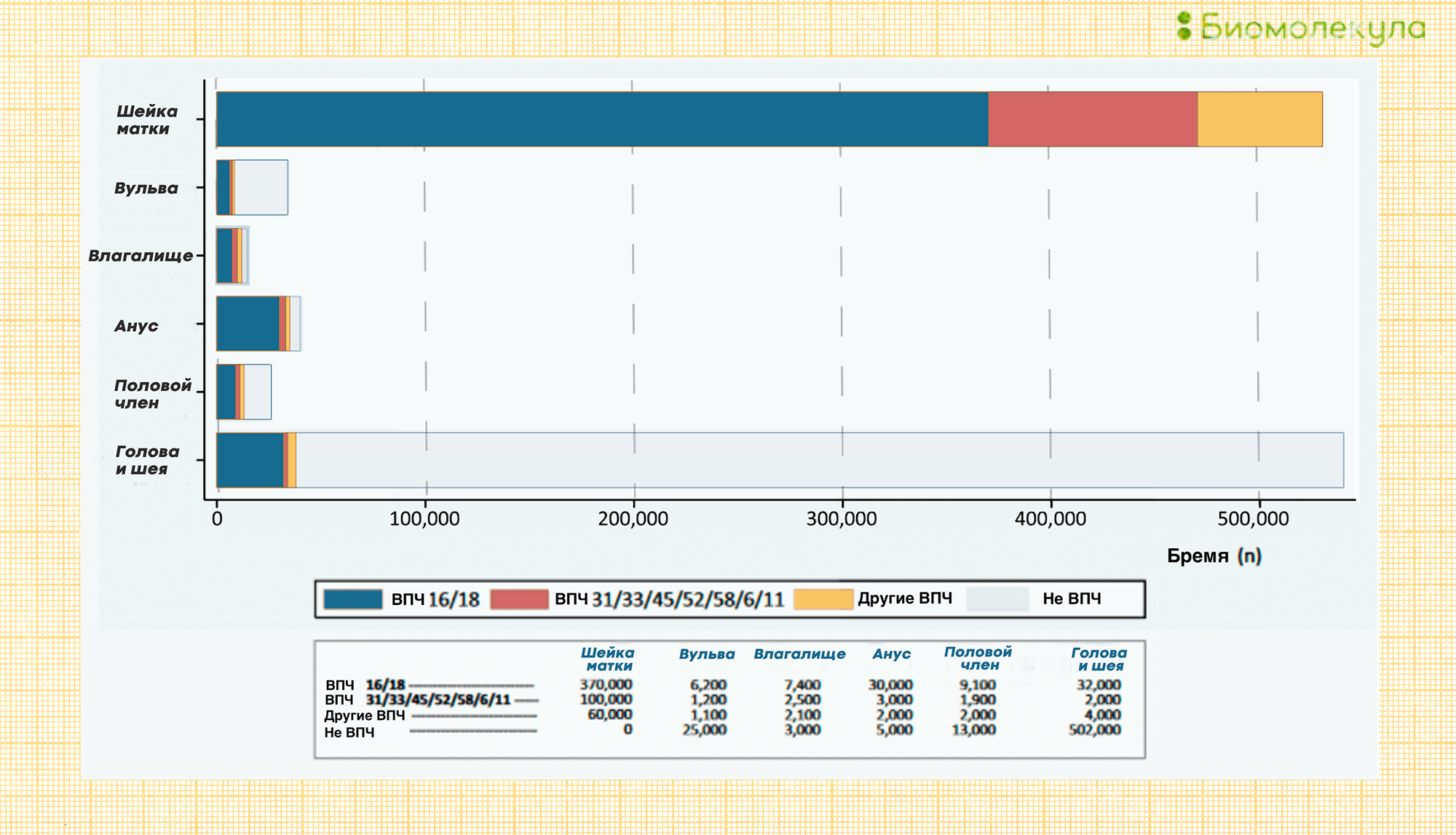
Среди всех злокачественных опухолей, связанных с ВПЧ (рис. 7), наибольшую опасность представляет рак шейки матки (рис. 8). По данным Всемирной организации здравоохранения (ВОЗ), ежегодно во всем мире диагностируется больше 500 тысяч новых случаев этого заболевания. С ним связано около 7,5% смертей от всех онкопатологий. При этом 70% всех случаев рака шейки матки и предраковых состояний связано с двумя типами ВПЧ — 16 и 18 [31]. А вместе с другими типами ВПЧ высокого онкогенного риска (31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73 и 82) они ответственны более чем за 95% всех случаев рака шейки матки. 19% приходится на типы 31, 33, 45, 52 и 58, остальные приводят к развитию онкозаболеваний реже. Если иммунная система женщины работает нормально, то рак шейки матки, если и развивается, то только спустя 15–20 лет после заражения. До этого женщина может не испытывать никаких симптомов и считать себя здоровой. При иммунодефиците, вызванном ВИЧ-инфекцией и другими причинами, этот срок сокращается до 5–10 лет.
Рисунок 7. Злокачественные опухоли, вызываемые вирусом папилломы человека у женщин и мужчин. Ежегодно папилломавирусные инфекции у женщин становятся причиной 530 000 случаев рака шейки матки, 18 000 случаев рака ануса, 8500 случаев рака вульвы, 12 000 случаев рака влагалища, 5500 случаев рака ротоглотки. У мужчин ВПЧ ежегодно вызывают 17 000 случаев рака ануса, 13 000 случаев рака полового члена, 24 000 случаев рака ротоглотки.
Рисунок 8. Распространенность разных типов рака, связанных с папилломавирусной инфекцией. На графике хорошо видно, что наиболее актуальна роль ВПЧ в развитии рака шейки матки.
Главными факторами риска развития рака ротовой полости и глотки считаются курение и частое употребление алкоголя. Но в последние годы врачи замечают тревожную статистику: эти опухоли всё чаще встречаются у молодых людей, которые не курят и не злоупотребляют спиртным. Этих пациентов объединяет другая особенность — до заболевания у них было много половых партнерш, и многие практиковали оральный секс. Это приводило к заражению ВПЧ высокого онкогенного риска со всеми вытекающими последствиями. К слову, лечить злокачественные опухоли головы и шеи, вызванные ВПЧ, легче, чем те, что связаны с курением и алкоголем. Они лучше поддаются облучению и химиопрепаратам. Но это слабое утешение. Очевидно, тут нужны эффективные меры профилактики [32].
Существуют ли эффективные методы лечения?
Эффективных противовирусных препаратов против ВПЧ не существует. Но в большинстве случаев они и не требуются: как правило, инфекция проходит сама в течение нескольких месяцев; 90% пациентов выздоравливают в течение двух лет. Если бородавки имеют большие размеры и причиняют дискомфорт, вызывают симптомы, или у пациента обнаружены предраковые изменения, прибегают к хирургическим методам. Важно понимать, что удаление новообразования, вызванного ВПЧ-инфекцией — это симптоматическое лечение. Оно не избавляет от вируса, поэтому в будущем может произойти рецидив [31], [35], [36].
Вирусные бородавки можно удалить разными способами:
- Крем «Имиквимод» — он работает как усилитель местной иммунной защиты: активирует выработку интерферона и цитокинов (воспалительных молекул).
- «Кондилин» — препарат местного применения в виде раствора. Обладает антимитотическим действием (не дает клеткам размножаться) и является клеточным ядом.
- «Вереген» — препарат местного применения, в котором действующими веществами являются катехины. Механизм его действия изучен плохо, но он помогает уничтожать остроконечные кондиломы, вызванные ВПЧ.
- Криохирургия — метод удаления новообразований с помощью очень низкой температуры. Обычно для этого применяют жидкий азот.
- Обычное иссечение — с помощью скальпеля, хирургических ножниц, сбривания новообразования, выступающего над поверхностью кожи.
- Электрохирургия — иссечение с помощью специального инструмента (электрокоагулятора), на который подается электрический ток. Он сильно нагревает и прижигает ткани.
- Лазерная хирургия.
- Удаление с помощью радиоволновой хирургии [35], [36].
После операций при дисплазии шейки матки в большинстве случаев женщина в будущем сможет завести детей. Но если у молодой женщины выявлен рак шейки матки, то с большой вероятностью после лечения беременность станет невозможной. Во-первых, нередко приходится полностью удалять матку. Во-вторых, лучевая терапия и химиотерапия поражают яичники, и, как правило, курс лечения приводит к бесплодию. Однако некоторые решения этой проблемы всё же доступны. Например, можно заранее сохранить свои яйцеклетки в банке половых клеток (они там будут находиться в «замороженном» состоянии), а потом воспользоваться услугой суррогатного материнства.
Можно ли защититься от папилломавирусной инфекции?
Рекомендации по профилактике ВПЧ-инфекции опираются на два главных фактора. Во-первых, главная опасность вирусов папилломы человека в том, что некоторые из них вызывают онкологические заболевания. Во-вторых, эти вирусы распространяются главным образом через половые контакты. Эксперты Всемирной организации здравоохранения предлагают три уровня профилактики в разных возрастных группах (табл. 3).
| Первичная профилактика — для девочек 9–14 лет (для профилактики заражения ВПЧ) | Вакцинация против ВПЧ |
| Первичная профилактика — для всех мальчиков и девочек (для профилактики заражения ВПЧ) |
|
| Вторичная профилактика для женщин 25 лет и старше (для своевременной диагностики предраковых изменений и рака) |
|
| Третичная профилактика — для всех женщин по показаниям (для повышения выживаемости при онкологических заболеваниях) | Своевременная диагностика уже возникшего рака с помощью скрининга и немедленное начало лечения. |
Эксперты из Американского общества рака рекомендуют такую схему скрининга:
- Регулярные скрининговые исследования проходить всем женщинам по достижении возраста 25 лет.
- Женщинам в возрасте 25–65 лет сдавать анализы на ВПЧ один раз в пять лет. Можно раз в пять лет выполнять тесты, которые сочетают определение ВПЧ с мазком Папаниколау, или раз в три года — только мазок Папаниколау.
- В 65 лет скрининг можно прекратить, но только если до этого женщина регулярно сдавала анализы, и у нее в течение последних лет не были обнаружены ВПЧ, атипичные клетки в мазках, и если в течение 25 лет у нее в шейке матки не было предраковых изменений.
- Если у женщины удалили матку (но не из-за рака или тяжелых предраковых изменений), то ей можно прекратить скрининг. Если у женщины было удалено тело матки, но осталась шейка, то скрининг нужно продолжить.
- Даже если женщина проходила вакцинацию против ВПЧ, ей нужно придерживаться всех вышеперечисленных рекомендаций [37].
Что касается мер профилактики заражения ВПЧ-инфекцией, то не все они одинаково эффективны. Например, презервативы обеспечивают некоторую защиту, но не на 100%. Наиболее надежная мера — вакцинация, но ее нужно проводить до того, как произошло заражение.
История создания «вакцины против рака»
Вакцины против ВПЧ были созданы благодаря разработкам двух профессоров из Квинслендского университета в Австралии: Яна Фрейзера и Цзянь Чжоу (рис. 11). Эти ученые еще в 1990-е годы начали работу по созданию вирусоподобных частиц, которые напоминали бы по своим антигенным свойствам ВПЧ и могли быть использованы для иммунизации. В 1991 году Фрейзер и Чжоу представили свои результаты научному сообществу. Затем последовали еще семь лет разработок и тестов, и вскоре были завершены испытания новой вакцины на людях. Было доказано, что она эффективно защищает против четырех типов ВПЧ: 6, 11, 16 и 18. Наконец, крупные клинические испытания показали, что прививка обеспечивает практически 100% защиту от ВПЧ 16 и 18 типов — основных виновников развития рака шейки матки. По итогам этих исследований новая вакцина в 2006 году была одобрена к применению американским Управлением по санитарному надзору за качеством продуктов и медикаментов (FDA), а также в Австралии. В 2007 году она была зарегистрирована уже в 80 странах мира. Препарат получил название «Гардасил». Изначально он предназначался для профилактики рака шейки матки у женщин. В 2009 году его одобрили для профилактики остроконечных кондилом, в 2010 году — для профилактики предраковых изменений ануса, вызванных ВПЧ, у представителей обоих полов [39], [40].
Рисунок 11. Цзянь Чжоу и Ян Фрейзер, создатели первой вакцины против вирусов папилломы человека
В 2007 году в Австралии была зарегистрирована вторая вакцина против ВПЧ — «Церварикс». В 2009 году ее одобрило и FDA, но в Америке она не получила большой популярности, потому что, в отличие от «Гардасила», защищала только от двух типов ВПЧ — 16 и 18 [39], [40].
Самой современной вакциной является «Гардасил 9», зарегистрированная в США в 2014 году. Она защищает от всех типов ВПЧ, против которых работает «классический» «Гардасил», и еще от пяти: 31, 33, 45, 52 и 58 [39], [40]. За счет такого большого охвата прививка «Гардасилом 9» способна предотвращать более 90% всех случаев рака шейки матки, анального канала, а также многие другие злокачественные опухоли, связанные с ВПЧ [40].
Интересно, что благодаря одному замечательному свойству иммунной системы прививки могут защищать не только от вирусов, против которых направлены. Речь идет о перекрестном иммунитете. Когда иммунная система «знакомится» с одним вирусом, она может распознавать и другие, родственные. Это происходит и в случае с вакцинами против ВПЧ.
Вакцины против ВПЧ сегодня
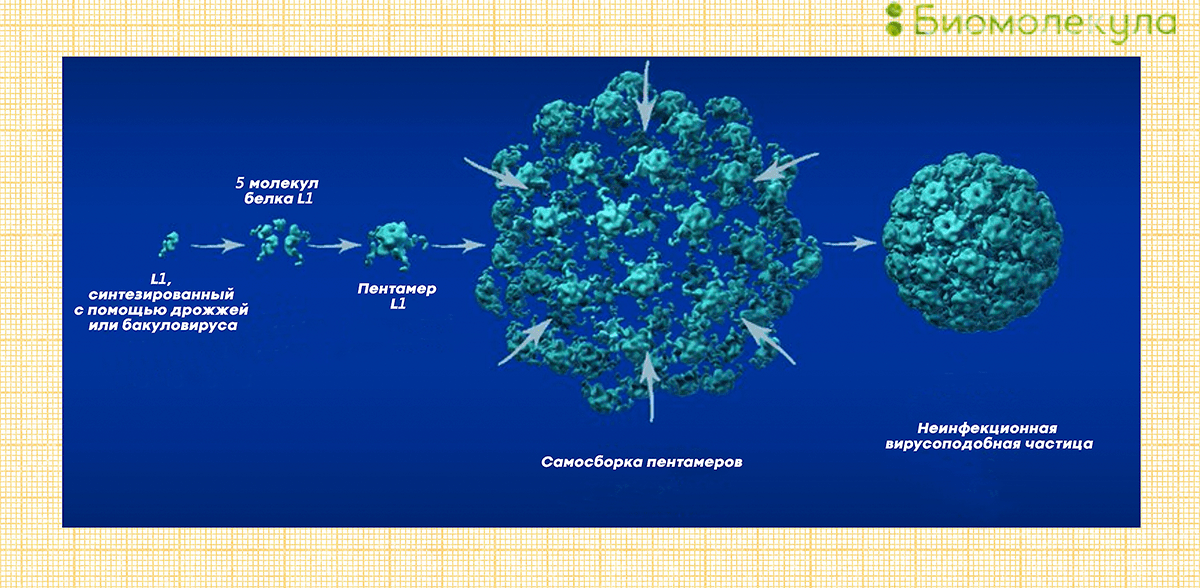
В современном мире доступны три вакцины против ВПЧ (их основные характеристики представлены в таблице 4). Все они созданы одним и тем же способом. В качестве антигена (агента, вызывающего иммунную реакцию) в них применяют искусственно синтезированные белки, подобные вирусным поверхностным белкам L1. Их получают с помощью методов генной инженерии в клетках бактерий, дрожжей, насекомых. Вместе L1-белки соединяются в структуру, напоминающую оболочку вируса : получаются своего рода «вирусы-зомби». Они выглядят для иммунной системы как вирусы, заставляют ее реагировать, но в них нет ДНК, и они не способны заражать клетки (рис. 12) [41].
О том, как происходит самосборка вирусных частиц, и для чего ее можно использовать, мы рассказывали в статье «Вирусы-платформы: яд во благо» [42].
Рисунок 12. Строение вирусоподобных частиц в вакцине «Гардасил». Вирусные белки L1, синтезированные с помощью дрожжей или бакуловируса, образуют пентамеры и собираются в сферическую оболочку. Но эта оболочка пустая — в ней нет ДНК, — а значит, она не может вызвать инфекцию. Зато в ответ на нее развивается иммунная реакция.
| «Гардасил» («Силгард») | «Церварикс» | «Гардасил-9» | |
|---|---|---|---|
| Тип вакцины | Рекомбинантная, вирусоподобные частицы из L1-белка | ||
| Производитель | Merck | GlaxoSmithKline | Merck |
| Типы ВПЧ, против которых защищает | Четырехвалентная (против четырех типов ВПЧ): 6, 11, 16, 18 | Двухвалентная (против двух типов ВПЧ): 16 и 18 | Девятивалентная (против девяти типов ВПЧ): 6, 11, 16, 18, 31, 33, 45, 52, 58 |
| Заболевания, от которых защищает |
|
|
|
| Против каких ВПЧ создает перекрестный иммунитет | 31, 45 | 31, 33 | нет необходимости, так как изначально защищает против всех основных типов ВПЧ, связанных с онкологическими заболеваниями |
В России сертифицированы только две вакцины: «Гардасил 9» в РФ пока получить нельзя [41]. Сейчас в нашей стране ведется разработка собственных препаратов. В 2020 году стало известно, что российская биофармацевтическая компания «НАНОЛЕК» и научно-производственная компания «КОМБИОТЕХ» стали партнерами и собираются производить отечественную вакцину против 6, 11, 16 и 18 типов ВПЧ [44]. В 2021 году пресс-служба российской фармацевтической компании «Р-Фарм» сообщила о подписании договора с китайской биотехнологической компанией Beijing Health Guard по разработке и коммерциализации вакцины против девяти типов ВПЧ. В рамках соглашения планируется провести III фазу клинических испытаний [45]. В марте 2022 года «НАНОЛЕК» уже объявил, что первая партия вакцины выйдет в 2024 году.
Кого и как нужно вакцинировать?
В 2016 году эксперты ВОЗ выпустили руководство, в котором отметили важную роль вакцинации против ВПЧ в профилактике рака шейки матки и других онкологических заболеваний. Они рекомендовали всем странам включить иммунизацию против вирусов папилломы в свои национальные календари профилактических прививок, причем в случае нехватки ресурсов в первую очередь вакцинировать женщин, которые не могут регулярно проходить скрининг. Рекомендации ВОЗ выглядят следующим образом:
- прививать в первую очередь нужно всех девочек в возрасте 9–14 лет до начала половой жизни;
- стандартная схема предусматривает введение двух доз вакцины с интервалом в 6 месяцев;
- максимальная продолжительность интервала между двумя дозами вакцины не установлена, но не стоит превышать 12–15 месяцев;
- если интервал между двумя дозами был меньше 5 месяцев, то нужно ввести третью дозу, причем не менее чем через шесть месяцев после первой;
- людей старше 15 лет и с ослабленным иммунитетом (в том числе с ВИЧ — вне зависимости от того, получает ли пациент лечение) нужно вакцинировать тремя дозами: вторая — спустя 1–2 месяца после первой, третья — через шесть месяцев после первой;
- вакцинацию мальчиков проводить рекомендуется, но не в приоритетном порядке, так как в первую очередь нужно защитить девочек от риска рака шейки матки — это особенно актуально для стран, в которых не хватает вакцин [43].
Похожие рекомендации представлены на сайте американских Центров по контролю и профилактике заболеваний (CDC), но там отдельно упоминаются взрослые люди:
- вакцинацию против ВПЧ рекомендуется проводить в плановом порядке детям в 11 и 12 лет (можно начинать с 9 лет);
- люди моложе 26 лет также могут пройти вакцинацию, если не делали этого в детстве — двумя или тремя дозами, в зависимости от возраста;
- непривитым людям старше 26 лет, желающим вакцинироваться, нужно проконсультироваться с врачом: в этой возрастной группе иммунизация не приносит большой пользы, потому что многие уже заражены — но для тех, кто не заражен, это эффективная мера профилактики. Для людей старше 45 лет вакцины против ВПЧ не лицензированы;
- вторую дозу нужно ввести через 6–12 месяцев после первой;
- если промежуток между первой и второй дозами составил меньше 5 месяцев, то нужно ввести третью дозу;
- три дозы вакцины нужно вводить людям 15–26 лет, а также лицам с ослабленным иммунитетом [46].
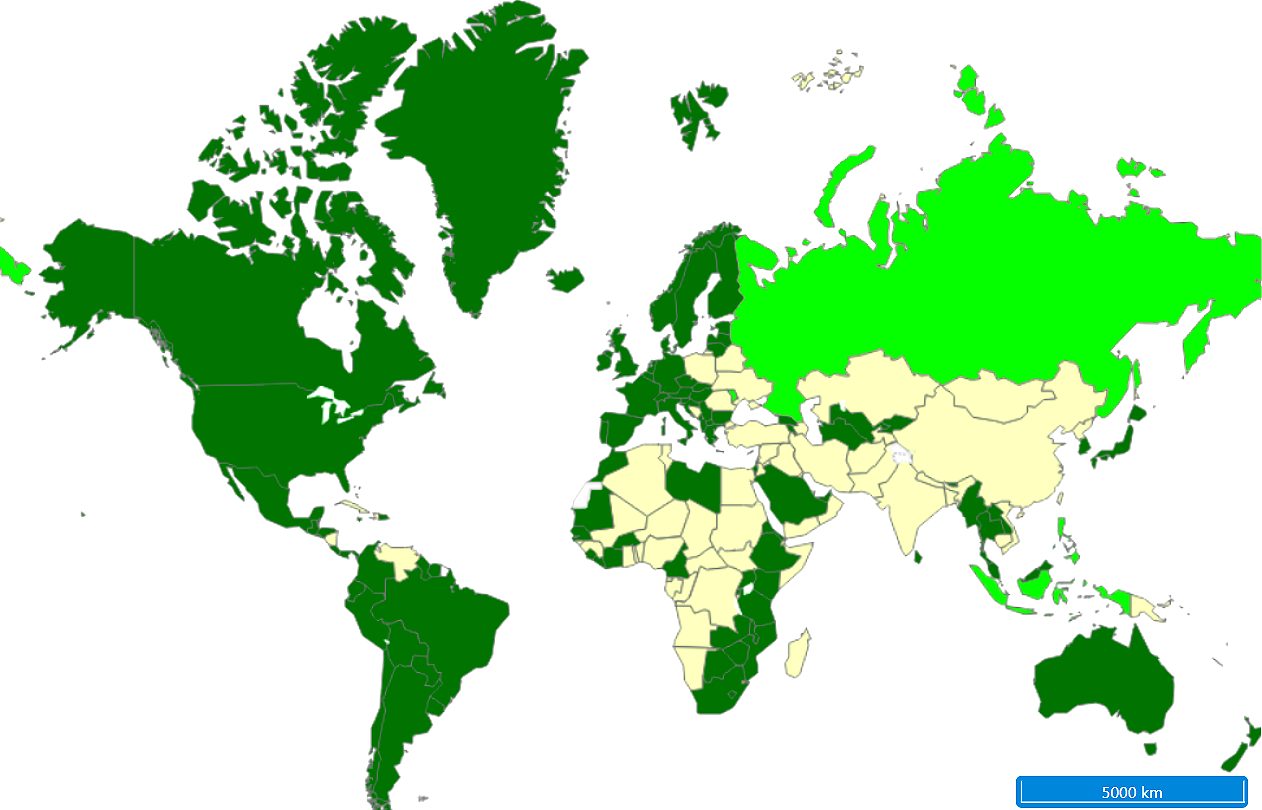
В настоящее время программы плановой вакцинации против ВПЧ введены уже во многих странах мира (рис. 13). В России этой прививки пока нет в Национальном календаре профилактических прививок, но она включена в «Идеальный прививочный календарь» Союза педиатров России, о котором мы рассказывали в статье «Вакцинация перед школой: гайд для родителей» [47]. Специалисты предлагают двухдозовую схему вакцинации для детей 9–13 лет и трехдозовую для тех, кто старше. Возможна ускоренная трехдозовая схема, когда вторую дозу вводят через один месяц после первой, а третью — через три месяца [48].
Ожидается, что вакцинация против ВПЧ войдет в российский Национальный календарь прививок в 2024 году, но в некоторых регионах, например, в Москве, ее уже сейчас можно пройти бесплатно по ОМС.
Рисунок 13. Состояние программ плановой вакцинации против ВПЧ в мире. Темным цветом отмечены страны, в которых введена плановая вакцинация. Полосатые страны — те, в которых плановая вакцинация введена частично, в отдельных регионах. Например, в России против ВПЧ прививают в рамках региональных календарей в Московской и Свердловской областях [49]. В некоторых странах в рамках национальных календарей прививают только девочек, так как именно для них в первую очередь опасны ВПЧ высокого онкогенного риска. Но есть и такие, где в программу включены мальчики.
Насколько эффективна вакцинация?
Тот факт, что все три вакцины против ВПЧ были зарегистрированы относительно недавно, вовсе не означает, что они пока еще плохо изучены. Как и любой новый лекарственный препарат, они прошли все необходимые клинические испытания, и ученые тщательно оценили их эффективность и безопасность (рис. 14).
Рисунок 14. Все три зарегистрированные ВПЧ-вакцины прошли клинические испытания, в которые были включены десятки тысяч участников. Эффективность и безопасность этих препаратов хорошо изучены.
Вакцины против ВПЧ показали высокую эффективность как в отношении защиты от самих вирусов, так и от связанных с ними онкологических заболеваний. После того, как в США началась вакцинация в 2006 году, в течение следующего десятилетия девочки-подростки стали заражаться ВПЧ на 86% реже, а женщины старше 20 лет — на 71% реже. Врачи-гинекологи стали выявлять меньше остроконечных кондилом и предраковых изменений в шейке матки. Когда вакцины стали широко применять в других странах, то там увидели похожие результаты [50].
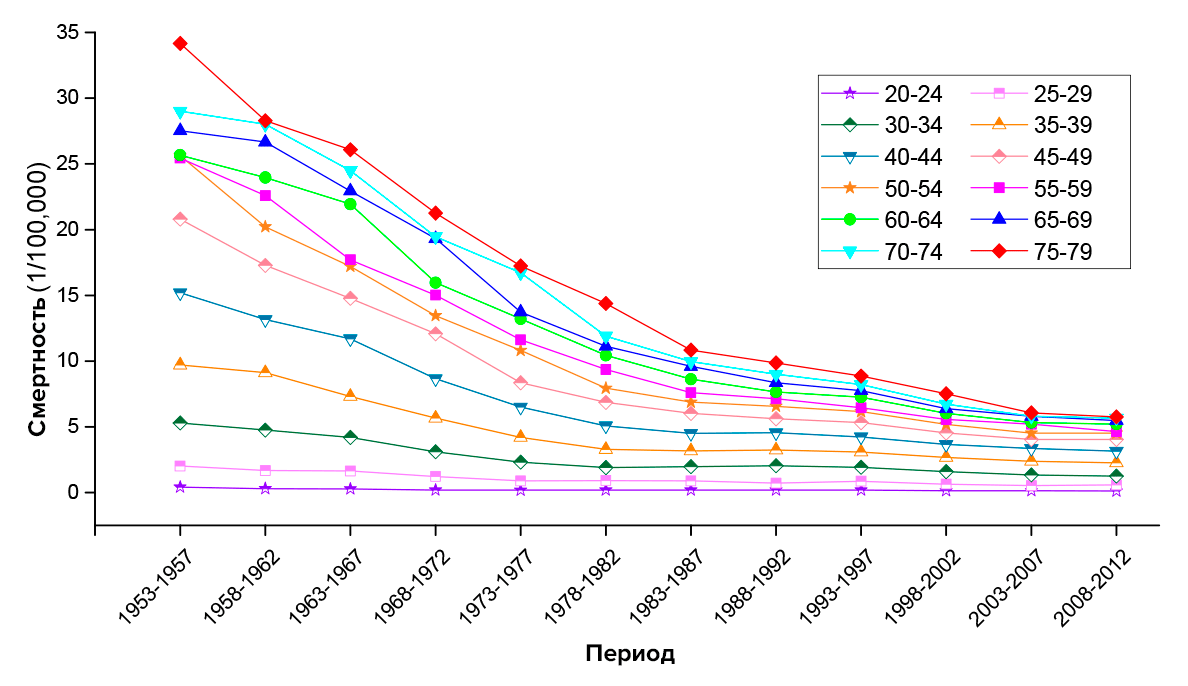
Рак шейки матки развивается спустя многие годы после заражения ВПЧ, поэтому сложно изучать, насколько хорошо от него защищают вакцины (рис. 15). Но в течение пяти лет инфекция может вызвать предраковые изменения, «рак на месте», и эти состояния можно использовать как индикаторы. Именно их отслеживали во время клинических исследований, и результаты показали, что вакцины действительно очень сильно снижают риск их развития. Например, обзор от 2006 года шести исследований, в которых участвовали 47 236 женщин, показал, что после вакцинации против ВПЧ на 93% снижается риск поражений шейки матки, влагалища, вульвы и области ануса [51], [52].
Рисунок 15. Динамика смертности от рака шейки матки на 100 000 населения в США в разных возрастных группах. Видно, как совершенствование методов лечения, скрининги и вакцинация помогли спасти много жизней.
Лабораторные исследования показывают, что практически у всех привитых, которые до этого не были заражены ВПЧ, вырабатывается много антител против возбудителя. Контрольные проверки спустя 10 лет и больше показывают, что защита сохраняется [50], [51].
Надо ли бояться побочных эффектов от вакцины?
Как и любые лекарственные препараты, вакцины против ВПЧ могут вызывать некоторые побочные эффекты. Но, как и у всех вакцин, они обычно легкие и быстро проходят — бояться не стоит. Возможные нежелательные реакции от прививки и рядом не стояли с той опасностью, которую создают вирусы папилломы высокого онкогенного риска — иначе новые вакцины не были бы зарегистрированы.
Например, с 2006 по 2014 год в США было введено 67 миллионов доз вакцины. После этого сообщалось о 25 176 случаев побочных эффектов, 92,4% из которых были легкими — они не представляли опасности для жизни, не вызывали долгосрочных проблем со здоровьем и не требовали госпитализации. Число смертельных случаев измерялось несколькими десятками, но, когда ученые проанализировали эти данные, то не нашли связи с прививкой. Чаще всего причиной становился сахарный диабет, другие инфекции, сердечная недостаточность, употребление наркотиков [55].
Во время клинических испытаний ученые чаще всего обнаруживали у участников лишь такие нежелательные реакции:
- Обмороки — весьма распространенное явление. Но связаны они не с вакциной, а с тем, что многие люди боятся уколов. Самая большая опасность в том, что во время падения можно получить серьезную травму. Поэтому после прививки человека просят 15 минут полежать или посидеть.
- У 20–90% испытуемых в месте укола возникает боль, покраснение, отек. Такая реакция характерна для многих вакцин, и она довольно быстро проходит.
- У 10–13% людей в течение 15 дней температура тела повышалась до 37,7 °С и более.
- Серьезных побочных эффектов не было обнаружено [46].
Одно из самых страшных осложнений после введения любых вакцин — анафилактический шок: тяжелая аллергическая реакция, которая может привести к смерти. Она возникает сразу после прививки, и на этот случай в любом прививочном кабинете есть противошоковый набор, чтобы сразу оказать помощь. Поэтому после прививки нужно полчаса посидеть возле прививочного кабинета.
В 2020 году австралийские ученые провели большой анализ — они проверили, как часто возникали побочные эффекты после введения 9 миллионов доз четырехвалентной вакцины «Гардасил» в течение 11 лет. Оказалось, что анафилактический шок развивается лишь у трех пациентов из миллиона [56].
Хотя вакцинация против ВПЧ безопасна, она всё же имеет некоторые противопоказания:
- Если у человека есть тяжелая аллергия на латекс, то его не стоит прививать двухвалентной вакциной «Церварикс». Она выпускается в предварительно заполненных шприцах, в наконечниках которых может содержаться латекс.
- Людям с тяжелыми аллергическими реакциями на пекарские дрожжи противопоказаны вакцины «Гардасил», потому что для них вирусные частицы производят как раз с помощью дрожжей.
- Если человек страдает тяжелыми хроническими заболеваниями, то вакцинацию нужно проводить с осторожностью, предварительно проконсультировавшись с лечащим врачом.
- При тяжелых острых заболеваниях вакцинацию нужно отложить до выздоровления.
- При легких острых заболеваниях, например, простуде, вакцинация обычно не противопоказана [46].
Следующий шаг: терапевтические вакцины
Существующие вакцины против ВПЧ защищают от опасных вирусов, только если привиться до заражения. Но многие женщины уже инфицированы, и эту проблему тоже нужно решать. Пока врачи могут предложить только регулярно проходить скрининги и надеяться, что вирусы папилломы не приведут к раку, или онкологическое заболевание будет обнаружено на ранней стадии, когда возможно эффективное лечение. Но в будущем ситуация может измениться.
Ученые уже не первый год занимаются разработкой терапевтических вакцин. Эти препараты направлены против двух онкогенов ВПЧ — E6 и E7. Именно они помогают клеткам становиться «бессмертными» и способствуют злокачественному перерождению. На данный момент созданы разные типы таких вакцин [57]:
- векторные — когда антигены возбудителя «загружают» в безвредные бактерии или вирусы и вводят их в организм;
- пептидные — состоят из белков вируса, против которых нужно сформировать иммунитет;
- ДНК- и РНК-вакцины — содержат генетический материал, который, попадая в организм, заставляет его синтезировать вирусные белки;
- вакцины на основе дендритных (антигенпрезентирующих — они «знакомят» T-лимфоциты с новыми антигенами) клеток — направлены не против самих ВПЧ, а против клеток, претерпевших злокачественную трансформацию [58];
- вакцины на основе раковых клеток — помогают сформировать иммунитет против опухолевых антигенов — аномальных белков, которые синтезируют эти клетки.
Многие из этих препаратов уже прошли доклинические, а некоторые даже клинические исследования. Но ни один пока не зарегистрирован и не применяется в клинической практике.
Заключение
Опыт применения вакцин против ВПЧ показал, что они безопасны, и при этом надежно защищают от вирусов, которые вызывают онкологические заболевания, и которыми очень легко заразиться.
Эксперты из Всемирной организации здравоохранения разработали глобальную стратегию по ликвидации рака шейки матки как проблемы общественного здравоохранения. Ожидается, что в течение ближайшего столетия это поможет сохранить более 62 миллионов женских жизней. Важной частью этой программы станет вакцинация против ВПЧ: до 2030 года профилактическими прививками должно быть охвачено не менее 90% девочек-подростков. Параллельно необходимо, чтобы 70% женщин прошли скрининг на рак шейки матки хотя бы дважды в жизни, и чтобы врачи своевременно выявляли и лечили 90% предраковых поражений.
Для врачей и ученых уже не стоит вопрос о том, нужно ли включать прививки от папилломавирусов в национальные прививочные календари. Несомненно, в ближайшее время это произойдет и в России. А для жителей нашей страны, которые хотят защитить свое здоровье и здоровье своих детей, не дожидаясь официальных предписаний, такая возможность есть уже сейчас.
Литература
- Хроника распространения SARS-CoV-2;
- Как вылечить COVID-19? (Спойлер: пока точно не знаем, но догадываемся);
- COVID-19: отвечаем на вопросы;
- Животные как объект для проведения испытаний вакцин против COVID-19: необходимость или излишество;
- Иллюзия уверенности;
- Пилюля от гриппа: современные противовирусные средства;
- Гепатит C: решенная проблема?;
- «Спутник V», «ЭпиВакКорону», «Модерну» делать будем? Ликбез по вакцинам против коронавируса;
- Гонки вакцин 2020;
- Неуловимый грипп;
- Объяснена различная вирулентность вирусов гриппа — возбудителей «испанки»;
- Syrjänen S. and Syrjänen K. (2008). The history of papillomavirus research. Cent. Eur. J. Public Health, Supplement. 16, S7–S41;
- Bakalar N. (2011). Human papillomavirus, 1985. The New York Times;
- Marianna Karamanou, Emmanovil Agapitos, Antonis Kousoulis, George Androutsos. (2010). From the humble wart to HPV: a fascinating story throughout centuries. Oncol Rev. 4, 133-135;
- M. J. Strauss, E. W. Shaw, H. Bunting, J. L. Melnick. (1949). «Crystalline» Virus-Like Particles from Skin Papillomas Characterized by Intranuclear Inclusion Bodies.. Experimental Biology and Medicine. 72, 46-50;
- Zhi-Ming Zheng. (2006). Papillomavirus genome structure, expression, and post-transcriptional regulation. Front Biosci. 11, 2286;
- Ellson Y. Chen, Peter M. Howley, Arthur D. Levinson, Peter H. Seeburg. (1982). The primary structure and genetic organization of the bovine papillomavirus type 1 genome. Nature. 299, 529-534;
- O. Danos, M. Katinka, M. Yaniv. (1982). Human papillomavirus 1a complete DNA sequence: a novel type of genome organization among papovaviridae.. The EMBO Journal. 1, 231-236;
- Киселев Л.Л., Абелев Г.И., Киселев Ф.Л. (2003). Лев Зильбер — создатель отечественной школы медицинских вирусологов. «Вестник Российской академии наук». 73(7), 647–659;
- Клещевой энцефалит: крошечный укус — серьезные последствия;
- SY Tan, Y Tatsumura. (2015). George Papanicolaou (1883–1962): Discoverer of the Pap smear. smedj. 56, 586-587;
- Увидевший вирусы в раке. Харальд цур Хаузен;
- Нобелевскую премию 2008 года по физиологии и медицине вручили за вирусологические исследования;
- John Doorbar, Nagayasu Egawa, Heather Griffin, Christian Kranjec, Isao Murakami. (2015). Human papillomavirus molecular biology and disease association. Rev. Med. Virol.. 25, 2-23;
- Kevin A. Ault. (2006). Epidemiology and Natural History of Human Papillomavirus Infections in the Female Genital Tract. Infectious Diseases in Obstetrics and Gynecology. 2006, 1-5;
- Juckett G. and Hartman-Adams H. (2010). Human papillomavirus: clinical manifestations and prevention. Am. Fam. Physician. 10, 1209–1214;
- Mark Schiffman, Philip E Castle, Jose Jeronimo, Ana C Rodriguez, Sholom Wacholder. (2007). Human papillomavirus and cervical cancer. The Lancet. 370, 890-907;
- Nicole Reddout, Todd Christensen, Anthony Bunnell, Dayne Jensen, Devin Johnson, et. al.. (2007). High risk HPV types 18 and 16 are potent modulators of oral squamous cell carcinoma phenotypes in vitro. Infect Agents Cancer. 2;
- Ching-Yi Cho, Yu-Cheng Lo, Miao-Chiu Hung, Chou-Cheng Lai, Chun-Jen Chen, Keh-Gong Wu. (2017). Risk of cancer in patients with genital warts: A nationwide, population-based cohort study in Taiwan. PLoS ONE. 12, e0183183;
- Maria Blomberg, Soren Friis, Christian Munk, Andrea Bautz, Susanne K. Kjaer. (2012). Genital Warts and Risk of Cancer: A Danish Study of Nearly 50 000 Patients With Genital Warts. The Journal of Infectious Diseases. 205, 1544-1553;
- Рак шейки матки. (2022). ВОЗ;
- Risk factors for oral cavity and oropharyngeal cancers. (2021). American Cancer Society;
- Braaten K.P. and Laufer M.R. (2008). Human papillomavirus (HPV), HPV-related disease, and the HPV vaccine. Reviews in obstetrics & gynecology. 1, 2–10;
- От поцелуя до лимфомы один вирус;
- Human papillomavirus (HPV) infection. (2021). CDC;
- Anogenital warts. (2021). CDC;
- The American Cancer Society guidelines for the prevention and early detection of cervical cancer. (2021). American Cancer Society;
- 12 методов в картинках: полимеразная цепная реакция;
- The history of the HPV vaccine. (2020). Noman;
- Benjamin J. Lieblong, Brooke E. E. Montgomery, L. Joseph Su, Mayumi Nakagawa. (2019). Natural history of human papillomavirus and vaccinations in men: A literature review. Health Sci Rep. 2, e118;
- Вакцинопрофилактика заболеваний, вызванных вирусом папилломы человека: федер. клинич. рекомендации. М.: «ПедиатрЪ», 2016. — 40 с.;
- Вирусы-платформы: яд во благо;
- Guide to introducing HPV vaccine into national immunization programmes. (2016). WHO;
- Рак можно предотвратить: НАНОЛЕК и НПК «Комбиотех» объявляют о начале совместного проекта по разработке и выводу на рынок первой полностью отечественной вакцины против вируса папилломы человека. (2020). «НАНОЛЕК»;
- «Р-Фарм» и Beijing Health Guard подписали соглашения по разработке и коммерциализации в России девятивалентной вакцины для профилактики ВПЧ. (2021). «Р-Фарм»;
- HPV vaccine recommendations. (2021). CDC;
- Вакцинация перед школой: гайд для родителей;
- Вакцинопрофилактика заболеваний, вызванных вирусом папилломы человека (руководства по профилактике заболевания/синдромов). Министерство здравоохранения РФ, 2017. — 25 с.;
- Распоряжение Правительства Российской Федерации от 29 марта 2021 г. № 774-р;
- HPV vaccine safety and effectiveness. (2021). CDC;
- Вакцины против вируса папилломы человека (документ по позиции ВОЗ). (2009). ВОЗ;
- Lidia Rosi Medeiros, Daniela Dornelles Rosa, Maria Inês da Rosa, Mary Clarisse Bozzetti, Roselaine Ruviaro Zanini. (2009). Efficacy of Human Papillomavirus Vaccines. International Journal of Gynecological Cancer. 19, 1166-1176;
- Гардасил (Gardasil). Vidal;
- Nicholas B. Schmuhl, Katherine E. Mooney, Xiao Zhang, Laura G. Cooney, James H. Conway, Noelle K. LoConte. (2020). No association between HPV vaccination and infertility in U.S. females 18–33 years old. Vaccine. 38, 4038-4043;
- White M.D. (2014). Pros, cons, and ethics of HPV vaccine in teens-Why such controversy? Translational andrology and urology. 3(4), 429–434;
- Anastasia Phillips, Megan Hickie, James Totterdell, Julia Brotherton, Aditi Dey, et. al.. (2020). Adverse events following HPV vaccination: 11 years of surveillance in Australia. Vaccine. 38, 6038-6046;
- Andrew Yang, Emily Farmer, T. C. Wu, Chien-Fu Hung. (2016). Perspectives for therapeutic HPV vaccine development. J Biomed Sci. 23;
- Yin W., Duluc D., Joo H., Oh S. (2016). Dendritic cell targeting vaccine for HPV-associated cancer. Cancer cell & microenvironment. 4, e1482;
- Jos Verssimo, Thales Allyrio Arajo de Medeiros Fernandes. (2012). Human Papillomavirus: Biology and Pathogenesis. Human Papillomavirus and Related Diseases — From Bench to Bedside — A Clinical Perspective;
- James Mitchell Crow. (2012). HPV: The global burden. Nature. 488, S2-S3;
- Beatriz Serrano, María Brotons, Francesc Xavier Bosch, Laia Bruni. (2018). Epidemiology and burden of HPV-related disease. Best Practice & Research Clinical Obstetrics & Gynaecology. 47, 14-26;
- Laia Bruni, Mireia Diaz, Leslie Barrionuevo-Rosas, Rolando Herrero, Freddie Bray, et. al.. (2016). Global estimates of human papillomavirus vaccination coverage by region and income level: a pooled analysis. The Lancet Global Health. 4, e453-e463;
- Jinyao Wang, Zhiqiang Bai, Zhenkun Wang, Chuanhua Yu. (2016). Comparison of Secular Trends in Cervical Cancer Mortality in China and the United States: An Age-Period-Cohort Analysis. IJERPH. 13, 1148.
Сергей Нетесов,
член-корреспондент РАН, Новосибирский государственный университет
«Коммерсантъ Наука» №6, сентябрь 2017
В мире интенсивно идет разработка лекарств от онкозаболеваний на основе вирусов. В нашей стране такие работы ведутся в Новосибирском университете, ГНЦ «Вектор», Институте химической биологии и фундаментальной медицины СО РАН и Институте молекулярной биологии РАН. Нами получены рекомбинантные штаммы различных вирусов, показавшие перспективность их использования для уничтожения раковых клеток. Проблема сейчас в получении финансирования на доклинические исследования и клинические испытания.
Прогнозы писателей-фантастов редко сбываются буквально. Но с рассказом Игоря Росоховатского «Шутка госпожи природы» именно так и произошло. В нем бедняк излечился от рака, съев батат, зараженный вирусом батата, в то время как богач умирает, хотя его лечили самыми современными методами. Рассказ был опубликован в 1962 году. А в 2015 году Управление по контролю пищи и лекарств США (FDA) разрешило применение рекомбинантного герпесвируса для лечения рецидивирующей меланомы (рака кожи) и рекомбинантного ортопоксвируса для лечения опухолей печени.
Да, конечно, нынешние онколитические вирусы — не вирусы растений. Но мы видим начало сознательного использования вирусов против онкозаболеваний: к списку методов лечения рака официально добавился метод разрушения опухолей с помощью вирусов.
Сомнения и перестраховка
Метод нельзя назвать новым, потому что первая посвященная ему научная публикация появилась еще в 1904 году. В ней было описано использование так называемого «фиксированного» (ослабленного) штамма вируса бешенства для лечения онкобольных. Но широкого распространения метод не получил как из-за непредсказуемости результатов, так и весьма значительной реактогенности тогдашней вакцины против бешенства.
Тем не менее в течение всего ХХ века к этому методу неоднократно возвращались. В частности, начиная с 1950-х годов в разных странах применялись слабо- или вообще не патогенные штаммы вирусов лихорадки Западного Нила, желтой лихорадки, вируса бешенства, аденовирусы, вирус болезни Ньюкасла, энтеровирусы, парамиксовирусы и некоторые другие непатогенные или слабопатогенные вирусы. При этом порой онкобольные полностью выздоравливали, наблюдались и временные улучшения. Но опять же отсутствие предсказуемости результатов, научно обоснованных принципов действия вирусов на опухоли и предубеждение контролирующих органов привели почти к полному прекращению применения этого подхода.
Начиная с 1950-х годов в разных странах применялись слабо- или вообще не патогенные штаммы вирусов лихорадки Западного Нила, желтой лихорадки, вируса бешенства, аденовирусы, вирус болезни Ньюкасла, энтеровирусы, парамиксовирусы и некоторые другие непатогенные или слабопатогенные вирусы
У нас работы в данном направлении были начаты в 1970-х годах профессором М. К. Ворошиловой в Институте полиомиелита и вирусных энцефалитов под Москвой. Она применяла для лечения онкозаболеваний вакцинные штаммы вируса полиомиелита и другие штаммы непатогенных энтеровирусов и в ряде случаев добилась серьезных успехов. Но предубеждения руководящих онкологов привели к запрету ее работ.
И в нашей стране, и в ряде других стран недоверие к потенциально полезным противораковым вирусам до недавнего времени превалировало из-за боязни их патогенных свойств. При этом врачи хорошо знают, что многие химиотерапевтические препараты для борьбы с онкозаболеваниями дают массу вредных побочных реакций. Но их применяют, и никакого предубеждения у врачей к ним нет. Между тем механизм действия большинства таких препаратов рассчитан на разницу в метаболизме раковых и нормальных клеток. Так что поражают эти препараты и раковые, и некоторые здоровые, но активно метаболизирующие, делящиеся клетки.
Первые официально испытанные вирусные онколитики
С 1990-х годов появилась теоретически намного более обоснованная концепция специальных онколитических вирусов. Впервые был выяснен, как тогда считали, механизм противораковой специфичности делеционного варианта аденовируса пятого серотипа с названием ONYX-015.
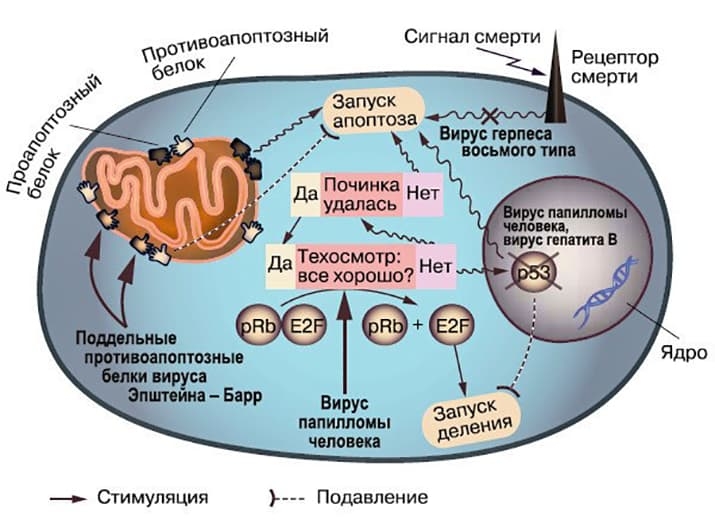
Дело в том, что в клетках человека и практически всех млекопитающих есть белок р53, который при начале каких-либо необычных процессов в клетке (в том числе при появлении в ней вирусов) запускает процесс апоптоза (запрограммированной клеточной смерти), чтобы не дать вирусу или вообще всей этой вдруг ставшей необычной клетке размножиться. Однако во многих опухолевых клетках ген белка р53 поврежден, а сам белок становится дефектным по этой своей функции, и в таких клетках ничто не сдерживает размножение вируса.
Но у аденовируса, в свою очередь, есть белок Е1В-55К, который связывает р53 и не дает ему запускать апоптоз. Таким образом, если из генома вируса удалить часть гена Е1В, где закодирован белок 55К, то такой вирус будет размножаться только в опухолевых клетках, где р53 и так не работает, а в нормальных он этого делать не сможет, так как клетки будут уходить в апоптоз и саморазрушаться.
Однако, как выяснилось позднее — в 2004 году, удаление части или целого гена E1B приводит к тому, что белок E1B-55K не выполняет еще ряд функций для размножения аденовируса. В опухолевых же клетках в его отсутствие эту функцию берет на себя не установленный до сих пор фактор. Также выяснилось, что есть много и других дефектов в клетках, которые приводят к их перерождению в раковые, и тогда такие аденовирусы не работают как лечебные препараты.
В конце 1990-х эта тематика по ряду причин пошла на спад. Тем не менее аналог ONYX-015, названный Н101 (онкорин), был официально разрешен для лечения больных с опухолями головы и шеи в Китае. Другой полученный в Китае рекомбинантный аденовирус, также с делецией гена Е1В, но с дополнительной вставкой человеческого гена р53 сейчас там также применяется для лечения онкобольных под названием гендицин.
С 1998 по 2003 год в ГНЦ вирусологии и биотехнологии «Вектор» силами лаборатории автора этой статьи был получен вариант аденовируса пятого серотипа с полностью удаленным геном Е1В и частично геном Е1А. Препарат на его основе был назван канцеролизином, было показано, что он обладает сходными с американским штаммом ONYX-015 и китайским онкорином онколитическими свойствами.
Данный штамм был проведен через полный цикл доклинических испытаний под руководством профессора ГНЦ ВБ «Вектор» А. Н. Сергеева. На основе их результатов канцеролизин был допущен к клиническим испытаниям первой фазы, которые в 2007 году прошли в РОНЦ им. Н. Н. Блохина с участием восьми пациентов-добровольцев. Испытания показали хорошую переносимость пациентами канцеролизина, а в двух случаях наблюдался и лечебный эффект, несмотря на то что у всех больных добровольцев была четвертая стадия развития болезни. К сожалению, финансирования на последующие испытания выделено в те годы так и не было, а позднее это потеряло актуальность из-за публикаций по разработкам вирусных онколитиков следующих поколений.
Препараты нового поколения
В 2010 году Новосибирский государственный университет получил мегагрант на исследования под руководством известного российского молекулярного биолога П. М. Чумакова, одним из ведущих исполнителей которого стал и автор настоящей статьи. В НГУ фактически с нуля была создана хорошо оборудованная научно-исследовательская лаборатория в комплексе с практикумом по микробиологии, подготовлен и опубликован ряд обзорных статей по онколитическим вирусам, и еще в 2012 году были получены и охарактеризованы первые кандидатные онколитические штаммы.
К настоящему времени уже вне рамок мегагранта усилиями неформального коллектива из сотрудников НГУ, ГНЦ ВБ «Вектор» и ИХБФМ СО РАН получен ряд рекомбинантных штаммов вируса осповакцины с высокими онколитическими характеристиками, которые на моделях in vivo показали хорошую перспективность. Кроме того, были охарактеризованы и паспортизованы онколитические штаммы парамиксовируса Сендай и сконструированы бактериальные плазмиды с полноразмерным геномом аденовируса 6 серотипа, крайне перспективные для получения новых рекомбинантных онколитических штаммов со встройками усиливающих онколизис генов.
Таким образом, имеются все основания для проведения дальнейших работ и особенно — для полноразмерных доклинических исследований, а впоследствии и клинических испытаний этих и подобных им перспективных онколитических вирусных штаммов. Сейчас наступило время преодолеть предубеждения и дать зеленый свет для финансирования разработок этих крайне перспективных препаратов, разработанных в России.
Работы в этом направлении продолжаются не только в НГУ, профессор П. М. Чумаков развивает эти исследования на энтеровирусах и парамиксовирусах в своей лаборатории в Институте молекулярной биологии РАН им. В. А. Энгельгардта в Москве. Заинтересовались ими и в ряде клиник России.
Могут ли вирусы быть полезными
Данное направление работ за рубежом в последние десять лет получило очень мощное развитие. В октябре 2015 года в США произошел кардинальный сдвиг в отношении этого направления разработок: как уже было сказано, FDA разрешило широкие клинические испытания третьей фазы генно-инженерного штамма герпесвируса с названием имлиджик (Imlygic) для лечения больных с рецидивирующей меланомой.
Исходный штамм герпесвируса, который содержит аттенуирующие (снижающие его патогенные свойства) мутации в геноме и экспрессируемый ген гранулоцит-макрофаг-колониестимулирующего фактора человека (ГМ-КСФ или GM-CSF), был разработан американской компанией BioVex Inc. В 2011 году эту компанию вместе с правами на препарат купил фармгигант Amgen. Этот же препарат был официально разрешен к применению и в Европе в конце 2015 года, информация о нем регулярно обновляется на сайте Imlygic.
В том же 2015 году аналогичное разрешение на проведение третьей фазы клинических испытаний было получено для препарата на основе рекомбинантного штамма вируса осповакцины пекса-век (Pexa-Vec), или JX-594, в отношении лечения гепатоцеллюлярной карциномы (рака печени). Данный препарат сконструирован на основе исходного штамма вируса осповакцины Wyeth, у которого для уменьшения реактогенности удален ген тимидинкиназы и встроен ген ГМ-КСФ человека. Его сейчас интенсивно исследуют на добровольцах. Результаты нескольких независимых клинических испытаний первой и второй фазы уже известны, они положительны, и поэтому клинические испытания третьей фазы для этого препарата проходят уже в нескольких десятках стран в 86 больницах, что говорит о его большой перспективности.
На последнем, 17-м Международном конгрессе по вирусологии в Сингапуре онколитическим вирусам была посвящена пленарная лекция профессора Гранта Макфаддена из США и две секции: «Вирусы как троянские кони» и «Вирусы и рак». Так что интерес к этому направлению возрос колоссально, и финансируется оно, как никогда ранее, в Канаде, США, Японии, Финляндии и других странах.
В этой связи возникает вопрос: а не может ли быть такого, что роль по крайней мере некоторых из вирусов для человеческого организма как раз и состоит в защите от раковых клеток, и лишь иногда они вызывают заболевания, выходя из-под контроля?
Такое предположение заслуживает внимания. Человечество уже очень много полезного создало из весьма вредоносных, на первый взгляд, веществ и микробов. А вирусы как лекарства очень интересны, поскольку являются высокоспецифичными микромашинами. Некоторые из них люди уже приспособили для своих нужд и применяют в качестве живых вакцин, лечебных препаратов (например, бактериофаги — вирусы бактерий вместо антибиотиков) и для избирательной борьбы с вредными насекомыми.
В свете событий, которые продолжаются уже почти два года, многим людям сложно воспринимать слово «вирусы» иначе как в негативном контексте. Но среди этих удивительных созданий (ученые до сих пор не могу решить, являются ли вирусы живыми) есть не только наши враги. Науке известен особый класс онколитических вирусов — они не вызывают заболеваний, но способны поражать и уничтожать раковые клетки. Именно о таких вирусах недавно подготовили обзор ученые из Университета штата Аризона (Arizona State University, США).
Вирусы — самые распространенные биологические объекты на земном шаре. Их намного больше, чем людей, и вообще чем любых живых существ. При этом сами вирусы занимают особое положение: они находятся где-то в области «темной материи» между живой и неживой природой.
Вирусы умеют паразитировать на всех формах клеточной жизни, включая человека, животных, растения, грибы и даже бактерии. Согласно современным представлениям, вирусы — не просто возбудители заболеваний, а глобальная сеть передачи генетической информации. Они играют огромную роль в развитии экосистем — и ее еще только предстоит изучить полностью.
Все вирусы можно условно разделить на две группы:
- «Специалисты» — те, которые заражают только строго определенные клетки и никак не влияют на остальные.
- «Универсалы» способны заражать разные организмы.
Онколитические вирусы, скорее, относятся к «специалистам». Они поражают опухолевые клетки, уничтожают их, но не влияют на здоровые ткани.
Профессиональные убийцы
Более века назад врачи заметили, что у некоторых онкологических пациентов с инфекциями опухоли самостоятельно регрессируют. Например, в конце XIX века были описаны случаи регрессии лейкозов при гриппе. Стало понятно, что некоторые вирусы помогают организму бороться с онкологическими патологиями. Конечно же, вскоре у ученых появилась идея использовать этот эффект для лечения.
Сегодня известен уже целый ряд онколитических вирусов, и их свойства изучаются в лабораториях по всему миру. Способность этих возбудителей поражать и убивать раковые клетки — лишь одно из полезных свойств. Куда важнее то, что онколитические вирусы умеют «будить» иммунную систему и помогают ей распознать присутствие злокачественной опухоли в организме.
Генная инженерия позволяет существенно улучшить онколитические вирусы, усилить их полезные способности. Это можно сделать, вырезав у возбудителя определенные исходные гены или вставив новые.
Вирусный десант
Одна из задач, которую приходится решать ученым, занимающимся «вирусной терапией» рака — решить, как доставить онколитические вирусы в злокачественную опухоль. Самый простой способ — ввести препарат непосредственно в опухолевую ткань. Но это невозможно, когда рак находится во внутренних органах, в которые нельзя просто ввести иглу. Препарат нужно вводить внутривенно. И здесь в его транспортировке помогают специальные клетки-носители.
В качестве клеток-носителей ученые рассматривают разные кандидатуры. Различаются и способы их применения. Иногда клетки заражают, а иногда вирусные частицы просто прикрепляют к их поверхности. Так или иначе, «профессиональные убийцы» достигают пункта назначения и делают свое дело.
В качестве одного из кандидатов на роль клеток-носителей рассматривают мезенхимальные стволовые клетки, полученные от самого пациента. Они не только являются отличным транспортом, но и способны усиливать противоопухолевые свойства онколитических вирусов.
Помощники иммунотерапии
Ученые считают, что онколитические вирусы станут отличным дополнением к уже существующим методам лечения в онкологии: химиотерапии, лучевой терапии, хирургии и особенно иммунотерапии.
Современная иммунотерапия сделала огромный шаг вперед, когда появились препараты из группы ингибиторов контрольных точек. Эти лекарства блокируют определенные молекулы, которые подавляют иммунную систему, мешают ей бороться со злокачественными опухолями.
Однако, ингибиторы контрольных точек эффективны только у 20–30% пациентов. Почему на них не реагируют остальные больные — зачастую сложно сказать. Возможно, у некоторых людей изначально возник иммунный ответ на злокачественную опухоль, а потом он был заблокирован. В таком случае иммунотерапия помогает, она снимает блокировку. У остальных иммунная реакция изначально не развивалась — поэтому ингибиторы контрольных точек не работают. И именно в таких случаях способны помочь онколитические вирусы. Когда в опухолевой ткани развивается инфекционный процесс, повышаются шансы на то, что иммунная система среагирует одновременно и на опухоль, и на инфекцию.
В настоящее время ингибиторы контрольных точек являются наиболее инновационными противоопухолевыми препаратами. Они зачастую более эффективны, чем классическая химиотерапия, лучше переносятся, помогают продлевать жизнь пациентов при поздних стадиях рака. В клиниках «Евроонко» доступны все оригинальные препараты последних поколений с доказанной эффективностью. Они всегда в наличии, и наши врачи готовы немедленно начать лечение.
Источник: sciencedaily.com.
Вирусно-генетическая теория возникновения опухолей, предложенная еще в 1940-х годах вирусологом Львом Зильбером (см. «МВ» № 1 от 5 января 2023 г.), в последнее время получает многочисленные подтверждения. Сегодня известно, что около 15 % новообразований человека связаны с вирусами. И хотя вирусы не являются единственной и основной причиной рака, они играют большую роль в этиологии злокачественных заболеваний.
Столетние исследования


Сейчас мы знаем, что геном многих онкогенных ретровирусов содержит сегменты, отличные от обычных вирусных генов. Эти сегменты представляют собой модифицированные клеточные гены, которые и обусловливают способность многих ретровирусов индуцировать образование опухолей. Они называются вирусными онкогенами (v-onc).
К середине 20-го века обнаружены вирусы, ассоциированные с опухолями у животных, в частности, открыты вирусы сарком и лейкозов мышей, кошек, обезьян, крупного рогатого скота. Позже было доказано, что практически у всех представителей животного мира имеются опухоли вирусного происхождения.
Основные положения теории Зильбера
Онкогенный вирус осуществляет наследственное превращение нормальной клетки в опухолевую из-за проникновения вирусного генома или его части в клетки животного. Два генома интегрируют (сливаются) между собой, придавая клетке совершенно новые свойства. Внедрившийся вирус (его геном) уже не играет роли в размножении трансформированных клеток, в образовании опухолей. Он, как правило, исчезает из крови и ткани, в которой была опухоль.
Опухоли, у которых вирусы идентифицированы в качестве этиологических факторов, обнаружены у многих видов млекопитающих и птиц. Они способны вызывать трансформацию клеток in vitro и индуцировать опухоли in vivo. В составе этих вирусов установлены либо специальные гены (онкогены), продукты которых непосредственно контролируют трансформированный фенотип зараженных клеток, либо гены, продукты которых индуцируют экспрессию других генов, участвующих в контроле пролиферации клеток.
Очень часто онкогенным вирусам приписывают свойства вирусов инфекционных. Причиной тому, видимо, являются достаточно хорошая информированность населения на бытовом уровне о вирусах, вызывающих инфекционные заболевания, и практически полная неосведомленность об онкогенных вирусах и их свойствах. И если внедрение инфекционного вируса в организм влечет за собой соответствующее заболевание, то, следуя логике обывателя, заражение онкогенным вирусом должно привести к возникновению соответствующей опухоли.
У многих представителей животного мира такая взаимосвязь, действительно, довольно часто наблюдается. Так, вирусы лейкоза кур, мышей, крупного рогатого скота вызывают соответствующие лейкозы; вирус папилломы кролика — папиллому у кроликов и т. д. Однако взаимоотношения между онкогенными вирусами и представителями животного мира гораздо сложнее и многообразнее.
Оказалось, что некоторые вирусы, считавшиеся онкогенными только для одного вида животных, способны вызывать опухоли у разных представителей млекопитающих (например, куриный вирус саркомы Рауса вызывает также опухоли у крыс, мышей, кроликов, змей и др.). В почках зеленой мартышки обнаружен вирус (SV-40), непатогенный для этого вида обезьян, но высокоонкогенный для некоторых видов млекопитающих, в частности хомяков.
Не менее сложной оказалась ситуация и с онкогенными вирусами человека: часть из них может персистировать в организме инфицированного всю жизнь, не вызывая новообразования и какой-либо другой патологии. Некоторые вирусы являются убиквитарными для человека (т. е. чрезвычайно широко распространены в популяции), благополучно с ним сосуществуя. После заражения онкогенным вирусом опухолевый процесс может возникнуть, но, вероятно, при сочетанном действии дополнительных факторов и наличии определенных условий.
Одно из чрезвычайно важных отличий инфекционного вируса от онкогенного заключается в том, что генетический материал опухолеродных вирусов, как правило, внедряется функционально и физически в геном клетки, нарушая ее нормальную жизнедеятельность и превращая в конечном итоге в злокачественную. При этом инфицированная клетка не гибнет, но усиленно размножается. Инфекционный же вирус, проникая в клетку, заставляет все ее ресурсы работать на себя, что крайне редко происходит с онкогенным вирусом. В этом случае процесс заканчивается созреванием вирусного потомства и гибелью клетки.
Другое важное отличие онкогенных и инфекционных вирусов состоит в том, что в геноме большинства ДНК- и РНК-содержащих онкогенных вирусов есть гены, которые кодируют белок, ответственный за превращение нормальной клетки в опухолевую. Причем попадание в организм животного вируса, содержащего онкоген (примером могут служить саркоматозные вирусы птиц и других животных), приводит к быстрому возникновению опухоли. У животного, зараженного вирусом, не содержащим онкогена (примером могут служить лейкозные вирусы мышей), латентный период возникновения новообразования может занять большую часть их жизни.
Следует отличать опухоли, индуцированные вирусами, от опухолей, в которых вирус присутствует в качестве «пассажира».
При вирусном происхождении опухоли заражение клеток предшествует ее появлению, и вирусные маркеры в организме возникают еще до формирования опухоли. В опухоли невирусного происхождения клетки могут быть заражены вирусом уже после ее появления.
Опухоль вирусного происхождения возникает из одной-единственной зараженной вирусом клетки. Для такой опухоли характерны моноклональность и интеграция вируса в одни и те же места генома опухолевой клетки. Обнаружена также корреляция между высокой заболеваемостью определенным типом рака и высокой инфицированностью населения определенным типом вируса. Для опухолей, индуцированных вирусом, характерно снижение заболеваемости определенным типом рака после вакцинации против соответствующего вируса и/или проведения других профилактических мер.
Исследования 1970–1980-х гг. показали, что онкогены РНК-содержащих вирусов (ретровирусов), а также некоторых ДНК-содержащих онкогенных вирусов имеют клеточное происхождение. Было доказано, что когда-то много лет назад регуляторные гены клетки были захвачены этими вирусами и уже в составе вирусного генома превратились в онкогены.
Открытие оказалось чрезвычайно важным для понимания механизма возникновения опухоли, т. к. стала очевидной возможность превращения нормальных клеточных генов в онкогены под воздействием спонтанных или вызванных какими-либо факторами генетических мутаций и без участия вирусов. И действительно, такие клеточные онкогены, не имеющие никакого родства с вирусными онкогенами, были обнаружены во многих опухолях невирусного происхождения человека и животных.
Не менее важным для понимания механизмов канцерогенеза оказалось и открытие в нормальной клетке генов-супрессоров (например, р53 или Rb), препятствующих превращению клетки в злокачественную. Инактивация генов-супрессоров и преобразование регуляторных клеточных генов в активно функционирующий онкоген представляется сегодня основным механизмом превращения нормальной клетки в опухолевую. Опухоли же, индуцированные вирусами, представляют собой лишь частный случай внесения онкогенов извне в клетку и инактивации в ней генов-супрессоров. Иначе говоря, вирус, наряду с химическими канцерогенами и лучевой энергией, следует рассматривать в качестве одного из возможных канцерогенных факторов, способных индуцировать опухоль.
Механизмы клеточной трансформации
Чтобы стать злокачественной, клетка должна приобрести по крайней мере 6 свойств — результат мутации генов, ответственных за деление, апоптоз, репарацию ДНК, внутриклеточные контакты и т. д.
На пути к злокачественности клетка, как правило:
- самодостаточна в плане сигналов пролиферации (что может быть достигнуто активацией некоторых онкогенов, например Н-Ras);
- нечувствительна к сигналам, подавляющим ее рост (что происходит при инактивации гена опухолевого супрессора Rb);
- способна ослабить или избежать апоптоза (что происходит в результате активации генов, кодирующих факторы роста);
- формирование опухоли сопровождается усиленным ангиогенезом (что может быть обеспечено активацией гена VEGF, кодирующего ростовые факторы эндотелия сосудов);
- генетически нестабильна;
- не подвергается клеточной дифференцировке;
- не подвергается старению;
- характеризуется изменением морфологии и локомоции, что сопровождается приобретением свойств к инвазии и метастазированию.
Поскольку мутации генов являются событиями случайными и достаточно редкими, их накопление для инициации клеточной трансформации может длиться десятилетиями. Трансформация клетки может произойти гораздо быстрее в случае высокой мутагенной нагрузки и/или дефектности (слабости) механизмов защиты генома (генов p53, Rb, репарации ДНК и некоторых других).
Комплексный анализ генома выявил драйверные гены, в том числе APC, KRAS, TGFBR2 и TP53, мутации которых часто фиксируются при колоректальном раке (например, мутация p53 обнаруживается примерно в 60 % случаев, и большинство мутаций относится к миссенс-типу в «горячих точках», что предполагает онкогенную роль мутантного p53 посредством механизмов «приобретения функции»). В случае же инфицирования клетки онкогенными вирусами кодируемые вирусным геномом белки, обладающие трансформирующим потенциалом, нарушают нормальные клеточные сигнальные связи, обеспечивая условия для активной клеточной пролиферации.
Характерной особенностью опухолевых заболеваний, ассоциированных с вирусами, является длительный латентный период. От момента инфицирования до проявления заболевания проходит от 10 до 40 лет.
Эксперты Международного агентства по изучению рака (МАИР) в качестве онкогенных для человека рассматривают: вирусы гепатита В и С, вызывающие рак печени; определенные типы (16 и 18) папилломавирусов человека, являющихся этиологическим агентом рака шейки матки и некоторых опухолей аногенитальной сферы; вирус Эпштейна — Барр, принимающий участие в возникновении целого ряда злокачественных новообразований; герпесвирус человека 8-го типа, играющий важную роль в возникновении саркомы Капоши, первичной выпотной лимфомы, болезни Кастельмана и некоторых других патологических состояний; вирус Т-клеточного лейкоза человека (HTLV-I), являющийся этиологическим агентом Т-клеточного лейкоза взрослых (у каждого 30-го из носителей HTLV-I развивается Т-клеточная лейкемия/лимфома; практически все матери пациентов с этим заболеванием являются носительницами HTLV-I), а также тропического спастического парапареза и ряда других неонкологических заболеваний; вирус иммунодефицита человека, не обладающий трансформирующими генами, но создающий необходимые условия (иммунодефицит) для возникновения рака.
Вирусы гепатита В и С относятся к числу вирусов непрямого действия, поскольку не содержат в своем составе онкогена. Онкогенный потенциал они проявляют путем активации клеточных генов, участвующих в процессах пролиферации.
Вирусный канцерогенез имеет ряд существенных особенностей, связанных с привнесением в клетку собственной генетической информации. В случае онкогенных ретровирусов можно утверждать, что они выступают либо в качестве агентов, активирующих клеточные протоонкогены (слабоонкогенные вирусы), либо несут трансформирующие последовательности, ведущие свое происхождение от тех же клеточных протоонкогенов. Причем имеющиеся мутационные различия в кодирующей последовательности вирусного онкогена и клеточного протоонкогена играют существенную роль в повышении его трансформирующей активности.
Что касается герпесвирусов, то их структура настолько сложна, что все имеющиеся экспериментальные данные об онкогенном потенциале отдельных участков генома этих вирусов пока носят предварительный характер. При этом выяснено, что герпесвирус ассоциирован с саркомой Капоши.
Механизм опухолевой конверсии под действием вирусов специфичен для каждого типа вируса, но, как правило, связан с нарушением функций клеточных генов, участвующих в процессах деления и пролиферации клеток. Это может быть прямая инактивация генов-супрессоров в результате взаимодействия с продуктами вирусных генов, как в случае вирусов папиллом, или результат трансактивирующего действия вирусных генов на клеточные гены, модулирующие пролиферацию клеток, как в случае вируса гепатита В.
Вирус может являться инициирующим фактором. Для полного проявления онкогенного потенциала вирусных генов необходимы дополнительные генетические изменения в геноме инфицированной клетки, приводящие к формированию моноклональной популяции клеток с неконтролируемой пролиферацией.
За последнее время произошел большой прогресс в изучении механизмов вирусного онкогенеза. К ключевым моментам можно отнести открытие мутационного эффекта вирусов и их онкогенов на геном млекопитающих, выявление инсерционного мутагенеза, вызываемого внедрением вирусов в геном, обнаружение влияния, оказываемого продуктами различных вирусных генов на экспрессию клеточных генов.
Вместе с тем накоплены данные, указывающие на то, что канцерогенез является многоэтапным процессом. Как правило, к злокачественному перерождению приводит каскад событий, затрагивающих множество различных клеточных и вирусных генов. При этом не всегда понятно, что служит основным сигналом, запускающим данный каскад.
Известно, что вирусы влияют на апоптоз клеток и этим пролонгируют или сокращают их выживание. В частности, показано, что вирус иммунодефицита человека индуцирует апоптоз в CD4+ T-лимфоцитов, вирус болезни Марека оказывает антиапоптотическое действие на Т-лимфоциты. При этом разные вирусы используют разные стратегии влияния на апоптоз клетки хозяина. Так, вирус простого герпеса в результате конвергентной эволюции приобрел белок, имеющий сходство с антиапоптотическими клеточными белками семейства Bcl-2. Становится очевидным, что влияние вирусов на апоптоз и, в частности, на его предотвращение может быть одним из механизмов вирусного канцерогенеза (см. рисунок).
Рисунок. Влияние вирусов на апоптоз.
Мутационная теория рака основывается на положении, что все канцерогены являются одновременно мутагенами. Выяснилось, что даже те канцерогены, у которых ранее мутагенное действие не было обнаружено, приобретали его, попадая в организм, в результате активации. Мутагенными оказались не только различные химические вещества и физические факторы, но и «живые канцерогены» — онкогенные вирусы. Это было установлено для таких онкогенных ДНК-содержащих вирусов, как SV40 и некоторые аденовирусы.
Таким образом, вирусные онкогенные последовательности являются чужеродным генетическим материалом, не участвуют в процессах размножения вируса и, более того, в подавляющем большинстве случаев делают вирус дефектным по репликации за счет замещения онкогеном части необходимых вирусных генов.
Общие биологические свойства онкогенных вирусов
Несмотря на различную организацию онкогенных вирусов человека, неодинаковый спектр их клеток-мишеней, они обладают рядом доказанных общих биологических свойств, а именно:
- вирусы лишь инициируют патологический процесс, усиливая пролиферацию и генетическую нестабильность инфицированных ими клеток;
- у инфицированных онкогенными вирусами лиц возникновение опухоли, как правило, событие нечастое: один случай новообразования среди сотен, иногда тысяч инфицированных;
- после инфицирования до возникновения опухоли проходит продолжительный латентный период, длящийся годами, иногда десятилетиями;
- у большинства инфицированных лиц возникновение опухоли не является обязательным, но они могут составить группу риска с более высокой возможностью ее возникновения;
- для злокачественной трансформации инфицированных клеток необходимы дополнительные факторы и условия, приводящие к селекции наиболее агрессивного опухолевого клона.
Доказанные дополнительные факторы, играющие роль коканцерогенов:
- наличие в продуктах питания афлатоксинов, а также токсические дозы алкоголя для вирусов гепатита В и С;
- использование моющих средств, содержащих деготь;
- табакокурение;
- длительная экспозиция к дыму;
- вирус простого герпеса 2-го типа;
- вирус папилломы человека 16/18-генотип;
- малярия;
- нитрозамины в продуктах питания (соленая и вяленая рыба);
- пестициды;
- некоторые типы красок;
- недостаточное питание (дети, снижение иммунокомпeтентности);
- мази, содержащие форболовые эфиры (для вируса Эпштейна — Барр);
- иммуносупрессанты.
Остается много вопросов, связанных, например, с биологией взаимоотношений между онкогенным вирусом и инфицированным хозяином, спектром типов клеток, естественно инфицированных этими вирусами in vivo, защитными механизмами, позволяющими вирусу персистировать в организме, несмотря на иммунологическую защиту.
Возникновение вирус-ассоциированных опухолей человека после длительного латентного периода свидетельствует о том, что даже в «вирусных» опухолях нужно несколько генетических событий для полного проявления онкогенного потенциала вирусных генов. Эти вторичные генетические процессы и механизмы их действия практически не изучены. Механизмы канцерогенеза, ассоциированные с вирусом гепатита С, неясны из-за отсутствия адекватных клеточных моделей и являются предметом исследований.
Важной задачей остается и разработка вакцин и/или других средств иммунной интервенции против возможных вирус-ассоциированных опухолей.
Согласно современным представлениям, образование злокачественных опухолей запускается из-за поломок на генетическом уровне внутри ранее нормальных клеток. Эти поломки запускают цепочку дальнейших нарушений, что приводит к безостановочному росту, делению и выживанию опухолевых клеток. Изначальные поломки могут быть вызваны различными факторами.
Некоторые инфекционные агенты (вирусы и бактерии) также выступают провокаторами поломок. К наиболее часто встречающимся онкогенным вирусам (то есть вирусам, при инфицировании которыми возрастает риск развития того или иного онкологического заболевания) относятся:
- некоторые штаммы (или варианты) вируса папилломы человека (ВПЧ),
- вирус Эпштейн-Барр (ВЭБ),
- вирус гепатита В,
- вирус гепатита С,
- герпесвирус, ассоциированный с саркомой Капоши (также его называют вирус герпеса 8 типа — ВГЧ-8).
Что касается бактериальных инфекций, они могут спровоцировать возникновение хронического воспаления, которое потенциально выступает фактором развития онкологических заболеваний. Наиболее убедительные данные о взаимосвязи между бактерией и злокачественным новообразованием существуют для Helicobacter pylori и рака желудка.
Какие инфекции и вирусы повышают риск развития рака?
-
Вирус папилломы человека (ВПЧ)
ВПЧ — это распространенная инфекция, передающаяся контактным путем и вызывающая развитие остроконечных кондилом и некоторых видов рака. Большинство людей инфицируются ВПЧ в течение жизни, однако это не приводит к болезни, так как иммунная система справляется с микроорганизмом. Обычно заражение происходит во время незащищенного полового контакта (вагинальный, анальный, оральный половой акт, контакт кожа к коже в области гениталий, обмен секс-игрушками). ВПЧ — это не один вирус, а группа вирусов, состоящая из более чем 100 представителей. Однако не все штаммы (варианты) этого вируса обладают онкогенным потенциалом. Наиболее опасны в этом плане штаммы 16 и 18, также штаммами высокого риска являются 31, 33, 45, 52, 58.
Какие онкологические заболевания вызывает ВПЧ?
Инфицирование этими штаммами ассоциировано с повышением риска следующих онкологических заболеваний:
- рак шейки матки,
- рак влагалища, вульвы,
- рак анального канала,
- рак полового члена,
- рак полости рта, горла.
Если собственная иммунная система не изгнала вирус, то он, попадая в здоровые клетки организма, вносит изменения в структуре ДНК, вызывая поломки и каскад изменений, ведущих к раку. От момента заражения ВПЧ до развития онкологического заболевания могут пройти годы, а иногда и десятилетия. Инфекция не проявляет себя симптомами длительное время.
Как защитить себя от инфицирования и развития рака?
Защита от инфицирования ВПЧ включает в себя вакцинацию (в западных странах доступна для мальчиков и девочек в возрасте 11-13 лет) и защищенные половые контакты (использование презервативов).
Доказано, что вакцинация против ВПЧ снижает риск развития интраэпителиальных неоплазий шейки матки (предраковое состояние), а также самого рака шейки матки. Данные о влиянии на другие виды рака (анальный канал, полости рта) более ограничены, однако в настоящий момент известно, что вакцина снижает частоту возникновения предраковых состояний для описанных выше раков. Важным является время вакцинации: в исследованиях было показано, что более раннее введение вакцины (11-13 лет, когда организм еще не инфицирован ВПЧ) значительно эффективнее, чем вакцинация, когда организм уже знаком с ВПЧ инфекцией. При вакцинации не инфицированного организма защита от интраэпителиальных неоплазий составила 99%, при введении позже, инфицированному организму — 61%.
Снизить смертность по причине онкологических заболеваний, ассоциированных с ВПЧ, помогает скрининг. Он эффективен по отношению к раку шейки матки и включает в себя:
- 21-29 лет: Пап-тест каждые 3 года;
- 30 — 65 лет: либо продолжить Пап-тест каждые 3 года, либо тестирование на ВПЧ + Пап-тест каждые 5 лет;
Описанная программа действует в западных странах. В России предложена следующая программа, входящая в диспансеризацию: с 18 до 64 лет один раз в три года – осмотр гинеколога, взятие мазка на цитологию.
-
Вирус Эпштейн-Барр (ВЭБ)
Этим вирусом инфицировано 90-95% всего взрослого населения. Инфицирование происходит в детстве, вирус передается воздушно-капельным путем по воздуху (капельки слюны во время кашля, чихания), через предметы быта, при поцелуях, то есть, через любые человеческие жидкости. Хроническое носительство вируса не сопровождается симптомами. Однако если человек инфицируется ВЭБ во взрослом возрасте, он может заболеть инфекционным мононуклеозом, который проходит в течение нескольких недель.
Какие онкологические заболевания вызывает этот вирус?
ВЭБ связан с лимфомой Ходжкина, лимфомой Беркитта, раком носоглоки. Однако, из всех людей, инфицированных ВЭБ, онкологическое заболевание разовьется лишь в 1% случаев. К сожалению, нет никаких критериев, которые могли бы указать: разовьется ли рак у человека, инфицированного ВЭБ, или нет. Поэтому нет и специфических вакцин, программ скрининга и т.д., которые были бы направлены на ВЭБ или связанные с ним злокачественные новообразования.
-
Вирусы гепатита В и С
Инфицирование происходит через кровь, сперму и другие биологические жидкости (половые контакты, инъекции, переливание крови, от матери к ребенку во время родов или с молоком). При адекватном иммунном ответе развивается острый гепатит, который обычно заканчивается выздоровлением (гепатит В). При неадекватном — гепатит перейдет в хроническую форму. Наибольшая опасность хронических форм заболевания представляет развитие цирроза печени в исходе заболевания.
Какие онкологические заболевания вызывает этот вирус?
Хроническое воспаление печени и цирроз ассоциированы с развитием агрессивной формы рака — гепатоцеллюлярной карциномы (первичный рак печени).
Как защитить себя от инфицирования и развития рака?
Вакцинация против гепатита B доступна в нашей стране и проводится в первые 24 часа жизни ребенка. Вторая вакцинация, согласно календарю прививок, проводится в 1 или 3 месяца жизни, третья — в 6 месяцев жизни. Также вакцинация проводится во взрослом возрасте медицинским и социальным работникам, сотрудникам детских учреждений, заведений общественного питания, донорских пунктов.
Против вируса гепатита С в настоящее время вакцины нет.
Общими правилами для снижения риска заражения является защищенные половые контакты, избегание пользования общими иглами, бритвенными, маникюрными принадлежностями и услугами нелицензированных тату-салонов.
-
Вирус герпеса 8 типа (ВГЧ-8) и вирус иммунодефицита человека (ВИЧ)
ВИЧ — это вирус, который может привести к развитию СПИДа (синдром иммунодефицита человека). Оба вируса, ВИЧ и ВГЧ-8, передаются через жидкости организма (половые контакты, общие иглы и другой инвазивный инструментарий, от матери к ребенку). ВИЧ воздействует на иммунную систему, подавляя активность иммунных клеток, которые противостоят инфекциям, а также опухолевой трансформации в организме. ВГЧ-8 — вирус, выявленный в клетках пациентов с саркомой Капоши (онкозаболевания, выявляемого на фоне ВИЧ-инфекции). Дело в том, что в норме иммунитет способен уничтожить проникший вирус. Однако при угнетении иммунной системы организм становится крайне уязвимым перед такими агентами.
Какие онкологические заболевания вызывают эти вирусы?
Пациенты, инфицированные ВИЧ, имеют большие риски развития следующих видов онкологических заболеваний:
- саркома Капоши (из-за присоединения ВГЧ-8 на фоне угнетения иммунитета),
- лимфома Ходжкина и неходжкинские лимфомы (в связи с активацией ВЭБ на фоне иммунодефицита),
- рак шейки матки, анального канала, рака полового члена, влагализа, вульвы, некоторых раков головы и шеи (присоединение ВПЧ-инфекции),
- гепатоцеллюлярный рак (инфицирование и усугубление течения вирусных гепатитов).
Как защитить себя от инфицирования и развития рака?
К сожалению, в настоящий момент не существует вакцины против ВИЧ. Однако общие правила для избежания заражения схожи с правилами, общими для всех инфекций, передающихся через биологические жидкости:
- защищенные половые контакты (презервативы),
- избегание использования общих инвазивных инструментов (иглы, бритвенные принадлежности, маникюрные наборы).
В случае наличия ВИЧ-инфекции необходима приверженность лечению (антиретровирусной терапии, АРВТ) для снижения риска присоединения инфекций и развития онкологических заболеваний.
Выводы
- Онкологические заболевания не заразны и не передаются от человека к человеку.
- К наиболее часто встречающимся онкогеннымм вирусам (или вирусам, при инфицировании которыми возрастает риск развития того или иного онкологического заболевания) относятся:
- некоторые штаммы (или варианты) вируса папилломы человека (ВПЧ),
- вирус Эпштейн-Барр (ВЭБ),
- вирус гепатита В,
- вирус гепатита С,
- герпесвирус, ассоциированный с саркомой Капоши (также его называют вирус герпеса 8 типа — ВГЧ-8).
- Существуют вакцины от ВПЧ, вируса гепатита В. Для других онкогенных вирусов вакцины не разработаны.
Что еще почитать?
- Статья о молекулярных механизмах развития онкологических заболеваний и вирусных инфекциях — на английском языке
- Информационный блок о ВПЧ от National Health Service — на английском языке
- Научная статья об инфекции ВЭБ и развитием онкологических заболеваний — на английском языке
- Статья о гепатите В от ВОЗ — на русском языке
- Статья о гепатите С от ВОЗ — на русском языке
- Статьи о ВИЧ- инфекции от центра контроля предотвращения заболеваний — на английском языке
- Статья о ВИЧ-инфекции от “центра специализированной помощи по профилактике и борьбе с онкологическими заболеваниями” — на русском языке.
Онколог, химиотерапевт, научный сотрудник НМИЦ им. Н.Н. Блохина. Выпускница Высшей школы онкологии.
2 сентября 2022
16 февраля 1970 года скончался человек, который доказал, что причиной рака могут быть вирусы — американский патолог Фрэнсис Пейтон Роус. В 1969 году получил за свои исследования в области рака и за открытие онкогенных вирусов Нобелевскую премию, которую разделил с Чарльзом Хаггинсом.
К вирусной теории рака за последние 100 с лишним лет несколько раз менялось отношение. Однако сегодня известно точно: некоторые вирусы вызывают рак, и у них даже есть для этого все необходимые механизмы. MedAboutMe выяснял, как распространенные вирусы становятся причиной рака.
Вирусная теория рака
О вирусах наука узнала в 1890-х годах. Открытие вирусов — это тот замечательный случай в науке, когда все факты указывают на существование объекта, но получить этот объект, увидеть его невозможно — из-за несовершенства технологий. Самые лучшие фильтры, с помощью которых ученые уверенно выделяли бактерий, пропускали более мелкие по размеру вирусы.
В 1903 году французский ученый А. Боррель первым предположил, что вирусы могут быть причинами раковых опухолей. Через несколько лет исследователи О. Банг и В. Эллерман пришли к выводу, что лейкоз у кур — результат вирусной инфекции.
Российский ученый И.И. Мечников в 1910 г., обсуждая причины рака в газете «Русское слово», также высказал предположение, что причина развития злокачественных опухолей кроется не только в самом организме, но имеет также «экзогенное начало» — в виде вируса.
А буквально еще через год американский ветеринар Ф. Раус наглядно продемонстрировал, что саркома у кур вызывается именно вирусом — позднее Раус как раз и получит за свое открытие Нобелевскую премию. В исследованиях Рауса самое примечательно то, что он наблюдал за вирусом, изучал его, не видя, не имея возможности встретиться с ним, так сказать, «лицом к лицу». Выделить вирус удалось только в 1940-х годах.
На сегодняшний день известно не так уж много вирусов, которые приводят к развитию злокачественных опухолей — всего 15% случаев рака у человека имеют вирусную природу, у животных этот показатель существенно выше.
Как вирус приводит к раку?
Известно, что вирус использует геном и ресурсы клетки, чтобы синтезировать компоненты, необходимые ему для сборки новых вирусных частиц. При этом возможна реализация одной из двух стратегий. Если при этом происходит разрушение клетки — мы наблюдаем инфекционный процесс, распространение вируса по организму. Если же геном вируса определенным образом интегрируется с геномом клетки-хозяина, последняя перестает подчиняться системам, регулирующим ее рост и размножение. Как следствие, развивается злокачественная опухоль, растущая по своим законам.
Немалая часть онковирусов — это ретровирусы. Их геном представляет собой одноцепочечную РНК. Когда РНК вируса проникает в клетку, она становится матрицей для двухцепочечной ДНК, которая, в свою очередь, и будет встраиваться в геном клетки-хозяина.
Некоторые из онковирусов имеют в геноме онкогены, контролирующие процесс трансформации клетки с измененным геномом из обычной в злокачественную. Другие онковирусы обладают генами, которые активируют нужные участки генома клетки-хозяина, задействованные в процессах клеточного деления и дифференциации.
Онкогенные вирусы и болезни
Все заболевания, вызываемые онковирусами, отличает характерная черта: с момента заражения до появления первых симптомов может пройти 10-40 лет, то есть эти болезни имеют продолжительный латентный период.
Какие же вирусы могут стать причиной развития онкологических болезней у человека?
Вирус Т-клеточного лейкоза взрослых
Вирус Т-клеточного лейкоза взрослых (ATLV), или Т-лимфотропный вирус человека (HTLV), вызывает заболевание, которое встречается на паре островов Японского моря и у представителей негритянской расы в некоторых странах Карибского бассейна. Наблюдения показали, что даже если пациенты с этой разновидностью лейкоза встречаются в других странах мира, выявляется их связь с указанными регионами.
Следует отметить, что раком заболевает только 5% инфицированных людей, остальные являются носителями вируса. В геноме этого ретровируса имеется 2 копии одноцепочечных РНК. В организме жертвы на их основе синтезируется ДНК, которая интегрируется в геном клетки. Основу опухоли составляют CD4-лимфоциты.
Эта болезнь проявляется после 50 лет — отсюда и уточнение в названии. Для нее характерны увеличение печени и селезенки, лимфатических узлов, поражения кожи, разрушение костной ткани.
Вирусы герпеса
Рак могут вызывать два представителя семейства ДНК-содержащих вирусов герпеса:
- Вирус Эпштейна-Барр (ВЭБ, вирус герпеса 4 типа).
Этот онковирус может стать причиной лимфомы Беркитта и рака носоглотки. Он способен размножаться, в частности, в В-лимфоцитах. При этом клетки не гибнут — в них запускается процесс неконтролируемого роста, что и приводит к образованию злокачественной опухоли. ВЭБ, по оценкам экспертов, имеется в крови у 90-95% взрослого населения и у половины детей младше 5 лет. Как видно, раком обладатели ВЭБ болеют редко, впрочем вирус вызывает целый ряд разнообразных заболеваний: от инфекционного мононуклеоза до лейкоплакии.
- Вирус герпеса 8 типа.
Этот вирус может стать причиной эпидемической разновидности саркомы Капоши. Вирус активизируется на фоне значительного иммунодефицита, поэтому чаще всего опухоль развивается у людей, больных СПИДом.
При саркоме Капоши эндотелий (внутренние стенки сосудов) разрастается, его структура меняется — стенки становятся «дырявыми». Эти изменения касаются и кровеносных, и лимфатических сосудов. У пациента развиваются поражения кожи, слизистых оболочек и внутренних органов, отеки, увеличение лимфатических узлов.
Вирусы гепатита
Вирусы гепатита В и С — ДНК-содержащие вирусы, способные спровоцировать формирование карциномы печени. Они не имеют онкогенов, поэтому являются вирусами непрямого действия. Это значит, что они «включают» гены клетки, которые запускают процесс неконтролируемого размножения и роста. Печень — активно регенерирующий орган. При поражении вирусами сначала развивается цирроз, начинается разрастание соединительной ткани, орган пытается регенерировать и восстановить свои функции, но под действием вируса происходит активизация процессов озлокачествления клеток и образования опухоли.
Следует отметить, что лишь у менее чем 5% взрослых зараженных людей развивается хронический гепатит В. И только у 20-30% из их числа будет диагностирован цирроз или рак печени. Сходная ситуация наблюдается и в отношении вируса гепатита С. Лишь 5% зараженных им людей получают рак.
Для защиты от вируса гепатита В еще в 1982 году ученые разработали вакцину. Она на 95% защищает от рака печени, ассоциированного с вирусом.
Вирус папилломы человека
Как и вирус Эпштейна-Барр, ВПЧ имеется у большинства взрослых людей. Считается, что к 30 годам не менее 70% людей хотя бы раз получали вирус от своего полового партнера, а среди молодых женщин половина является обладательницами ВПЧ. Неудивительно, если учитывать, что в ходе первого полового акта треть девушек получает вирус.
Однако и в этом случае повальной гибели людей от рака шейки матки не наблюдается. Из 130 штаммов вируса папилломы человека лишь 14 входят в группу высокого онкогенного риска. Чаще всего в тканях злокачественных опухолей шейки матки находят 16 и 18 типы: в 55% случаев — ВПЧ 16 типа и в 15% случаев — ВПЧ 18 типа. При этом 25% случаев рака шейки матки вообще не связаны с вирусной инфекцией.
ВПЧ имеет собственные онкогены, которые запускают процесс трансформации клеток. Утешает то, что дисплазия шейки матки, которая считается предраковым состоянием при поражении вирусами из группы высокого онкогенного риска, легко диагностируется при регулярных посещениях гинеколога и успешно лечится.
Вакцинация против рака
На самом деле, это, конечно, не очень правильное выражение — «вакцинация против рака». Заражение ВПЧ — это вовсе не 100%-ная гарантия заболевания раком шейки матки. А данная разновидность рака может развиться и без участия вируса — такое случается намного реже, но все же бывает. Аналогичная ситуация и с вирусами гепатитов В и С, и с вирусом Эпштейна-Барр, и др. Поэтому правильно говорить о вакцинации против возбудителей онкологических заболеваний.
Пока в распоряжении человечества имеются вакцины только против двух из перечисленных заболеваний: против ВПЧ и гепатита В. И то — вакцина против ВПЧ защищает лишь от двух онкогенных штаммов, 16 и 18-го, зато самых распространенных.
Выводы
- Вирусы — далеко не единственная причина образования злокачественных опухолей.
- Кроме вирусов, есть и другие организмы, которые обладают онкогенными свойствами — бактерии, гельминты.В то же время есть множество разновидностей рака неинфекционной природы.
- Некоторые вирусы вызывают рак у одних живых существ и никогда не делают этого у других.
- При заражении онковирусами вовсе не обязательно разовьется рак. А если и разовьется, то с высокой долей вероятности лет через 20-30, а то и больше. В большинстве случаев болезнь оказывается просто инфекцией, не вызывающей озлокачествления клеток организма-хозяина. Но чтобы максимально снизить риски, необходимо своевременно обращаться к врачу и лечиться, не дожидаясь худшего варианта развития событий.
- Наконец, если есть возможность — надо вакцинироваться и защитить себя от патогенов, способных вызвать рак.
Онкология / Под ред. Чиссова В.И., Дарьялова С.Л. – 2007
Клиническая онкология / Под ред. Брюсова П.Г., Зубапева П.Н. – 2012
Диагностика ВПЧ — обусловленных злокачественных опухолей кожи / Минуллин И.К., Усманова С.Р. // Практическая медицина – 2005 – №4(13)
Белок теплового шока повышает иммуногенность онкобелка е7 вируса папилломы человека в составе химерной конструкции (е7 ВПЧ-HSP70) / Свешников П.Г., Солопова О.Н., Курбатова Е.А., Шевчик Ю.С., Барановский П.М., Ульянов А.М., Боков М.Н., Киселев В.И. // Журнал микробиологии, эпидемиологии и иммунобиологии – 2010 – №3
На днях появилась информация о расследовании дела по «финансированию» иностранными фармкомпаниями ряда руководителей российских медучреждений и медработников. Точнее, речь о «проталкивании» лекарственных средств «за большие деньги». Об этом доложил президенту директор Росфинмониторинга, упомянув о выявлении таких случаев в 30 субъектах и передаче только по одной схеме 500 миллионов. Дело ведут ФСБ и Росфинмониторинг. Правда, конкретные регионы и компании не обозначены.
В конце директор ведомства дословно изрек следующее: «Надо сейчас, особенно в этих условиях, когда санкционное [давление], появление лекарств, и когда нас вынуждают жить по этим правилам, надо пресекать. Мы сейчас с ФСБ разбираемся, постараемся». Сократив все лишнее в путанной речи докладчика, получим: «в условиях санкционного давления надо пресекать появление лекарств, и мы с ФСБ постараемся».
Вероятно, идет процесс не столько «проталкивания» препаратов иностранной фармой, сколько ее выталкивание с российского рынка. Очевидно, в наше смутное время все структуры стараются внести лепту в развитие отечественной промышленности и импортозамещение буквально любой ценой. Однако цена здоровья людей высоковата для подобного пути. Возможно, вскружил голову опыт производства российских бигмаков.
Неужели в самом деле?
Для начала сложно представить описанное в реальном воплощении. Требования современного комплаенса (внутреннего контроля) в фармотрасли куда строже российских законов, в том числе о конфликте интересов. Это сужает деятельность фармы до коридора образовательных мероприятий, аналитики, исследований, благотворительной помощи и подобных активностей.
В 2016 году до России добрались так называемые «солнечные» нормы, согласно которым компании – члены Ассоциации международных фармацевтических производителей (AIPM) обязаны ежегодно раскрывать информацию о платежах в пользу специалистов и организаций здравоохранения. Из года в год фарма исправно публикует отчеты, обозначая по пунктам кому, что, за что и когда. Кроме того, информация о поддержке мероприятий подается в Росздравнадзор, что дает возможность мониторить и контент.
Возможно, именно эти суммы возбудили интерес Росфинмониторинга и ФСБ. А может, пожертвования в виде лекарственных средств лечебным учреждениям. Чем, собственно, не «проталкивавание»? А может, и вовсе простое назначение препаратов пациентам. Остается только гадать, так как фактология в докладе отсутствует; даже неясно, что передано на 500 миллионов – лекарств или денег. А посыл «надо пресекать появление лекарств» свидетельствует о большей близости к Кремлю, чем к здравоохранению и здравомыслию.
За что аборигены съели Кука?
На данном этапе российская медицина едва ли состоятельна без иностранных лекарств. Конечно, российские компании развились за последние годы и сумели, кроме дистрибуции и производства дженериков, наладить выпуск и некоторых оригиналов, однако плевать в иностранный колодец определенно рановато. В онкологии на долю иностранных лекарств уже в 2019 году приходилось порядка 72% от всего объема затрат на закупку, а в 2021 году и по итогам 4 месяцев 2022 года показатель достиг рекордных 83%. Конечно, если считать в упаковках, заметен обратный тренд, однако до полноценного импортозамещения нам еще далеко, особенно учитывая тот факт, что большинство отечественных препаратов зависимо от импортных фармсубстанций. Вливание миллиардов в «Газпром нефть» порождает только фантазии о способности нефтянки производить сырье для фармсубстанций.
Помимо этого, образование врачей все годы стоит на плечах фармкомпаний. Профессиональные конференции, мероприятия и конгрессы проходят при их поддержке, что является мировой нормой и не нарушает требований антикоррупционного законодательства. Последние 20–25 лет российские ученые благодаря фарме получили выход на международные профессиональные площадки: участие в мировых конгрессах и клинических исследованиях, доступ к подпискам на научные журналы, порталы и многое другое, что дало мощнейший толчок к развитию не только отечественной медицины, но и отечественной фармпромышленности. Образовательные программы и издательская деятельность внутри России также все годы щедро спонсируются иностранной фармой, притом в основном производителями оригинальных препаратов. Большинство дженериковых компаний ориентированы больше на бизнес, нежели на развитие профсообщества.
Фарма выполняет огромную работу по аналитике и совершенствованию отрасли, вкладывает колоссальные средства в клинические, молекулярно-генетические исследования и др. Все это позволяет нашим пациентам получить ранний доступ к современной терапии и, соответственно, повышает качество медицинской помощи.
Уход западной фармы приведет к деградации медицинского образования и сузит возможности пациентов. Поэтому информация о расследовании ФСБ, конечно, вызывает интерес – но больше тревогу, как любая первая серия плохого детектива.
Все не так, ребята
Ну и наконец, механизмы работы и продвижения препаратов иностранными и отечественными фармкомпаниями в целом идентичны, поэтому не совсем ясно, чем «проталкивание» одних отличается от «проталкивания» других. Разве что отечественному производителю дано в этом больше преимуществ и возможностей.
К примеру, введено правило «второй лишний» (победа в тендерах достается поставщику препарата, производство которого организовано в одной из стран ЕАЭС), которое с 2024 года планируется распространить на все стратегически значимые препараты. В пилот уже попали 4 онкопрепарата: бевацизумаб, иматиниб, ритуксимаб и трастузумаб.
Кроме того, в марте принят закон о расширении границ допустимого снятия патентной защиты, отменена выплата компенсаций правообладателям из «недружественных» стран, т. е. всем, а в мае Правительство РФ даже допустило экспорт лекарств, произведенных без согласия патентообладателя.
Глава Минпромторга Денис Мантуров на удивление доступно прокомментировал новые нормы: «В случае отказа поставлять в РФ иностранные лекарства может быть применена процедура принудительного лицензирования, и Россия будет производить их собственными силами».
Иначе говоря, теперь уход с рынка грозит потерей патента, притом даже без права получения роялти. Все это принято рассматривать как механизм импортозамещения. Но ряд мер выходит за рамки международного соглашения по торговым аспектам прав интеллектуальной собственности (ТРИПС), носит избыточный характер и может привести к увеличению доли контрафактных и некачественных товаров.
Будет ли когда-нибудь у мартышки дом?
Бесспорно, отечественному производителю нужно дать зеленый свет, однако для этого совершенно не обязательно ломать чужой светофор. В наше время это может на раз перекрыть все дорожное движение, что лишит пациентов достойного лекобеспечения, а врачей – возможности учиться и развиваться.
И без того иностранные фармкомпании еще весной прекратили клинические исследования препаратов и заморозили большую часть активностей. Однако жесткие санкции не коснулись медицины, и поставки большинства оригинальных препаратов сохранены, несмотря на сложности логистики и фиксацию старых цен на ЖНВЛП. Поэтому неясно, о каких условиях санкционного давления доложено президенту, и уж тем более неясно – кто кого вынуждает «жить по этим правилам».
Хочется верить, что уважаемые знатоки отличат market access (доступ на рынок) от «проталкивания», а импортозамещение от зачищения, ведь дезинформация первого лица, как известно, может привести к плачевным последствиям. Никто не мешает нашей фарме органично, спокойно и без «хакерских атак» встраиваться в современную фарминдустрию, хотя, как ни крути, это займет годы, несмотря на придворные клятвы о «достигнуть, перестигнуть, первыми в мире и без раскачки».
5/07/2022, 16:21
Комментарий к публикации:
Медвестник
Инфекция, вызванная онкогенными вирусами, является причиной 15,4% заболеваний раком по всей земле. Первый онкогенный вирус, который был идентифицирован — это куриный вирус саркомы Рауса в 1911 году. Десятилетиями позже были обнаружены серии других онкогенных вирусов, в том числе вирус папилломы Шопа (вирус папилломы кроличьего хвоста), вирус опухоли молочной железы мыши, аденовирус, вирус SV40 (обезьяний вирус sv40). Теория опосредованного вирусом онкогенеза в итоге была экспериментально продемонстрирована в 1976 году Гарольдом Вармусом и Майклом Бишопом путем превращения инфицированных клеток в опухолевые вирусом саркомы (ген v-src вызывает образование опухоли после захвата протоонкогена человеческой клетки в результате трансдукции).
Несмотря на то, что онкогенные вирусы нашли в исследованиях онкогенной активности животных клеток, они были не в состоянии преобразовать человеческие клетки. Теория вирусного онкогенеза в человеческой клетке оставалась спорной до 1965 года, когда вирус Эпштейн-Барр (EBV) был обнаружен в клетках лимфомы Беркитта. В ходе последующих исследований, в том числе выделении Т-лимфотропного вируса человека (HTLV) из клеток Т-клеточной лимфомы и выявлении роли папилломовирусов человека с высокой онкогенной активностью в развитии рака шейки матки, был определен путь для понятия человеческих онкогенных вирусов. Обнаружение связи между герпес-вирусом и саркомой Капоши (KSHV) и лимфомой и между полиомавирусом клеток Меркеля (MCV) и карциномой клеток Меркеля (MCC) подчеркнуло возможность открытия еще большего количества онкогенных вирусов с помощью современных технологий. Далее каждый вирус будет рассмотрен отдельно.
Вирус Эпштейн-Барр
Вирус Эпштейн-Барр (ВЭБ, EBV) — ДНК-содержащий вирус, который преимущественно поражает B-лимфоциты, также является митогеном для них; вызывает лимфопролиферативные болезни (лимфома Беркитта, носоглоточная карцинома, NK-клеточная лейкемия, лимфома Ходжкина и т.д.), а также инфекционный мононуклеоз. Вирионы вируса были обнаружены при электронной микроскопии биоптата лимфомы Беркитта в начале 1964 года Энтони Эпштейном и Ивонной Барр.
Строение. ВЭБ имеет вирусный капсидный антиген (VCA), ядерные антигены-EBNAs 1, 2, 3, 3a, 3b, 3c; латентные мембранные протеины (LMPs) 1, 2 и две маленькие Эпштейна-Барр-кодируемые РНК (EBER) молекулы — EBER1 и EBER2. EBNAs и LMPs являются ДНК-связывающими белками, считающимися необходимыми для развития инфекции и фиксации.
Рисунок 1. Строение ВЭБ и связанный с этим механизм развития инфекции
Промотор репликации плазмидного вектора показан оранжевым. Короткие толстые зеленые стрелки представляют экзоны, кодирующие латентные белки: (EBNAs 1, 2, 3A, 3B and 3C, and EBNA‑LP, LMPs 1, 2A and 2B, BHRF1,BARF1). Короткие голубые стрелки сверху представляют наиболее транскрибириуемые полиаденилированные ВЭБ-кодируемые РНК (EBER1, EBER2). Средняя длинная зеленая линия представляет транскрипцию ВЭБ при 3-ем типе латентности, в которой белки EBNA транскрибированы с промотора Ср или Wp. Различные EBNA кодированы индивидуальными мРНК, которые сгенерированы различным сплайсингом одного и того же длинного первичного транскрипта. Внутренняя красная линия представляет транскрипт EBNA1, который берет начало от промотора Qp при 1 и 2 типе латентности.
Функции LMP1:
- необходим для трансформации В-лимфоцитов;
- функционирует как конститутивный активатор рецептора ФНО и имеет сходство с CD-40 рецептором;
- активирует сигнальные пути, которые делают вклад в онкогенный эффект.
В зависимости от набора экспрессируемых вирусных генов в пораженных клетках выделяют три типа латентности (I, II и III тип), характерные для различных видов лимфом: I тип подразумевает избирательную экспрессию EBNA-1 при ВЭБ-положительной лимфоме Беркитта; II тип заключается в экспрессии EBNA-1, LMP-1 и LMP-2 и является отличительным признаком ВЭБ-положительной ходжкинской лимфомы, периферических T/NK-клеточных лимфом; латентность III типа, характеризуемая экспрессией всего набора из девяти латентных белков ВЭБ, наблюдается при лимфопролиферативных поражениях, возникающих у пациентов с тяжелым иммунодефицитом (после трансплантации паренхиматозных органов или стволовых клеток, ВИЧ-инфекции). Тип латентности определяет восприимчивость инфицированных клеток к различным иммунотерапевтическим тактикам. Индуцированные ВЭБ злокачественные новообразования связаны с экспрессией латентных генов. У большинства иммунокомпетентных носителей ВЭБ вирус не индуцирует опухолевый процесс. Новообразования развиваются при комплексном взаимодействии ВЭБ, иммуногенетических факторов, факторов внешней среды (паразитарных инфекций — чаще, малярии, недоедании, потреблении пищи, содержащей канцерогены) и иммунодефицита (ВИЧ-инфекция, трансплантация).
Папилломавирусы человека
Описано около 200 папилломавирусов. Вирусы передаются при контактах через микротравмы кожи и слизистых оболочек, а также половым путем. Папилломавирусы человека вызывают доброкачественные кожные, генитальные, оральные и конъюнктивальные папилломы; индуцируют пролиферацию эпителия, обладают онкогенным потенциалом. С папилломавирусом, особенно ПВЧ-5 и ПВЧ-8, тесно связано развитие немеланомных разновидностей рака кожи. Различают низкоонкогенные папилломавирусы, вызывающие бородавки, которые не малигнизируются, и высокоонкогенные, способные вызвать рак шейки матки, — ПВЧ-16, 18, 31, 33, 35, 45, 51, 52, 58.
Строение. Капсид икосаэдрический, состоит из двух капсидных белков (L1-L2), формирующих 72 пентамера. Геном — двунитевая циркулярная ДНК; имеет в зависимости от вируса восемь ранних генов (E1-E8) и два поздних гена (L1-L2). Гены E6-E7 обладают онкогенной активностью.
Патогенез. В целом, для развития продуктивного поражения ВПЧ (высокого или низкого риска) требуется, чтобы вирус имел доступ к эпителию базального слоя как только эпителиальный барьер был подвержен риску. Папилломавирусы должны инфицировать делящуюся клетку, чтобы стать признанными как малое количество копий ядерной эписомы, и для развития стойкого поражения первичная инфицированная клетка, вероятно, должна быть похожа на долгоживующую эпителиальную стволовую клетку или похожую на нее. Кроме того, связанные с заживлением ран изменения в местном микроокружении, включая увеличение количества факторов роста, могут играть ключевую роль в создании резервуара инфекции в базальном слое. Способность ВПЧ инфицировать, и реплицироваться, и управлять прогрессированием рака зависит от функции вирусного белка, положении в эпителии, где эти белки экспрессируются. Как только инфицированные базальные клетки поделились и в конечном итоге вошли в парабазальный слой, они начинают проходить программу экспрессии генов, которая связана с дифференциацией. Амплификация вирусного генома обычно происходит в срединно-эпителиальных слоях, тогда как сбор и выход вируса происходит вблизи наружной поверхности эпителия.
Несмотря на то, что эффективная амплификация генома требует комбинированного действия множественных продуктов вирусного гена, включая E6, E7, E2 и кодированную вирусом геликазы E1, поддержание репликации в базальном слое эпителия может зависеть от факторов репликации клетки хозяина. Программа, зависящая от дифференциации, которая происходит в надбазальных слоях эпителиальной клетки, включает как временные изменения в активности промотора, так и изменения в шаблонах сплайсинга мРНК, которые облегчают производство различных продуктов вирусных генов на разных стадиях во время программы дифференциации. Функция вирусного белка далее регулируется посттрансляционной модификацией, включая фосфорилирование и протеолитическое деление клетки.
Рисунок 2. Патогенез продуктивного поражения ВПЧ
Cчитается, что прекращение регулирования гена экспрессии ВПЧ высокого риска зависит от конкретных характеристик базальной клетки, которую заражает вирус, а также от восприимчивости этой зараженной клетки к внешним стимулам, таким как гормоны и факторы роста. Большинство видов рака шейки матки возникает в зоне трансформации и слизистой оболочки шейки матки; область шейки матки, состоящая первоначально из столбчатого эпителия, затем подвергается метаплазии. Предполагается, что стратифицированные (разделенные) слои внешней шейки матки поддерживаются «обычными» эпителиальными стволовыми клетками, которые расположены в базальном слое. Природа этих клеток не установлена. Напротив, стратифицированные слои зоны трансформации и один слой столбчатых ячеек — это линия слизистой оболочки шейки матки, как полагают, поддерживается резервными клетками шейки матки. Хотя резервные клетки достаточно обильны в местах метаплазии, недавние исследования дополнительно предположили, что стволоподобные клетки второго типа кубического вида, которые расположены более точно в стыке переходной зоны (squamocolumnar junction), тоже проявляют резервную функцию.
Герпесвирус, ассоциированный с саркомой Капоши
KSHV, или человеческий герпесвирус 8, был обнаружен в 1994 году как член семейства гамма-герпеса человека, присоединившись к ВЭБ. Инфекция иммунокомпрометированных индивидуумов с KSHV была связана с развитием саркомы Капоши, полученной из эндотелиальных клеток, и по меньшей мере двумя B-лимфоцит лимфопролиферативными заболеваниями: первичная выпотная лимфома и многоцентричная болезнь Кастлмана. Однако изучение патогенеза и онкогенеза KSHV затруднено отсутствием значимой модели животных и восприимчивой клеточной культуры.
Онкогенное действие. Две иммортализованные клеточные линии, KS Y-1 и SLK, когда-то использовались для исследований KS и KSHV, но в KS Y-1 были также обнаружены клетки линии рака мочевого пузыря T 24, что затруднило дальнейшую работу. Первичные эмбриональные метанефрические мезенхимальные клетки-предшественники почек крысы восприимчивы к инфекции и трансформации KSHV, но из них распространяются ограниченное количество инфекционных вирионов. Линии B-клеток, полученные из первичной выпотной лимфомы, обычно заражаются KSHV на латентной стадии и могут быть индуцированы для получения малого количества вирионов KSHV, но первичные B-лимфоциты из периферической крови или тонзиллярной ткани являются устойчивыми к инфекции KSHV, и для их инфицирования может потребоваться совместный рост с KSHV-позитивными клетками.
KSHV кодирует несколько важных белков, которые обладают некоторой онкогенной активностью для индуцирования пролиферации клеток, иммортализации, трансформации и передачи сигналов; производства цитокинов; иммунного контроля; антиапоптозной активности; и ангиогенеза. К ним относятся вирусные латентные белки, латентный ассоциированный ядерный антиген (LANA), vFLIP (FADD (Fas-ассоциированный белок с доменом смерти), подобный ферменту, ингибирующему синтез интерферона или ингибирующему белок каспазы 8 (FLICE)), vCyclin и вирусные литические белки G-белкового рецептора (vGPCR), интерферон-регуляторный фактор 1 (vIRF-1) и K1. Хотя истинную онкогенную природу каждого белка еще предстоит определить, накопление доказательств указывает на то, что каждый из них вносит свой вклад в онкогенез KSHV. Таким образом, полный спектр вызванной KSHV злокачественности может потребовать, чтобы несколько онкогенных продуктов работали вместе в присутствии клеток хозяев и экологических факторов. Например, как LANA, так и vIRF-1 нацелены на клеточный опухолевый супрессор p53. LANA также ингибирует pRB и PP2A.vCyclin, активатор CDK4 6,198, подавляет p27kip1, ингибитор CDK199 и вызывает реакцию на задержку старения G1, результаты от гиперактивации NF-κB. vFLIP и K1 активируют путь сигнала NF-κB для предотвращения апоптоза B-клеток. vGPCR и K1 влияют на сигнальные пути AKT и NF-κB и способствуют ангиопролиферативному и воспалительному поражению саркомой Капоши.
Т-лимфотропный вирус человека (HTLV)
T-лимфотропный вирус человека (HTLV) относится к семейству ретровирусов, является возбудителем T-клеточного лимфолейкоза взрослых. Вирус впервые был изолирован в 1980 году от больного Т-лимфомой.
Геном. Gag, Pol и Env являются вирусными структурными белками, другие — вирусными регуляторными/вспомогательными белками. За исключением гена hbz, который кодируется минус-цепью провирусного генома HTLV из 3′-LTR, все остальные гены кодируются плюсовой нитью по направлению 5′-LTR. Следует отметить, что 5′-LTR часто удаляется или метилируется по мере прогрессирования заболевания. Кроме того, на поздних стадиях лейкемиогенеза в гене tax часто возникают нонсенс- или миссенс-мутации. Хотя белок tax и ген HBZ индуцируют опухоли у трансгенных мышей, а p12 проявляет слабую онкогенную активность, ни один из вирусных белков/генов, кроме tax, не требуется для опосредованного HTLV-1 опухолеобразования. Продукт tax гена действует на терминальные повторы LTR, стимулируя синтез вирусной иРНК, а также образование рецепторов IL-2 на поверхности зараженной клетки.
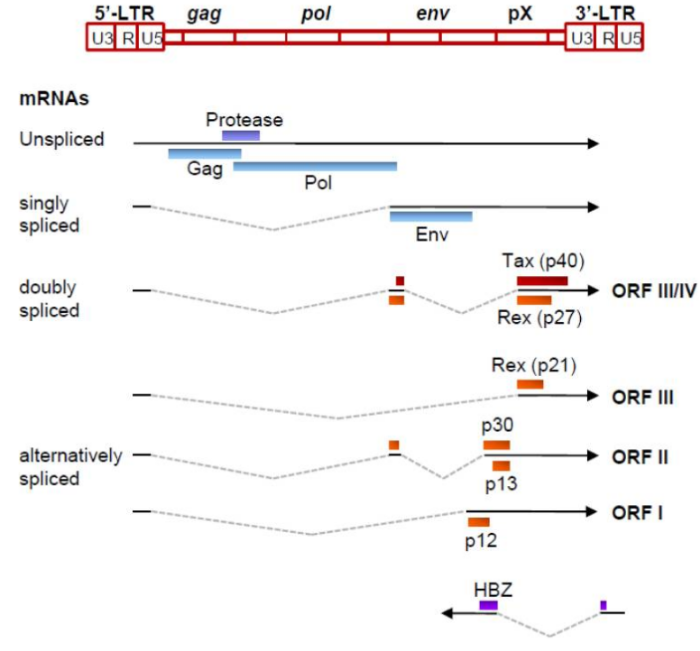
Рисунок 4. Клеточные пути вирусного онкобелка tax
Патогенез. Проникновение HTLV-1 в клетку человека охарактеризовывает начало выживания и репликации вируса. HTLV-1 связывается с рецептором клеток, имеющих необходимый антиген, что инициирует процесс инвазии. Рецепторный комплекс состоит из транспортера глюкозы (GLUT1), гепаринсульфат протеогликана (HSPG) и рецептора VEGF-165 нейропилина-1 (NRP-1). HTLV-1 взаимодействует с HSPG. Процесс слияния происходит через комбинацию GLUT1 с HSPG/NRP-1, после чего ядро, содержащее вирусную РНК, доставляется в цитоплазму клеток-мишеней. После обратной транскрипции HTLV-1 встраивает свой геном в генома хозяина, чтобы сформировать провирус, окруженный двумя LTR на 5′ и 3′ концах. Затем провирус транскрибируется и кодирует структурные, регуляторные и вспомогательные белки. Впоследствии вирусные геномные РНК и Gag, Env и Gag-Pol белки переносятся в плазматическую мембрану, чтобы начать собираться в зрелую вирусную частицу.
Вирусы гепатита
Вирус гепатита В (HBV) и вирус гепатита С (HCV) представляют собой несвязанные вирусы, имеющие тропность к гепатоцитам и реплицирующиеся в них. Около 2 миллиардов человек инфицированы HBV, и более 350 миллионов человек становятся хроническими носителями. Только 5-10% взрослых, которые приобретают инфекцию, становятся хроническими носителями, у 30% развиваются прогрессирующие хронические заболевания печени: гепатит, фиброз, цирроз и, наконец, гепатоцеллюлярная карцинома (HCC).
Геном. Геном вируса гепатита B представляет собой одну двухцепочечную кольцевую ДНК длиной около 3200 нуклеотидов (длина генома различна у разных изолятов). Одна из цепей («плюс-цепь») ДНК короче другой (ее длина составляет 1700-2800 нуклеотидов). Вторая цепь тоже не является замкнутой и к ее 5’-концу ковалентно присоединена молекула полимеразы (P). В геноме вируса найдено 4 гена: S, С, Р, X, кодирующих соответственно HBsAg, HBcAg, полимеразу и белок-регулятор экспрессии генов. Кроме того, там есть регуляторные последовательности ДНК, ответственные за синтез белков и репликацию вируса. Гены частично перекрываются, что обусловливает малый размер генома.
Патогенез. HCC, индуцированная посредством HBV и HCV, развивается в области воспаления и регенерации, что является результатом хронического повреждения печени, а это в свою очередь указывает на то, что патогенез HCC иммунно-опосредован. Эти вирусы постоянно реплицируются в культуре клеток без явных повреждений и смерти клеток, подразумевая, что они являются не цитопатическими. Постоянная репликация вируса является фактором риска для образования HCC, потому что воспаление часто приводит к длительным хроническим заболеваниям печени CLD без выведения вируса. В этом контексте HBV и HCV генерируют белки, подавляющие иммунитет, который должен контролировать хронические инфекции. HBV- и HCV-кодированные белки изменяют экспрессию гена хозяина и клеточный фенотип, что является признаком рака. Эти изменения способствуют независимой от фактора роста пролиферации, сопротивлению к ингибированию роста, инвазии тканей и метастазированию, ангиогенезу, перепрограммированию энергетического метаболизма и устойчивости к апоптозу. Хроническое воспаление также способствует генетической нестабильности в клетках опухоли. Вклад HBV в развитие HCC включает в себя экспрессию гена гепатита Bx (HBx) и, возможно, усеченные пре-S или S-полипептиды карбоксимицина; основной белок и неструктурные (NS) белки NS3 и NS5A HCV способствуют онкогенной трансформации. Изменения в экспрессии гена хозяина, которые способствуют возникновению опухолевого генеза, также, похоже, поддерживают репликацию вируса и/или защиты вирусных гепатоцитов от иммунного опосредованного повреждения и разрушения.
Рисунок 5. Роль иммунитета в развитии исходов острых инфекций
Иммунитет играет важную роль в исходе острых инфекций. Быстрый, сильный и мультиспецифичный ответ против многих белков вирусов гепатита В (HBV) и гепатита C (HCV) приводит к острой инфекции, устраняемой клеткой-хозяином.
Источники
-
Oncogenes and RNA splicing of human tumor viruses. Masahiko Ajiro & Zhi-Ming Zheng.(September 2014)
-
Carcinogenic human papillomavirus infection. Mark Schiffman, John Doorbar, Nicolas Wentzensen, Silvia de Sanjosé, Carole Fakhry, Bradley J. Monk, Margaret A. Stanley & Silvia Franceschi.( December 2016)
-
Human T-cell lymphotropic virus type 1 and its oncogenesis Lan-lan ZHANG, Jing-yun WEI, Long WANG, Shi-le HUANG, Ji-Long CHEN.(2017)
-
Immunoblastic Lymphoma in Persons with AIDS-Associated Kaposi’s Sarcoma: a Role for Kaposi’s Sarcoma–Associated Herpesvirus. Eric A Engels M.D., Stefania Pittaluga M.D., Denise Whitby Ph.D., Charles Rabkin M.D., Yoshiyasu Aoki M.D., Elaine S Jaffe M.D. & James J Goedert M.D.(may 2003)
-
Kaposi’s sarcoma-associated herpesvirus ORF34 is essential for late gene expression and virus production. Mayu Nishimura, Tadashi Watanabe, Syota Yagi, Takahiro Yamanaka & Masahiro Fujimuro( march 2017)
-
Саркома Капоши: патогенез и основы терапии Н.С. Потекаев, Г.А. Паньшин, Н.П. Теплюк, Н.С. Арсентьев, Е.Ю.,Вертиева,Г.И. Махов, Е.С. Сизова, В.С. Пауков, М.Г. Карташова. (март 2013)
-
Human T-Cell Lymphotropic Virus: A Model of NF-κB-Associated Tumorigenesis. Zhaoxia Qu and Gutian Xiao(June 2011)
-
Immune responses and immunopathology in acute and chronic viral hepatitis. Eui-Cheol Shin, Pil Soo Sung & Su-Hyung Park(July 2016)
-
Pathogenic mechanisms in HBV and HCV-associated hepatocellular carcinoma. Alla Arzumanyan, Helena M. G. P. V. Reis and Mark A. Feitelson(February 2013) Epstein–Barr virus: more than 50 years old and still providing surprises. Lawrence S. Young, Lee Fah Yap & Paul G. Murray( September 2016)
-
Медицинская микробиология, вирусология и иммунология. В.В. Зверев, А. С. Быков.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.