Сегодня заболевания сердечно-сосудистой системы входят в первую тройку причин смертности, а инфаркт миокарда является самой опасной для человека патологией сердца. Несмотря на то, что во многих случаях это серьезное заболевание можно предотвратить, люди часто беспечно относятся к себе, забывая не только о здоровом образе жизни, но даже игнорируя характерные для кардиопатологии сигналы организма. В Тюменском кардиологическом научном центре первыми пациентов, у которых случился острый инфаркт миокарда, встречают врачи анестезиологи-реаниматологи. Они оценивают их состояние, лечат, сопровождают на операцию, и знают, как тяжело переносится сердечный приступ. Мы попросили анестезиолога-реаниматолога Тюменского кардиоцентра, кандидата медицинских наук Юлию Крошкину рассказать о том, что такое инфаркт, как распознать его первые симптомы и почему при боли за грудиной нужно срочно вызывать скорую помощь.
Инфаркт миокарда (сердечный приступ) – одна из клинических форм ишемической болезни сердца, протекающая с развитием ишемического некроза участка миокарда, обусловленного абсолютной или относительной недостаточностью его кровоснабжения.
Юлия Сергеевна, в каком состоянии попадают в реанимацию пациенты?
Как правило, в реанимацию попадают пациенты с инфарктом миокарда с подъемом сегмента ST – это самая тяжелая форма заболевания, поэтому у них тяжелое или крайней степени тяжести состояние. Таких пациентов чаще всего привозят на скорой помощи. Как врачам сориентироваться, что это именно инфаркт миокарда и пациента нужно везти в кардиоцентр? Прежде всего, по изменениям в кардиограмме, характерным для сердечного приступа, а также соответствующим клиническим проявлениям – боли за грудиной давящего, сжимающего характера, иногда отдающие в левую руку. Когда человек поступает в кардиоцентр, у него берут анализы, в том числе маркеры некроза миокарда. Есть определенные показатели крови, которые показывают, случился ли инфаркт. Всем пациентам делают УЗИ сердца и в экстренном порядке отправляют на коронароангиографию (прим. Процедура исследования сосудов сердца), где в условиях операционной определяется дальнейшая тактика ведения пациента.
Многое зависит от скорой помощи – насколько быстро они доехали до пациента и привезли его в больницу. Очень важен период времени от момента инфаркта до восстановления кровотока в сердце. Сердце, как и все органы, кровоснабжается сетью артерий. И когда какая-то из них по любой причине закрывается, то прекращается кровоснабжение участка, к которому она подходила. Сначала появляется ишемия, потом этот участок отмирает – происходит некроз, а в дальнейшем появляется рубец. Основная задача – восстановить кровоток в поврежденной артерии, либо медикаментозно, либо с помощью операции. Чем быстрее он восстановится, тем лучше – меньше будет зона некроза, меньше осложнений, пациент будет лучше себя чувствовать. Поэтому на этапе скорой помощи зависит, как быстро медики приехали, как быстро сориентировались, что у человека инфаркт, как быстро его доставили в тот центр, где смогут прооперировать. В Тюмени до недавнего времени это были Тюменский кардиоцентр и Тюменская областная больница №1. Сейчас еще добавился госпиталь «Мать и дитя». В догоспитальном этапе считается, что с момента первого медицинского контакта с пациентом до постановки диагноза должно пройти не более 10 минут. До момента госпитализации должно пройти не более 120 минут.
А что в случае сердечного приступа зависит от самого пациента?
Нередко человек не может адекватно оценить свое состояние и ждет «а может и так пройдет».
Не всегда все зависит от врачей, к сожалению. Основная беда для грамотных людей – это Интернет. Они сами себе ставят диагноз, сами начинают лечиться. Очень важно – как только появилась боль за грудиной, надо сразу вызывать скорую помощь. Пусть это окажется остеохондроз или какая-то другая болезнь, которая не приводит к смерти. Но лишний раз лучше перестраховаться и вызвать скорую помощь, чем пропустить инфаркт. Такие пациенты у нас не редкость. Оказывается, первые боли возникли, например, 30 числа, потом стало вроде бы полегче, потом человек заболел повторно через неделю. А по факту выявляется, что инфаркт случился 30-го, а 8-го следующего месяца — уже рецидив. Таких пациентов потом намного сложнее лечить, у них больше осложнений. В поликлинике запись может быть через день, на завтра назначат кардиограмму, а счет может идти на минуты. В приемном отделении, куда пациента привезет «скорая», сделают все сразу. Врачи посмотрят и решат, надо ли госпитализировать больного. На самом деле, много пациентов, которые обращаются поздно. Терпят до последнего, боятся идти на больничный.
Чаще инфаркты случаются у мужчин или женщин?
К своему здоровью более ответственно все-таки относятся женщины. Мужчины зачастую затягивают с визитом к врачу. Если говорить о группах риска, то мужчины чаще болеют инфарктом миокарда. Женщины с инфарктом миокарда, особенно в молодом возрасте, — нонсенс. Женщины появляются в группе риска в постмепнопаузальный период. Пока они менструируют, здоровы, у них нет сопутствующих заболеваний крови, они не пьют препараты, повышающие свертываемость крови, то они не в зоне риска. Кстати, в зоне риска находятся женщины, принимающие оральные контрацептивы, которые увеличивают свертываемость крови. Поэтому, когда поступает молодая пациентка с инфарктом миокарда, то первое, что мы спрашиваем – какие лекарства она принимает. Также мужчины больше курят и больше алкоголизируются, чем женщины, и тяжелее переносят стрессы. Это тоже увеличивает риск инфаркта. По статистике, после первого инфаркта мало кто бросает курить, а после второго бросают процентов 80. Потому что повторные инфаркты протекают гораздо тяжелее. Сердце уже дискредитировано, на нем есть рубец, оно хуже сокращается. У женщин в молодом возрасте препятствуют тромбообразованию еще и женские половые гормоны. Пока яичники нормально функционируют, то риск инфаркта минимальный.
На что, помимо боли, необходимо обратить внимание, чтобы вовремя заметить инфаркт и обратиться к врачу?
Локализации инфаркта бывают разные – передние, задние. Нижние инфаркты, бывает, что проявляются изжогой. Человек думает, что у него нарушено пищеварение. Иногда бывает, что на первое место выступает одышка. Но чаще всего все-таки на первом плане будет боль, которая может отдавать в левую половину тела – шею, руку.
А можно ли пропустить инфаркт, перенести его на ногах?
Человек может находиться в состоянии стресса и не понимать, что с ним происходит что-то серьезное. Это характерно для мелкоочаговых инфарктов, когда клиника смазанная на фоне ОРВИ, стресса. Человек говорит, что у него никогда не было инфаркта, а на кардиограмме рубец. В диагнозе мы ставим «постинфарктный кардиосклероз неуточненной давности».
Сколько инфарктов способно перенести сердце человека?
Максимум, мне кажется, пять инфарктов. Потом сердце превращается в вялый мешочек, который плохо сокращается. Каждый последующий инфаркт переносится хуже, чем предыдущий.
Как долго пациент восстанавливается после инфаркта?
У нас в реанимации все пациенты лежат с инфарктами миокарда. Казалось бы, диагноз у всех одинаковый, но болезнь протекает по-разному, у каждого есть какая-то особенность. В целом, если больной поступил без осложнений, то он около трех суток находится в реанимации, около недели – в отделении неотложной кардиологии и потом на амбулаторном этапе – около двух месяцев. Нередко думают, что мы подлечим за два дня и отпустим. Но лечение требует времени.
Инфарктов сегодня становится больше или меньше?
Цифры стабильные. Может быть, это удивительно, но примерно всегда одинаковые проценты заболевших и осложнений.
Расскажите о наиболее интересных случаях в вашей практике?
Каждый по-своему уникален. Был пациент, ведущий спортивный образ жизни, — катался на лыжах, упал на лыжне, потерял сознание. Его увидел в лесу другой лыжник, пока транспортировали в город – инфаркт. Вроде бы человек прекрасно себя чувствовал, никогда ничем не болел… Также к нам одновременно с инфарктами миокарда попали два анестезиолога из другой больницы. Сами себя лечили, думали, что пройдет, терпели и ходили на работу.
Что нужно делать, чтобы предотвратить инфаркт миокарда?
Разговариваем с родственниками пациента с инфарктом, они недоумевают: «Как так, он не пил, не курил, ел нормальную пищу, и вдруг случился инфаркт миокарда». Но такое состояние вдруг не случается. Основная причина развития инфаркта миокарда – это отложение холестерина в коронарных артериях – атеросклероз. Процесс роста атеросклеротической бляшки не происходит внезапно, а развивается годами. Особенно так происходит у возрастных пациентов.
Не пить, не курить, следить за питанием, за массой тела, измерять артериальное давление. У гипертоников риск возникновения инфаркта в разы выше, чем у людей с нормальным давлением. Также нужно следить за холестерином – хотя бы раз в год проходить обследование у терапевта, записывать кардиограмму и сдавать липидный спектр. Высоким холестерин бывает и у худеньких, и у активных людей. Причина либо в питании, либо в генетической предрасположенности. Для нормализации состояния часто достаточно соблюдать диету. Обязательно нужно лечить и контролировать сопутствующие заболевания, особенно сахарный диабет. Но инфаркт миокарда – это не всегда атеросклероз. Случается, что на фоне ОРВИ на чистых сосудах развилось воспаление, возник отек. На фоне стресса происходит спазм артерии.
Какую роль в профилактике инфарктов играет активный образ жизни?
Здоровый образ жизни, активность – это профилактика лишнего веса. Можно просто ходить, подниматься пешком по лестнице. После инфаркта у нас есть специальная система реабилитации. Всех пациентов осматривают, консультируют врачи по лечебной физкультуре. С нашими пациентами занимаются уже через несколько дней после инфаркта – начинают с минимальных движений, объем и продолжительность которых со временем увеличивается.
УДК 616.127-005.8-07
М.М. МАНГУШЕВА1, С.Д. МАЯНСКАЯ1, Г.Г. ИСХАКОВА2
1Казанский государственный медицинский университет МЗ РФ, г. Казань 2Госпиталь для ветеранов войн, г. Казань
К вопросу о трудностях ЭКГ диагностики инфаркта миокарда
Контактная информация:
Маянская Светлана Дмитриевна — доктор медицинских наук, профессор кафедры госпитальной терапии Адрес: 420012, г. Казань, ул. Бутлерова, д. 49, тел. +7-905-316-99-66, e-mail: Smayanskaya@mail.ru
Проблемы диагностики острого инфаркта миокарда обусловлены запаздыванием изменений на ЭКГ, наличием неспецифических признаков, характерных для многих состояний, не связанных с ИБС. В статье представлены наиболее частые трудности ЭКГ интерпретации инфаркта миокарда. Они могут быть вариантом нормальной ЭКГ, отражать некоронарогенные изменения миокарда, служить отражением острой коронарной патологии, требующей неотложной терапии или быть результатом вторичных изменений при блокадах ножек пучка Гиса, синдроме WPW, гипертрофии ЛЖ и т.д., а также связаны с особенностями локализации ИМ или рецидивирующим его течением. Отмечено, что на ранних стадиях заболевания при соответствующей клинической картине заподозрить ИМ по ЭКГ помогают: появление как отрицательной, так и положительной динамики по сравнению с предыдущими ЭКГ высоких заостренных зубцов Т, реципрокных изменений, нарушений ритма проводимости; регистрация дополнительных отведений ЭКГ, а также длительное мониторирование ЭКГ при ПБЛНПГ или синдроме предвозбуждения желудочков. При затруднении интерпретации необходимо учитывать данные клинической картины и дополнительных методов диагностики.
Ключевые слова: ЭКГ, инфаркт миокарда, элевация сегмента ST, депрессия сегмента ST, инфарктоподобные изменения, трудности интерпретации ЭКГ.
DOI: 10.32000/2072-1757-2019-2-15-20
(Для цитирования: Мангушева М.М., Маянская С.Д., Исхакова Г.Г. К вопросу о трудностях ЭКГ диагностики инфаркта миокарда. Практическая медицина. 2019. Том 17, № 2, C. 15-20)
M.M. MANGUSHEVA1, S.D. MAYANSKAYA1, G.G. ISKHAKOVA2
1Kazan State Medical University, Kazan
2Hospital for War Veterans of the city of Kazan, Kazan
The question of the difficulties of ECG diagnosis of myocardial infarction
Contact details:
Mayanskaya S.D. — D. Sc. (medicine), Professor of the Department of Hospital Therapy
Address: 49 Butlerova St., Kazan, Russian Federation, 420012, tel. +7-905-316-99-66, e-mail: Smayanskaya@mail.ru
The problems of diagnosing acute myocardial infarction (MI) are due to delay in ECG late changes, presence of non-specific signs characteristic of many conditions that are not associated with ischemic heart disease (IHD). The article presents the most frequent difficulties of ECG interpretation of myocardial infarction. They can be a variant of a normal ECG, reflect noncoronary myocardial changes, serve as a reflection of acute coronary pathology requiring emergency treatment, or be the result of secondary changes in blockade of the His bundle branch, WPW syndrome, LV hypertrophy, etc., as well as associated with localization of MI or its recurrent course. It is noted that in the early stages of the disease, with an appropriate clinical picture, it is possible to suspect IM on ECG: the appearance of both negative and positive dynamics compared with previous ECG, high pointed T teeth, reciprocal changes, conduction rhythm disturbances; registration of additional ECG leads, as well as long-
term monitoring of ECG with total block of the His bundle branch or ventricular preexposure syndrome. In case of difficulty of interpretation, it is necessary to take into account the data of the clinical picture and additional diagnostic methods.
Key words: ECG, myocardial infarction, STsegment elevation, ST segment depression, infarction-like changes, difficulties in ECG interpretation.
(For citation: Manusheva M.M., Mayanskaya S.D., Iskhakova G.G. The question of the difficulties of ECG diagnosis of myocardial infarction. Practical medicine. 2019. Vol. 17, no. 2, P. 15-20)
Электрокардиография (ЭКГ), безусловно, является самым изученным и наиболее точным методом диагностики инфаркта миокарда (ИМ). Однако, из-за возникающих сложностей в интерпретации ЭКГ, врача на этом пути часто подстерегают ошибки, которые избежать бывает очень непросто. Это может быть обусловлено как большим разнообразием и особенностями самого нарушения коронарного кровообращения, так и тем, что изменения сегмента ST и зубца Т не являются специфическими и могут отражать целый ряд различных патологических состояний.
При всем этом существует диапазон допустимых показателей девиаций сегмента ST ниже и выше изолинии. Так, его депрессия до 0,5 мм или эле-вация менее 1 мм допустимы в стандартных отведениях. Для отведений V^V2 допускается элевация сегмента ST до 3 мм, а для V-6 — до 2 мм [1].
Трудности интерпретации ЭКГ-изменений при ИМ прежде всего могут быть связаны с тем, что признаки острого нарушения коронарного кровообращения на ЭКГ зачастую могут запаздывать и появиться через 2, а то и 7 дней от начала заболевания [2].
Запаздывание развития ЭКГ-изменений по отношению к клинической симптоматике характерно для многих пациентов, но чаще для лиц старшей возрастной группы. Иногда окончательный диагноз можно установить лишь при условии динамического наблюдения ЭКГ проявлений и оценки биомаркеров повреждения миокарда.
В свое время Н.А. Мазур (1985) выделил 5 вариантов изменений ЭКГ в течение первого часа развития ИМ: 1) подъем сегмента ST с патологическим зубцом Q или без него или 2) депрессия сегмента ST, обращенного выпуклостью в сторону смещения; 3) появление реципрокных изменений ЭКГ раньше, чем прямых; 4) образование патологического зубца Q раньше типичных изменений реполяризации (псевдорубцовая стадия) или даже 5) отсутствие изменений ЭКГ, что, по данным разных авторов, встречается в 3-35% случаях ИМ [3].
Имеющиеся нарушения реполяризации за несколько дней, а при локализации процесса на нижней стенке — за несколько часов, могут исчезнуть и, таким образом, завершить процесс динамических изменений характерных именно для ИМ [4]. В этих случаях диагностика мелкоочагового ИМ становится практически невозможной, а при крупноочаговом поражении уже формально регистрируется рубцовая стадия, что, естественно, затрудняет определение давности Им [5-7].
Особенно сложным, с точки зрения интерпретации ЭКГ, является развитие ИМ в, так называемых, «немых» зонах миокарда. К ним относятся базаль-ные отделы задней и переднебоковой стенок левого желудочка (ЛЖ), задняя часть межжелудочковой перегородки, правый желудочек (ПЖ), предсердия,
папиллярные мышцы, которые не отражаются при регистрации ЭКГ в стандартных отведениях или отражаются только в виде косвенных реципрокных изменений [7].
Интрамуральный ИМ характеризуется неспецифическими изменениями в виде довольно глубоких симметричных отрицательных зубцов Т и, в дальнейшем, при ретроградном распространения тромбоза может возникнуть окклюзия крупной ветви или основного ствола коронарной артерии с развитием крупноочагового Им.
Изолированный заднебазальный ИМ встречается довольно редко, и интерпретировать ЭКГ при этой локализации бывает очень сложно. Его признаки можно выявить только в дополнительных отведениях V7-9, D по Небу или в отведениях по Слопаку, при которых, диагностическим критерием будет являться подъем сегмента ST на 0,5 мм (>1 мм у мужчин в возрасте 40 лет) [8].
При высоком переднебоковом ИМ регистрируется глубокий, но не широкий зубец Q в отведении aVL, а для более точного выявления зоны инфаркта необходимы дополнительные грудные отведения V4-6, снятые на два межреберья выше обычного уровня [9].
При инфаркте ПЖ прямые ЭКГ-признаки можно обнаружить только в дополнительных правых грудных отведениях V3R-4R, причем, чем более заметные изменения на правограмме, тем точнее диагноз. В большинстве случаев объем поражения миокарда ПЖ невелик, поэтому правожелудочковая недостаточность развивается нечасто, однако может иметь место и при нижнем ИМ без вовлечения в процесс ПЖ [10].
Одновременное возникновение острого ИМ передней и задней стенок ЛЖ наблюдается редко, поскольку они имеют разные источники кровоснабжения. Однако развитие острого переднезаднего ИМ возможно, если атеросклеротическая бляшка закрывает просвет только одной из коронарных артерий [8, 9].
При окклюзии другой артерии, некроз может охватить не только бассейн ее непосредственного кровоснабжения, но и область, коллатерального кровообращения. В этих случаях происходит как взаимное нивелирование зубцов Q, так и изменение конечной части желудочкового комплекса [4]. По данным наблюдения А.В. Шпектор и Е.Ю. Васильевой, даже при чрезвычайно обширных передне-задних ИМ изменении ЭКГ нередко ограничивались только незначительной депрессией сегмента ST в грудных отведениях [11]. Неслучайно, что в Рекомендациях Европейского общества кардиологов (ESC) 2017 года по диагностике и лечению ИМ с подъемом сегмента ST, отмечается, что у пациентов с острой окклюзией огибающей коронарной артерии, венозного шунта или ствола левой коронар-
ной артерии, может отсутствовать подъем сегмента ST во время регистрации ЭКГ, что часто приводит к ошибкам ранней диагностики ИМ [8].
Изолированный ИМ предсердий практически не встречается в клинической практике. Он диагностируется по изменению конфигурации зубца Р, подъему или депрессии сегмента PQ, возникновению нарушений ритма (фибрилляция и трепетание предсердий, предсердная экстрасистолия, синоа-урикулярные и атриовентрикулярные блокады) [12].
ИМ папиллярных мышц не имеет надежных ЭКГ критериев. В этом случае помогают данные ау-скультации (появление грубого систолического шума в области верхушки сердца) и эхокардио-графии (ЭхоКГ) (нарушение движения створок митрального клапана и увеличение митральной регур-гитации) [12].
Вариантная стенокардия, вследствие появления характерных изменений на ЭКГ и соответствующей клинической картины, требует особого упоминания. При спазме крупных субэпикардиальных коронарных артерий, могут появляться так называемые «транзиторные» отрицательные зубцы Т, что заставляет проводит дифференциальную диагностику с ИМ [13]. Однако, наиболее патогномоничным для вазоспастической стенокардии следует считать подъем ST сегмента в отведениях II, III, aVF, реже в отведениях I, aVL и грудных. При этом необходимо отметить, что спазм мелких интрамуральных и субэндокардиальных ветвей коронарных артерии, наоборот, сопровождается депрессией ST сегмента (обычно строго горизонтальное смещение). Отличить вариантную стенокардию от ИМ можно только в динамике: если дело ограничилось преходящим спазмом коронарных артерий, то уже через 20-30 минут ЭКГ нормализуется [14, 15].
Значительную сложность представляет диагностика повторного ИМ. Хроническая аневризма сердца регистрируется примерно на третьей неделе с момента начала ИМ в связи с отсутствием типичной динамики ЭКГ. Подъем сегмента ST, связанный с развитием хронической аневризмы сердца, наблюдается, как правило, только в тех отведениях, где желудочковый комплекс представлен зубцом QS
или, по крайней мере, очень глубоким патологическим зубцом Q и маленьким r. Подъем сегмента ST в отведениях, где зубец R сохраняет достаточную амплитуду, обычно указывает на свежие изменения [16]. Все это, безусловно представляет серьезные затруднения в диагностике ИМ. Для того, чтобы разобраться в ситуации, приходится учитывать клинические данные, а также результаты лабораторных и ЭхоКГ исследований [17].
Если рубец и свежий очаг некроза одинаковые по величине, то признаки первого инфаркта могут вообще исчезнуть с ЭКГ. При этом возможна даже своеобразная «нормализация» или «псевдонормализация» ЭКГ-картины. [4], например, подобная «псевдонормализация» ЭКГ-признаков постинфарктного рубца в переднеперегородочной зоне наблюдается при возникновении повторного острого ИМ в заднебазальном участке миокарда ЛЖ. Таким образом, резкое исчезновение зубца Q, ранее отражавшего старые рубцовые изменения, особенно после затяжного интенсивного ангинозного приступа, можно объяснить только свежим некрозом на противоположной стенке желудочка [18].
Трудно диагностировать повторный ИМ в рубцовой зоне. Деформированный зубец Q, без сомнения, может маскировать свежие признаки повреждения миокарда. В таком случае необходимо внимательно отслеживать динамику зубца Q с формированием комплексов Qr или, даже, QS. Нередко острый ИМ проявляется только изменениями сегмента ST и зубца Т. Выявить все эти динамические изменения можно лишь при сравнении с ЭКГ, снятой до развития повторного ИМ [19, 1].
И, наконец, блокада левой ножки пучка Гиса (БЛНПГ), которая практически не позволяет поставить точный диагноз ИМ. Так или иначе, само возникновение полной БЛНПГ при наличии соответствующей клинической картины и отсутствии блокады на предыдущих ЭКГ должно рассматриваться как возможный признак ИМ. Неслучайно, в Рекомендациях ESC, 2017 года по диагностике и лечению ИМ с подъемом сегмента ST, особое место отводится ИМ при БЛНПГ. В этом случае диагноз ставится на основании клинической картины,динамики
Рисунок 1.
Полная БЛНПГ. QS в отведении V1-4, глубокий зубец S в отведении V5-6 свидетельствуют об обширных очаговых изменениях передней стенки левого желудочка [14] Figure 1.
Total block of the His bundle branch. QS in lead V1-4, deep prong S in the lead V5-6 indicate extensive focal changes in the anterior wall of the left ventricle [14]
ЭКГ, наличия ЭКГ-микропризнаков ИМ и исследования биомаркеров. В качестве ЭКГ-микропризнаков ИМ при БЛНПГ наиболее часто рассматривают наличие зубца Q в отведениях 1, aVL, V5-6, а также в отведениях II, III, aVF, раннюю, в первые 0,03с, «зазубренность» зубца R в отведениях I, aVL, V5-6, «зазубренность» на восходящем и нисходящем колене зубца S в отведениях V3-5, глубокий зубец S в отведениях V5-6 и несоответствие конечной части желудочкового комплекса виду полной БЛНПГ [20] (рис. 1).
Однако, зубец Q и положительные зубцы T в V5-6, I и aVL отведениях при БЛНПГГ могут регистрироваться при других патологических состояниях, таких как выраженная гипертрофия ЛЖ, особенно, при гипертрофической кардиомиопатии с изолированным поражением межжелудочковой перегородки [21]. Отсутствие прироста или уменьшение амплитуды зубца R в отведениях V1-4, известное под названием феномен «провала» зубца R, в области переходной зоны следует также оценивать осторожно [22, 1].
Между тем, в ESC Рекомендациях уделяется большое внимание девиации сегмента ST при БЛНПГ и отмечается, что заподозрить острый ИМ у этих пациентов помогают: конкордантная элевация сегмента ST >1 мм в отведениях с положительным комплексом QRS, конкордантная депрессия сегмента ST >1 мм в отведениях V1-3 и дискордантная элевация сегмента ST >5 мм в отведениях с отрицательным комплексом QRS [8].
Таким образом, даже бесспорный признак ИМ на фоне ПБЛНПГ, как правило, не позволяет высказаться с определенностью о его локализации, давности и масштабности поражения.
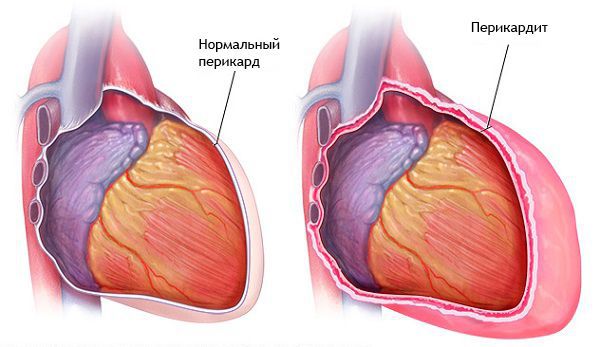
В настоящее время в литературе обсуждаются различные ситуации, сопровождающиеся элева-цией сегмента ST, но не связанные с ишемической болезнью сердца (ИБС). К ним, прежде всего, относятся сердечные причины, такие как: синдром ранней реполяризации желудочков (СПРЖ) и синдром Бругада (СБ), перикардит в острой фазе, миокардит, аритмогенная дисплазия правого желудочка, травмы сердца, опухоли сердца, а также внесердечные причины: нарушение мозгового кровообращения (НМК), левосторонний пневмоторакс, аневризма аорты с расслоением, электролитные нарушения (гиперкалиемия, гиперкальциемия), интоксикации, гипотермия. Депрессия сегмента ST, несвязанная с ИБС, наблюдается значительно чаще. Среди сердечных причин можно упомянуть различные поражения и перегрузку миокарда (миокардиты, кардиомиопатии, аортальный стеноз, митральный стеноз, пролапс митрального клапана, артериальная гипертензия и т.д.), вторичные изменения при гипертрофии желудочков, предвоз-буждение желудочков сердца, тахикардии и тахи-аритмии, посттахикардиальный синдром. Гораздо больше внесердечных причин данных изменений. Это — гипервентиляция, симпатикотония (в том числе гипертиреоз), нарушения мозгового кровообращения, органические заболевания и травма головного мозга, анемия, заболевания легких с выраженной дыхательной недостаточностью, курение, состояние голода и, наоборот, прием большого количества пищи, электролитные нарушения (гипо-калиемия), системных заболеваниях соединительной ткани, как рефлекторное влияние при острых заболеваниях желудочно-кишечного тракта (жКт), таких как панкреатит, холецистит, язва желудка,
желчнокаменная болезнь и т.д. [23]. Нельзя забывать и о шоке различной этиологии, а также о воздействии целого ряда лекарственных препаратов: сердечных гликозидов, некоторых антиаритмических и обезболивающих средств, фенотиазинов и многое другое [24]. Аналогичные состояния могут быть причинами высоких положительных или, наоборот, негативных или сглаженных зубцов Т, которые также не связаны с ИБС.
При НМК, осложненном субарахноидальным и другим кровоизлиянием, а также при тромбозах, опухолях, сотрясении мозга и повышении внутричерепного давления чаще всего регистрируются гигантские положительные или отрицательные зубцы Т с удлиненным интервалом QT (за счет слияния отрицательного зубца Т и волны и), преимущественно в I, aVL, V4-6 отведениях [25]. Они склонны к обратному развитию и обычно исчезают через некоторый период.
ИМ и НМК могут сочетаться более чем в 20% случаев, особенно у лиц пожилого и старческого возраста. В таких случаях определить первопричину заболевания не всегда просто. У лиц с выраженным атеросклерозом мозговой артерии может возникнуть тромбоз (или спазм) мозговых и коронарных артерий одновременно. Во всяком случае, при выявлении инфарктоподобных изменений у больного с острым нМк, необходимо уделять особое внимание качественному, тщательному сбору анамнеза, наличию факторов риска, детализации жалоб больного и наличию тропонина в крови.
WPW синдром нередко требует проведения дифференциальной диагностики с ИМ, так как отрицательная дельта-волна может углубить непатологические зубцы Q до патологических или снизить амплитуду зубца Я, формируя желудочковые комплексы типа QR или QS. Отрицательная дельта-волна во II, III и aVF отведениях может напоминать картину нижнедиафрагмального ИМ, в правых грудных отведениях — признаки переднеперегородочного ИМ, в I и aVL отведениях может симулировать ИМ переднебоковой стенки ЛЖ. Положительная дельта — волна А способна симулировать заднебазальный ИМ, увеличивая амплитуду зубцов Я в V1-2 отведениях [5, 26].
Особое диагностическое значение приобретает, так называемый, синдром волны 3 — термин, включающий два синдрома: синдром Бругада (СБ) и СПРЖ. В настоящее время критерии обоих синдромов пересмотрены. Для СПРЖ характерно наличие в конечной части комплекса QRS «зазубрины» или «сглаженности»; причем «зазубрина» должна располагаться выше изолинии. Так, точка 3р должна быть >0,1 мВ в 2 или более последовательных отведениях стандартной ЭКГ в 12 отведениях, кроме отведений V1-Vз. При этом, измеренная в отведениях, в которых «зазубрина» или «сглаженность» отсутствуют, продолжительность комплекса QRS <120 мс [27] (рис. 2). Обычно большие трудности диагностики возникают при варианте СРРЖ с отрицательными зубцами Т, особенно, у пациентов с клиникой болевого синдрома в прекордиальной области. В таких случаях требуется длительное клиническое и ЭКГ-наблюдение, определение активности биомаркеров и использование ЭхоКГ.
Наличие СПРЖ не исключает ИМ, хотя и маскирует его. В литературе описаны три варианта сочетания СПРЖ с ИМ: 1) впервые появляющийся СРРЖ в момент развития ИМ и исчезающий в восстановительный период; 2) существующий до развития ИМ
Рисунок 2.
СПРЖ. Подъем сегмента ST в I, II, III, aVF, aVL, V2-V6 отведениях, волна J на нисходящем колене зубца R I II III VF aVL V2-V6 «Зазубрина» на конечной части комплекса QRS, конкордантость подъема сегмента ^^ .
Figure 2.
Early ventricular repolarization syndrome. ST segment elevation in I, II, III, aVF, aVL, V2-V6 leads, J on the descending knee of the wave R I II III aVF aVL V2-V6. «Notch» at the end of the QRS complex, concordance of ST segment elevation , , , , ,
и исчезающий после него; 3) исчезающий в остром периоде ИМ и появляющийся вновь в восстановительном периоде [28].
Для СБ предлагаются следующие критерии. Прежде всего, это — 1-й тип подъема сегмента ST >2 мм (0,2 мВ) в V1-3. 2-й тип характеризуется подъемом сегмента ST >0,5 мм (обычно >2 мм в V2) в одном и более правых прекордиальных отведениях ^1-3), измеряемым по выпуклой части ST, с последующим положительным зубцом Т в V2 и его вариабельной морфологией в VI. 3-й тип характеризуется подъемом сегмента ST седловидной или сводчатой формы <1 мм. В случае, если 1-й тип подъема сегмента ST демаскируется под действием блокаторов натриевых каналов, для подтверждения диагноза СБ требуется наличие документированной фибрилляции желудочков (ФЖ) или полиморфной желудочковой тахикардии (ЖТ), синкопе вследствие предполагаемой аритмогенной причины, случаи внезапной сердечной смерти в семейном анамнезе у лиц моложе 45 лет с негативным заключением аутопсии или ночное агональное дыхание. Кроме того, подтверждением СБ является индуцируемость ЖТ/фЖ одним или двумя экстрастимулами при стимуляции ПЖ [27, 29].
2-й тип или 3-й типы подъема сегмента ST не могут заменить спонтанный 1-й тип, несмотря на вероятность их трансформации в 1-й тип при определенных условиях. При этом, появление ЭКГ-признаков 1-го типа могут быть использованы в диагностике СБ только в случае, если сопровождается одним из критериев, указанных выше [30].
При воспалительных заболеваниях сердца ЭКГ-признаки, как правило, неспецифичные, что, безусловно, усложняет диагностику и выводит на первый план клинические особенности заболевания. Однако есть и характерные для той или иной пато-
логии моменты. Так, патогномоничный ЭКГ-признак перикардита — конкордантное смещение сегмента ST вогнутой формы. При перикардите инверсия Т происходит только после возвращения ST к изолинии, в то время как для острой стадии ИМ характерно сочетание отрицательного зубца Т с сохраняющимся подъемом сегмента ST. При этом отсутствует патологический зубец Q [31].
ЭКГ при миокардите отличается большим разнообразием признаков за счет воспалительных некротических изменений в миокарде: патологический зубец Q, элевация сегмента ST с переходом в глубокий отрицательный зубец Т, дающие повод (особенно при болевом варианте миокардита) к ошибочной диагностике инфаркта миокарда. В остром периоде заболевания могут регистрироваться разнообразные нарушения ритма и проводимости сердца, за частую совокупные. При этом, ЭКГ-картина характеризуется быстрой сменой патологических признаков [4].
Острые поражения ЖКТ могут провоцировать появление депрессии сегмента St, инверсии зубца Т и, иногда зубца Q в III (II), aVF отведениях, которые приходится дифференцировать с Им. При диагностике следует учитывать наличие отягощенного по ИБС анамнеза, цианоза, одышки, глухого I тона, болезненности при пальпации живота, симптомов раздражения брюшины, данных определения активности ферментов в крови и анализа ЭКГ в динамике. Вместе с тем, следует иметь в виду, что при остром ИМ, особенно, при нижнедиафрагмальной локализации, отмечается отек, точечные кровоизлияния и более тяжелое поражение поджелудочной железы [32].
При появлении инфарктоподобных изменений на ЭКГ у онкологических больных при отсутствии соответствующих анамнестических данных и кли-
нических указаний на хроническую ИБС следует предполагать метастазирование опухоли в миокард. Диагноз уточняется при анализе ЭхоКГ [33].
Наиболее часто приходится сталкиваться с проблемой дифференциального диагноза ИМ и тромбоэмболии легочной артерии (ТЭЛА). Прежде всего, это связано со сходной клиникой, появлением неспецифических изменений сегмента ST, зубца Т. При массивном ТЭЛА в III, aVF отведениях определяется зубец q(Q) разной степени выраженности, не превышающий по продолжительности 0,03 сек. и по глубине 25% зубца R, при этом, в отличие от ИМ отсутствует патологический зубец Q во II отведении. Между тем, выраженный зубец S в I, aVL отведениях, патогномоничный для ТЭЛА, не характерен для неосложненного ИМ в области задней стенки Лж. Кроме того, при ТЭЛА появляются ЭКГ-признаки, характерные для остро возникшей перегрузки правых отделов сердца в правых грудных отведениях [34].
Таким образом, инфарктоподобные неспецифические изменения ЭКГ сами по себе, взятые в отрыве от клинической картины, не могут служить основанием для подтверждения окончательного диагноза ИМ, поэтому ЭКГ нужно всегда анализировать в купе с жалобами, анамнезом и дополнительными методами исследованиями.
Мангушева М.М. http:/orcid.org/0000-0002-6425-4216. Маянская С.Д. http:/orcid.org/0000-0001-6701-5395. Исхакова Г.Г. http:/orcid.org/0000-0003-2122-3652.
ЛИТЕРАТУРА
1. Орлов В.Н. Руководство по электрокардиографии. — М.: Медицинское информационное агентство, 2017. — 560 с.
2. Шалаев С.В. Проблемы диагностики острого инфаркта миокарда // Сердце: журнал для практикующих врачей. — 2002. — Т. 1, №1. — С. 16-18.
3. Мазур Н.А. Внезапная смерть больных ишемической болезнью сердца. — М.: Медицина, 1985. — 193 с.
4. Мангушева М.М. Трудности и ошибки ЭКГ-диагностики инфаркта миокарда // Журнал международной медицины. — 2015. — T. 15, №4. — C. 15-24.
5. Дощицин В.Л. Клиническая электрокардиография. — М.: Мед. информ. агенство, 1999. — 373 с.
6. Атрощенков Д.В. Энциклопедия клинической кардиологии. — Литагент «Научная книга», 2009. — 400 с.
7. Vesterinen P., Vaananen H., Stenroos M., et al. Localization of prior myocardial infarction by repolarization variables // International Journal of Cardiology. — 2008. — №124. — P. 100-106.
8. Ibanez B., James S., Agewall S., et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC) // European Heart Journal. — 2018. — Vol. 39, №2. — P. 119-177.
9. Power B., Seppelt I. Book Chapter: Acute cardiac syndromes, investigations and interventions in book: Oh’s Intensive Care Manual, 2019. — №20. — P. 181-203.
10. Ослопов В.Н., Богоявленская О.В., Ослопова Ю.В., Макаров М.А., Хабибуллина Р.Т. с соавт. К вопросу ЭКГ диагностики инфаркта правого желудочка // Практическая медицина. — 2010. — Т. 44, №5. — С. 13-15.
11. Шпектор А.В., Васильев Е.Ю. Кардиология: ключи к диагнозу. — М.: ВИДАР, 1996. — 352 c.
12. Люсов В.А., Волов Н.А., Гордеев И.Г. ЭКГ при инфаркте миокарда: атлас. — М.: ГЭОТАР-Медиа, 2009. — 76 с.
13. Hirano Y., Uehara H., Nakamura H., et al. Diagnosis of vasospastic angina: Comparison of hyperventilation and cold-pressor
stress echocardiography, hyperventilation and cold-pressor stress coronary angiography, and coronary angiography with intracoronary injection of acetylcholine // International Journal of Cardiology. — 2007. — №116. — P. 331-337.
14. Де Луна А.Б. Руководство по клинической ЭКГ. — М.: Медицина, 1993. — 704 с.
15. Conti C.R.: Large vessel coronary vasospasm: diagnosis, natural history and treatment // Am. J. Cardiol. — 1985. — №55. — Р. 41B-49B.
16. Исаков И.И., Кушаковский М.С., Журавлева Н.Б. Клиническая электрокардиография. Руководство для врачей. — Изд. 2-е, переработ. и доп. — Л.: Медицина,1984. — 272 с.
17. Суворов А.В. Клиническая электрокардиография. — Нижний Новгород: Изд-во НМИ, 1993. — 124 с.
18. Руксин В.В. Неотложная кардиология. — СПб: Невский диалект, 2001. — 501 с.
19. Сыркин А.Л., Маркова А.И., Райнова Л.В. Рецидивирующий инфаркт миокарда. — М.: Медицина, 1981. — 120 с.
20. Wackers F.J. The diagnosis of myocardial infarction in the presence of left bundle branch block // Cardiol. Clin. — 1987. — №5. — P. 393-401.
21. Jain S., Ting H.T., Bell M., et al. Utility of left bundle branch block as a diagnostic criterion // Am. J. Cardiol. — 2011. — Vol. 107, №8. — P. 1111-1116.
22. Madias J.E., Sinha A., Ashtiani R., et al: A critique of the new ST-segment criteria for the diagnosis of acute myocardial infarction in patients with left bundle-branch block // Clin. Cardiol. — 2001. — №24. — P. 652-655.
23. Albrecht C.A., Laws F.A. ST segment elevation pattern of acute myocardial infarction induced by acute pancreatitis // Cardiol. Rev. — 2003. — №11. — P. 147-51.
24. Pollack M.L. ECG Manifestations of Selected Extracardiac Diseases // Emerg. Med. Clin. N. Am. — 2019. — Article in Press.
25. Sommargren C.E., Zaroff J.G., Banki N., et al. Electrocardiographic repolarization abnormalities in subarachnoid hemorrhage // J. Electrocardiol. — 2002. — №35 (Suppl). — P. 257262.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
26. Воробьев Л.В. Синдром WPW, акценты ЭКГ диагностики // Успехи современного естествознания. — 2015. — №1-5. — С. 751755.
27. Беленков Ю.Н., Снежицкий В.А., Гизатулина Т.П., Шпак Н.В., Кузнецов В.А. с соавт. Пересмотр диагностических критериев синдромов J-волны: новые концепции и их актуальность для практики кардиолога (по материалам экспертного согласительного документа APHRS/EHRA/HRS/SOLAEGE 2016 г.) // Кардиология. — 2018. — Т. 58, №11. — С. 41-52.
28. Большаков Т.Ю., Шульгин В.А. Особенности электрокардиографии при сочетании синдрома ранней реполяризации желудочков и инфаркта миокарда. — Кардиология. — 1988. — №11. — С. 116-119.
29. Nagase S., Hiramatsu S., Morita H., et al. Electroanatomical correlation of repolarization abnormalities in Brugada syndrome: detection of type 1 electrocardiogram in the right ventricular outflow tract // J. Am. Coll Cardiol. — 2010. — №56. — P. 2143-2145
30. Antzelevitch C., Gan-Xin Yan., Ackerman M.J. et al. J-Wave syndromes expert consensus conference report: Emerging concepts and gaps in knowledge: endorsed by the Asia Pacific Heart Rhythm Society, the European Heart Rhythm Association, the Heart Rhythm Society, and the Latin American Society of Cardiac Pacing and Electrophysiology (Sociedad Latinoamericana de Estimulacion Cardiaca y Electrofisiologia [SOLAECE]) // Heart Rhyth. — 2016. — №0. — P. 1-30.
31. Гиляревский С.Р. Диагностика и лечение заболевания перикарда: Современные подходы, основанные на доказательной информации и клиническом опыте. — М.: Медиа Сфера, 2004. — 132 с.
32. Yu A.C., Riegert-Johnson D.L. A case of acute pancreatitis presenting with electrocardiographic signs of acute myocardial infarction // Pancreatol. — 2003. — №3. — P. 515-517.
33. Яндиева Р.А., Сарибекян Э.К., Мамедов М.Н. Кардиотоксич-ность при лечении онкологических заболеваний // Международный журнал сердца и сосудистых заболеваний. — 2018. — Т. 6, №17. — С. 4-12
34. Rodger M., Makropoulos D., Turek M., et al. Diagnostic value of the electrocardiogram in suspected pulmonary embolism // Am. J. Cardiol. — 2000. — №86. — P. 807-809.
Инфаркт миокарда — это грозное заболевание, являющееся одной из основных причин смертности среди населения. Суть данной патологии заключается в нарушении кровоснабжения какого-либо участка сердечной мышцы с последующим возникновением в нем зоны некроза. Главным условием для благоприятного прогноза при такой болезни является ее своевременная диагностика. Один из наиболее информативных диагностических методов — это электрокардиографическое исследование (ЭКГ). В этой статье мы поговорим об ЭКГ-признаках инфаркта миокарда по стадиям, в зависимости от размера очага.
Может ли ЭКГ не показать инфаркт миокарда?
Электрокардиография — это диагностический метод, направленный на регистрацию электрических импульсов, образующихся при работе сердца. Для проведения исследования на теле пациента крепятся специальные электроды, снимающие показания в двенадцати отведениях:
- Трех стандартных отведениях;
- Трех усиленных от конечностей отведениях;
- Шести грудных отведениях.
Несмотря на то, что ЭКГ считается ведущим методом диагностики инфаркта миокарда, иногда при данном заболевании на электрокардиограмме обнаруживаются не очень убедительные изменения или они вовсе отсутствуют. Такая ситуация может возникать не только в первые часы от развития ишемии, но и даже в более позднем периоде.
В 2019 году ученые из Казанского государственного медицинского университета опубликовали работу, по результатам которой было установлено, что инфарктоподобные неспецифические изменения ЭКГ, взятые в отрыве от клинической картины, не могут служить основанием для подтверждения окончательного диагноза инфаркта миокарда, поэтому ЭКГ всегда нужно анализировать в совокупности с жалобами, анамнезом и дополнительными исследованиями.
Признаки инфаркта миокарда на ЭКГ по стадиям
Всего выделяют четыре стадии инфаркта миокарда:
- Острейшую;
- Острую;
- Подострую;
- Стадию рубцевания.
Для каждой из этих стадий будут характерны свои изменения на электрокардиограмме.
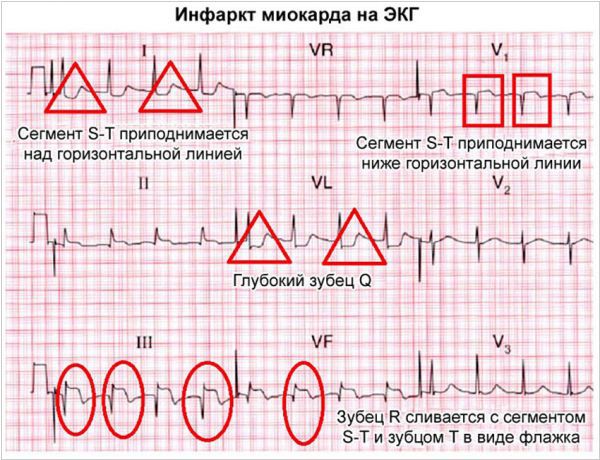
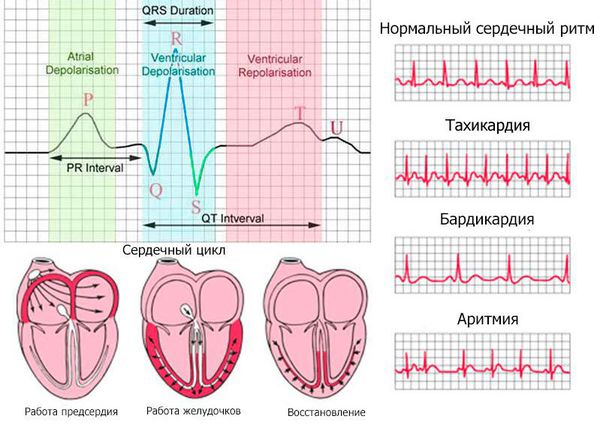
Острейшая стадия (длится от нескольких минут до нескольких часов) характеризуется увеличением высоты зубца Т, смещением относительно изолинии сегмента ST, слиянием сегмента ST с зубцом Т с образованием монофазной кривой по типу «кошачьей спинки».
Острая стадия (продолжается в течение 1-2, максимум 3 недель) проявляется образованием патологического зубца Q, снижением зубца R, формированием отрицательного зубца Т, постепенным смещением ST к изолинии.
Подострая стадия (длится до 1,5-2 месяцев) сопровождается возвращением ST к изолинии, сохранением патологического зубца Q, уменьшением глубины зубца Т.
Стадия рубцевания характеризуется сохранением ST на изолинии, уменьшением амплитуды зубца Q, возвращение зубца Т к изолинии (может даже стать слабо положительным).
Изменения на ЭКГ в зависимости от размера очага
В зависимости от размеров участка ишемии принято выделять крупноочаговый и мелкоочаговый инфаркты миокарда. Крупноочаговый инфаркт, в свою очередь, может быть трансмуральным и субэпикардиальным.
При трансмуральном инфаркте на ЭКГ выявляются:
- Глубокий и расширенный зубец Q;
- Высокое расположение сегмента ST;
- Отрицательный зубец Т в подостром периоде.
При субэпикардиальном поражении обнаруживаются схожие признаки, главным отличием является наличие зубца R.
Мелкоочаговый инфаркт бывает интрамуральным и субэндокардиальным. Основным маркером интрамурального повреждения является отрицательный зубец Т. При субэндокардиальном инфаркте обнаруживается снижение ST ниже изолинии.
Руководство по электрокардиографии / Орлов В.Н. // Медицинское информационное агентство – 2017
К вопросу о трудностях ЭКГ диагностики инфаркта миокарда / Мангушева М.М., Маянская С.Д., Исхакова Г.Г. // Практическая медицина – 2019 – №2
Изменения в кардиограмме при ишемии. Лицензия: Envato Elements Item
Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет.
Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн.
Цели: максимально амбициозные.
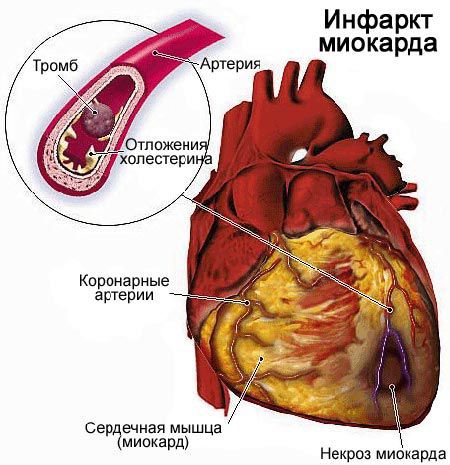
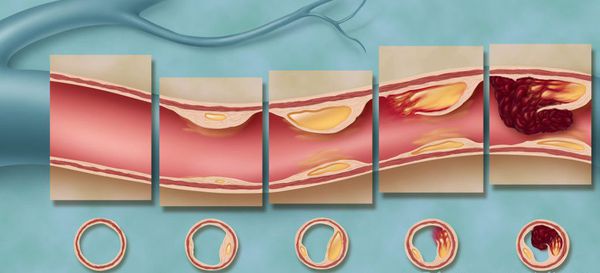
Ишемическая болезнь сердца возникает при закупорке сосудов, вызванных атеросклерозом. В результате в сердечную мышцу перестает поступать кровь, и она начинает испытывать нехватку кислорода и питательных веществ (ишемию). Прогрессирование этого процесса приводит к инфаркту, при котором участок в сердечной мышце перестает снабжаться кровью, кислородом и отмирает.
Граница между тяжёлой формой ишемической болезни и инфарктом очень тонкая, поэтому столь серьезный диагноз обязательно нужно подтвердить лабораторными показателями. Но даже малейшее подозрение на инфаркт требует срочной медицинской помощи, поскольку может вызвать кардиогенный шок и остановку сердца.
Типы ИБС, определяемые на ЭКГ
Существует несколько типов ИБС, которым соответствуют определенные изменения на ЭКГ:
Субэндокардиальная ишемия, возникающая со стороны эндокарда – внутренней оболочки сердца. Характеризуется изменениями зубца Т, который может превышать свой максимальный размер в 0,5 мм. Иногда он может практически сравниваться по величине с зубцом R – самым высоким на кардиограмме, хотя в норме должен составлять примерно 1/4 – 1/8 его высоты.
Субэпикардиальная ишемия возникает с наружной стороны сердца, ближе к его внешней оболочке – эпикарду. Характерный признак такого нарушения – отрицательный зубец Т в основных отведениях, который в норме должен быть положительным.
При трансмуральной ишемии, захватывающей всю толщу миокарда также обнаруживается отрицательный зубец Т. Однако он более глубокий, чем при субэпикардиальном повреждении.
При более глубоких повреждениях миокарда наблюдаются другие изменения на ЭКГ:
- При выраженном ишемическом повреждении тканей в области эндокарда – внутреннего слоя сердца наблюдается депрессия сегмента ST, который опускается на всех основных отведениях.
- При повреждении тканей в области наружной части сердца – перикарда — сегмент ST будет приподнят.
- Для глубокого трансмурального повреждения, захватывающего всю толщину сердечной ткани, характерен следующий за зубцом R полукруглый сегмент ST, имеющий характерный вид “кошачьей спинки”.
- При повреждениях, захватывающих большую зону миокарда, может обнаруживаться сразу несколько признаков ишемии. Например, наблюдается отрицательный зубец Т в сочетании с изменениями на участке ST.
Инфаркт на ЭКГ – признаки инфаркта на кардиограмме
Инфаркты практически всегда сопровождаются изменениями на ЭКГ. Они настолько характерны, что по изменениям кардиограммы можно узнать тип инфаркта. А по отведению, каждое из которых отвечает за определенный участок миокарда, можно выяснить, где именно произошло омертвение тканей:
- При трансмуральном инфаркте, охватывающем всю толщу миокарда, от полного комплекса зубцов остается отрицательный зубец QS. Если гибель тканей произошла ближе к наружной стороне сердца, часть импульсов будет проходить, поэтому кардиограмма сохранит зубцы. Однако они будут изменены – зубец Q станет очень глубоким, практически равным по величине зубцу R. А зубец R в этом случае может быть уменьшен.
- При интрамуральном инфаркте, возникшем в глубине тканей, но не охватывающем всю их толщу, на кардиограмме пропадает зубец Q. Такая же картина может наблюдаться, если очаг вплотную прилегает к эндокарду.
Обычно инфаркт не бывает изолированным . Он, как правило, сочетается с признаками поражения тканей и их ишемии Поэтому на кардиограмме могут наблюдаться изменения и в других зубцах. Их локализацию можно увидеть на отведениях, отвечающих за определенный участок миокарда.
Изменения на ЭКГ также зависят от стадии инфаркта:
- На первой острейшей стадии, длящейся несколько часов, вначале регистрируются изменения сегмента ST, который становится выгнутым, приобретая характерный вид «кошачьей спинки». Зубец Q на такой кардиограмме отсутствует. В этот момент некроза в миокарде еще нет, а имеется только зона поражения. Позже на ЭКГ виден отрицательный зубец Q, который также переходит в “кошачью спинку”.
- На следующий острой стадии инфаркта некроз миокарда сочетается с поражением тканей, поэтому кардиограмма имеет вид, характерный для обоих нарушений. Виден глубокий отрицательный рубец Q, за ним следует сниженный зубец R, поднятый фрагмент ST и отрицательный зубец T. Эта стадия длится до 3 недель.
- Подострая стадия характеризуется исчезновением зоны ишемии и наличием только зоны некроза. Это также отражается на кардиограмме. На ней виден глубокий отрицательный зубец Q, затем сниженный зубец R, потом после этого наблюдается линия ST, которая может быть выше или ниже нормы, а затем – нормальный положительный зубец Т. Глубокий отрицательный зубец Q может сохраняться много лет после инфаркта.
Некоторые случаи инфаркте миокарда не сопровождаются типичными изменениями на ЭКГ. Поэтому при любых болях в области сердца, особенно не снимаемых нитратами и другими препаратами, расширяющими сосуды миокарда, назначается кровь на биохимию (сердечные показатели) и общий анализ для определения количества лейкоцитов и СОЭ.
Продолжение статьи
- Текст 1. Расшифровка ЭКГ: как правильно расшифровать кардиограмму. Датчики, отведения ЭКГ.
- Текст 2. Основные элементы ЭКГ: что содержит график кардиограммы
- Текст 3. Расшифровка ЭКГ: наиболее важные показатели кардиограммы с примерами нарушений
- Текст 4. Изменения на кардиограмме при гипертрофических процессах в миокарде
- Текст 5. Изменения в кардиограмме при ишемической болезни сердца (ИБС) и инфаркте миокарда
- Текст 6. Изменения на ЭКГ при сердечных блокадах
Инфаркт миокарда
Электрокардиограмма (ЭКГ)
Эхокардиография (УЗИ сердца)
- Инфаркт
- Причины
- Симптоматика
- Диагностика
- Лечение
Инфаркт
По сей день иногда звучат, преимущественно от людей старшего поколения, примерно такие народно-кардиологические обороты: «Этак можно и инфаркт получить, то бишь разрыв сердца» (обычно имеется в виду потрясение от неожиданности или, скажем, от радостной новости). Земной поклон нашим несокрушимым дедам и бабушкам, и пусть все новости только радуют их усталые сердца.
Однако в терминологию, учитывая исключительную важность темы, все же стоит внести определенность.
Инфаркт — это не разрыв сердца. Более того, даже не обязательно речь идет именно о сердце: ничуть не слаще, скажем, инфаркт головного или спинного мозга, инфаркт почки или кишечника.
И определение, которое с автоматической назойливостью дает инфаркту одна из крупнейших поисковых систем в Интернете: «…прекращение тока крови при спазме артерий или их закупорке», – это тоже неправильно. Инфаркт не «прекращение тока крови», а результат такого прекращения, результат всегда патологический и, как правило, тяжелый.
Поэтому будем стремиться к точности определений и ясности формулировок. Тема действительно слишком серьезна.
Любая живая ткань состоит, как известно, из клеток. Для нормальной работы и эффективного выполнения своих функций эти клетки должны дышать, питаться и избавляться от шлаковых продуктов метаболизма (обмена веществ). Все эти процессы обеспечиваются кровотоком или, говоря точнее, перфузией – постоянным «пропитыванием», сквозным проливанием крови через ткань, за что отвечает система капилляров, самых мелких кровеносных сосудов. В капиллярную систему поступает артериальная кровь, приносящая в ткань питательные вещества и связанный эритроцитами кислород. Затем по малым, большим и магистральным венам кровь отводится к легким, печени, почкам – для нового цикла фильтрации, детоксикации, обогащения и газообмена.
Насосную функцию, то есть прокачивание крови под давлением по этой сложной сосудистой системе, выполняет сердечная мышца, или миокард. Сократительная активность сердца начинается еще в утробе матери, на первых неделях беременности, и безостановочно продолжается до последней минуты жизни человека. Верно и обратное: последняя минута наступает вследствие того, что останавливается ритмичное чередование сокращений (систола) и расслаблений (диастола).
Однако миокард как полая насосная мышца (анатомически и гистологически устроенная весьма сложно) состоит из живых тканей, которым тоже необходимы питание и кислород. В этом смысле миокард не отличается от прочих органов: ему самому нужна тканевая перфузия крови, непрерывная и достаточно интенсивная, учитывая работу в пожизненном режиме 24/7 без выходных и праздничных дней. Кровоснабжение сердца осуществляется по специальному артериально-венозному контуру. За внешнее сходство с атрибутом монаршества собственный круг кровообращения миокарда называют коронарным, или венечным.
Недостаточно объемный «пролив» крови через ткань (любую, не только сердечную) носит название гипоперфузия. Широко известный термин «ишемия» на разных этапах развития медицины трактовался по-разному; сегодня под ишемией понимают патологическое состояние ткани, развивающееся вследствие гипоперфузии, причем облигатными (обязательными для употребления термина или постановки диагноза) признаками ишемии являются нарушения всех основных процессов, обеспечиваемых тканевым кровоснабжением – питания, оксигенации (насыщение кислородом) и отвода шлаков.
Таким образом, ишемическая болезнь сердца (ИБС), – хроническое голодание и/или «засорение» тканей миокарда, обусловленное недостаточным функционированием коронарного контура кровообращения. Факторов риска и прямых причин развития ИБС, как и ее клинических вариантов, известно множество, но сейчас важнее другое: такая ситуация неизбежно приводит к перегрузке, преждевременному износу, дегенеративно-дистрофическим изменениям в тканях и разнообразным сбоям в работе сердечной мышцы (например, к приступам стенокардии). В условиях постоянной ишемии миокард, мозг, почка и любой другой орган просто не может в полном объеме выполнять свои функции – подобно тому, как задыхающийся и живущий впроголодь атлет не сможет заниматься профессиональным спортом.
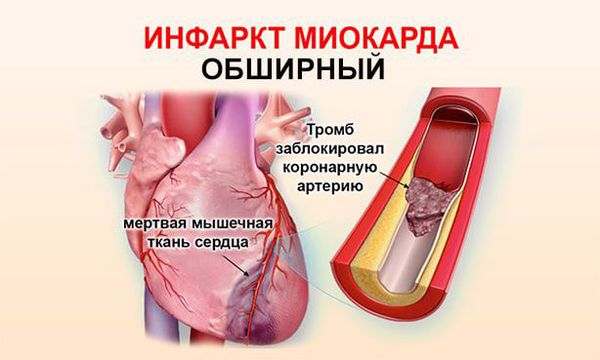
Инфаркт представляет собой одновременную массовую гибель клеток на локальном участке ткани. Другими словами, это быстрый очаговый некроз, наступающий вследствие резкого сокращения кровоснабжения (неполная ишемия) или полного прекращения перфузии (тотальная ишемия).
- Инфаркт миокарда
- — омертвение одного или нескольких участков сердечной мышцы, наступившее по той причине, что в этих участках перестала циркулировать кровь коронарного круга.
В отношении инфаркта миокарда сегодня доступно огромное количество информации. Не всегда она, как показано выше, достоверна и точна, но это в любом случае лучше, чем полное непонимание нормальных и патологических процессов, происходящих в собственном организме. Останавливаться на подробностях эпидемиологии мы здесь не станем, однако кратко отметим четыре наиболее существенных и тревожных момента.
Во-первых, сердечнососудистые заболевания (в первую очередь ИБС и инфаркты) в статистических показателях ненасильственной летальности упорно удерживают лидерство: их доля в общей структуре смертности, по оценкам ВОЗ, превышает 30%.
Во-вторых, показатели летальности по России в два с половиной раза выше, чем в среднем по Европе; втрое выше, чем в США; в девять раз выше, чем в Японии.
В-третьих, инфаркт постоянно «молодеет»: усредненный возраст первичных больных с ИБС и инфарктами год от года устойчиво снижается.
В-четвертых, 80% инфарктов миокарда можно было предотвратить.
Причины
Факторы, длительным действием которых обусловлено подавляющее большинство инфарктов миокарда – это ишемическая болезнь сердца (иногда ее небезосновательно называют «инфарктом, растянутым во времени»), атеросклероз и артериальная гипертензия. О каждом из этих заболеваний написаны тысячи больших томов, однако полной ясности пока нет: обнаруживаются все новые и новые данные об их этиологии, патогенезе, клинике. Эти «три источника и три составные части» инфаркта находятся между собой в тесной и сложной взаимосвязи; они чаще всего действуют одновременно и потенцируют друг друга.
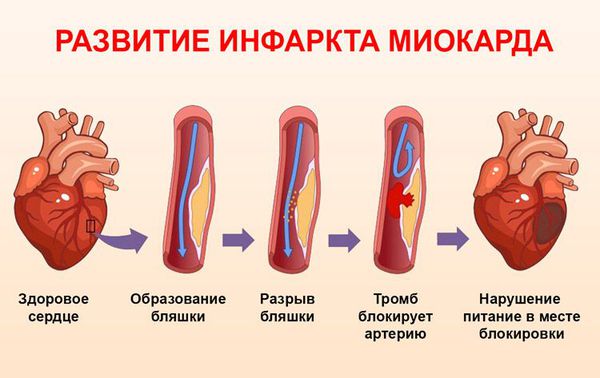
Непосредственной причиной острой ишемии и последующего некроза практически всегда оказывается тромбоэмболия – закупорка одного из коронарных сосудов сгустком крови, зацепившимся за атеросклеротическую бляшку, или самой бляшкой при достижении ею значительных размеров и отрыве от сосудистой стенки, или липидным комком (жировая эмболия в 90% случаев обусловлена скелетной травмой, особенно переломами трубчатых костей), или пузырьком воздуха (воздушная эмболия встречается редко). Кроме того, инфаркт миокарда возможен при длительном спазме коронарных артерий и некоторых пороках анатомического строения.
К дополнительным факторам риска относятся: пожилой возраст, экологические вредности, наличие ревматических заболеваний, тяжелых инфекций, сахарного диабета, уже перенесенного инфаркта в анамнезе, эмоциональные и физические перегрузки, особенно внезапные (включая резкий подъем после сна), а также мужской пол. Но главный фактор сердечнососудистого риска отлично известен, скучен и настолько банален, что воспринимается уже почти как норма, а не как грубая патология. Этот фактор состоит из всего того, что мы собираемся «бросить с понедельника», дабы начать «новую здоровую жизнь». Всё собираемся да собираемся, да откладываем до следующего раза.
И зря откладываем, надо заметить, поскольку буквально с каждым месяцем наше курение, ожирение, переедание, злоупотребление, круглосуточное сидение и лежание, наслаждение всякой малосъедобной гадостью, нежелание пройтись пешком, если можно подрулить, – становятся все опасней. Снисходительно посмеиваясь над теми молчаливыми утренними и вечерними тенями в спортивных костюмах, кто «бежит трусцой от инфаркта», мы очертя голову несемся в противоположном направлении.
Симптоматика
Казалось бы, что тут долго говорить: раз инфаркт, значит, сильно болит сердце. Если повезло, – приехали, увезли и откачали до следующего раза; прочитали нудную лекцию о вреде курения, рекомендовали санаторий и сдали напряженно улыбающимся родственникам. А коли не повезло – ну что ж, упал и умер, судьба такая, все под богом…
На самом деле клиника инфаркта миокарда, несмотря на фактически однотипный этиопатогенетический механизм, удивительно разнообразна. И исходы отнюдь не столь однозначны. Даже в критической ситуации сердце так просто не сдается; чувство ответственности за нашу жизнь развито у миокарда неизмеримо лучше, чем наша ответная о нем забота.
И на обыденном уровне, и в специальной литературе постоянно обсуждаются случаи инфарктов, перенесенных «на ногах» и диагностированных ретроспективно, иногда через много лет, на случайной ЭКГ. Такое действительно случается, и нередко: согласно некоторым публикациям, до 35-40% инфарктов миокарда в остром периоде остаются неидентифицированными, и именно наличие омертвевшего, зарубцевавшегося и не функционирующего участка резко повышает риск повторного инфаркта, теперь уже «большого» и, увы, с большой вероятностью фатального. Изредка встречаются безболевые формы, несколько чаще – атипичные. В этом случае инфарктом имитируется клиника астматического приступа, желудочно-кишечных заболеваний (с тошной, рвотой, абдоминальным болевым синдромом и пр.), внезапного психического расстройства (с галлюцинациями и психомоторным возбуждением), острого нарушения мозгового кровообращения и т.д.
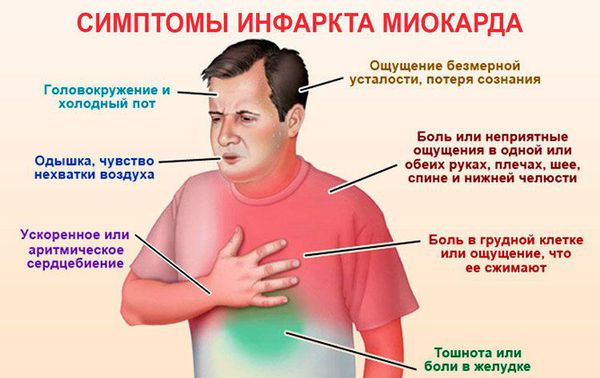
Однако опытные «сердечники» и их близкие хорошо знают, на что обратить внимание. Классическая схема развития инфаркта включает следующее:
- резкая загрудинная боль, чаще слева, не купируемая нитроглицерином и не отпускающая в течение получаса и более (важно, что Скорая должна быть вызвана значительно раньше, уже через 5-7 мин после того, как станет очевидным отсутствие эффекта!);
- бледность кожных покровов, потливость, тотальная слабость, головокружение;
- острая нехватка воздуха;
- аномальный (учащенный или редкий) пульс;
- мучительный апродуктивный кашель;
- ажитация (тревога), панический страх смерти;
- полуобморочное или обморочное состояние.
Следует еще раз повторить, что этот общий сценарий очень вариативен. Например, симптоматика может сравнительно плавно манифестировать и затем скачкообразно усугубляться по мере отмирания новых участков миокарда. При обширном многоочаговом инфаркте вероятен т.н. кардиогенный шок, исход которого летален в 90-95% случаев. А иногда не успевает появиться ни симптоматика, ни ее вариации: у абсолютно здорового, как казалось ему и окружающим, человека инфаркт может манифестировать первой и последней остановкой сердца.
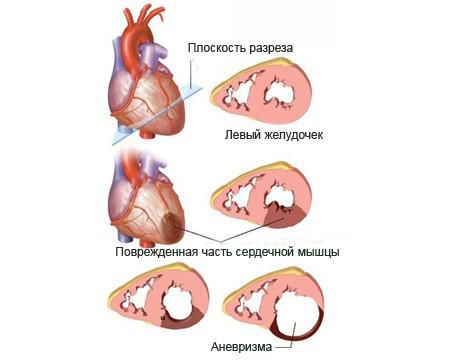
Следует знать и помнить, что даже при более благоприятном развитии острая ишемия оставляет очень незначительный запас времени на то, чтобы сделать ее транзиторной: через 20-30 минут изменения в тканях уже необратимы. Кроме того, даже если сам инфаркт пережит более или менее удачно, его последствия и осложнения могут оказаться значительно тяжелее: тромбозы, инсульты, постинфарктный синдром, инвалидизирующая ХСС (хроническая сердечная недостаточность), госпитальная пневмония и мн.др., не говоря уже о серьезных тревожно-депрессивных и невротических (кардиофобических, ипохондрических и т.п.) расстройствах.
Диагностика
Врачебно-фельдшерский состав служб неотложной помощи видит инфаркты, к сожалению, часто. Протокол диагностики, в том числе дифференциальной, хорошо отработан и позволяет свести вероятность ошибки практически к нулю. Столь же быстро и четко осуществляется госпитализация больного. Диагностическим стандартом остается электрокардиограмма, а также ЭхоКГ (УЗИ сердца), биохимический анализ крови, а в более спокойном отдаленном периоде – коронарография, сцинтиграфия и т.п
Лечение
В свою очередь, протоколы реанимации, купирования острой симптоматики и дальнейшего ведения больных с инфарктом миокарда тщательно разработаны, подробно прописаны (с целью предусмотреть все мыслимые и немыслимые варианты развития ситуации) и подтверждены мировой кардиологической практикой. Тем не менее, они продолжают постоянно совершенствоваться и уточняться: любой инфаркт – это всегда опасно для жизни и непредсказуемо на всех последующих этапах.
Первоочередной задачей является, конечно, восстановление коронарного кровообращения и ритмичной сердечной деятельности. С этой целью проводится интенсивная тромболитическая терапия, по показаниям – дефибриляция, экстренное кардиохирургическое вмешательство (аортокоронарное шунтирование, ангиопластика, принудительное аортальное наполнение и т.д.). К задачам первой очереди относится также купирование интенсивного болевого синдрома и дыхательной недостаточности, а также нормализация АД и стабилизация психического статуса. В дальнейшем назначают антиагреганты, антикоагулянты, тромболитики, бета-адреноблокаторы, однако эти схемы очень индивидуальны и специальны (на всякий случай уточним, что речь о каком бы то ни было самолечении не идет вообще).
Для иллюстрации всех сложностей острого, непосредственно постинфарктного и реабилитационного периодов в англоязычной литературе часто употребляется оборот «the golden hour» – досл. «золотой час». Имеется в виду своеобразная ступенчатая тенденция в статистике летальности: критическими являются первый час, а затем, если больной его пережил, – первые сутки, первая неделя, месяц и год.
По этому поводу заметим, что в кардиологических отделениях, да и за их пределами, упорно бытуют рассказы о чудесных исцелениях. Дескать, сам рассказчик (или сосед по палате, «один знакомый» и т.д.) сразу после инфаркта отпихнул санитаров, подмигнул медсестрам, пружинисто и бодро вскочил на ноги, выкурил полпачки сигарет, выпил с врачом бутылочку коньяку, – эта сюжетная линия почему-то особенно любима народными сказителями, – да и поехал домой (варианты: пошел пешком из Петербурга в Москву; четырнадцать раз отжал штангу; побежал играть в футбол в больничном дворе; съел тазик плова, и т.п.).
Но не будем слишком строги; возможно, это одна из форм стихийной коллективной психологической защиты, и в этом качестве басни действительно могут быть полезны (не случайно существует такое психотерапевтическое направление, как сказкотерапия).
В действительности же 60-70% больных не удается довезти до медучреждения. При грамотном и квалифицированном оказании неотложной помощи – уже в стационаре умирает каждый пятый. Из пожилых людей, перенесших острый период инфаркта, каждый четвертый умирает в течение первого месяца. Примерно каждый десятый уже спасенный, казалось бы, пациент умирает от повторного инфаркта в течение первого года.
Эта статистика чудовищна. И какие здесь, спрашивается, могут быть сигареты с футболом, когда нужно ловить буквально каждое слово врача и думать лишь о том, чтобы не нарушить предписанный режим – сначала строго постельный, затем очень осторожный в пределах палаты, затем щадящий госпитальный, а затем – особый, индивидуально-расписанный, реабилитационно-профилактический на всю, как говорится, оставшуюся жизнь. Чтобы длилась она как можно дольше.
Увы, радостное предвкушение и нетерпеливое ожидание выписки зачастую отвлекает, не давая внимательно выслушать, запомнить, а лучше всего – в деталях записать все, что скажет кардиолог стационара, а затем и тот врач, кто будет наблюдать и сопровождать в дальнейшем. Однако повторим: знать и как можно четче понимать происходящее должен и сам больной, и ближайшее его окружение. Невнимательности инфаркт не прощает.
Дата публикации 13 ноября 2019Обновлено 3 августа 2021
Определение болезни. Причины заболевания
Инфаркт миокарда (Myocardial infarction, heart attack) — это развитие некроза (омертвения) сердечной мышцы из-за остро возникшей недостаточности кровотока, при которой нарушается доставка кислорода к сердцу. Может сопровождаться болью в разных частях тела, потерей сознания, тошнотой, потливостью и другими симптомами [5].
Инфаркт миокарда является одной из наиболее острых клинических форм ишемической болезни сердца (ИБС).
Мужчины болеют инфарктом миокарда значительно чаще (примерно в 5 раз), чем женщины [6]. Эта закономерность особенно выражена в молодом и среднем возрасте. Инфаркты у женщин случаются в среднем на 10-15 лет позже по сравнению с мужчинами. Это может быть связано с более поздним развитием атеросклероза под влиянием защитного действия женских половых гормонов (эстрогенов) и меньшим распространением вредных привычек среди женщин. Заболеваемость инфарктом миокарда значительно увеличивается с возрастом.
Факторы риска развития инфаркта миокарда делятся на три группы:
- Факторы, которые можно скорректировать или устранить: курение, высокий уровень холестерина липопротеинов низкой плотности в крови, артериальная гипертензия.
- Факторы, которые хуже поддаются коррекции: сахарный диабет, снижение уровня липопротеинов высокой плотности (иначе их называют «хорошим холестерином»), ожирение, менопауза и постменопауза, употребление алкоголя, стресс, питание с избыточной калорийностью и высоким содержанием животных жиров, высокое содержание в крови липопротеина (А), высокий уровень гомоцистеина.
- Факторы, которые нельзя скорректировать или устранить: пожилой возраст, мужской пол, наследственность — раннее развитие инфаркта миокарда у родителей или кровных родственников до 55 лет.
Этиологические факторы инфаркта миокарда можно разделить на две группы:
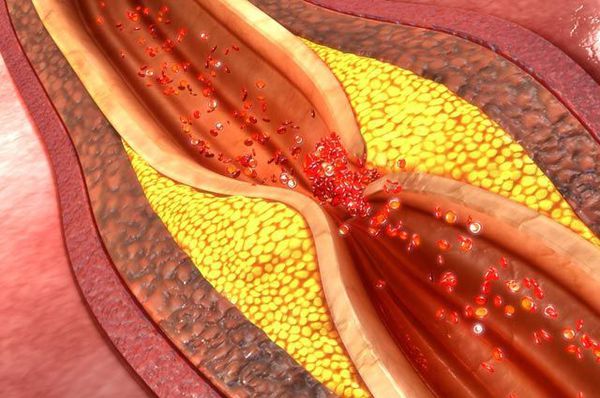
1. Атеросклеротическое поражение сердечных артерий и развитие в них тромбов при разрыве атеросклеротической бляшки.
2. Неатеросклеротическое поражение коронарных артерий, возникшее из-за воспалительного процесса в стенках артерий различной этиологии. Воспаление возникает в результате:
- травмы артерии;
- радиационных повреждений (в том числе при лучевой терапии рака),
- снижения коронарного кровотока из-за спазма коронарных артерий, расслоения аорты или коронарной артерии, эмболии (закупорки коронарных сосудов);
- врождённых аномалий коронарных сосудов;
- несоответствия между потребностями миокарда в кислороде и его доставкой;
- нарушения свёртывания крови.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы инфаркта миокарда
Симптоматика инфаркта миокарда зависит от периода развития заболевания: прединфарктного, острейшего, острого, подострого и постинфарктного.
Прединфарктный период инфаркта миокарда. В прединфарктном периоде могут возникать кардиальные (касаются работы сердца) и некардиальные симптомы. К кардиальным сиптомам относятся: боли за грудиной, одышка, сердцебиения, аритмии. К некардиальным — слабость, потливость, головокружения, ощущение тяжести и боли в области желудка (в эпигастрии). В прединфарктном периоде могут наблюдаться только некардиальные симптомы при наличии аритмии и одышки (или без), но сам период проходит без болевых ощущений. При осмотре пациента можно обнаружить небольшой цианоз (посинение) губ, пространства под ногтевыми пластинами, аритмичный пульс, повышение болевой чувствительности кожи в области сердца.
Острейший период инфаркта миокарда. Болевой синдром — самый характерный симптом острейшего периода типичного инфаркта миокарда. У большинства пациентов наблюдаются чрезвычайно интенсивные боли сжимающего, давящего характера. Больные сравнивают давление с обручем или железными клещами, или с тяжёлой плитой, лежащей на груди. Могут ощущаться интенсивные жгучие (пожар в груди, ощущение кипятка, льющегося на грудь) или кинжальные боли. Болезненные ощущения сильнее, чем при обычном приступе стенокардии. Их интенсивность зависит от размера инфаркта миокарда и возраста больного. Тяжёлый и длительный приступ боли чаще наблюдается при обширных инфарктах. Более интенсивные боли наблюдаются у молодых больных по сравнению с лицами пожилого и старческого возраста. Нужно отметить, что слабо выраженные боли при инфаркте миокарда могут быть у больных с сахарным диабетом из-за повреждения вегетативной нервной системы и снижения болевой чувствительности.
Локализация боли:
- за грудиной (чаще всего);
- часто распространяется на прекордиальную зону (слева от края грудины) или на всю переднюю поверхность грудной клетки;
- в загрудинной области и справа от края грудины;
- в подложечной области (эпигастрии).
При осмотре больного кожные покровы бледные, повышена их влажность, отмечается цианоз (посинение) губ, ушей, носа, пространств под ногтями. Может наблюдаться небольшое увеличение частоты дыхания. Часто наблюдается учащение пульса до 90-100 ударов в минуту, однако в начале болевого приступа может возникать непродолжительное урежение ритма сердца (брадикардия), пульс может быть аритмичным.
Боль часто иррадиирует (распространяется) в другие части тела, как правило — в левую руку, иногда в обе, иногда появляется ощущение сильной сжимающей боли в запястьях (симптом «наручников», «браслетов»). Реже отдаёт в левое плечо, левую лопатку, область между лопаток, шею, нижнюю челюсть, ухо, глотку. Совсем редко — в правую руку и другие части тела. Возможны случаи, когда боль воспринимается больным преимущественно в зоне иррадиации, что затрудняет диагностику.
Для инфаркта очень характерен волнообразный характер боли в области сердца. Боль постепенно нарастает, усиливается, иногда становится невыносимой, затем её интенсивность несколько снижается. Однако вскоре боль снова нарастает и становится ещё сильнее. В среднем боли продолжаются несколько десятков минут (всегда больше 20-30 минут), иногда несколько часов, в некоторых случаях в течение одних-двух суток (при увеличении зоны некроза сердечной мышцы).
Во время приступа интенсивной боли при очень сильном возбуждении могут появляться галлюцинации.
В отдельных случаях боль в области сердца может быть не очень интенсивной или даже отсутствовать совсем. У таких больных развиваются атипичные формы инфаркта миокарда, когда на первый план выступает не болевой приступ, а другие проявления (например, аритмии или удушье).
Острый период инфаркта миокарда. В остром периоде окончательно формируется очаг некроза, боль обычно к этому моменту исчезает. Если боль сохраняется, то это может быть связано с расширением зоны инфаркта. Пульс учащённый, артериальное давление снижается.
Атипичные формы инфаркта миокарда. В ряде случаев могут возникать атипичные формы инфаркта миокарда. Они формируются из-за пожилого возраста, развитие инфаркта на фоне тяжело протекающей артериальной гипертензии или сердечной недостаточности, а также у тех, кто уже перенёс инфаркт ранее. Другими факторами являются: повышение порога болевой чувствительности, поражение вегетативной нервной системы с иннервацией (переходом от очага заболевании) боли в сердце (к примеру, при сахарном диабете или у больных алкоголизмом). Симптомы зависят от формы атипично протекающего инфаркта миокарда.
| Форма инфаркта миокарда | Симптомы |
|---|---|
| Периферическая форма с нетипичной локализацией боли | Боль различной интенсивности в области левой руки, левой лопатки, горла (по типу болей при ангине), шейно-грудного отдела позвоночника, нижней челюсти (воспринимается как зубная боль). Боль в области сердца отсутствует или неинтенсивная. Могут возникать слабость, головокружения, потливость, внезапное появление сердцебиений, аритмий, падение артериального давления. |
| Абдоминальная форма при диафрагмальном (заднем) инфаркте | Интенсивные боли наблюдаются в эпигастрии (верхней части живота), иногда в области правого подреберья или во всей правой половине живота. Боли часто сопровождаются тошнотой, рвотой, не приносящей облегчения, вздутием живота вследствие непроходимости кишечника и желудка. Возможно развитие желудочно-кишечного кровотечения. Живот болезненный в верхней половине, в правом подреберье, мышцы передней брюшной стенки напряжены. |
| Астматическая форма — сердечная астма | Возникает внезапный приступ удушья с кашлем и выделением пенистой мокроты розового цвета, характерны холодный пот и посинение конечностей. В нижних отделах лёгких можно услышать мелкопузырчатые хрипы. Боли в области сердца отсутствуют или выражены очень слабо. |
| Коллаптоидная форма (кардиогенный шок при повторных, обширных сквозных инфарктах миокарда) | Внезапно развивается обморочное состояние, беспокоят головокружения, потемнение в глазах, артериальное давление падает. Боль в области сердца отсутствует или не интенсивна. Появляется холодный пот, пульс частый и слабый, возможно появление аритмии. |
| Отёчная форма (при обширных и повторных инфарктах, приводящих к развитию сердечной недостаточности) | Появляется одышка, слабость, беспокоят сердцебиения, перебои в работе сердца, отёки в области голеней и стоп, в наиболее тяжёлых случаях наблюдается асцит (скопление жидкости в брюшной полости). |
| Аритмическая форма | Нарушение ритма в виде приступообразной мерцательной аритмии или тахикардии, частой экстрасистолии (аритмических сокращений), внезапно развивающейся атрио-вентрикулярной блокады. Болевой синдром в области сердца отсутствует. Наблюдается чаще при обширных, острых или повторных инфарктах, особенно у пожилых больных. Характерны клинические проявления ишемии головного мозга: головокружения, шум в ушах, потемнение в глазах, обморочные состояния. |
| Цереброваскулярная форма | На первый план выступают симптомы ишемии (недостаточного кровоснабжения) мозга. Чаще наблюдается у лиц пожилого возраста с выраженным поражением артерий головного мозга атеросклерозом, чаще у мужчин. Симптомы обусловлены динамическим нарушением мозгового кровоснабжения. Наблюдаются головокружения, потемнение в глазах, шум в ушах, тошнота, обмороки, преходящие нарушения зрения, слабость в конечностях, очаговая неврологическая симптоматика. Боли в области сердца, как правило, отсутствуют, артериальное давление чаще снижено. Реже наблюдается органическое нарушение мозгового кровообращения. Обычно в этом случае наблюдается тромбоз артерий мозга и развивается ишемический инсульт. Органическое нарушение кровоснабжения мозга проявляется парезами (снижением силы мышц), нарушением речи, очаговой неврологической симптоматикой. Могут развиваться нарушения психики в виде снижения критики своего состояния, галлюцинаций, иногда психозов. |
| Стёртая (малосимптомная) форма | Интенсивная боль в области сердца отсутствует. Наблюдаются нерезкие симптомы: непродолжительная слабость, потливость, ощущение нехватки воздуха. Симптомы быстро проходят. Больные не обращают на них внимание, не идут к врачу, им не проводится ЭКГ-исследование. Иногда наблюдается форма инфаркта миокарда совсем без симптомов, которая выявляется случайно при обнаружении на ЭКГ рубцовых изменений сердечной мышцы. |
| Комбинированная атипичная форма | Наблюдается сочетание клинических признаков из различных атипичных форм. |
Патогенез инфаркта миокарда
В основе развития инфаркта миокарда лежат три компонента:
1. Разрыв атеросклеротической бляшки.
2. Тромбоз (образование тромба и закупорка им коронарной артерии).
3. Вазоконстрикция (резкое сужение коронарной артерии).
Разрыв атеросклеротической бляшки или эрозия её поверхности происходит следующим образом. В бляшке развивается воспалительная реакция, мощным стимулятором которой является окисление проникающих в неё липопротеинов низкой плотности (одной из вредных фракций холестерина). После чего в бляшку поступают макрофаги (клетки, пожирающие другие вредоносные для организма клетки) и начинают продуцировать ферменты, разрушающие фиброзную покрышку бляшки. Прочность покрышки снижается и происходит разрыв.
Факторы, провоцирующие надрыв или разрыв атеросклеротической бляшки:
- накопление в бляшке окисленных липопротеинов низкой плотности;
- значительное давление крови на края бляшки;
- выраженный подъём артериального давления;
- курение;
- интенсивная физическая нагрузка.
В области повреждения бляшки происходит прилипание и склеивание тромбоцитов, что приводит к закупорке коронарной артерии. При разрыве бляшки кровь поступает внутрь, взаимодействуя с ядром бляшки. Тромб сначала образуется внутри бляшки, заполняет её объем, а затем распространяется в просвет коронарной артерии. При внезапном полном закрытии просвета коронарной артерии тромбом развивается сквозной инфаркт миокарда — некротизируется (омертвевает) вся толща сердечной мышцы. Сквозной инфаркт миокарда протекает тяжелее и более опасен в плане осложнений и смертельного исхода, чем мелкоочаговый несквозной инфаркт миокарда.
При неполной закупорке коронарной артерии (если тромб растворяется спонтанно или при помощи лекарств) формируется несквозной (нетрасмуральный) инфаркт миокарда.
В развитии закупорки просвета коронарной артерии большую роль играет спазм артерии, который обусловлен нарушением функции эндотелия, влиянием сосудосуживающих веществ, которые выделяют тромбоциты во время образования тромба. В итоге это приводит к спазму артерий, а тромбоциты начинают склеиваться ещё активней.
Развитие спазма коронарных артерий увеличивает степень её закупорки, вызванной атеросклеротической бляшкой и тромбом. Ток крови прекращается, что вызывает некроз миокарда [6][7].
Классификация и стадии развития инфаркта миокарда
Инфаркт миокарда можно классифицировать следующим образом [6]:
1. По глубине и обширности некроза на основе данных ЭКГ:
1.1. Крупноочаговый (обширный) QS или Q-инфаркт (ИМ с патологическим зубцом QS и Q на ЭКГ):
- крупноочаговый трансмуральный (т.е. сквозь всю стенку миокарда) (ИМ с патологическим зубцом QS);
- крупноочаговый нетрансмуральный (ИМ с патологическим зубцом Q).
1.2. Мелкоочаговый «не Q»инфаркт миокарда (без патологического зубца Q):
- субэндокардиальный (очаг некроза располагается только во внутренних субэндокардиальных слоях стенки сердца);
- интрамуральный (очаг некроза расположен в средних мышечных слоях стенки сердца).
2. По локализации инфаркта миокарда:
- инфаркт левого желудочка: передний; переднеперегородочный; верхушечный; переднебоковой; боковой; задний; заднебоковой; передне-задний;
- инфаркт миокарда правого желудочка;
- инфаркт миокарда предсердий.
3. По периодам развития инфаркта:
- прединфарктный (продромальный) — период нарастания тяжести уже имеющейся у пациента ишемической болезни сердца; продолжается от нескольких часов до 1-го месяца, наблюдается у 70-80% больных; одним из вариантов этого периода могут быть впервые возникшая стенокардия или рецидив стенокардии после длительного безболевого периода; наблюдается у больных после ранее перенесенного инфаркта или аорто-коронарного шунтирования; возможен безболевой вариант продромального периода;
- острейший — от момента возникновения недостаточного кровоснабжения миокарда до начала формирования очага некроза сердечной мышцы; продолжительность колеблется от 30 минут до 2-х часов (максимально до четырёх часов); опасен в плане возникновения жизнеугрожающих осложнений;
- острый — окончательно образуется очаг некроза, в нем формируется миомаляция (размягчение некротизированной мышечной ткани); продолжается от 2 до 14 дней, опасен в плане возникновения жизнеугрожающих осложнений;
- подострый — формируется полные замещение некротических масс молодой соединительной тканью, образующейся при процессах заживления дефектов в различных тканях и органах, на фоне очага некроза формируется рубец из соединительной ткани; длительность колеблется от 6 до 8 недель при неосложнённом инфаркте в зависимости от размера зоны некроза, возраста больного, а также наличия или отсутствия осложнений;
- постинфарктный (ближайший — 2-6 месяцев, отдалённый — после полугода) — на месте некроза миокарда полностью формируется рубец из соединительной ткани; сердечно-сосудистая система максимально полно адаптируется к новым условиям функционирования, когда омертвевший зарубцевавшийся участок сердечной мышцы выключается из сократительной функции.
4. По особенностям клинического течения:
- затяжное течение, рецидивирование, повторный инфаркт миокарда;
- неосложнённый инфаркт миокарда; инфаркт миокарда с осложнениями;
- типичное течение (классический вариант), атипичный инфаркт миокарда.
Осложнения инфаркта миокарда
Осложнения при инфаркте усугубляют течение заболевания и определяют его прогноз. Чаще всего встречаются следующие осложнения:
- Нарушения сердечного ритма и проводимости. Наблюдаются у 90-95 % больных в первые сутки после инфаркта. За такими нарушениями важно следить, так как они способны привести к смерти. Тяжёлые аритмии (например приступообразная желудочковая тахикардия) могут провоцировать развитие сердечной недостаточности. Степень выраженности и характер нарушений зависят от обширности, глубины, локализации инфаркта миокарда, а также от предшествующих заболеваний. Возможно возникновение аритмий сердца даже после восстановления кровотока (возникают так называемые «реперфузионные аритмии») [9].
- Острая сердечная недостаточность. К развитию острой сердечной недостаточности приводят обширные, сквозные инфаркты. Наиболее тяжёлая степень острой сердечной недостаточности левого желудочка проявляется сердечной астмой и отёком лёгких. Возникает выраженное удушье, ощущение нехватки воздуха, сильное чувство страха смерти. Больной ведёт себя беспокойно, судорожно хватает ртом воздух, находится в вынужденном полувозвышенном или сидячем положении. Дыхание частое, поверхностное. При прогрессировании недостаточности появляются кашель с отделением пенистой розовой мокроты и «клокочущее» дыхание, на расстоянии слышны влажные хрипы (симптом «кипящего самовара»). Симптомы указывают на развитие отёка лёгких. При прогрессировании левожелудочковой недостаточности и присоединении недостаточности правого желудочка у больного появляются чувство тяжести и боль в правом подреберье, что связано с острым набуханием печени. Видно набухание шейных вен, которое усиливается при надавливании на увеличенную печень. Появляется отёчность голеней и стоп.
- Кардиогенный шок. Развивается при крайней степени левожелудочковой недостаточности, из-за которой снижается сократительная функция миокарда. Это не компенсируется повышением тонуса сосудов и приводит к нарушению кровоснабжения всех органов и тканей, прежде всего жизненно важных. Систолическое артериальное давление падает до 80-70-ти мм рт. ст. и ниже [5].
- Аневризма левого желудочка. Это ограниченное выбухание тканей сердца, которые подверглись размягчению, истончению и потеряли сократительную способность. Из-за аневризмы определённый объём крови выключается из циркуляции. Постепенно на этом фоне может развиться сердечная недостаточность. При аневризме сердца могут развиваться тромбоэмболические осложнения. Часто возникают приступообразные нарушения ритма. Опасность заключается ещё и в том, что аневризма может расслоиться и разорваться.
- Ранняя постинфарктная стенокардия. Это частые приступы стенокардии напряжения и покоя, возникающие в госпитальном периоде. Иногда может развиваться при недостаточном растворении тромба с помощью тромболитической терапии. При стенокардии прогноз неблагоприятный, так как она может предвещать рецидив инфаркта и даже внезапную смерть.
- Перикардит. Воспаление наружной оболочки сердца наблюдается при сквозном и обширном инфаркте. При перикардите, как правило, прогноз благоприятен.
- Тромбоэмболические осложнения. Закупорка кровеносного сосуда тромбом может произойти из-за повышения свёртывающей активности крови, атеросклеротического поражения артерий, тромбоза в зоне инфаркта миокарда, наличия тромба в аневризме левого желудочка. Возникновению тромбоэмболических осложнений способствуют воспаления внутренней оболочки стенок вен нижних конечностей, длительный постельный режим и выраженная недостаточность кровообращения. Важно отметить, что в связи с активным применением терапии, направленной на растворение тромба, тромбоэмболии возникают нечасто, всего лишь у 2-6 % больных.
- Тромбоэндокардит. Это асептическое (без участия микробов) воспаление внутренней стенки сердца с образованием пристеночных тромбов в области некроза.
- Нарушения мочеиспускания. После инфаркта может возникнуть значительное снижение тонуса мочевого пузыря и задержка мочеиспускания. Наиболее часто это имеет место в первые дни заболевания у мужчин пожилого возраста с доброкачественной гиперплазией (увеличением) предстательной железы. Появляются жалобы на невозможность помочиться, ощущение переполненности мочевого пузыря и боли внизу живота.
- Осложнения со стороны желудочно-кишечного тракта. У больных могут возникать острые эрозии и язвы желудочно-кишечного тракта. Причина их развития — выброс в кровь высоких доз глюкокортикоидных гормонов как ответ на стресс, что усиливает выделение желудочного сока. При застойной сердечной недостаточности развиваются отёк слизистых и гипоксия (недостаточное насыщение кислородом), вызывающие изменения слизистой оболочки желудочно-кишечного тракта. Острые эрозии и язвы желудка и двенадцатиперстной кишки проявляются болями после еды, возможны ночные и «голодные» боли, изжога, рвота. У лиц пожилого возраста частым осложнением инфаркта становится парез (непроходимость) желудочно-кишечного тракта из-за уменьшения тонуса кишечной стенки и паралича мускулатуры кишечника. Основные симптомы — икота, ощущение переполненности желудка после еды, рвота, выраженное вздутие живота, отсутствие стула, разлитая болезненность живота при ощупывании.
- Постинфарктный аутоиммунный синдром Дресслера. Развивается у 3-4 % больных со 2 по 8 неделю после начала инфаркта миокарда. Иммунная система при этом синдроме начинает атаковать собственные клетки, воспринимая здоровые ткани в качестве чужеродных элементов. Это проявляется в виде следующих симптомов: перикардит (воспаление перикарда), плеврит (воспаление плевры), пневмонит (воспаление в тканях лёгких), лихорадка, повышение в крови эозинофилов, увеличение СОЭ (скорости оседания эритроцитов). Часто в воспалительный процесс вовлекаются суставы, развивается синовит (воспаление в синовиальной оболочке сустава), чаще поражаются крупные плечевые, локтевые, лучезапястные суставы.
- Синдром передней грудной клетки. Синдром плеча и руки. Развиваются у больных с остеохондрозом межпозвонковых дисков шейно-грудного отдела позвоночника спустя несколько недель и даже месяцев после возникновения инфаркта миокарда. При синдроме передней стенки грудной клетки возникает поражение грудинно-рёберных суставов. Появляется припухлость и боль в окологрудинных областях, усиливающиеся при надавливании на грудину и грудинно-рёберные сочленения, при поднятии рук кверху. При синдроме плеча и руки возникают боли в левом плечевом суставе (чаще всего), также могут быть боли в правом или в обоих плечевых суставах. Боли усиливаются при движении.
- Психические нарушения. Нарушения психики обычно развиваются на первой неделе заболевания из-за нарушения гемодинамики мозга, гипоксемии (понижения содержания кислорода в крови) и влияния продуктов распада некротического (омертвевшего) очага миокарда на головной мозг. Чаще всего расстройства психики наблюдаются у больных старше 60-ти лет с атеросклерозом сосудов головного мозга. Возникают психотические (оглушённость, оцепенение, делирий, сумеречные состояния) и непсихотические реакции (депрессивный синдром, эйфория).
Диагностика инфаркта миокарда
Постановка диагноза в большинстве случаев не представляет трудностей. Врач опирается на типичную клиническую картину, данные электрокардиографии и определение в крови биомаркеров некроза сердечной мышцы.
При подозрении на инфаркт миокарда сразу же необходимо выполнить ЭКГ (электрокардиография). Если есть возможность, рекомендуется сравнить ЭКГ, записанную в момент болевого приступа, с ранее зарегистрированной ЭКГ. ЭКГ следует записывать неоднократно, делая динамическое ЭКГ-наблюдение: иногда в первые часы и даже несколько первых дней ЭКГ-признаки инфаркта неубедительны, и только на последующих ЭКГ появляется характерная картина болезни. В стационаре наиболее целесообразно проводить ЭКГ-мониторирование в течение 24 часов от начала развития инфаркта миокарда.
Лабораторные исследования включают в себя:
- Общий анализ крови. Отражает резорбционно-некротический синдром. Начиная с 4-6-го часа инфаркта миокарда на фоне нормальных значений СОЭ начинает появляться лейкоцитоз (повышение числа лейкоцитов) нередко со сдвигом формулы влево. Лейкоцитоз сохраняется до четырёх дней и к концу первой недели снижается. Начиная со второго дня инфаркта миокарда постепенно начинает расти СОЭ. К началу второй недели заболевания число лейкоцитов нормализуется. Сохранение лейкоцитоза и/или умеренной лихорадки более недели свидетельствует о возможном наличии осложнений: плеврита, пневмонии, перикардита, тромбоэмболии мелких ветвей лёгочной артерии и др.
- Биохимический анализ сыворотки крови. Маркерами гибели клеток сердечной мышцы (миоцитов) являются изменения концентрации в крови креатинфосфокиназы (КФК), лактатдегидрогеназы (ЛДГ), аспартатаминотрансферазы (АСАТ), а также содержание в крови миоглобина, кардиотропонинов Т и I (TnI и TnT) [2].
Эхокардиография позволяет выявить такие осложнения острого инфаркта миокарда, как образование пристеночных тромбов в полостях сердца, появление аневризмы сердца, разрыв межжелудочковой перегородки или отрыв сосочковых мышц. С помощью эхокардиографии выявляется важнейший признак инфаркта миокарда — нарушения локальной сократимости миокарда. Эти нарушения соответствуют распространённости некроза.
Экстренная селективная коронарная ангиография проводится в тех случаях, когда ЭКГ и анализ активности ферментов не дают результатов, либо же их интерпретация затруднена (например, в условиях наличия сопутствующих заболеваний, «смазывающих» картину). Исследование представляет собой рентгеновский снимок сосудов сердца, в которые предварительно введено контрастное вещество. С помощью ангиографии (коронарографии) можно установить закупорку коронарной артерии тромбом и снижение сократимости желудочка. С помощью этого метода оценивают, можно ли провести аортокоронарное шунтирование или ангиопластику — операции, восстанавливающие кровоток в сердце [7].
Лечение инфаркта миокарда
Пациента с острым инфарктом необходимо оперативно доставить в стационар для профилактики осложнений и повышения шансов на выживание. Система оказания помощи больным инфарктом миокарда включает следующие этапы:
- Догоспитальный этап. Помощь оказывают бригады скорой помощи, они же транспортируют больного в стационар.
- Госпитальный этап. Помощь оказывается в специализированных сосудистых отделениях.
- Реабилитационный этап. Реабилитация проводится в специальных отделениях больниц или специализированных кардиологических санаториях.
- Диспансерное наблюдение и амбулаторное лечение. Диспансеризация в постинфарктном периоде осуществляется в областных или городских кардиологических центрах или в кардиологических кабинетах поликлиник [6].
На догоспитальном этапе решаются следующие задачи:
- устанавливается точный диагноз. Если это не удаётся, допустимо установление ориентировочного синдромного диагноза в максимально короткое время;
- под язык больному дают таблетку нитроглицерина (или использовать нитросодержащий спрей) и 0,25-0,35 г аспирина;
- боль снимается введением обезболивающих;
- ликвидируется острая недостаточность кровообращения и нарушения ритма сердца;
- больного выводят из состояния кардиогенного шока;
- при клинической смерти производят реанимационные мероприятия;
- как можно скорее транспортируют больного в стационар.
Дальнейшая терапия определяется стадией (периодом) инфаркта миокарда. В остром и острейшем периоде цель лечения — предотвращение увеличения очага омертвения миокарда, устранение боли и других симптомов. Важно восстановить ток крови по сердечным артериям и купировать боль. Интенсивность боли в этом периоде настолько велика, что пациент может погибнуть из-за остановки сердца. Необходимо провести профилактику тяжёлых осложнений. При переходе болезни в подострую стадию и в постинфарктном периоде цель терапии — снижение риска рецидива приступа и возможных осложнений.
Для лечения острого инфаркта миокарда используются лекарственные препараты из различных фармакологических групп:
Обезболивающие препараты. Анальгетики из группы наркотических обезболивающих (морфин, промедол, омнопон) в сочетании с анальгином, антигистаминными препаратами (димедрол). Наиболее эффективной является нейролептанальгезия, когда используется комбинация анальгетика фентанила с сильным нейролептиком дроперидолом. Эффективность применения этих препаратов заметна уже через несколько минут. Исчезает не только боль, но и страх смерти, немотивированная тревога и психомоторное возбуждение. Для снятия психомоторного возбуждения могут использоваться транквилизаторы (диазепам). Для уменьшения гипоксии (снижения кислорода в тканях) используются ингаляции кислорода с помощью носового катетера.
Тромболитическая терапия. Важно восстановить ток крови и растворить тромбы, чтобы омертвение сердечной мышцы на распространялось дальше. Чем меньше зона некроза, тем выше шансы больного на успешную реабилитацию и ниже риск опасных для жизни осложнений. Немедленное применение препаратов (желательно в течение первого часа после приступа) позволяет достичь максимальную эффективность лечения. Допускается временной лимит в пределах трёх часов. Для растворения тромба внутривенно вводятся тромболитические препараты, например, стрептокиназа, урокиназа, альтеплаза. Доза зависит от веса пациента.
Восстановление коронарного кровотока возможно также с помощью хирургического лечения — стентирования или аорто-коронарного шунтирования. Баллонный катетер вводится в узкий участок артерии под контролем рентгеноскопии. При этом атеросклеротическая бляшка «раздавливается», а просвет артерии сердца увеличивается. Затем в просвет сосуда может быть установлен стент (металлический каркас).
Антиагреганты. Препараты из этой группы влияют на клетки крови (тромбоциты и эритроциты). Действие антиагрегантов препятствует слипанию тромбоцитов, улучшая кровоток. Основным применяемыем препаратом является аспирин (ацетилсалициловая кислота). Противопоказания к применению аспирина: кровотечения из желудочно-кишечного тракта, обострение язвы желудка или двенадцатиперстной кишки.
Используются также ингибиторы P2Y12-рецепторов тромбоцитов, которые блокируют активацию тромбоцитов. Основные блокаторы — тикагрелор, прасугрел и клопидогрел.
Внутривенные/подкожные антикоагулянты. При остром коронарном синдроме для профилактики тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА) в остром периоде применяется нефракционированный гепарин (НФГ), который вводится внутривенно. Эноксапарин, который используется также для профилактики венозных тромбоэмболий, вводится подкожно.
Чтобы ограничить зону ишемии и некроза миокарда необходимо кроме восстановления кровотока в артериях сердца уменьшить гемодинамическую нагрузку на сердце. С этой целью используются нитраты и бета-блокаторы.
Нитраты. Оказывают противоболевой эффект, уменьшают потребность миокарда в кислороде, увеличивают коронарный и коллатеральный (обходной) кровоток, снижают нагрузку на сердечную мышцу, ограничивают размеры очага поражения миокарда. Особенно эффективна комбинация их с бета-блокаторами, приводящая к быстрой положительной динамике ЭКГ и снижению риска внезапной смерти [10].
Бета-адреноблокаторы оказывают антиаритмическое действие. Цель применения бета-адреноблокаторов (пропранолола, метопролола, атенолола) — уменьшение частоты и силы сердечных сокращений, что поможет уменьшить нагрузку на сердце и потребность миокарда в кислороде. Бета-блокаторы продолжают применять при отсутствии побочных эффектов и противопоказаний неопределённо длительное время [1].
Прогноз. Профилактика
Общий уровень смертности от инфаркта миокарда составляет примерно 30 %, от 50 до 60 % больных умирают на догоспитальном этапе. Летальность в стационаре составляет около 10 %.
Клинические характеристики, предсказывающие высокую (до 90 %) смертность у больных:
- пожилой и старческий возраст (31 % общей смертности);
- низкое систолическое артериальное давление (24 %);
- высокая частота сердечных сокращений (12 %);
- передняя локализация инфаркта миокарда (6 %).
Смертность среди больных сахарным диабетом и женщин несколько выше.
Смертность среди пациентов с первичным инфарктом миокарда составляет 8-10 % в первый год после острого инфаркта миокарда. Большинство смертей происходит в первые 3-4 месяца. Постоянная желудочковая аритмия, сердечная недостаточность и сохраняющаяся ишемия являются маркерами высокого риска смерти. Низкая переносимость физических нагрузок также ассоциируется с плохим прогнозом.
Профилактика инфаркта миокарда подразделяется на первичную и вторичную [3].
Первичная профилактика проводится при наличии каких-либо проблем с сердцем, но до того, как произошёл инфаркт. В неё входят:
- Физическая активность — малоподвижный образ жизни отрицательно влияет на сердечно-сосудистую систему, а занятия спортом помогают сбросить избыточный вес, повышающий риск атеросклероза и нагрузку на сердце.
- Отказ от вредных привычек — курение табака способствует развитию и прогрессированию атеросклероза. Алкоголь следует употреблять в небольшом количестве. Излишнее употребление алкоголя оказывает токсическое действие на сердечную мышцу и другие органы, может вызывать аритмии и сосудистый спазм (сужение сосудов).
- Правильное питание — включение в ежедневный рацион свежих овощей, фруктов и зелени. Жирное мясо (свинину) лучше заменить на мясо птицы или кролика. Полезны рыба и морепродукты. Необходимо ограничить приём соли. При экстрасистолии нельзя употреблять пряности, так как они могут спровоцировать развитие аритмии.
- Контроль над стрессом — отдых, полноценный сон (не менее восьми часов в сутки). Стрессы и депрессии могут провоцировать инфаркт, так как под их влиянием происходит спазм сосудов сердца. Некоторым людям необходимо пройти курс лечения у психолога.
- Регулярные посещения кардиолога — после 40 лет осмотр рекомендуется делать ежегодно. Обязательно необходимо делать ЭКГ-исследование, проводить определение липидного профиля (общего холестерина и его фракций), контролировать уровень сахара в крови.
- Контроль за давлением — разрыв атеросклеротической бляшки зачастую провоцирует повышенное артериальное давление. При выявленной артериальной гипертензии необходим своевременный постоянный приём гипотензивных (снижающих артериальное давление) препаратов, назначенных кардиологом.
Вторичная профилактика инфаркта миокарда необходима тем, кто уже перенёс инфаркт. Она направлена на предотвращение повторного инфаркта миокарда и длится всю жизнь. Помимо мер, которые применяются для первичной профилактики инфаркта, обязательно постоянное применение медикаментозных препаратов, назначенных врачом:
- двойная антиагрегантная терапия (аспирин и второй антиагрегант — тикагрелор или клопидогрел) в течение года после инфаркта миокарда для снижения риска сердечно-сосудистых событий; первичная профилактика аспирином не нужна;
- бета-блокаторы для уменьшения частоты сердечных сокращений и снижения уровня артериального давления;
- статины для снижения уровня холестерина и предотвращения прогрессирования атеросклероза;
- нитраты для купирования болевых приступов при возобновлении стенокардии;
- ингибиторы АПФ или сартаны для нормализации артериального давления, а также при наличии признаков сердечной недостаточности.
Обязателен регулярный контроль за состоянием больного, уровнем артериального давления, показателями биохимии (в частности уровнем печёночных ферментов и показателями липидного профиля), изменениями на ЭКГ, эхокардиографии. При необходимости проводится суточное мониторирование ЭКГ.