Проблемы диагностики и лечения рассеянного склероза
Статьи
Опубликовано в журнале:
Мир Медицины »» №5-6’2000 »» Новая медицинская энциклопедия Диагностика и лечение с позиций доказательной медицины
За последнее десятилетие рассеянный склероз из неизлечимой болезни перешел в категорию частично управляемых. В этих условиях точная диагностика становится необходимым инструментом, определяющим последующее лечение. О проблемах диагностики и лечения рассеянного склероза рассказывает канд. мед. наук, доцент кафедры невропатологии и нейрохирургии СПбГМУ им. акад. И.П. Павлова Наталья Агафоновна Тотолян.
Вопросам диагностики и лечения рассеянного склероза (PC) ежегодно посвящаются десятки публикаций в отечественной медицинской литературе. Тем не менее, анализ частоты диагностических ошибок при постановке диагноза «рассеянный склероз» показывает, что эта проблема остается весьма актуальной. По данным клиники неврологии СПбГМУ им. акад. И.П. Павлова за 1998-1999 гг., частота ошибочного — ложно положительного или ложно отрицательного -диагноза при направлении в стационар составила 37% (30 случаев из 81). При этом большинство пациентов (66) имели «стаж» заболевания от 1 до 10 лет и прошли различные диагностические процедуры. Лишь у 15 имел место первый эпизод PC (дебют), именно в этой подгруппе ошибочный предварительный диагноз был установлен у 10 человек (67%).
Причины столь частых диагностических ошибок (иногда ценою в 5-10 лет) во многом определяются крайне широким спектром клинических проявлений болезни. С 1983 года в исследовательскую и клиническую практику вошли и стали общепринятыми разработанные международной группой экспертов критерии диагностики PC (табл. 1). Однако за годы их применения стало очевидным, что перечень заболеваний, сходных с PC как по клиническим проявлениям, так и по данным дополнительных методов исследования, постоянно растет (табл. 2).
Таблица 1
|
КРИТЕРИИ ДИАГНОЗА РАССЕЯННОГО СКЛЕРОЗА (C.M. POSER ET AL., 1983) |
|
| КАТЕГОРИЯ | КРИТЕРИИ |
| Клинически достоверный | 1) 2 обострения + 2 клинических очага 2) 2 обострения + 1 клинический очаг +1 параклинический очаг* |
| Достоверный, подтвержденный лабораторно | 1) 2 обострения + 1 клинический или параклинический очаг + олигоклональные полосы или повышенный синтез IgG в ЦСЖ 2) 1 обострение + 2 клинических очага+ олигоклональные полосы или повышенный синтез IgG в ЦСЖ 3) 1 обострение + 1 клинический очаг + 1 паракпинический очаг + олигоклональные полосы или повышенный синтез IgG в ЦСЖ |
| Клинически вероятный | 1) 2 обострения + 1 клинический очаг 2) 1 обострение + 2 клинических очага 3) 1 обострение + 1 клинический очаг + 1 параклинический очаг |
| Вероятный, подтвержденный лабораторно | 2 обострения + олигоклональные полосы или повышенный синтез IqG в ЦСЖ |
* — очаг, зарегистрированный методами МРТ или вызванных потенциалов
Таблица 2
|
ЗАБОЛЕВАНИЯ, ТРЕБУЮЩИЕ ДИФФЕРЕНЦИАЛЬНОГО ДИАГНОЗА С РС |
|||
|
ГРУППА ЗАБОЛЕВАНИЙ И/ИЛИ НОЗОЛОГИЧЕСКАЯ ФОРМА |
ВОЗМОЖНО СХОДСТВО С PC ПО ПАРАМЕТРАМ: |
||
| КЛИНИЧЕСКИМ | МРТ | ЦСЖ | |
| ВАСКУЛИТЫ: Синдром Шегрена Узелковый периартериит Системная красная волчанка Гранулематоз Вегенера Гигантоклеточный артериит |
+ + + + |
+ + |
+ + + |
| ДРУГИЕ СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ: Протромботические состояния Субкортикальная артериосклеротическая энцефалопатия (Бинсвангера) CADASIL Мигрень |
+ + |
+ + |
|
| ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ: Острый диссеминированный энцефаломиелит Саркоидоз Болезнь Бехчета Паранеопластические синдромы Хроническая воспалительная демиелинизирующая полиневропатия Острая воспалительная полиневропатия (Гийена-Барре) |
+ + + + |
+ + + + + |
+ + + + |
| ИНФЕКЦИИ: Вирусные энцефалиты Нейроборрелиоз Инфекция HTLV-I СПИД Нейросифилис Подострый склерозирующий панэнцефалит Прогрессирующий краснушный энцефалит Хронические грибковые менингиты Прогрессирующая мультифокальная лейкоэнцефалопатия Туберкулез |
+ + + + |
+ + + + + + + |
+ + + + |
| ГЕРЕДИТАРНЫЕ ЗАБОЛЕВАНИЯ: Адренолейкодистрофия Зрительная атрофия Лебера Спиноцеребеллярные дегенерации Митохондриальные энцефалопатии Лейкодистрофии |
+ + + + |
+ + + + + |
+ + |
| ДРУГИЕ ЗАБОЛЕВАНИЯ: Подострая комбинированная дегенерация спинного мозга (дефицит витамина В12) Мальформация Арнольда-Киари Экстра- и интрамедуллярные компрессионные поражения спинного мозга Опухоли головного мозга Множественные метастазы в головной мозг |
+ + |
+ + |
В практической работе для точной диагностики PC на ранних стадиях болезни (при первом обострении и особенно при первично-прогрессирующем течении) недостаточно только клинических данных, так же как инструментальные и лабораторные тесты не всегда могут обеспечить необходимую точность диагностики. Следует также отметить, что в публикациях о многочисленных предлагаемых «методах диагностики» PC (различных иммунологических тестах, электрофизиологических методах, методах функциональной нейровизуализации, нейроофтальмологических тестах) не отражена их реальная значимость — в большинстве случаев отсутствует анализ диагностической эффективности: чувствительности и специфичности. В дальнейшем практическое использование этих методов зачастую вызывает разочарование, главным образом, в связи с низкой специфичностью.
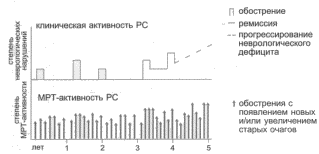
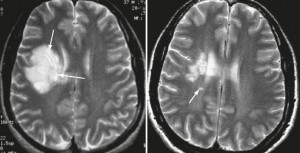
Рис. 1. Соотношение клинических и МРТ-проявлений активности РС.
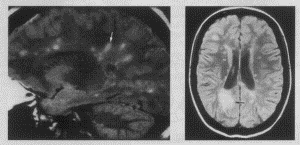
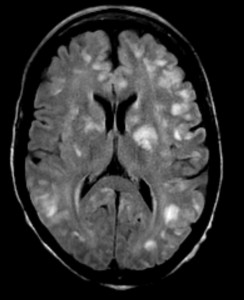
Рис. 2, 3. Типичное расположение очагов РС на МР-томограммах.
- Чувствительность
диагностического метода определяется как процент положительных результатов теста при наличии
диагностируемого заболевания.
диагностического метода определяется как процент отрицательных результатов теста при отсутствии диагностируемого заболевания.
Алгоритм современной диагностики PC
Для PC справедливы общие законы диагностики: первостепенное значение имеют клинические данные, а результаты дополнительных методов исследования подтверждают или исключают диагноз.
Клинические данные
Первые клинические симптомы могут включать
- развивающиеся подостро расстройства чувствительности (ее снижение или парестезии в конечностях),
- мышечную слабость в одной или нескольких конечностях,
- ухудшение зрения на один глаз (поражение зрительного нерва),
реже — системное головокружение с тошнотой, шаткость, иногда — симптомы поражения других черепных нервов, и в единичных случаях — дисфункцию мочевого пузыря. Особенно характерно развитие этих симптомов в возрасте 20-45 лет. Установление при неврологическом осмотре признаков многоочаговости процесса делает диагноз PC более вероятным. Вышеперечисленные симптомы, особенно их сочетания, по меньшей мере в половине случаев оказываются проявлениями PC. Однако только клинических данных недостаточно для точного диагноза. Еще сложнее диагностическая ситуация, когда имеют место редкие проявления болезни, а также ее начало после 50 лет или в детском возрасте.
Магнитно-резонансная томография
Следующим шагом после клинического предположения о PC является магнитно-резонансная томография (МРТ) — метод выбора инструментальной диагностики PC. Это неинвазивное и безопасное исследование позволяет визуализировать патологические очаги в центральном нервной системе, демонстрируя необходимую для диагностики диссеминацию процесса в пространстве (многоочаговость) и во времени (очаги «разного возраста», а также исследование в диамике). Это наиболее информативный инструментальный метод диагностики PC. Его чувствительность при разных формах PC -85-95%. Однако общепринятые МРТ-критерии PC (табл. 3) следует использовать лишь в качестве базисных. Разработаны дополнительные МРТ-характеристики, которые повышают специфичность метода. Они включают определенные варианты локализации и ориентации очагов, особенности проявлений отека вещества мозга и накопления контраста, а также изменения, наблюдаемые в динамике.
МРТ головного мозга является необходимой, а МРТ спинного мозга — желательной в диагностике PC. Последняя очень важна в мониторинге течения болезни и абсолютно необходима при спинальных формах PC. Следует особо подчеркнуть, что МРТ может служить эффективным методом диагностики только при соблюдении определенных условий:
- должна выполняться в соответствии со схемами, принятыми для оценки PC,
- должна проводиться на аппаратах с достаточной мощностью поля (0.5-1.5 Тесла). Использование аппаратов с низкой мощностью поля (0.05 Тесла) резко снижает диагностические возможности метода и служит источником ошибок.
Таблица 3
|
ДИАГНОСТИЧЕСКИЕ МРТ-КРИТЕРИИ РС |
|
| АВТОР, ГОД | КРИТЕРИИ |
| Paty D.W. et al.,1988 | Для лиц, моложе 50 лет, не имеющих факторов риска инсульта: 1) наличие 4 очагов или 2) наличие 3 очагов, 1 из которых перивентрикулярный 3) диаметр очагов в первом и втором случаях более 3 мм |
| Fazekas F. et al., 1988 | Включая лиц, старше 50 лет, имеющих факторы риска инсульта: 1) очаги, примыкающие к телам боковых желудочков 2) очаг субтенториальной локализации 3) очаг размером не менее 6 мм. Необходимо наличие не менее двух критериев |
Лабораторная диагностика PC
Несколько факторов определяют особенности современной лабораторной диагностики PC:
- 1. Не существует патогномоничного лабораторного теста, позволяющего безоговорочно устанавливать диагноз PC. По современным представлениям, PC является иммунологически-опосредованным заболеванием, сопровождающимся аутоиммунными реакциями с расширяющимся спектром аутоантигенов. Уже в дебюте болезни может выявляться сенсибилизация к нескольким аутоантигенам, а по мере прогрессирования PC спектр аутоиммунных реакций расширяется: появляются признаки аутоагрессии ко многим компонентам нервной ткани. Подобные аутоиммунные реакции могут наблюдаться при других хронических заболеваниях нервной системы. Ведущие биохимические сдвиги при PC определяются демиелинизацией в ЦНС. Однако выявление продуктов распада миелина также является неспецифическим, поскольку миелин разрушается при различных патологических процессах (опухолевом, сосудистом, травматическом и др.)
2. Высокую информативность в диагностике PC имеют только показатели цереброспинальной жидкости (ЦСЖ). Это определяется тем, что PC относится к органоспецифическим заболеваниям, причем органы-мишени (головной и спинной мозг) являются «забарьерными». Для PC не характерны системные клинические проявления. oОтсутствуют и эффективные лабораторные показатели, опирающиеся на системные сдвиги, то есть на параметры крови. Попытки найти «неинвазивные» тесты, используя для анализа другие биологические жидкости (слюну, мочу, слезную жидкость), также оказались безуспешными. Современные диагностические лабораторные показатели часто учитывают соотношение параметров ЦСЖ с соответствующими параметрами сыворотки крови.
Наиболее информативные из них приведены в табл. 4.
Таблица 4
|
ПОКАЗАТЕЛИ ЦСЖ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ДИАГНОСТИКИ РС |
||
| ПОКАЗАТЕЛЬ | ЧУВСТВИТЕЛЬНОСТЬ, % | СПЕЦИФИЧНОСТЬ, % |
| Индекс IgG Олигоклональные полосы IgG Содержание СЛЦ-к* Индекс СЛЦ-к |
70 85-95 97 97 |
80 85-95 87 98 |
* — свободные легкие цепи иммуноглобулинов к-типа
Они отражают очень характерные для PC сдвиги в гуморальном звене иммунного ответа, а именно: повышенную продукцию иммуноглобулинов и их компонентов в пределах нервной системы. Два показателя (индекс IgG
и олигоклонапьные полосы IgG) входят в международные критерии. Первый из них отражает количественные изменения в синтезе IgG. Он рассчитывается по формуле lgGцсж/lgGсыв: альбуминцсж /альбумисыв — и учитывает дисфункцию гемато-энцефалического барьера при PC. Олигоклональные полосы отражают главным образом качественные изменения синтеза IgG, так как у здоровых людей иммуноглобулины в ЦСЖ поликлональны. Индекс IgG уступает по информативности олигоклональным полосам, и в последнее время используется реже. Показатель содержания свободных легких цепей иммуноглобулинов к-типа (СЛЦ-к) признан по оценке международных экспертов как один из наиболее информативных. Он не включен в критерии PC главным образом из-за отсутствия стандартных наборов для выполнения этого теста.
Рядом лабораторий Санкт-Петербурга этот тест на основе отечественных реактивов уже в течение десяти лет успешно используется для диагностики PC. По сравнению с определением концентрации в ЦСЖ, оценка индекса СЛЦ-к (по формуле, аналогичной индексу IgG) еще более информативна. Оценка чувствительности и специфичности метода проведена с использованием данных тестирования более 500 больных PC и более 200 больных групп сравнения, причем последние включали подгруппы заболеваний, сходных с PC по клиническим, МРТ- и ЦСЖ-критериям. Метод дает возможность эффективной диагностики PC уже при первых клинических проявлениях (с длительностью симптомов менее 1 месяца): его чувствительность на ранних этапах болезни составляет 85%. Определение содержания СЛЦ-к в ЦСЖ и индекса СЛЦ-к является доступным и недорогим тестом, который в сегодняшних условиях можно считать методом выбора лабораторной диагностики PC.
Наряду с «общими иммунологическими чертами», при PC имеют место и более вариабельные иммунологические показатели. Более того, в последние годы с помощью иммуногистохимических и иммуноцитохимических методов получены новые патоморфологические данные, указывающие на наличие патоморфологических вариантов PC. На практике эта неоднородность заболевания может проявляться еще одним сложным аспектом: разным ответом (или отсутствием ответа) на проводимое лечение. В этих условиях целесообразен поиск показателей, характеризующих различные «варианты» PC и позволяющих прогнозировать эффект лечения.
Лечение PC
Основные факторы, определяющие современные подходы к лечению
Последнее десятилетие изучения PC привнесло ряд факторов, которые сегодня невозможно игнорировать при лечении больного PC.
- 1. МРТ-исследованиями показано, что патологический процесс при PC проявляет почти постоянную активность: при частоте клинических обострений 0.5-1 раз в год обострения по данным МРТ регистрируются 8-10 раз в год в виде новых очагов или увеличения имевшихся ранее (рис. 1). Фактор непрерывной активности патологического процесса определяет необходимость непрерывного лечения PC.
- Отсутствие новых симптомов в период клинической ремиссии PC не свидетельствует о стабилизации патологического процесса, а может быть связано с отсутствием в очагах грубых нарушений проведения импульсов (воспаление без выраженной демиелиниэации и повреждения аксонов) или с локализацией очагов в функционально малозначимых зонах.
- 2. Клиническая гетерогенность PC, а также фактор плацебо-эффекта потребовали изменения условий оценки эффективности лечения, направленного на модификацию течения болезни. 3/4 случаев PC характеризуются клиническими обострениями (от нескольких дней до нескольких месяцев) и спонтанными ремиссиями, часто с полным регрессом симптомов (длительностью от 1-2 месяцев до 10-15 лет). При этом даже у одного больного длительность очередного обострения или ремиссии непредсказуема. В 1/4 случаев симптомы болезни неуклонно прогрессируют. В этих условиях получить доказательства эффективности лечения крайне сложно. Основными критериями эффективности лечения являются частота клинических обострений (за 1-2 года до и после начала лечения) и динамика МРТ-изменений. Оптимальными условиями для оценки эффективности являются проспективные, мультицентровые, рандомизированные, двойные слепые, плацебо-контролируемые клинические испытания. 3. Существование разных клинических форм болезни, генетические различия, а также новые факты, указывающие на патоморфологическую неоднородность PC, свидетельствуют о целесообразности дифференцированного подхода с оценкой результатов лечения в разных подгруппах.
4. В лечении тяжелых заболеваний все больше внимания уделяется понятию «связанного со здоровьем качества жизни». Если ценой за стабилизацию болезни могут быть тяжелые осложнения, то назначение лечения требует взвешенного подхода и оценки соотношения предполагаемой пользы с одной стороны и побочных эффектов, риска осложнений — с другой. Улучшение связанного со здоровьем качества жизни должно быть основной целью лечения.
Направления лечения и проблемный подход
Лечение PC (табл. 5) включает:
- I. Лечение, направленное на замедление прогрессирования патологического процесса
II. Лечение, направленное на уменьшение тяжести и длительности обострения
III. Симптоматическое лечение
IV. Поддерживающую реабилитацию
Лишь для незначительной части препаратов и процедур, наиболее часто используемых в лечении PC, получены доказательства эффективности. Многие препараты используют при PC на основании экспериментальных и эмпирических предпосылок. Нынешнее положение дел отражает мнение одного из ведущих экспертов в области PC, профессора J.H. Noseworthy (Mayo Clinic, США): «Оптимальное лечение обострений PC неизвестно, а многие врачи и пациенты имеют выраженные личные предпочтения». На практике это означает, во-первых, что к любому лечебному воздействию, пока не доказана его эффективность на уровне современных требований, следует относиться как к пробному, а когда речь идет о новых средствах — как к экспериментальному. Во-вторых, лечение и контроль за ним должны осуществляться учреждениями здравоохранения, имеющими соответствующую специализацию. Следует особо отметить, что быстрый прогресс знаний в области PC ежегодно обусловливает проведение новых клинических испытаний с исследованием десятков перспективных препаратов.
К лекарствам с доказанной эффективностью при лечении PC относятся препараты бетта-интерферонов (в России зарегистрированы Бетаферон (интерферон-бетта-1b) и Ребиф (интерферон-бетта-1а), а также глатирамера ацетат (Копаксон).
- Международная федерация обществ больных PG выпускает специальный сборник под редакцией международного экспертного совета, посвященный оценке эффективности используемых методов лечения. В 2000 году готовится новое издание этого сборника и планируется его перевод на русский язык. Эта информация также доступна в электронном варианте: www.ifms.org.uk.
Таблица 5
|
ПРЕПАРАТЫ И МЕТОДЫ ВОЗДЕЙСТВИЯ, |
|
ЛЕЧЕНИЕ, НАПРАВЛЕННОЕ НА ЗАМЕДЛЕНИЕ ПРОГРЕССИРОВАНИЯ БОЛЕЗНИ: — Интерферон -бетта-1b (бетаферон, бетасерон} — Интерферон -бетта-1а (ребиф, авонекс) — Глатирамера ацетат (копаксон) — Индукторы альфа/бетта интерферонов (неовир) — Интерфероны-альфа (реаферон, виферон) — Азатиоприн — Препараты иммуноглобулина человека для в/в введения |
|
ЛЕЧЕНИЕ, НАПРАВЛЕННОЕ НА КУПИРОВАНИЕ ОБОСТРЕНИЯ: — Глюкокортикостероиды (метилпреднизолон, преднизолон, дексаметазон) — Афферентные методы (гемосорбция, плаэмосорбция, плазмаферез, энтеросорбция) — Пентоксифиллин (трентал) — Гепарин |
| метаболическая терапия (нейропротвкторное, энтиоксидантное, мембраностабилизирующее действие, усиление репаративных процессов): витамины Е, А, С, B1, B6, В12, РР; ацетилцистеин; актовегин; церебролизин; лецитин и др. |
|
СИМПТОМАТИЧЕСКОЕ ЛЕЧЕНИЕ: — Спастичности — баклофен, тизанидин (сирдалуд), диазепам, дантролен, треонин — Хронической усталости и патологической утомляемости — амантадин, флуоксетин (прозак), сертралин (золофт), нефазодон (серзон), дезипрамин (норпрамин) — Нарушений координации, нистагма — пропранолол, карбамазепин, изониазид, баклофен — Тремора — карбамазепин, изониазид, глютетимид, габапентин, ондансетрон, методы функциональной нейрохирургии — Дисфункции мочевого пузыря — оксибутинин (дриптан), имипрамин — при сфинктерно-детрузорной диссинергии и остаточной моче <100 мл; адиуретин-SD — при никтурии — Половой дисфункции — йохимбин, альпростадил, производные папаверина — Пароксизмальных симптомов (невралгия тройничного нерва, дизартрия, симптом Лермитта) — карбамазепин, фенитоин, клоназепам, баклофен — Симптомов, связанных с нарушением проведения по нервному волокну — гликозиды наперстянки (?), блокаторы кальциевых каналов (?), аминопиридин — Хронических болей — амитриптилин при дизестезиях; мизопростол при боли, связанной с воспалением; нестероидные противовоспалительные препараты; электростимуляция нервов, задних канатиков |
|
КОМПЛЕКСНАЯ ПОДДЕРЖИВАЮЩАЯ РЕАБИЛИТАЦИЯ — Физическая терапия с использованием индивидуального проблемного подхода — Адаптация к неврологическому дефициту в повседневной и профессиональной деятельности (трудотерапия) — Психологическая и социальная адаптация — Решение вопросов, связанных с нарушениями речи, глотания, функций кишечника и мочевого пузыря, патологической утомляемостью |
Вопросы, которыми нельзя пренебречь при лечении больных PC
и с которыми сталкивается каждый больной PC и его лечащий врач,
а ответы на них либо противоречивы, либо вообще трудно найти в литература
Как лечить первое обострение PC?
В последние годы появились серьезные публикации, указывающие предпочтительность лечения первого обострения (в частности, неврита зрительного нерва) коротким курсом пульс-терапии кортикостероидами (1 г метилпреднизолона в/в в сутки в 2-4 приема, в течение 3 дней) с последующим коротким курсом преднизолона внутрь (1 мг/кг/день в течение 11 дней). Такое лечение существенно отдаляет срок последующего обострения (т.е. переход в клинически достоверный PC), в отличие от стандартного перорального курса кортикостероидов, который, наоборот, может ускорить рецидив.
Когда начинать активное лечение иммуномодуляторами (в частности, препаратами интерферонов-бетта)?
Не показано такое лечение после первого обострения, особенно при минимальных изменениях по данным МРТ: при доброкачественном естественном течении болезни отдаленные эффекты иммуномодуляторов неизвестны. По этой же причине не назначают такое лечение в возрасте до 18 лет. Показаниями являются частые выраженные обострения, имеющие следствием риск нарастания инвапидизации.
В каких случаях при обострении предпочтительнее назначать кортикостероиды?
Назначая кортикостероиды, прежде всего рассчитывают на мощное противоотечное, противовоспалительное и мембраностабилизирующее действие. Поэтому их использование целесообразно тогда, когда обострение проявляется тяжелыми симптомами (поражения спинного мозга, ствола мозга), и быстрое купирование отека и воспаления может способствовать более полному регрессу симптомов. Необоснованные курсы лечения гормонами могут способствовать активации некоторых вирусных нейроинфекций и последующей резистентности к лечению.
Существует ли профилактика обострений РС?
Основной фактор риска обострений — вирусные инфекции (но не бактериальные): ОРВИ, желудочно-кишечные, герпетические. Поэтому профилактика и адекватное лечение вирусных инфекций может благоприятно сказаться на течении РС. Травмы (за исключением электротравмы) и хирургические вмешательства не являются фавором риска обострений.
o После ОРВИ в 10-30% случаев развивается обострение PC.
Как беременность влияет на течение РС и лечение?
Последние исследования показали, что в целом беременность не ухудшает (а иногда улучшает) течение PC. Риск обостренй в период беременности существенно снижается, а в течение 1 года после родов — возрастает, однако в общей сложности (9 месяцев беременности и 1 год после родов) частота обострений остается прежней. Риск обострений в течение года после аборта возрастает же степени, что и после родов. Это связано с резким переходом от физиологической иммуносупрессии во время беременности к новым условиям иммунорегуляции и ее срыву. Женщины, больные PC, должны избегать внеплановых беременностей. При планировании беременности за 3 месяца отменяют иммуномодуляторы и предполагают возобновление лечения после родов (в период риска), индивидуально решая вопрос грудного вскармливания.
Прием каких препаратов противопоказан или потенциально опасен при PC?
Противопоказаны при PC препараты интерферона-гамма, которые провоцируют обострение. С осторожностью следует относиться к значению иммуномодуляторов, в том числе индукторов интерферонов, усиливающих продукцию интерферона-гамма. Требует тщательных испытаний применение при PC препаратов, обладающих иммуностимулирующими свойствами, так как за счет усиления продукции (провоспалительных цитокинов, а также активации факторов фагоцитоза они могут индуцировать возрастание активности процесса. Не следует назначать больным РС индометацин в связи с возможностью провокации обострения. Из группы нестероидных противовоспалительных препаратов безопасными считаются аспирин и парацетамол, а о безопасности других средств этой группы сведений нет. На состоянии больных РС могут неблагоприятно сказаться любые «истощающие» воздействия: строгая диета, голодание, чрезмерные физические нагрузки, плазмаферез с большими объёмами удаляемой плазмы (особенно в фазе затихающего клинического обострения). Можно ли проводить вакцинации при PC? Развитие острого диссеминированного энцефаломиелита после вакцинаций, а также возможность обострения PC при активации иммунной системы ставят вопрос о безопасности иммунизации против вирусных инфекций при PC. На него нет однозначного ответа. Проверены на безопасность при PC лишь отдельные вакцины (в частности противогриппозные). Вакцинацию против гриппа рекомендуется проводить пациентам, имеющим высокий риск заболевания или осложнений. Другие вакцины, особенно недавно разработанные, нуждаются в проверке на их безопасность при PC. Однако на сегодняшний день нет оснований говорить о высоком риске вакцинаций при PC.
Где должны лечиться больные PC?
Такое сложно контролируемое заболевание, как РС, требует обязательного участия служб, оказывающих специализированную помощь. Оптимальные формы помощи должны включать:
— систематические амбулаторные консультации специалистов в областит РС: врача-невролога, специалиста по физическим методам лечения и др.;
— лечение обостpeний, курсы реабилитации и профилактического лечения в условиях специализированного стационара;
— для пациентов с умеренной и тяжелой инвалидизацией — систематическую реабилитационную помощь на дому, оказываемую мультидисциплинарной бpигaдoй, с использoвaниeм проблемного подхода.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Причины и течение рассеянного склероза
– Существует ошибочное мнение, что рассеянный склероз – это болезнь пожилых, что-то связанное с нарушением памяти. А как на самом деле?
– На самом деле рассеянный склероз – заболевание, которое развивается преимущественно у молодых людей. Средний возраст дебюта варьируется от 20 до 40 лет. Но бывают случаи, когда заболевание начинается в пожилом возрасте. Часто таким пациентам долго не могут поставить правильный диагноз, так как все симптомы списываются на возрастные изменения. Название заболевания, и правда, может сбивать с толку, но рассеянный склероз не имеет никакого отношения ни к рассеянности внимания, ни к бытовой трактовке термина – «склероз» как снижение памяти. Под склерозом здесь понимается замещение здоровой нервной ткани рубцом из соединительной ткани, а под рассеянностью – то, что поражаются разные участки нервной системы, а приступы происходят в разные моменты.
– Как развивается заболевание?
– Заболевание является аутоиммунным, то есть случается «атака» иммунной системы на оболочку нервных волокон в головном и спинном мозге. Нерв похож на электрический кабель, он состоит из центральной части – аксона и оболочки – миелинового волокна. Последняя и является мишенью при РС, поэтому заболевание относится к демиелинизирующим. При повреждении миелина нервные импульсы проводятся более медленно и могут возникать различные симптомы, в зависимости от того, какая именно часть нервной системы повреждена.
Часто первым заметным человеку проявлением заболевания становится снижение зрения, чаще на один глаз. Могут возникать болевые ощущения при движении глазом. Также среди симптомов – онемение, покалывание, слабость в руке или ноге, нарушение походки, координации движений, трудности с мочеиспусканием. Симптомы заболевания разнообразны, потому что поражаться может как головной, так и спинной мозг.
– Эта симптоматика является постоянной?
– Чаще всего заболевание протекает с периодами обострений и ремиссий. Во время обострения появляются симптомы, которые сохраняются несколько дней или недель, а затем могут исчезнуть даже без лечения, и до следующего эпизода человека может ничего не беспокоить. Из-за этого пациенты часто обращаются к врачу не сразу. Это также может создать иллюзию, что лечение не требуется, но это не так. Если происходит тяжелое обострение, восстановление может быть неполным, и чем больше обострений происходит, тем более выражены такие остаточные симптомы. Через какое-то время после начала заболевания обострения могут прекратиться, начнется неуклонное прогрессирование заболевания. Эту стадию называют вторично-прогрессирующей. Терапия нацелена не только на предотвращение обострений, но и на то, чтобы предотвратить такое прогрессирование.
Диагностика заболевания
– На основании каких исследований ставится диагноз?
– На основании клинической картины и данных МРТ, с помощью которых выявляются очаги – зоны, где происходит повреждение нервной ткани в результате воспалительного процесса. Но просто на основании МРТ поставить диагноз невозможно – схожие изменения могут встречаться при других заболеваниях – даже у здоровых людей. Так что результаты обследования необходимо всегда сопоставлять с клинической картиной. Важным методом исследования также является анализ спинномозговой жидкости на олигоклональный иммуноглобулин G. Этот анализ положительный у 85% пациентов с РС и позволяет подтвердить диагноз.
– С чем можно спутать рассеянный склероз?
– В первую очередь нужно дифференцировать рассеянный склероз с другими демиелинизирующими заболеваниями, например острым рассеянным энцефаломиелитом или оптикомиелитом. На втором месте идут системные аутоиммунные заболевания, например системная красная волчанка и такие инфекции, как болезнь Лайма. Но дифференциальный ряд очень широкий: от банальной мигрени, при которой могут встречаться небольшие очаги на МРТ, до редких наследственных заболеваний.
– Возможно, предрасположенность к РС позволяет определить генетическое тестирование?
– Нет, сделать какой-либо генетический тест, который однозначно покажет, что у человека в будущем разовьется рассеянный склероз, невозможно. Но определенная генетическая предрасположенность все же есть: выявлено более 200 генов, ассоциированных с более высоким риском возникновения заболевания. В основном это гены, связанные с работой иммунной системы, но каждый из них в отдельности лишь несущественно повышает риск.
– Если заболевание не является наследственным, то для него не характерны семейные случаи?
– Семейные случаи встречаются, но реже. У меня есть пациенты, у которых болеет кто-то из родителей, либо брат или сестра, но это скорее исключение. Риск для ребенка родителя с РС составляет около 2,5%, это чуть выше, чем для любого человека в популяции. Но у родственников пациентов с рассеянным склерозом повышена вероятность аутоиммунных заболеваний в целом – это может быть, например, заболевание щитовидной железы, псориаз или сахарный диабет.
– Какие меры необходимо принимать для профилактики заболевания?
– Есть два доказанных метода профилактики рассеянного склероза: первый – достаточный уровень витамина D. Он снижает риск развития рассеянного склероза, а также может влиять на ход течения заболевания. Второй – отказ от курения.
Лечение рассеянного склероза: подходы и результативность
– Как лечат рассеянный склероз?
– Существует немало современных препаратов, влияющих на течение рассеянного склероза. Они позволяют остановить активность заболевания и предотвратить его прогрессирование. Это очень динамично развивающаяся сфера – постоянно проводятся клинические исследования, на рынок выходят новые препараты. Лечение подбирается индивидуально – в зависимости от типа течения, степени активности заболевания, переносимости и пожеланий пациента.
Существует два подхода к терапии. Первый – так называемая стратегия эскалации, когда лечение начинают с менее эффективной терапии (первой линии), и если отклика на нее нет, то переходят к более эффективной, но сопряженной с большими рисками терапии второй линии.
Второй подход заключается в раннем использовании высокоэффективных препаратов. Согласно результатам исследований, второй подход сопряжен с более хорошими исходами в долгосрочной перспективе, в частности, с меньшим риском прогрессирования заболевания в будущем.
– Доступны ли современные схемы лечения в России?
– В России для терапии РС используются те же препараты, что и во всем мире. Но могут быть проблемы с доступностью таких лекарств. В нашей стране препаратами для лечения РС пациентов обеспечивает государство по программе «14 высокозатратных нозологий». Но в виду того, что высокоэффективные препараты для лечения РС очень дорогие, обычно большинству пациентов по умолчанию назначают препараты первой линии. Вторая линия обычно резервируется для пациентов с агрессивным течением, и получить ее сложнее.
– Санкции, введенные весной в отношении России другими государствами, как-то отразились на доступности терапии для пациентов с рассеянным склерозом?
– Пропали многие оригинальные препараты, их заменили российские дженерики, переносимость которых у некоторых пациентов хуже. Ранее высокоэффективные препараты были доступны российским пациентам в рамках клинических исследований. В марте многие иностранные компании, к сожалению, приостановили проведение исследований на территории РФ, что отразилось на доступности инновационных лекарств.
Трудности: комплаенс и низкая осведомленность
– С какими проблемами вы сталкиваетесь на практике?
– Самый тяжелый момент для меня – это, когда пациент отказывается от терапии. Из-за того, что между обострениями человек может чувствовать себя хорошо, ему может показаться, что терапия не нужна. Очень непросто объяснить молодому человеку, у которого нет никаких симптомов, что ему нужно постоянное лечение. Это большая работа. К сожалению, я регулярно вижу пациентов, которые после постановки диагноза не продолжили наблюдение у невролога и не получали лечение. Они возвращаются сейчас, спустя 10–15 лет со значительными инвалидизирующими изменениями. Это всегда очень грустно. Я стараюсь объяснить все риски и опции терапии, поощряю пациентов в стремлении активно участвовать в принятии решений и брать ответственность за свое здоровье.
– С какими сложностями сталкиваются люди с рассеянным склерозом?
– В том, что касается медицинской помощи – существует недостаток квалифицированных специалистов, которые работают с этим заболеванием, особенно в регионах. В результате вместо способов разрешения конкретной проблемы пациент может услышать: «А что вы хотите, у вас же РС». Бывают трудности с лекарственным обеспечением: чтобы получить эффективную терапию, иногда приходится пройти все круги бюрократического ада. На личном уровне – несомненно, может быть трудным принять такой диагноз, иногда может потребоваться помощь психолога. Человеку предстоит решить, рассказывать ли окружающим о диагнозе, например коллегам по работе.
До сих пор сохраняется проблема низкой осведомленности общества об этом заболевании, и можно услышать такие комментарии: «Такая молодая и уже склероз».
Кроме того, есть невидимые симптомы РС, например, хроническая утомляемость, которые незаметны окружающим, и они могут не понимать, почему человеку трудно что-то делать, ведь выглядит он здоровым. Чтобы было легче преодолеть эти моменты, важно найти проверенные источники информации. Другие пациенты могут тоже стать важным кругом поддержки.
– Иногда люди, услышав диагноз «рассеянный склероз», делают вывод, что их жизнь теперь весьма ограничена – им нельзя путешествовать или иметь детей. Корректно ли так думать?
– Конечно, нет, люди с рассеянным склерозом могут вести обычный образ жизни, работать, путешествовать и становиться родителями. Планируя беременность, важно заранее обсудить это со своим неврологом и все спланировать. Мне часто задают неожиданные вопросы, например, можно ли делать татуировки. Конечно, можно! Главное, наблюдаться у врача, которому вы доверяете, и оставаться приверженным терапии.
С.К. Евтушенко, И.Н. Деревянко, Донецкий государственный медицинский университет им. М. Горького
Резюме
В работе описаны формы, типы и варианты течения РС. Приведены современные критерии ранней диагностики РС (McDonald et al., 2001), дан их подробный анализ и практические рекомендации по их использованию. В обзоре обсуждается роль современных методов диагностики РС — МРТ головного мозга, вызванных потенциалов и изменений СМЖ. Определены особенности диагностики и течения РС у детей. Приводятся наиболее распространенные оценочные неврологические шкалы, которые используются для определения тяжести неврологических нарушений, степени инвалидности больных с РС (FS, EDSS Kurtzke J.F.), оценка состояния больного с РС и оценка степени восстановления нарушенных функций у больных РС согласно шкале NRS (Sipe J.et al.,1984)
Рассеянный склероз (РС) — серьезное неврологическое заболевание с множеством непредсказуемых особенностей, сложной и действенной совокупностью неизвестных механизмов, определяющих проявления и течение РС [2].
Этиология заболевания до сих пор не известна. Наиболее признанной является мультифакториальная теория, подразумевающая необходимость действия внешнего фактора, вероятнее всего, инфекционного, на лиц с генетической предрасположенностью [5, 11].
Течение РС индивидуально. Нет двух больных с одинаковыми клиническими проявлениями патологического процесса, у каждого из них свой индивидуальный набор симптомов и их сочетание. Невозможно сегодня предсказать длительность ремиссий и частоту обострений, степень восстановления функций и скорость прогрессирования необратимых нарушений.
Распознавание множественного склероза на ранних этапах и сегодня один из самых трудных и сложных разделов в учении о нем. Кроме того, частый моносимптомный дебют, наличие различных клинико-инструментальных диссоциаций создает дополнительные трудности в ранней постановке достоверного диагноза [1, 4].
До настоящего времени широко использовались диагностические критерии, основанные на клинических признаках Kurtske J.(1961,1983), Schumacher J. (1965); D.Mc. Alpine с соавт. (1972); Шмидта Е.В. с соавт. (1980); Poser C. (1983) и др., однако они все периодически дополняются и усовершенствуются. Недостатком этих систем является отсутствие учета степени выраженности признаков и лабораторных данных, что не позволяет следить за динамикой заболевания.
Тем не менее, анализ частоты диагностических ошибок при постановке диагноза «рассеянный склероз» показывает, что эта проблема остается весьма актуальной [5, 8]. Высоко количество как ложноположительных, так и ложноотрицательных диагнозов РС. Больные годами получают различные диагностические и лечебные процедуры до того, как устанавливается правильный диагноз.
Совершенствование стандартного набора диагностических критериев с использованием лабораторных и инструментальных методов, четкая осведомленность и широкое внедрение в практическую деятельность неврологов единых критериев диагностики РС позволит более точно на ранних этапах устанавливать диагноз, провести дифференциальную диагностику и определять соответствующую тактику ведения больных.
Целью нашей работы является проведение анализа существующих общепринятых международных критериев и собственного опыта работы по ранней диагностике рассеянного склероза, составление диагностического алгоритма, позволяющего практическому неврологу повысить сроки и качество достоверности постановки диагноза, своевременно определить стратегию и тактику ведения этой сложной категории больных.
Рассеянный склероз — хроническое прогрессирующее демиелинизирующее заболевание, характеризующееся многоочаговостью поражения белого вещества центральной нервной системы, ремиттирующе-прогредиентным течением, вариабельностью неврологических симптомов, преимущественным поражением лиц молодого возраста [5, 11].
Согласно Международной классификации болезней десятого пересмотра (МКБ-10), рассеянный склероз относится к IV классу «Заболевания нервной системы» (G00-G99), блоку «Демиелинизирующие заболевания нервной системы» (G35-G37), обозначается кодом G35.
Клиника РС
В многообразии клинических проявлений РС можно выделить две группы симптомов.
Первая группа включает наиболее распространенные классические симптомы, которые являются непосредственным проявлением поражения проводящих путей мозга. Сюда же входят симптомокомплексы, отражающие особенности клинических проявлений многоочагового демиелинизирующего процесса.
Ко второй группе относятся редкие клинические проявления заболевания.
Типичные клинические симптомы
Симптомы поражения пирамидного пути:
-
наиболее частое поражение при РС (85-97%);
-
в зависимости от локализации очага возникают геми- или парапарезы, реже монопарезы;
-
наиболее часто страдают нижние конечности, реже верхние; они вовлекаются позднее;
-
клинически проявляются патологические пирамидные рефлексы, повышение надкостничных, сухожильных рефлексов, снижение или полное отсутствие брюшных рефлексов. Последний симптом — это тонкое, раннее проявление заинтересованности поражения пирамидного пути.
От быстрого появления симптома Бабинского без снижения силы в ногах (характерная клинико-функциональная диссоциация) и утраты поверхностных брюшных и подошвенных рефлексов до спастической нижней параплегии с верхним центральным парапарезом и псевдобульбарными расстройствами, иногда с симптомами насильственного смеха и плача.
Центральные парезы и параличи сопровождаются изменениями мышечного тонуса — как спастикой, так и гипотонией, дистонией. Одной из проблем для больных РС представляется повышение тонуса по спастическому типу. Как правило, оно наблюдается у больных с нижними парапарезами.
Поражение боковых и задних столбов вначале заболевания проявляется комплексом флексорных и экстензорных стопных и кистевых патологических рефлексов, феноменом складного ножа и неустойчивостью в позе Ромберга. В дальнейшем при дегенерации петли гамма-нейронов развивается интенсивная спастика мышц, симптомы спинального автоматизма, появляются постоянные клонусы стоп и коленных чашечек, сгибательные контрактуры в коленных суставах с приведением ног к животу. По мере захвата поперечника мозга усиливаются амиотрофии, а при вовлечении в процесс вегетативных волокон и центров появляются трофические расстройства в виде пролежней и декубитальных язв.
Симптомы поражения мозжечка (в 62-87% случаев)
Больные жалуются на нарушение походки и равновесия. Клинически проявляются нарушениями координации и снижением мышечной силы. Характерно пароксизмальное нарастание атаксии до невозможности ходить. От эпизодического головокружения, неровности почерка, одностороннего интенционного тремора в конце выполнения пальце-носовой пробы и малозаметной для окружающих шаткости при ходьбе до грубой статической и динамической атаксии с выраженной гиперметрией, делающих затруднительным или невозможным целенаправленные движения. Скандирование речи и грубый аксиальный тремор резко ограничивают речевое общение с окружающими и самостоятельный прием пищи. Триада Шарко (нистагм, скандирование, интенционное дрожание), впечатляющая первых исследователей РС, в настоящее время растворилась в разнообразной клинической картине заболевания, а дебют и прогрессирование мозжечкового синдрома всегда требуют проведения дифференциального диагноза с первичными церебеллярными атрофиями.
Симптомы поражения ствола мозга и черепных нервов (в 36-81% случаев)
Очаги демиелинизации зачастую образуются во внутримозговых частях нервов, поэтому могут отмечаться симптомы как центрального, так и периферического поражения двигательных черепных нервов, чаще III, V, VI, VII пары нервов. Наиболее частым клиническим симптомом поражения ствола мозга являются глазодвигательные нарушения, которые вызывают двоение. От легких признаков двоения и дрожания предметов перед глазами, мелкоразмашистого монокулярного горизонтального нистагма при отведении глаз в сторону за молоточком врача до спонтанного ротаторного нистагма при взгляде прямо, выраженной дизартрии и поперхивании при еде, а в далеко зашедших случаях — до невозможности глотать и говорить. Характерен для РС синдром межъядерной офтальмоплегии, связанный с очагами демиелинизации в системе заднего продольного пучка. Типичны для РС дискоординированные движения глазных яблок, их разностояние по вертикали или горизонтали (косоглазие), недоведение глазных яблок кнутри и кнаружи. Типичным поражением верхних отделов ствола мозга является вертикальный нистагм. Часто при РС наблюдается горизонтальный нистагм, асимметричный нистагм с ротаторным компонентом, «саккадирующие» движения глазных яблок, односторонний нистагм. Характерен симптом дискоординированного движения глазных яблок, недоведение глазных яблок в стороны, межъядерный офтальмопарез, иногда наблюдается легкий птоз. Редко встречаются изменения зрачковых реакций. Одним из основных проявлений РС является нистагм как следствие поражения верхних отделов ствола.
Симптомы нарушения чувствительности (у 56-92% пациентов)
Один из наиболее частых симптомов РС — изменение глубокой и поверхностной чувствительности. Чаще на ранних стадиях отмечается небольшое расстройство болевой чувствительности, дизестезия в дистальных отделах конечностей. Ощущение ватных ног. Широкий диапазон проявлений от жалоб на онемение щеки, голени, пальцев ног или объективного снижения вибрационного чувства от лодыжек до реберных дуг, выявляемого с помощью камертона или паллиэстезиометра, до пароксизмальной тригеминальной невралгии, проприоцептивной атаксии, хронической дизестезии конечностей, ночных крампи синдрома Экбойма и мышечно-скелетных болей. Характерен чувствительный феномен Лермитта, заключающийся в ощущении удара электрического тока в руках или спине при резких поворотах или форсированном сгибании головы. Особенностью нарушений чувствительности является то, что больные не могут четко их описать и часто предъявляют жалобы на онемение и жжение в конечностях.
Симптомы зрительных нарушений (в 36-52% случаев):
-
снижение остроты зрения,
-
изменение полей зрения,
-
часто ретробульбарный неврит является первым симптомом заболевания.
При офтальмологическом исследовании выявляются:
-
центральные скотомы,
-
сужение полей зрения,
-
преходящее снижение остроты зрения.
Большинство исследователей считают, что у 80% больных ретробульбарный неврит или оптический неврит (ОН) может быть первым, а иногда и единственным проявлением РС, при этом в 13% случаев ОН возникает уже на фоне общей клиники РС. Активное наблюдение за больными с односторонним ОН через 15 лет выявило в 60% случаев достоверный РС. Большую помощь в ранней диагностике РС и определении прогноза при наличии ОН оказывает магнитно-резонансная томография (МРТ). Так, у больных с моносимптомным ОН МРТ в 40-70% случаев выявила очаги демиелинизации в других отделах мозга.
Классическая картина ОН (вне зависимости от этиологии) характеризуется острым снижением зрения в течение нескольких часов, иногда в течение 1-2-х дней или недели. Изменения зрения, как правило, сопровождаются появлением центральной или парацентральной скотомы, сужением полей зрения на 10-30%. Снижение зрения сопровождается изменением цветового зрения с потерей тона и цвета, преобладанием серого цвета, сужением полей зрения на зеленый и/или красный цвета. Пациенты могут отмечать разницу между глубиной восприятия и стереоскопическим зрением, что является патогномоничным признаком РС. Возникает мелькание предметов и нарушение восприятия быстро перемещающегося объекта. Больных беспокоит повышенная чувствительность к яркому свету. Потеря яркости, нарушение контрастности выявляются более чем у половины больных РС.
Диагноз ретробульбарного неврита ставится, когда на фоне зрительных нарушений пациенты предъявляют жалобы на боль, усиливающуюся при движении глаз или при надавливании на глазное яблоко, особенно при взгляде вверх. Болевые ощущения связаны с раздражением оболочек ЗН при тракции основаниями верхней и внутренней прямой мышц. Боль может сохраняться в течение нескольких часов или дней, предшествовать потере зрения или сопровождать ее. Частым симптомом является головная боль, локализующаяся в лобно-теменной или лобно-затылочной областях.
Важным клиническим симптомом при ОН является нарушение зрачковых реакций, проявляющихся вялостью зрачковой реакции или даже парадоксальной реакцией — сужением зрачка на свет при длительном освещении.
При впервые возникшем ретробульбарном неврите в первые недели на глазном дне, как правило, изменений не отмечается. Картина глазного дна зависит от локализации процесса в зрительном нерве; интенсивности воспалительных изменений; давности процесса. При папиллите диск зрительного нерва гиперемирован, границы стерты, отмечается его отек, иногда выраженный из-за коллатерального отека. Уже в острой стадии ОН могут появляться признаки нисходящей атрофии диска зрительного нерва: побледнение височных половин диска (преимущественно страдает папилло-макулярный пучок), сужение артерий и дистрофические изменения в макулярной области.
При РС течение ОН имеет ряд особенностей: развитие билатеральных и повторных (возвратных) ретробульбарных невритов, как правило, восстановление зрения в последующем (полное или частичное); субклинические изменения глазного дна и изменения ЗВП у 80% больных; изменения ЗВП, полей зрения для интактного глаза при одностороннем ОН; наличие преходящего снижения остроты зрения, цветоощущения и изменения полей зрения под влиянием внешних факторов, например, повышения температуры тела (феномен Uhthoff); снижение контрастной чувствительности в области высоких пространственных частот. Наибольшую помощь в диагностике ОН при РС оказывает МРТ.
Симптомы нарушения функции тазовых органов (в 26-53% случаев)
Это один из первых и наиболее часто встречающихся симптомов при РС. Наиболее рано проявляются нарушения мочеиспускания по центральному типу, могут быть как учащения, так и задержка мочи, а также императивные позывы. На более поздних стадиях это, как правило, недержание мочи. У мужчин может быть снижение потенции, связанное с повреждением спинного мозга очагом демиелинизации.
Постоянным сопровождением спинального синдрома являются тазовые расстройства от легких императивных позывов к мочеиспусканию, запоров и задержек мочи до необходимости катетеризации мочевого пузыря и специальных приемов эвакуации кала. В финальных стадиях развивается недержание мочи и кала.
Нейропсихологические симптомы (в 65-95% случаев):
-
неврозоподобные астенические и обсесcивно-фобические синдромы;
-
нарушение памяти, остроты мышления и всевозможные нарушения эмоционального характера;
-
депрессия с состояниями апатии и тревоги;
-
часто эйфория, сочетаемая со снижением интеллекта (эйфорическая деменция);
-
у женщин истерические реакции, что является причиной несоответствия жалоб больной и объективной неврологической симптоматики.
Редкие клинические проявления
-
Пароксизмальные состояния 5-17% (короткие сенсорные и моторные расстройства, тонические спазмы, гемифациальные спазмы, острые приступы икоты и зевоты).
-
Вегетативные нарушения (симпатоадреналовые кризы, приступы гипотонии, брадикардии).
-
Симптомы поражения периферической нервной системы (синдром полинейропатии, множественные мононевропатии, развитие мышечной атрофии).
Полиморфизм РС сильно затрудняет раннюю диагностику. Число и диапазон ошибок остаются значительными. Особый акцент в клинической диагностике необходимо делать на следующие важнейшие критерии диагностики:
-
начало болезни в молодом возрасте;
-
полиморфизм клинических проявлений;
-
мерцание «симптомов» даже на протяжении суток;
-
волнообразное течение болезни;
-
наличие клинических диссоциаций.
Основными клиническими диссоциациями можно считать:
-
высокие, спастичные с клонусами рефлексы при легком или умеренном нарушении объема движений;
-
клонусы стоп, патологические рефлексы при низких проприоцептивных рефлексах;
-
выраженные пирамидные симптомы в виде нижнего парапареза со спастическими рефлексами, клонусами при снижении мышечного тонуса;
-
разная степень выраженности гиперрефлексии в верхних и нижних конечностях, между коленными и ахилловыми рефлексами;
-
диссоциации между поверхностными и глубокими брюшными рефлексами;
-
диффузное снижение мышечного тонуса (отсутствует » тонический угол» при сгибании конечностей) при одновременном выявлении симптома «складного ножа» (признака спастичности);
-
нарушение вибрационного чувства в руках и ногах с дискоординацией выполнения динамических проб при сохранности суставно-мышечного чувства;
-
побледнение височной половины дисков зрительных нервов при нормальной остроте зрения или падение остроты зрения при нормальном глазном дне;
-
наличие тазовых нарушений при нерезко выраженном пирамидном синдроме;
-
коллоидно-белковая диссоциация в ликворе;
-
клинико-МРТ-диссоциации (несоответствие клинической степени тяжести и объему поражения головного мозга, несовпадение появления очагов на МРТ и их регресс не совпадают во времени с клиническими стадиями обострения и ремиссии, несоответствие клинической картины и локализации выявленных очагов демиелинизации, наличие множественных очагов на МРТ при моносимптомном дебюте).
Учитывая результаты собственных наблюдений, особое значение в ранней диагностике РС отводится определению вибрационной чувствительности с помощью камертона Grafco-c-128 (USA) на верхних и нижних конечностях. Нормальным считали сохранение ощущений вибрации в течение 15-20 секунд.
Помогает в диагностике РС раннее выявление переднего и заднего межъядерного офтальмопареза [7]. МЯОП выявляется при медленном движении глазных яблок и при взоре, фиксированном на предмете (молоточке). Клиника МЯОП зависит от уровня поражения. Различают передний МЯОП, развивающийся при поражении пучка на уровне ядер глазодвигательных нервов, — это парез внутренней прямой мышцы на стороне поражения и мононуклеарный нистагм с другой, и задний, возникающий при поражении заднего продольного пучка на уровне ядер отводящего нерва и проявляющийся при медленном взгляде влево. При этом сокращается внутренняя прямая мышца и не сокращается наружная прямая мышца правого глаза. Практически всегда наблюдается мононуклеарный нистагм справа.
Нарушение ассоциированных движений глазных яблок всегда характеризуется поражением одного глаза. Другой глаз движется свободно или опережает первый. При этом содружественные движения при обычном исследовании («посмотрите направо, посмотрите налево») часто сохраняются, что приводит к заключению об отсутствии патологии.
Для более достоверного и более объективного подтверждения МЯОП нами была использована модифицированная методика его выявления при помощи «лингвоокулярной пробы», предложенной Евтушенко С.К. [7]. Определение проводилось в два этапа. На первом больного просят показать язык и держать его вытянутым, а на втором — медленно из положения крайнего отведения двигать глазными яблоками вслед за молоточком влево и вправо. При этом сразу можно сразу отметить, как одно из глазных яблок отстает. По окончании исследования возможно появление мононуклеарного нистагма.
С помощью «лингвоокулярной нагрузки» в процессе движения глазных яблок «включается» подъязычный нерв, что увеличивает рефлекторную нагрузку и исключает возможность функциональной недостаточности. Описанный прием особенно информативен при выявлении заднего офтальмопареза.
ФОРМЫ РС
В зависимости от его преимущественной локализации традиционно выделяют церебральную, спинальную и цереброспинальную формы PC. Хотя ряд ученых считает, что они, по существу, являются этапами развития РС. Так, в начальной стадии преобладают церебральные симптомы, в развернутой — цереброспинальные, в поздней — спинальные. Предложенные ранее атипичные формы (оптическая, стволовая, корковая, «гиперкинетическая», псевдотуморозная, гемиплегическая, полиомиелитическая и БАС-подобная и др.) принято считать атипичными вариантами течения с преобладанием поражения того или иного отдела ЦНС [6, 10].
Церебральная форма характеризуется развитием моно- или гемипареза центрального типа, нарушением зрения, координации движений, нейропсихологическими изменениями.
Спинальная форма характеризуется симптомами поражения спинного мозга на различных уровнях. Ведущими в клинической картине являются нижний спастический парапарез, различной степени выраженности тазовые расстройства, нарушения чувствительности.
Цереброспинальная форма характеризуется многоочаговостью поражения уже в начальной стадии, симптомами поражения мозжечковых и пирамидных образований в головном и спинном мозге, зрительной, глазодвигательной, вестибулярной и других систем.
Атипичные варианты течения РС
При оптическом варианте ведущим клиническим синдромом является снижение остроты зрения, которое через некоторое время проходит полностью самостоятельно или на фоне лечения. В дальнейшем аналогичные явления могут развиваться в другом глазу. Реже одновременно снижается зрение на оба глаза. При офтальмоскопическом обследовании выявляются признаки ретробульбарного неврита: побледнение диска зрительного нерва, как правило его височной стороны, сужение полей зрения (вначале на красный и зеленый цвет), скотомы.
Стволовой вариант имеет особенно неблагоприятное течение. Проявляется головокружением, шаткостью, дрожательным гиперкинезом. Могут быть альтернирующие синдромы, быстро меняющие свою структуру, при которых наиболее часто на одной из сторон страдают глазодвигательные нервы, на другой преобладает пирамидная симптоматика.
Корковый вариант протекает с эпиприпадками Джексоновского типа с клоническими судорогами.
Мозжечковый (гиперкинетический) вариант чаще проявляется как стволово-церебеллярная, реже — как чисто церебеллярная. Возникают интенционное дрожание в верхних и нижних конечностях, горизонтальный, редко вертикальный крупноразмашистый нистагм, скандированная речь (триада Шарко); статическая и динамическая атаксия; расстройства почерка (макрография).
Псевдотуморозный вариант сопровождается головной болью, часто напоминая гипертензионную, сопровождаясь тошнотой и рвотой, застойными дисками зрительных нервов. Степень его выраженности меняется с появлением побледнения височных половин зрительного нерва. Наряду с застоем, может выявляться концентрическое сужение полей зрения, центральные и парацентральные скотомы, свидетельствующие о наличии ретробульбарного неврита. Головные боли обычно совпадают с острыми проявлениями РС и проходят по мере развития заболевания
Гемиплегический вариант — вариант, при котором на первый план выступает гемиплегия, что настораживает в отношении опухолевого процесса или ОНМК. Степень выраженности гемипареза изменяется, имея тенденцию к ремиттирующему течению. У этих больных выявляются другие уровни поражения НС (преходящая слабость в конечностях, противоположных гемиплегии, диплопия, тазовые расстройства).
Полиомиелитический вариант — когда амиотрофии сочетаются с понижением проприоцептивных рефлексов.
БАС-подобный вариант — когда амиотрофии сочетаются с повышением проприоцептивных рефлексов.
Психотический вариант — вариант, при котором преобладают психопатологические симптомы.
Течение РС носит хронический характер. В большинстве клиник приняты следующие термины для обозначения периодов (стадий) заболевания.
СТАДИИ PC:
Обострение (экзацербация) — появление нового симптома или группы симптомов, усугубление уже имеющейся неврологической симптоматики после стабилизации или улучшения состояния на протяжении месяца и более. Длительность обострения — от 24-х часов до 8-ми недель, в этот период ни один из симптомов не регрессирует.
Ремиссия — уменьшение выраженности или отчетливое исчезновение симптомов длительностью не менее суток. При длительности ремиссии более месяца она расценивается как стойкая.
Хроническое прогрессирование — нарастание тяжести симптомов на протяжении не менее двух месяцев без стабилизации или улучшения.
Стабилизация — отсутствие обострений, ремиссий и хронического прогрессирования на протяжении хотя бы одного месяца.
Дебют РС — это впервые возникшие проявления заболевания, чаще всего в виде моносимптома.
«Псевдообострение» (декомпенсация) — короткое ухудшение состояния с усилением имевшихся ранее симптомов заболевания на фоне перенесенной ОРВИ с повышением температуры тела, после стресса, однако появившаяся неврологическая симптоматика быстро регрессирует либо реально не изменяет тяжесть состояния больного. В этих случаях ухудшение состояния больного не связано с образованием новых очагов или увеличением объема уже имеющихся. Этот феномен, скорее, можно объяснить преходящим блоком проведения нервного импульса по демиелинизированному волокну, вызванному временным изменением гомеостаза [6].
ТИПЫ ТЕЧЕНИЯ РС
Учитывая стадийный характер клинической картины РС, различают следующие варианты (типы) течения PC:
-
ремиттирующее — когда обострение сменяется ремиссией;
-
первично-прогрессирующее — с самого начала заболевания наблюдается неуклонное прогрессирование, без четких периодов обострений и ремиссий;
-
вторично прогрессирующее — когда после обострений и ремиссий в анамнезе наступает стадия хронического прогрессирования с периодами стабилизации, но с остаточной неврологической симптоматикой.
При ремиттирующем течении могут быть варианты:
-
Рецидивирующе-ремиттирующее течение (25-51%) — наиболее частый вариант, протекающий с обострениями и полными или частичными ремиссиями без признаков хронического прогрессирования, который в 2/3 случаев в последующем трансформируется в неуклонно прогрессирующий, на который могут наслаиваться обострения. Время от первых клинических проявлений до начала прогрессирования — в среднем 10-15 лет.
-
Ремиттирующе-прогрессирующее — углубление имеющихся неврологических симптомов, наличие остаточной неврологической симптоматики после каждого обострения. На фоне постоянного прогрессирования возникают четкие периоды обострения. Во время ремиссии отмечается постепенное усиление симптомов заболевания.
-
Прогредиентное (прогрессирующее) течение — с незначительными облегчениями в самочувствии на фоне постоянного, но медленного ухудшения функций нервной системы — 40%.
Выделяют:
-
вторично-прогрессирущий РС (ВПРС) является последующей стадией ремиттирующего РС, отличается характерной динамикой клинических симптомов с постепенным нарастанием двигательных, координаторных нарушений без четких ремиссий;
-
первично-прогрессирующий РС (ППРС) — неуклонное прогрессирование с самого начала заболевания без четко очерченных ремиссий и обострений. ППРС отличается тяжелым течением с локализацией очагов демиелинизации и дегенеративно-дистрофических изменений в стволе, коре головного мозга, спинном мозге с более быстрой инвалидизацией больных. При данном типе течения РС в центральной нервной системе преобладает дегенеративный процесс над воспалительным, с начала заболевания имеет место нарастание неврологических симптомов, преимущественно спинальных, редко вовлекается оптическая сфера.
Также выделяют течение РС:
-
доброкачественное (клинически мягкое), с длительными и глубокими ремиссиями, практически отсутствие инвалидизации через 15 лет от начала заболевания — 20% случаев;
-
злокачественное (болезнь Марбурга) — быстрое развитие выраженных нарушений (вплоть до смертельного исхода) при массивном поражении ствола мозга — 15%.
Особо выделяют варианты РС:
-
оптикомиелит Девика (азиатский вариант) — преимущественное поражение зрительного нерва и спинного мозга;
-
лейкоэнцефалит Шильдера (демиелинизирующее заболевание у детей с образованием больших сливных очагов).
Рассеянный склероз у детей. Наши данные свидетельствуют о возможности не только развития РС в детском возрасте, но и его выявления с помощью клинических и дополнительных методов исследования [6]. Ввиду сложности диагностики и дифференциальной диагностики начальных стадий РС у детей возрастает роль дополнительных методов, прежде всего ЗВП, КТ и особенно МРТ. У детей имеются определенные особенности дебюта, ранних проявлений и течения РС, что в сочетании с иммуногенетическими особенностями наводит на мысль о некоторой клинико-иммуногенетической самостоятельности РС с началом в детском возрасте или в качестве самостоятельного заболевания. Учитывая также, что РС зачастую «зарождается» в детском и юношеском возрасте, чтобы затем проявиться развернутой клинической картиной уже во взрослом, необходимо обратить достаточное внимание на изучение этиологических и патогенетических механизмов именно в период инициальных и ранних проявлений РС. Тем самым может быть внесен существенный вклад в изучение этого тяжелого заболевания. Возраст начала РС у детей составляет 4-14 лет. Преобладают моносимптомное начало, ремиттирующее течение с частыми обострениями и относительно хорошим восстановлением функций во время ремиссий [6]. Анализ преморбидного периода и первых признаков болезни у пациентов с достоверным рассеянным склерозом показал возможность дебюта заболевания в детском и юношеском возрасте. Чаще всего это преходящая слабость в ноге или руке, реже в обеих ногах, которая проходила после отдыха без лечения. Реже наблюдалось онемение в них, которое незаметно исчезало. Особого внимания заслуживает поражение отдельных черепных нервов у детей и подростков, которые детскими неврологами оцениваются как самостоятельные заболевания: ретробульбарный неврит, невропатия лицевого нерва, глазная форма миастении [6, 12].
Диагностика РС
Диагноз РС основан, в первую очередь, на клинических критериях. Основным критерием клинически «достоверного» РС является диссеминация «в месте и во времени», т.е. выявление признаков не менее двух отдельно расположенных очагов в ЦНС, возникновение которых разделено по времени периодом не менее чем в месяц (т.е. эти очаги должны возникнуть не одновременно). Очень важно, что всегда диагноз РС должен ставиться в последнюю очередь, при исключении других причин подобного многоочагового поражения мозга.
Для обследования пациентов с подозрением на РС определен оптимальный диагностический алгоритм:
-
Клиническая картина, выявление неврологического поражения.
-
Офтальмологическое обследование.
-
МРТ головного мозга, спинного мозга.
-
Исследование вызванных потенциалов мозга.
-
Наличие олигоклональных IgG-связей в ликворе.
Инициальные симптомы, при которых можно заподозрить PC (могут периодически исчезать):
-
сужение поля и остроты зрения;
-
головная боль;
-
нарушения координации движений, системное головокружение с тошнотой, шаткость;
-
нарушение кожной чувствительности (ее снижение или парестезии в конечностях);
-
дисфункция мочевого пузыря;
-
снижение силы мышц;
-
синдром хронической усталости.
Выделение этого заболевания в отдельную нозологическую форму принадлежит французскому невропатологу Жану Мартену Шарко (Charcot), который обратил внимание на возникновение заболевания в молодом возрасте, ремиттирующий характер его течения и многоочаговость (рассеянность) поражения головного и спинного мозга в форме мелких островков глиосклероза (бляшек) и в 1868 г. описал известную «триаду» симптомов (нистагм, интенционный тремор, скандированная речь — триада Шарко [14]), определявшую клиническую картину рассеянного склероза в течение столетия. Позже, в 1936 г. австрийский невропатолог О.Марбург (O. Marburg) [15] предложил дополнить триаду Шарко такими симптомами, как отсутствие или вялость рефлексов и побледнение височных половин сосков зрительных нервов, а вместо скандированной речи ввел другой симптом — спастический парез (мышечная слабость) ног (пентада Марбурга), а в 1976 г. Д.А. Марков расширил и эти критерии — секстада Д.А. Маркова (зрительные нарушения с сужением полей зрения на цвета, немотивированным колебаниями зрения, вестибулопатии, непостоянные глазодвигательные расстройства (преходящее двоение), поражение пирамидной системы, изолированное снижение вибрационной чувствительности, коллоидно-белковая диссоциация в ликворе). Описанные симптомы остаются основополагающими в клинической диагностике РС и на современном этапе .
В 1965 г. Шумахером предложены диагностические критерии достоверного РС [23], включающие:
1) наличие объективной неврологической симптоматики; 2) поражение 2-х или более систем ЦНС; 3) выявление 1-го или 2-х паттернов: два или более эпизода, сохраняющиеся от суток до месяца; медленное или ступенчатое прогрессирование в течение 6-ти месяцев; 4) возраст больных не менее 10 и не более 50 лет; 5) поражение белого вещества мозга; 6) симптомы не могут быть объяснены другими причинами. Недостатком этих критериев является ограничение по возрасту в связи с учащением случаев более раннего и позднего дебюта заболевания; отсутствие учета степени выраженности признаков и лабораторных данных, что не позволяет следить за динамикой заболевания.
Для диагностики более сложных случаев, где не всегда удавалось достоверно диагностировать PC, Мак Альпином (1972) предложены три степени надежности распознавания PC [19]:
-
Достоверный РС: прогрессирующая нижняя параплегия; сочетание пирамидных и мозжечковых расстройств; поражение зрительного нерва; наличие ремиссий.
-
Вероятный РС — многоочаговое начало с хорошей ремиссией и мерцанием все той же симптоматики без признаков рецидива и прогрессирования в течение года и более.
-
Сомнительный РС: средний возраст; прогрессирующая нижняя параплегия; отсутствие отчетливых ремиссий.
С 1983 года в исследовательскую и клиническую практику вошли и стали общепринятыми разработанные международной группой экспертов во главе с С.М. Poser [22] критерии диагностики PC, которые включают лабораторно подтвержденный достоверный РС, когда диссеминация «в месте» доказывается наличием субклинических очагов дополнительными методами обследования, которые помимо клинических признаков включают еще и данные параклинических методов (компьютерной томографии, магнитно-резонансной томографии (МРТ), регистрации вызванных потенциалов головного мозга, определение олигоклонального IgG в ликворе). Однако за годы их применения стало очевидным, что перечень заболеваний, сходных с PC как по клиническим проявлениям, так и по данным дополнительных методов исследования, постоянно растет, перечень заболеваний, с которыми неврологу необходимо дифференцировать РС, представлен в табл. 2 [4, 5, 7, 12]. Очень важно, что всегда диагноз РС должен ставиться в последнюю очередь, при исключении других причин подобного многоочагового поражения мозга. При наличии одного эпизода с многоочаговым поражением головного мозга и с последующей ремиссией наиболее предпочтителен диагноз острого рассеянного энцефаломиелита (ОРЭМ), который во многих случаях клинически неотличим от первой атаки РС.
На сегодняшний день общепризнанными критериями диагностики рецидивирующее-ремиттирующего РС считаются новые диагностические критерии McDonald et al., 2001 [20]. Благодаря использованию зарегистрированных с помощью магнитно-резонансного исследования рассеивания «во времени» и «пространстве», эти критерии позволяют у ряда пациентов раньше диагностировать рассеянный склероз, чем стандартные способы диагностики клинически значимого рассеянного склероза. У многих больных уже на ранних стадиях заболевания при магнитно-резонансной томографии (МРТ) мозга выявляются множественные очаги, подтверждающие диссеминацию «в месте». Это могут быть очаги повышенной интенсивности на Т2-взвешенных изображениях (особенно при использовании программы FLAIR) в белом веществе и черные «дыры» на Т1-взвешенных изображениях, связанные с атрофией нервных волокон. При использовании контрастного усиления препаратами гадолиниума (магневиста) на Т1-взвешенных изображениях можно выявить активные очаги, так как парамагнитный контраст накапливается в зонах повышения проницаемости ГЭБ и активного воспаления.
Вызванные потенциалы повышают качество ранней диагностики РС и используются как метод выявления субклинических очагов у больных с вероятным и возможным диагнозом РС, подтверждая диссеминацию очагов в определенном месте.
Главное преимущество вызванных потенциалов — высочайшая чувствительность в определении электрофизиологических изменений в белом веществе (очагов), которые не сопровождаются неврологическими симптомами. Выявление 2-3-х бессимптомных очагов позволяет трансформировать вероятный диагноз рассеянного склероза в определенный вследствие доказательства диссеминации очагов демиелинизации в пространстве. Метод вызванных потенциалов позволяет обнаружить нарушение зрительных ВП в виде исчезновения или увеличения латентных периодов преимущественно основного пика P100, а также снижения его амплитуды и нарушения формы ответа. Удлинение латентности и снижение амплитуды пиков N140 и P190 также свидетельствует о замедлении проведения, а следовательно о поражении зрительных трактов. Проведенные нами исследования продемонстрировали важное значение метода ЗВП в ранней диагностике РС как у взрослых, так и у детей, особенно если отсутствуют соответствующие жалобы и признаки изменения зрения при офтальмологических исследованиях. ЗВП позволяют выявить субклинические «немые» очаги демиелинизации, нарушающие проведение импульсов по волокнам зрительного анализатора. Вместе с тем, изменение параметров ЗВП не обладает специфичностью и определяется и при других заболеваниях. ЗВП дополняют данные МРТ и повышают точность ранней диагностики РС до 78%. Диагностическое значение коротколатентных стволовых ВП на акустическую стимуляцию имеет исчезновение I, III и/или V пиков или значительное увеличение латентности III и V пиков с увеличением межпикового интервала I-V. Данное исследование особо информативно при выявлении субклинических очагов в стволе мозга.
Соматосенсорные ВП (ССВС) при стимуляции срединного нерва обращают внимание на увеличение латентности, снижение амплитуды и деформацию пиков Р13, Р22, Р37, при стимуляции заднего малоберцового нерва регистрируются пики N 22, P37. Наибольшая информативность этого исследования имеется при спинальной форме РС.
Считаем необходимым акцентировать внимание практического невролога на то, что, согласно используемым критериям диагностики McDonald et al., 2001, анализ спинномозговой жидкости считается положительным при выявлении нарушений, определяемых по одному из следующих результатов:
-
наличие олигоклональных IgG-связей, которые отличаются от таких связей в сыворотке;
-
повышенный индекс IgG.
Во многих клиниках мира для доказательства связи между иммунологическими и неврологическими симптомами проводят исследование СМЖ на наличие повышенного уровня иммуноглобулинов класса G(IgG), которые при изоэлектрическом фокусировании образуют олигоклональные группы. Высокую информативность в диагностике PC имеют только показатели цереброспинальной жидкости (ЦСЖ). Это определяется тем, что PC относится к органоспецифическим заболеваниям, причем органы-мишени (головной и спинной мозг) являются «забарьерными». Для PC не характерны системные клинические проявления.
К сожалению, на сегодняшний день в Украине нет стандартных наборов для выполнения этого теста, но в перспективе его проведение также расширит диагностические возможности. Многие клиницисты ошибочно принимают повышение обычных суммарных IgG в сыворотке крови, определяемый в наших лабораториях как диагностический критерий РС, что не корректно. Клиника имеет опыт подтверждения достоверного РС при помощи исследования олигоклональных IgG в ликворе у 15‑ти пациентов, проведенного в лаборатории Люблина, благодаря совместной работе с Львовским центром по изучению рассеянного склероза, руководимом д.м.н. Негрич Т.И.
Наиболее информативным и перспективным методом топической диагностики PC является МРТ [1, 6, 12]. Именно она дает возможность прижизненной визуализации многоочаговости поражения ЦНС при PC и в динамике позволяет судить о стадии процесса демиелинизации у конкретного больного. Однако результаты МРТ, взятые изолированно (без учета клинической картины заболевания), не являются абсолютным критерием в постановке диагноза PC. Ибо нами доказаны диссоциации между клинической степенью тяжести заболевания и степенью поражения демиелинизирующим процессом головного и спинного мозга по данным МРТ, что значительно осложняет выбор тактики ведения таких пациентов[7]. На основании МРТ головного мозга «рассеивание во времени» можно выявить по снимкам, полученным более чем через 3 месяца после начала обострения.
В качестве базисных МРТ-критериев РС принято использовать следующие параметры.
Для практической деятельности невролога предлагаем разработанный и апробированный на базе неврологического отделения ИНВХ АМН Украины им. Гусака В.К. следующий алгоритм диагностики РС.
ЛАБОРАТОРНЫЕ ПРИЗНАКИ, ПОДТВЕРЖДАЮЩИЕ ДИАГНОЗ РАССЕЯННОГО СКЛЕРОЗА
Положительная картина МРТ
3 пункта из 4-х нижеследующих:
-
1 очаг, накапливающий контраст или 9 гиперинтенсивных очагов в Т2 режиме при отсутствии очагов, накапливающих контраст;
-
1 или более субтенториальный очаг;
-
1 или более очаг вблизи коры головного мозга;
-
3 или более перивентрикулярных очага.
При этом 1 спинальный очаг может заменять 1 церебральный. Очаги должны быть более 3 мм в диаметре. Спинальные очаги не должны вызывать утолщения спинного мозга, распространяться более чем на 2 сегмента и занимать весь поперечник спинного мозга.
МРТ критерии «рассеянности в пространстве»: накопление контраста через 3 или более месяца в очагах, не соответствующих предшествующей атаке, или если накопление контраста отсутствует, следует повторить исследование еще через 3 месяца. Выявление новых очагов в Т2 или накопление контраста свидетельствуют о «рассеянности во времени».
Положительный ликвор: олигоклональные антитела в ликворе (при отсутствии в сыворотке) или повышение индекса IgG.
При проведении МРТ необходимо помнить о важности проведения МРТ-исследования как головного, так и спинного мозга, о наличии МРТ-негативных форм РС и о целесообразности МРТ-мониторирования, о роли использования контрастирования для выявления новых очагов обострения и подтверждения распространенности РС во времени [8].
На современном этапе для клинической оценки функционального состояния проводящих систем пациента при PC используется шкала FS (Kurtzke)[17].
С ее помощью оцениваются:
-
симптомы поражения пирамидного тракта,
-
симптомы поражения путей мозжечка,
-
симптомы поражения черепных нервов из-за поражения белого вещества ствола мозга,
-
симптомы поражения проводников чувствительности,
-
нарушения функций тазовых органов,
-
зрительные нарушения из-за поражения зрительного нерва,
-
нейропсихологические симптомы.
ОЦЕНКА ФУНКЦИОНАЛЬНЫХ СИСТЕМ ПО КУРТСКЕ (Functional system, 1989)
I. Пирамидная система
0 — норма;
1 — признаки патологии без двигательных нарушений;
2 — минимальные двигательные нарушения;
3 — от легкого до умеренного парапареза или гемипареза (явная слабость, но большинство движений может выполняться непродолжительное время, слабость представляет для больного проблему); выраженный монопарез (движения практически полностью отсутствуют);
4 — выраженный парапарез или гемипарез (движения затруднены), умеренный тетрапарез (двигательные возможности ограничены, движения могут выполняться непродолжительное время); или моноплегия;
5 — параплегия, гемиплегия или выраженный тетрапарез;
6 — тетраплегия.
II. Мозжечок
0 — норма;
1 — патологические симптомы без координаторных нарушений;
2 — легкая атаксия (явный тремор или неловкость движений, легкие нарушения координации);
3 — умеренно выраженная туловищная атаксия или атаксия в конечностях (тремор или неловкость движений нарушают все виды движений);
4 — тяжелая атаксия во всех конечностях (большинство двигательных функций трудновыполнимо);
5 — невозможность выполнения координированных движений в связи с атаксией.
Укажите «+» в случае, если имеется слабость (3-й степени или более выраженная в связи с поражением пирамидной системы)
III. Стволовые функции
0 — норма;
1 — только патологические симптомы;
2 — умеренно выраженный нистагм или другие легкие нарушения;
3 — грубый нистагм. Выраженная слабость наружных глазодвигательных мышц или умеренное нарушение функций других черепно-мозговых нервов;
4 — выраженная дизартрия, или какое-либо другое нарушение функций;
5 — невозможность глотать или говорить.
IV. Чувствительность
0 — норма;
1 — снижение вибрационной чувствительности или двумерно-пространственного чувства в одной или двух конечностях;
2 — легкое снижение тактильной или болевой, или глубокой чувствительности и/или умеренное снижение вибрационной чувствительности в одной или двух конечностях; или снижение вибрационной чувствительности (двумерно-пространственного чувства) в трех или четырех конечностях;
3 — умеренное снижение тактильной или болевой или глубокой чувствительности и/или существенное снижение вибрационной чувствительности в одной или двух конечностях; или легкое снижение тактильной или болевой чувствительности и/или умеренное снижение во всех пробах на глубокую чувствительность в трех или четырех конечностях;
4 — выраженное снижение тактильной или болевой чувствительности или потеря проприоцептивной чувствительности, изолированные или в сочетании друг с другом в одной или двух конечностях; либо умеренное снижение тактильной или болевой чувствительности и/или грубое снижение проприоцептивной чувствительности в более чем двух конечностях;
5 — выпадение всех видов чувствительности в одной или двух конечностях; или умеренное снижение тактильной или болевой и/или потеря проприоцептивной чувствительности почти на всей поверхности туловища.
V. Функции тазовых органов
(брать за точку отсчета позывы на мочеиспускание или наиболее грубые нарушения будьто мочеиспускание или дефекация)
0 — норма;
1 — легкая задержки мочеиспускания или императивные позывы;
2 — умеренно выраженная задержка или императивные позывы на мочеиспускание или дефекацию или редко возникающее неудержание мочи (периодическая самокатетеризация, сдавление руками мочевого пузыря для его опорожнения ил эвакуация кала при помощи пальцев);
3 — частое недержание мочи;
4 — требуется практически постоянная катетеризация (и постоянные вспомогательные меры для эвакуации стула);
5 — утрата функции мочевого пузыря;
6 — утрата тазовых функций.
VI. Функция зрения
0 — норма;
1 — скотома с остротой зрения (корригируемой) выше 0,6 (20/30);
2 — скотома на стороне худшей остроты зрения с максимальной остротой зрения (корригируемой) от 0,6 (20/30) до 0,35 (20/59);
3 — большая скотома на стороне худшего зрения либо ограничение полей зрения, с максимальной остротой зрения (корригируемой) от 0,35 (20/60) до 0,15-0,2 (20/99);
4 — на стороне хуже видящего глаза выраженное ограничение полей зрения с максимальной остротой зрения (корригируемой) от 0,2 (20/100) до 0,1 (20/200); 3 степень плюс максимальная острота зрения у лучше видящего глаза от 0,35 (20/60) и ниже
5 — максимальная острота зрения у хуже видящего глаза (корригируемая) менее 0,1 (20/200); 4 степень плюс максимальная острота зрения у лучше видящего глаза от 0,35 (20/60) и ниже;
6 — 5 степень плюс максимальная острота зрения у лучше видящего глаза от 0,35 (20/60) и ниже.
VII. Церебральные функции
0 — норма;
1 — только нарушения настроения (не влияющие на балл EDSS);
2 — легкое снижение мыслительных процессов;
3 — умеренное снижение мыслительных процессов;
4 — выраженное снижение мыслительных процессов;
5 — деменция либо некомпетентность больного.
VIII. Другие функции
(какие-либо другие неврологические симптомы, связанные с РС)
а) Спастичность:
0 — нет;
1 — легкие (выявляемые только при специальных пробах);
2 — умеренные (легкое нарушение функции);
3 — выраженные (выраженные нарушения функции).
б) Другие:
0 — нет;
1 — укажите какие-либо другие симптомы, связанные с РС.
Проведенный анализ по функциональным системам лежит в основе оценки инвалидизации больных. Следующим этапом на основании степени выявленных нарушений по основным проводящим системам (шкала FS) оценивается инвалидизация больных по расширенной шкале инвалидизации по Куртске (Expanded Disebility Status Scale, EDSS) [18]. Она же используется для оценки эффективности проводимой терапии. Т.е. существует как бы шкала в шкале, т.к., не проведя оценку по шкале FS, нельзя установить степень инвалидизации по EDSS.
Нами адаптирована шкала EDSS при установлении группы инвалидности для пациентов РС, исходя из положения о I, II, III группе инвалидности.
Расширенная шкала инвалидизации по Куртске (Expanded Disebility Status Scale, EDSS, 1983)
0.0 — Норма в неврологическом статусе по всем ФС.
1.0 — Признаков инвалидизации нет. Минимальные признаки нарушений (1 степени) в одной функциональной системе (ФС), исключая церебральную.
III группа инвалидности устанавливается:
1.5 — Признаков инвалидизации нет. Минимальные признаки нарушений (1 степени) в более чем одной ФС (за исключением церебральной).
2.0. — Легкие признаки инвалидизации нарушений (2 степени) в одной ФС.
2.5 — Легкие признаки инвалидизации нарушений (2-й степени) в двух ФС.
0.0 — Умеренные признаки инвалидизации нарушений (3-й степени) в одной ФС либо легкие признаки инвалидизации (2 степени) в 3-х или 4-х ФС. Ходячий.
3.5 — Ходячий. Умеренные признаки инвалидизации нарушений (3-й степени) в одной ФС и в 1-2 ФС — 2-й степени. Либо в 2-х ФС — 3-й степени. Либо в 5 ФС — 2-й степени.
1.0 — Ходячий, посторонней помощи не требует. Самообслуживание сохранено. Проводит в повседневной активности около 12 часов в день. Относительно выраженные признаки инвалидизации (4 степени) в 1 ФС либо сочетание меньших степеней инвалидизации, но превышающее значения предыдущих баллов. Может пройти без посторонней помощи или остановки около 500 м
4.5 — Ходячий, посторонней помощи не требует. Повседневная активность не нарушена. Может ходить в течение всего дня. Возможна необходимость в небольшой помощи. Относительно выраженные признаки инвалидизации (4 степени) в 1 ФС либо сочетание меньших степеней инвалидизации, превышающее значения предыдущих баллов. Может пройти без посторонней помощи или остановки около 300 м.
II группа инвалидности устанавливается:
5.0 — Может пройти без посторонней помощи или остановки около 200 м. Повседневная активность нарушена. В 1 ФС — 5-я степень либо сочетание меньших степеней инвалидизации, превышающее значения для 4,0 баллов.
5.5 — Может пройти без посторонней помощи или остановки около 100 м. Повседневная активность ограничена. В 1 ФС — 5-я степень либо сочетание меньших степеней инвалидизации, но превышающих степени, оговоренные в пункте 4,0.
1.0 — Ходьба с периодической/односторонней постоянной поддержкой около 100 м и или без отдыха. 3 степень в более чем 2-х ФС.
6.5 — Ходьба с постоянной двусторонней поддержкой около 20 м без отдыха. 3 степень более чем в 2-х ФС.
I группа инвалидности устанавливается:
7.0 — Не может пройти даже 5 м без помощи. Прикован к инвалидной коляске, в которой передвигается самостоятельно. Посторонняя помощь не требуется. Повседневная активность в инвалидной коляске 12 часов в день. 4-я степень более чем в 1 ФС. Очень редко 5-я степень только в пирамидной системе.
7.5 — Может пройти всего несколько шагов. Передвигается только в инвалидной коляске. Требуется помощь в передвижении. Не может находиться в инвалидной коляске в течение всего дня. 4-я степень более чем в одной ФС.
8.0 — Прикован к кровати/стулу или передвигается в инвалидной коляске. Может находиться вне постели большую часть дня. Основные функции самообслуживания сохранены. Активно пользуется руками. 4-я степень в нескольких ФС.
8.5 — Прикован к постели большую часть дня. В некоторой степени может пользоваться руками. Самообслуживание частичное. 4-я степень в нескольких ФС.
8.0 — Беспомощный, прикованный к постели больной. Может вступать в контакт и есть. 4-я степень в большинстве ФС.
9.5 — Полностью беспомощный, прикованный к постели больной. Не может полностью вступать в контакт или есть/глотать. 4-я степень практически во всех ФС.
10.0 — Смерть из-за рассеянного склероза.
Стадии EDSS ниже 4-х баллов характеризуют пациентов, способных проходить без поддержки более 500 м, а точная стадия определяется баллами оценки ФС. Стадии между 4,0 и 5,0 баллами определяются как баллами оценки ФС, так и пройденным расстоянием. Общее правило — балл определяется по самому низкому из этих двух показателей. Стадии 5,5-8,0 определяются исключительно пройденным расстоянием, использованием кресла-коляски или необходимостью помощи при перемещении. Балл EDSS не должен быть ниже любого из баллов ФС (кроме зрения и ФС кишечника/мочевого пузыря). В определение стадий 6,0 и 6,5 включено как описание необходимой поддержки, так и расстояние ходьбы. Если пациент может пройти более 100 м с двумя тростями или костылями, его состояние оценивается баллом 6,0. Если пациент может пройти значительно более 10 м, но не более 100 м с двумя тростями или костылями, его состояние оценивается баллом 6,5.
Пример формулировки диагноза 1:
Рассеянный склероз, цереброспинальная форма, с выраженным парезом правого отводящего нерва (3 балла), умеренной дизартрией (2 балла), выраженным нижним парапарезом (3 балла), легкой атаксией (1 балл), легким снижением вибрационной чувствительности в нижних конечностях (1 балл), умеренным нарушением функции ходьбы (2 балла); ремиттирующее течение, стадия обострения (EDSS = 3,5 балла). В приведенном примере общий балл по EDSS определяется наличием у больного 3-х баллов по двум ФС. Такой пациент должен быть признан инвалидом III группы.
Пример формулировки диагноза 2:
Рассеянный склероз, преимущественно спинальная форма, с умеренно выраженным нижним парапарезом (2 балла), легким снижением вибрационной чувствительности в нижних конечностях (1 балл), умеренным нарушением функции ходьбы (2 балла), императивными позывами к мочеиспусканию (1); ремиттирующее течение, стадия обострения (EDSS = 2,5 балла). В приведенном примере общий балл по EDSS определяется наличием у больного 2-х баллов по двум ФС. Такой пациент должен быть признан инвалидом III группы
Пример формулировки диагноза 3:
Рассеянный склероз, цереброспинальная форма, с выраженным снижением интеллекта (4), выраженным спастическим нижним парапарезом (4 балла), умеренным снижением вибрационной чувствительности в нижних конечностях (2 балл), выраженным нарушением функции ходьбы (3 балла), недержанием мочи (4); ремиттирующее течение, стадия обострения (EDSS =5,0 баллов). В приведенном примере общий балл по EDSS определяется наличием у больного 4 баллов по трем ФС. Такой пациент должен быть признан инвалидом II группы.
В клинической практике и в целях экспериментальных исследований для оценки степени выраженности обострений и оценки степени восстановления нарушенных функций на фоне проведенного лечения при РС используется шкала NRS, 1984 [24].
Таким образом, определяя тактику лечения больного РС, невролог должен четко представлять, какой процесс у каждого больного, установить достоверный диагноз РС, чтобы быть уверенным в назначении той или иной терапии как оптимальной для данного типа и фазы заболевания, уметь проводить оценку эффективности проводимого лечения, используя представленный материал.
Литература
1. Бисага Г.Н., Головкин В.И., Лытаев С.А., Михайленко А.А. Современные методы диагностики рассеянного склероза // Журн. невропатол. и психиатр.- 1996. — Т.96, №6. — С. 40-43.
2. Бисага Г.Н. Рассеянный склероз. Современные представления, диагностика и лечение. — Санкт-Петербург: Аспект плюс, 2001. — 41 с.
3. Бринар В.В., Позер Ч.М. Лабораторные методы в диагностике рассеянного склероза // Журн. невропатол. и психиатр.- 2002. — Т. 102, №1. — С. 7-14.
4. Вінничук С.М., Мяловицька О.А. Розсіяний склероз: Навчальний посібник. — К., 2001. — 56 с.
5. Гусев Е.И., Демина Т.Л., Бойко А.Н. Рассеянный склероз. — Москва, 1997. — 463 с.
6. С.К. Евтушенко, В.Н. Ефименко Клинико-инструментальные и иммунологические исследования рассеянного склероза у детей // Журн. невропатол. и псих. — 2000. — № 3. — С. 83-86.
7. Деревянко И.Н., Евтушенко С.К., Антимонов И.А. Особенности топизации очагов демиелинизации и МРТ-мониторинга при рассеянном склерозе // Рассеянный склероз: лечение и оздоровление.- Мат. 9-го симпозиума Всероссийского общества рассеянного склероза. — Санкт-Петербург, 2000. — С. 31-33.
8. Евтушенко С.К., Деревянко И.Н. Магнитно-резонансная томография в диагностике рассеянного склероза // Журнал невологии и психиатрии им. С.С. Корсакова. — 2001.- Т.101.- №4.- С. 61-64.
9. Евтушенко С.К. Значение клинической диагностики межъядерного офтальмопареза для определения очага поражения и симптоматики при обострении хронической текущей нейроинфекции // Журн. невропат. и псих. — 1991. — № 2. — С. 44-47.
10. Жулев Н.М., Скоромец А.А., Трофимова Т.Н., Тотолян Н.А. Cовременная диагностика рассеянного склероза. — Санкт-Петербург: Изд-во СПбМАПО, 1998. — 28 с.
11. Рассеянный склероз. Избранные вопросы теории и практики // Под редакцией И.А. Завалишина, В.И. Головкина. — Москва. — 2000. — 639 с.
12. Рассеянный склероз: клинические аспекты и спорные вопросы: Пер. с англ. / Под ред. А. Томпсона, К. Полмана, Р. Холфельда: Санкт-Петербург: Политехника, 2001.- 422 с.
13. Шмидт Е.В., Хондкариан О.А., Завалишин И.А. Организация эпидемиологических исследований и клинические критерии диагноза рассеянного склероза // Журн. невроп. и псих. — 1980. — № 2. — С.161-165
14. Charcot J.M. Sclerose en plagues. Lecons sur maladies du systeme nerveux // Paris, 1875. — V. 1. — P. 168-240
15. Marburg O. Die sogenannte acute multiple sclerosis // Psuchiat.Neurol. — 1906. — V.27. — P. 213-220
16. Barkhoff F., Fillipi M., Losseff N. et al. Towards specific magnetic resonance imaging criteria in the early diagnosis of multiple sclerosis // Neurology. — 1995. — Vol.45(4). — A 398.
17. Fazekas F., Offenbacher H., Fuchs S. et al. Criteria for an increased specificity of MRI interpretation in elderly subjects with suspected multiple sclerosis // Neurology. — 1988. — Vol. 38(12). — P. 1822-1825.
18. Kurtzke J.F. Rating neurological impairment in multiple sclerosis: an expanded disability status scale (EDSS) // Neurology. — 1983. — №3. — Р . 1444-1452.
19. McAlpine, Lunsdene, Acheson E.M. Multiple sclerosis: a reappraisal — 2 ed. — Edinburg, London, Livingstone. — 1972. — 308 p.
20. McDonald W., Compston A., Edan G. et al. Recommended Diagnostic Criteria for Multiple Sclerosis: Gguidelines from the International Panel on the Diagnosis of Multiple Sclerosis// Annals of Neurology. — 2001. — Vol. 50. — P.121-127.
21. Paty D.W., Oger J.J.F., Katrikoff L.F. MRI in the diagnosis of clinical evaluation, evoked potentials, oligoclonal banding and CT // Neurology. — 1988. — Vol. 38(2). — P. 180-184.
22. Poser C.M., Paty D., Scheinberg L. et al. New diagnostic criteria for multiple sclerosis guidelines for reseatch protocols // Ann Neurol. — 1983. — Vol. 13(2). — P. 227-231.
23. Schumacher G.A., Beeb G.W., Kibler R.F. et al. Problems of experimental trias of therapy in multiple sclerosis // Ann N 4 Acad Sci. — 1965. — Vol. 122 (5). — P. 552-568.
24. Sipe J.C., Knober R.L.,Braheny S.L.A neurologic rating scale (NRS) for use multiple sclerosis // Neurology. -1984. — Vol.34(10). — P. 1368-1372.
— Почему второе мнение имеет решающее значение для диагностики рассеянного склероза?
—Возможно, основным фактором является то, что не существует конкретного биомаркера, анализа или обследования, которое стопроцентно подтвердило бы этот диагноз. Симптомы этого заболевания настолько разнообразны, что клинически определить его практически невозможно. В то же время, очаги на МРТ, которые видит врач, могут быть признаками совсем другой проблемы. Поэтому в случае с рассеянным склерозом во многих странах второе мнение рекомендовано.
— С каким жалобами чаще всего обращаются люди к врачу при рассеянном склерозе?
— Самые распространенные симптомы — нарушение чувствительности и снижение зрения. Кроме того, первоначальные симптомы этого заболевания могут включать двигательные нарушения, двоение в глазах, слабость, усталость, головокружение, невнятную речь, тремор и проблемы с контролем мочевого пузыря и кишечника. Или сочетание нескольких таких состояний. Как и будут ли возникать эти симптомы, зависит от пораженных нервов.
— Какие диагнозы в первую очередь исключают при диагностике рассеянного склероза?
— При дифференциальной диагностике в первую очередь врач исключает некоторые воспалительные, инфекционные и наследственные заболевания. Основное — это острый рассеянный энцефаломиелит. Кроме того, рассеянный склероз дифференцируется от других заболеваний, при которых поражается белое вещество головного и/или спинного мозга: опухоли ЦНС, нейродегенеративные заболевания, миелопатии, ВИЧ-энцефалопатия, головокружение различного генеза, гиповитаминоз В12 и другие. То есть, из этого списка видно, насколько сложно диагностировать именно рассеянный склероз.
— А есть данные о том, при каких нарушения чаще всего ошибочно выставляется рассеянный склероз?
— Недавно было опубликовано исследование, из которого следует, что чаще всего рассеянный склероз неверно диагностируется при мигрени, фибромиалгии, конверсионных расстройствах, оптикомиелите и ассоциированными с ним заболеваниями.
— Какие последствия неправильной диагностики могут быть?
— Если у человека не рассеянный склероз, а другое заболевание, то его нужно выявить и назначить правильное лечение. Если же пациент начнет принимать препараты от рассеянного склероза, то он может столкнуться с побочными эффектами. В то же время, очень важно вовремя диагностировать именно рассеянный склероз, потому что чем раньше начать принимать препараты, тем медленнее будет прогрессировать заболевание и тем лучше будет эффект от лечения. Это доказано многочисленными исследованиями.
Диагноз рассеянный склероз может быть ошибкой
Группа ученых из Университета Калифорнии в Лос-Анджелесе (UCLA) и Университета Вермонта в Берлингтоне пришла к выводу, что многие люди с диагнозом рассеянный склероз на самом деле страдают от другой болезни и проходят неправильное лечение.
Рассеянный склероз (РС) – это аутоиммунная болезнь, при которой иммунная система разрушает миелиновую оболочку собственных нервов, что приводит к нарушению проведения нервных импульсов. Некоторые симптомы РС похожи на проявления инсульта, мигрени и других болезней.
В ходе исследования были проанализированы истории болезней 241 пациента с диагнозом рассеянный склероз. Оказалось, что в 110 случаях есть сомнения в правильности поставленного диагноза. Если точнее, то в 51 случае речь шла о доказанной ошибке, а в 59 случаях – о вероятной ошибке диагностики.
Из 110 выделенных случаев у 22% пациентов оказалась мигрень (отдельно или в сочетании с другими патологиями), фибромиалгия – у 15% больных, неспецифические и нелокализованные неврологические симптомы с аномальной МРТ – в 12% случаев, конверсионные психосоматические расстройства – в 11% случаев и оптический нейромиелит – в 6% случаев.
Треть пациентов из этой группы жили с ошибочными диагнозами по 10 лет и более, причем в 72% случаев была возможность поставить правильный диагноз. В большинстве же случаев лечения от несуществующего РС длилось 4 года и более. В 4% случаев пациенты даже участвовали в исследования экспериментальных препаратов для лечения РС.
В результате неправильно поставленного диагноза 70% получали болезнь-модифицирующую терапию, которая уменьшала проявления заболевания, а 31% пациентов в результате неправильного лечения получили дополнительные патологии.
По оценкам исследователей, стоимость ненужного лечения, которое получали участники проекта с неправильным диагнозом рассеянный склероз, составляет почти 10 млн долларов. При этом люди страдали от побочных эффектов лекарств, которые были им не нужны, и не получали лечение от реально болезни.
Читайте далее
Тревожность и как с ней бороться
Тревогу может испытывать любой человек в связи со стрессом, неприятностями. Но бывает, что, вроде, беспокоиться не о чем, а тревога мучает всё равно.
Опубликовано 23.04.2019 06:47, обновлено 17.04.2020 16:08
Ссылка на первоисточник:
Читайте также

Как правило, дебют болезни происходит в молодом возрасте, до 45 лет, но в настоящее время описаны случаи развития данной патологии и в детском, и в пожилом возрастах. Чаще заболевают женщины. Кроме того, выявлена закономерность более частого развития заболевания в странах с хорошими санитарными и гигиеническими условиями.
Некоторые ученые связывают это с поздним созреванием иммунитета у детей, растущих в благополучной санитарной обстановке. Нет однозначного мнения о наследственной его природе. Однако, доказано, что основными факторами риска являются хронические стрессовые ситуации и инфекции (вирус Эпштейна–Барр). Важными являются пониженный уровень витамина D, курение, факторы окружающей среды, питание.

Важным фактором для успешного лечения рассеянного склероза является его диагностика на ранней стадии развития.
Как выявить рассеянный склероз самостоятельно
Данная патология, как правило, выявляется по характерным симптомам и при сборе анамнеза. Довольно часто у больных выявляются признаки поражения пирамидного тракта: парапарез, монопарез, гемипарез.
Характерны оптический неврит, горизонтальный и вертикальный нистагмы, диплопия. Вестибулярные изменения при поражении структур мозжечка, спастический паралич, скандированная речь и макрография, статическая и динамическая атаксия, тремор, изменения чувствительности, симптом Лермитта, изменения функции тазовых органов, в том числе сексуальной, изменения настроения, психических и интеллектуальных функций.

В связи с таким разнообразием проявлений заболевания, пациенту следует при наличии любых неврологических изменений, а особенно при сочетании нескольких, обратиться за консультацией к квалифицированному неврологу. Самостоятельно можно лишь заподозрить рассеянный склероз при наличии вышеперечисленных клинических форм, но диагностика должна проводиться в медицинском учреждении.

Диагностика РС в лечебном учреждении
Выделяют основные формы течения РС:
- Ремиттирующий, характеризуется периодами обострения и ремиссии, которая может длиться до нескольких лет.
- Вторичный прогрессирующий РС, в этом случае также выделяют стадии обострения и ремиссии, но характерно наступление стадии хронического прогрессирования, с усиливающейся остаточной симптоматикой.
- Первично — прогрессирующий рассеянный склероз, постоянное усиление признаков изменения ЦНС, без обострений и ремиссии.
Достоверная постановка диагноза рассеянный склероз возможна только в стенах лечебных учреждений, достаточно оснащенных современной аппаратурой и имеющих в штате высококвалифицированных специалистов-неврологов.
На данный момент не существует специфического для РС теста или маркера, кроме своеобразного клинического течения и характерных морфологических изменений, однако, врачами-неврологами используется так называемые шкалы.
В них достоверно рассеянный склероз может быть выявлен при соблюдении обязательного требования — «диссеминации во времени и месте». Заключается оно в появлении не менее двух очагов патологического процесса, которые разбросаны во времени не меньше, чем на один месяц. Чаще всего для этой цели используются шкала критериев Позера.
Критерии Мак-Дональда
Новые характеристики для постановки диагноза рассеянный склероз, в которых впервые начали использовать результаты МРТ для подтверждения рассеивания процесса в пространстве и во времени.
На сегодняшний день, важнейшими методами для постановки диагноз РС, являются:
- магнитно-резонансная томография головного и спинного мозга;
- анализ наличия олигоклональных групп иммуноглобулинов G (IgG) в спинно-мозговой жидкости (СМЖ);
- а также оценка изменения вызванных потенциалов (ВП).
Самым главным инструментом для диагностики мультиочагового процесса в мозге считается МРТ, но эти изменения не являются специфичными только для РС, часто они выявляются при других заболеваниях ЦНС.
МРТ-критерии рассеивания процесса в пространстве следующие: обнаружение одного Т1-гиперинтенсивного очага, либо девяти Т2 очагов; одного субтенториального очага; или одного и более очагов около коры головного мозга; а также трех и более паравентрикулярных очагов.
МРТ очаги рассеянного склероза
При наличии хотя бы трех из этих критериев можно говорить о диссеминации процесса в пространстве. Касательно разобщения во времени, критерии следующие: обнаружение нового Т1 очага, через 3 месяца после предыдущей атаки, либо дополнительные Т2 очаги также через 3 месяца после клинических проявлений.
Необходимо отметить, что при достоверном рассеянном склерозе данные МРТ недостаточно сопоставимы с клиникой. Новые очаги в мозге возникают чаще, чем клинические обострения.


Шкала EDSS
Еще одна шкала, характеризующая состояние больного рассеянным склерозом, носит название EDSS. В ней находят отражения функциональные нарушения, также она помогает оценить тяжесть инвалидизации пациента.
| Баллы по шкале EDSS | Клиническая картина |
|---|---|
| 1.0-1.5 | Нет нарушений. |
| 2.0-2.5 | Амбулаторный пациент, с минимальными или незначительными нарушениями. |
| 3.0-3.5 | Пациент с умеренными нарушениями, может присутствовать слабость, монопарез. |
| 4.0 | Достаточно выраженная слабость, но больной может пройти без отдыха 500м, обслуживает себя полностью сам. |
| 4.5 | Пациент может пройти самостоятельно до 300м в день, необходима минимальная помощь. |
| 5.0 | Пациент может работать, но неполный рабочий день, самостоятельно способен пройти 200м. |
| 5.5 | Занятость также неполный рабочий день, может пройти 100м без поддержки и отдыха. |
| 6.0 | Ходит только с помощью, на расстояние 100м, поддержка односторонняя. |
| 6.5 | Возможна только ходьба до 20м, с двусторонней поддержкой |
| 7.0 | Передвижение только в кресло-коляске, может самостоятельно ей управлять весь день. |
| 7.5 | Передвигается только в кресле-коляске и только с помощью, ограниченное время. |
| 8.0 | Активность пациента только в пределах кровати или кресла, обслуживает себя, используя руки. |
| 8.5 | Больной старается использовать руки в обслуживании, но требуется помощь. |
| 9.0 | Пациент находится только в кровати, сохраняется способность к общению и питанию. |
| 9.5 | Абсолютно беспомощен, невозможно общение, глотание. |
Данная шкала сопоставима с группами инвалидности. Баллы 3,0-4.5 соответствует третьей группе инвалидности, 5.0-7,0 –второй, а 7.5-9.5 первой группе.
Шкала EDSS (кликабельно)
Диагностические тесты и лабораторные анализы
Характерным для РС также будет повышение концентрации иммуноглобулинов G (IgG) и выявление олигоклональных антител в СМЖ методом изоэлектрического фокусирования. Необходимо иметь в виду, что наличие олигоклональных антител в СМЖ отмечается у больных мигренями, неврологическими проявлениями ВИЧ, воспалительными заболеваниями мозга.
В постановке диагноза также используются данные изменения характеристик вызванных потенциалов (ВП). Они не являются тестом для рассеянного склероза, но могут быть использованы как метод объективизации наличия скрытых клинически очагов у больных с вероятным 
Довольно часто при рассеянном склерозе отмечается лимфоцитарный плеоцитоз в СМЖ. Также значение имеет выявление клонов Т-клеток, чувствительных к антигенам миелина, рецепторов к цитокинам, продуктов расщепления миелина, и других участников воспаления и аутоиммунных реакций.
Перечисленные изменения не являются строго специфичными для РС, но, комплексная оценка данных клинических, иммунологических, инструментальных и биохимических методов исследования позволяет определить характер течения заболевания, стадию, остроту, эффективность проводимой терапии.
Дифференциальный диагноз РС: таблица
Дифференциальная диагностика рассеянного склероза достаточно сложна, особенно с теми заболеваниями, которым присущи свойства диссеминации процесса. Кроме того, РС не имеет ни одного характерного признака, его клиника отличается полиморфизмом, это и вызывает трудности в постановке диагноз.
В 10–15% случаев ставится ошибочный диагноз, и на самом деле пациент имеет другое схожее с рассеянным склерозом, заболевание.
| Заболевание | Дифференциальный диагноз с РС |
|---|---|
| Острый рассеянный энцефаломиелит (ОРЭМ) | Монофазное течение, инфекционное заболевание в анамнезе.
Диагноз определяется по динамике процесса. |
| Хронический боррелиозный энцефаломиелит | Сведения о контакте с клещом.
Сочетанное поражения ЦНС и периферической нервной системы. Наличие антител к боррелии в СМЖ. |
| ВИЧ | Серологическое исследование крови и СМЖ. |
| Саркоидоз | Определение ангиотензин конвертирующего энзима в анализе крови, биопсия доступного очага. |
| Антифосфолипидный синдром (АФС), синдром Шегрена, синдром Бехчета | Гемолитическая анемия, тромбоцитопения, нахождение антифосфолипидных антител, артериальные и венозные тромбозы, хроническое не вынашивание беременности. |
| Системная красная волчанка (СКВ) | Системное поражение суставов, почек, кожи, позитивная серологическая реакция («волчаночные клетки»), высокий титр антинуклеарных антител. |
| Наследственные миелинопатии (болезнь Александера, адренолейкодистрофия, суданофильная лейкодистрофия) | Данные о семейном анамнезе, нарастающий характер симптоматики, признаки поражения ЦНС и периферической НС. |
| Болезнь Лебера, синдром MELAS | Диагноз подтверждается на основании исследования метаболизма митохондрий. |
| Опухоли ЦНС | Верификация по результатам биопсии очага. |
Исходя из выше сказанного, диагностика рассеянного склероза должна проводиться с учетом всех имеющихся анамнестических, наследственных, инструментальных и лабораторных данных. При анализе информации должны быть задействованы новейшие критерии оценки и диагностические шкалы, что позволит свести к минимуму неточности в диагностике и минимизировать процент постановки неверных диагнозов.
Мы уже публиковали большой материал на тему, ошибается ли МРТ. Если говорить коротко, то процент ошибок МРТ зависит в меньшей степени от качества аппаратуры, и в большей степени — от уровня квалификации врача-рентгенолога (радиолога), который анализирует снимки МРТ исследования. Давайте посмотрим, какие распространенные ошибки расшифровки МРТ встречаются в практике врачей, а также расскажем, что делать при врачебных ошибках.
ТИПИЧНЫЕ ОШИБКИ МРТ ГОЛОВНОГО МОЗГА
Ошибочный диагноз рассеянный склероз. Болезни, похожие на рассеянный склероз на МРТ – это дисциркулярторная энцефалопатия, различные виды васкулитов, ангиопатий, и т.д. Эти заболевания проявляются множественными очагами в белом веществе. Такж не всегда множественные очаги демиелинизации в головном мозге на МРТ представляют собой рассеянный склероз.
Неточное описание МРТ при рассеянном склерозе. В заключении МРТ при рассеянном склерозе должно быть точно указано количество и размеры перивентрикулярных, юкстакортикальных, субтенториальных очагов; характеристики контрастного усиления при рассеянном склерозе, МРТ-признаки активности рассеянного склероза.
Киста или опухоль головного мозга? Часто врачи не могут разобраться в том, что нашли на МРТ – кисту или опухоль мозга. Здесь поможет только опытный диагност – нейрорадиолог со стажем.
Не установлена причина эпилепсии у детей. МРТ головного мозга при эпилепсии у детей требует более тщательного анализа, и ее правильная расшифровка – дело высокой квалификации. Неопытный рентгенолог может проглядеть тонкие, скрытые изменения (фокальная кортикальная дисплазия, гетеротопия серого вещества и т.д.)
Диагностические ошибки при микроаденоме гипофиза. Увы, этот диагноз зачастую ставится по МРТ необоснованно. Причина тому – плохое знакомство врачей с нормальными вариантами строения гипофиза.
Ошибки при диагностике ВИЧ-инфекции. Если у вас ВИЧ-инфекция — расшифровка снимков МРТ может быть очень сложной. Нужно исключить многочисленные ВИЧ-ассоциированные инфекции и опухоли.
Ошибочный диагноз микроцефалии, гидроцефалии и врожденных пороков головного мозга. Все эти состояния требуют точного знания детской рентгенологии, без большого опыта в расшифровке МРТ у детей высок шанс ошибиться.
Ошибочный диагноз рака мозга, глиобластомы, опухоли головного мозга. Иногда за опухоль принимаются другие состояния – инсульт, кровоизлияние, псевдотуморозная форма рассеянного склероза и т.п. Нередко в заключении МРТ нечетко описана локализация опухоли, ее размеры, степень контрастного усиления опухоли и т.д. – все это влияет на точность диагностики.
Псевдотуморозная форма рассеянного склероза — болезнь Шильдера. Как правило, по МРТ ставится неверный диагноз опухоль мозга.
Первичное заключение по МРТ — рассеянный склероз. Экспертный пересмотр МРТ снимков и анализ клинической картины установил правильный диагноз: системный васкулит.
ЧТО ДЕЛАТЬ, ЕСЛИ ДИАГНОЗ НЕВЕРНЫЙ?
Показать снимки МРТ другим специалистам! Можно обратиться к опытным врачам-нейрорадиологам и послать им МРТ с диска на повторную консультацию. Например, врачи Национальной телерадиологической сети осуществляют пересмотр результатов МРТ и выдают свое экпертное заключение по МРТ головного мозга. Этой службой пользуются не только пациенты, но и российские клиники. Сложные и спорные диагностические случаи стекаются к узким специалистам. Получить Второе мнение по МРТ головного мозга просто — достаточно взять диск с записью МРТ и загрузить его через специальную форму.
Читать подробнее о Втором мнении по КТ и МРТ
Читать подробнее о телемедицине
Кандидат медицинских наук, член Европейского общества радиологов
Рассеянный склероз
Версия: Клинические рекомендации РФ 2022 (Россия)
Категории МКБ:
Рассеянный склероз (G35)
Разделы медицины:
Неврология
Общая информация
Краткое описание
Разработчик клинической рекомендации:
- Всероссийское общество неврологов
- Национальное общество нейрорадиологов
- Медицинская ассоциация врачей и центров рассеянного склероза и других нейроиммунологических заболеваний
- Российский комитет исследователей рассеянного склероза
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 июня 2022 года – с 1 января 2024 года.
Возрастная категория: Взрослые, Дети
Пересмотр не позднее: 2024
Дата размещения:13.07.2022
ID:739
Определение заболевания или состояния (группы заболеваний или состояний)
Рассеянный склероз (РС) – это хроническое демиелинизирующее заболевание, в основе которого лежит комплекс аутоиммунновоспалительных и нейродегенеративных процессов, приводящих к множественному очаговому и диффузному поражению центральной нервной системы, следствием которого является инвалидизация пациентов и значительное снижение качества жизни [1].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
G35.0 – Рассеянный склероз
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Типы течения рассеянного склероза [1]:
Ремиттирующий рассеянный склероз (РРС) – тип течения РС, характеризующийся наличием обострений, между которыми не отмечается прогрессирование инвалидизации. В период ремиссии могут иметься признаки стойкого неврологического дефицита [5].
Вторично-прогрессирующий рассеянный склероз (ВПРС) – тип течения РС, возникающий после периода ремиттирующего РС и характеризующийся наличием подтвержденного прогрессирования инвалидизации, независимого от обострений [5].При данной форме РС могут сохраняться типичные обострения заболевания, между которыми наблюдается подтвержденное прогрессирование РС.
Первично-прогрессирующий РС (ППРС) – тип течения РС, характеризующийся подтвержденным прогрессированием инвалидизации с момента появления первых симптомов заболевания, с возможными периодами стабилизации состояния, во время которых не происходит нарастания неврологического дефицита. Достаточным считается непрерывное нарастание симптомов в течение 1 года, для диагностики используется специальный раздел критериев МакДональда 2017 года [5].При данной форме могут наблюдаться типичные обострения заболевания, между которыми имеется подтвержденное прогрессирование инвалидизации, однако заболевание дебютирует не с обострений, а с прогрессирования [5].У детей и подростков с РС практически всегда наблюдается РРС, иногда с активным началом по типу острого рассеянного энцефаломиелита (ОРЭМ), с переходом в ВПРС. ППРС при начале РС в возрасте до 16 лет встречается крайне редко, такие случаи всегда нуждаются в тщательном уточнении диагноза [6–8].
С 2013 года внедряется новая классификация типов течения заболевания, в рамках которой выделяют неактивный РС (без обострений и без признаков активности РС по данным МРТ), активный РС (наличие обострений или признаков активности РС по данным МРТ), РС с прогрессированием и РС без прогрессирования [9]. Постепенный переход на данную классификацию представляется целесообразным, однако, существенно затрудняет использование ПИТРС, содержащих в инструкциях по применению в разделе «показания» ремиттирующий, вторично-прогрессирующий и первично-прогрессирующий РС [9].
С учётом особенностей течения выделяют особые формы РС:
— Злокачественный РС (болезнь Марбурга) – острая форма тяжёлого течения РС, характеризующаяся быстрым усилением инвалидизации без ремиссий и в самых тяжёлых случаях – развитием летального исхода в течение нескольких месяцев от момента начала заболевания. Характерно развитие массивных очагов в стволе мозга, на МРТ эти очаги, как правило, активно накапливают парамагнитный контраст. Вариант по типу болезни Марбурга может начинаться как сразу после дебюта РС, так и сменять на определенном этапе типичное течение РС. Частота развития такого варианта РС не превышает 5%.
— Быстропрогрессирующий рассеянный склероз – тип течения РРС на фоне отсутствия терапии ПИТРС (наивные пациенты). При данном типе в течение одного года наблюдения имеют место два или более обострения с подтвержденным усилением инвалидизации и выявлением 1 или более контрастируемого очага на Т1-ВИ или увеличением количества очагов на Т2-ВИ по данным МРТ головного и/или спинного мозга в сравнении с предшествующим исследованием. Общепризнанная дефиниция данного типа течения РС была приведена в отчете РКИ финголимода** при подгрупповом анализе эффективности [10]. Ключевым моментом данного определения является инвалидизирующий характер обострений. Недостаточный объем данных из РКИ в настоящий момент не позволяет с высокой долей достоверности сравнивать эффективность терапии при данной форме РС [11]. Данные будущих исследований, возможно, смогут уточнить и расширить формулировку и предоставить больше доказательств ее целесообразности.
— Высокоактивный рассеянный склероз (ВАРС) – это клинико-радиологические характеристики течения РС, возникающие на фоне проводимой терапии ПИТРС, на основании которых необходимо принятие решения об эскалации терапии (Приложение А3.7).
Стадии заболевания:
Обострение рассеянного склероза – субъективные (сообщаемые пациентом) и/или объективные (выявляемые при неврологическом осмотре) симптомы, характерные для острого воспалительного демиелинизирующего процесса в ЦНС (фокального или мультифокального), либо в виде усугубления уже имеющихся неврологических симптомов, либо в виде появления новых неврологических симптомов, не наблюдаемых ранее, с острым или чаще подострым началом, длительностью свыше 24 часов, с полным или неполным регрессом симптомов, при условии отсутствия лихорадки, других признаков инфекционного заболевания, предшествующих метаболических нарушений, явлений стресса [5].
В случае последовательного появления симптомов они считаются одним обострением, если новый симптом или группа симптомов, или отчетливое ухудшение уже имевшихся симптомов появляется в период от 24 часов до 30 дней с момента появления первого; и считаются двумя разными обострениями, если от начала первого до начала второго имеется период стабильного или улучшающегося состояния длительностью не менее 30 дней [5]. В соответствии с критериями МакДональда в редакции 2017 года понятия «обострение», «атака», «экзацербация» являются синонимами [5].
Ремиссия рассеянного склероза – период отсутствия обострений, прогрессирования и ухудшения симптомов в течение, как минимум, 30 дней; в случае появления нового симптома или группы симптомов, или отчетливого ухудшения уже имевшихся симптомов в срок до 30 дней включительно ремиссия не фиксируется, состояние расценивается как продолжающееся обострение.
Подтверждённое прогрессирование инвалидизации – стойкое нарастание неврологических нарушений (по Расширенной шкале статуса инвалидизации пациента (EDSS), Приложения Г1 и Г2) по сравнению с исходным уровнем, вне периода обострений и не связанное с перенесённым ранее обострением. Подтвержденное прогрессирование выставляется тогда, когда у пациента сохраняется или увеличивается балл EDSS по сравнению с датой первого зафиксированного нарастания неврологических нарушений минимум через 6 месяцев, при условии отсутствия обострений в период измерения. Значимым нарастанием неврологических нарушений является увеличение EDSS на ≥ 1,5 балла при исходном балле EDSS = 0, на ≥ 1,0 балл для пациентов с исходным EDSS = 1,0 – 5,5 баллов, или ≥ 0,5 балла – для пациентов с исходным уровнем EDSS ≥ 6,0 [9]. Самый ранний период, когда подтвержденное прогрессирование может быть зафиксировано, составляет 3 месяца. Более достоверным и важным для рутинной практики можно считать подтвержденное прогрессирование инвалидизации через 6 месяцев.
Подтверждённое усиление инвалидизации – стойкое ухудшение неврологических нарушений (по шкале EDSS (Приложения Г1 и Г2) после окончания обострения, которое было подтверждено как минимум двумя измерениями EDSS, одно из которых было выполнено не ранее 30 дней с момента начала обострения, а второе – не менее чем через 3 месяца после этого [10]. Усиление инвалидизации можно рассматривать как вклад обострения в накопление инвалидизации пациента. При этом необходимо учитывать, что после тяжелых обострений пациент может иметь увеличение балла по шкале EDSS на самых ранних этапах, но это не является прогрессированием.
Подтверждённое уменьшение инвалидизации – стойкое уменьшение неврологических нарушений по шкале EDSS (Приложения Г1 и Г2) по сравнению с исходным баллом EDSS. Подтвержденное уменьшение выставляется, когда у пациента уменьшение балла EDSS по сравнению с первым зафиксированным уменьшением неврологических нарушений сохраняется в течение 6 месяцев. Уменьшением неврологических нарушений является снижение EDSS на 1,0 балл по сравнению с исходным баллом [11]. У пациентов, которые имеют длительность обострения более 30 дней с постепенным снижением балла EDSS, данное снижение не может быть рассмотрено как уменьшение. Базовой точкой расчета для измерения улучшения является точка измерения EDSS после завершения обострения. Уменьшение инвалидизации необходимо рассматривать как наилучший результат снижения воспалительной активности и реабилитационной помощи пациентам с РС.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Имеется полигенная наследственная предрасположенность к РС. В настоящее время выделено более 200 генетических факторов, формирующих эту предрасположенность. Реализация предрасположенности происходит при участии внешних факторов, среди которых на первом месте рассматриваются вирусные инфекции (особенно ретровирусы и вирус Эпштейн — Барр), недостаток витамина Д, раннее начало курения, изменения микробиома кишечника и другие факторы [2].
Продуцируемые Т- и В-клетками системно и локально в ткани провоспалительные цитокины вызывают активацию аутореактивных Т-лимфоцитов, приводят к аутоиммунному воспалительному поражению ткани ЦНС. Уже на ранних стадиях заболевания отмечаются нейродегенеративные изменения. Активация клонов сенсибилизированных клеток наряду с недостатком противовоспалительной, регуляторной систем, способствует хронизации процесса. Вторично активированные макрофаги и микроглия также секретируют провоспалительные цитокины [3].
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Во всем мире имеется нарастание числа случаев РС, что связано как с улучшением диагностики и повышением возможностей патогенетической и симптоматической терапии, так и с истинным увеличением заболеваемости по неясным пока причинам. По данным публикации «Атлас РС Международной Федерации пациентов рассеянным склероз» (MSIF) с 2008 по 2013 годы распространенность РС возросла на 10% за 5 лет с 30 до 33 случаев на 100000 населения. При отсутствии адекватного современного лечения в среднем через 10 лет до 50% пациентов имеют трудности в выполнении профессиональных обязанностей, через 15 лет более 50% имеют трудности в самостоятельном передвижении, а при длительности РС более 20 лет – проблемы в самообслуживании [4].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Поражение зрительного нерва: односторонний оптический неврит (часто при ретробульбарной локализации очага – ретробульбарный неврит), часто в сочетании с болью при движении глазного яблока и снижением остроты зрения или появление скотом, длящимся от 2 до 4 недель; менее характерным является двусторонний оптический неврит без боли или с постоянной болью, полная и стойкая утрата зрения, отёк диска зрительного нерва и другие изменения на глазном дне.
Поражение мозжечка и его путей: статическая и динамическая мозжечковая атаксия – неустойчивость при ходьбе, дисметрия и мимопопадание в координаторных пробах, мегалография, асинергии, интенционное дрожание, мозжечковая дизартрия (скандированная речь).
Поражение ствола головного мозга: межъядерная офтальмоплегия, нистагм (центральный), парез отводящего нерва, гипестезия половины лица; менее характерны: снижение слуха, невралгия тройничного нерва, центральный или периферический парез лицевого нерва.
Поражение спинного мозга: моно- и гемипарезы, нижний парапарез, утрата чувствительности по проводниковому типу, симптом Лермитта, императивные позывы на мочеиспускание, неудержание мочи, задержки мочеиспускания; менее характерны: полный поперечный миелит, сегментарные нарушения чувствительности, радикулопатии, выпадение вибрационной чувствительности, сенситивная атаксия, недержание кала.
Поражение больших полушарий головного мозга: субкортикальный когнитивный дефицит (снижение памяти и внимания, скорости выполнения нейропсихологических тестов), хроническая усталость или утомляемость, центральный гемипарез, депрессия, реже тревожность, эйфоричность, менее характерными являются гемианопсии, острые нарушения поведения и эпилептические приступы.
Диагностика
2. Диагностика заболевания или состояния (группы заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики
- Рекомендуется всем пациентам с 18 лет с подозрением на РС для раннего подтверждения диагноза использование критериев МакДональда (редакция 2017 года) (Приложение А3.1) [12].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: Использование критериев МакДональда в редакции 2017 года обладает более высокой чувствительностью у пациентов на ранних стадиях заболевания, чем редакция критериев 2010 года (Приложение А3.7) или применением МРТ-критериев MAGNIMS 2016 (Приложение А3.4), что позволяет раньше установить диагноз РС. Следует, однако, учитывать, что специфичность критериев в редакции 2017 года ниже, чем в редакции 2010 года[12]. Для подтверждения диагноза рекомендуется использование алгоритма, разработанного на основе критериев МакДональда (редакция 2017 года) с целью наиболее ранней постановки диагноза (Приложение Б – 1,1 и 1,2 [5]. У пациентов с атипичным дебютом рекомендовано использовать критерии МакДональда в редакции 2010 года (Приложение А3.2) [12]. Тщательное проведение дифференциальной диагностики снизит риск ошибочной постановки диагноза РС [12–14].
- Рекомендуется у всех пациентов младше 18 лет с подозрением на РС при отсутствии энцефалопатии/общемозговой симптоматики в дебюте для подтверждения диагноза использование критериев МакДональда (редакция 2017 г., Приложение А3.1) [5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Международное исследование по валидации критериев МакДональда в редакции 2017 года для популяции пациентов младше 18 лет продемонстрировало результаты, позволяющие использовать их в диагностике РС у детей [15]. Проспективное когортное исследование с участием пациентов младше 18 лет также продемонстрировало результаты, позволяющие использовать критерии МакДональда в редакции 2017 года для данной популяции [16].
- Рекомендуется у всех пациентов младше 18 лет с подозрением на РС при наличии энцефалопатии/общемозговой симптоматики в дебюте для подтверждения диагноза РС использование критериев Международной группы по изучению детского рассеянного склероза (редакция 2013 г., Приложение А3.11) [17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Исследований, оценивающих характеристики критериев Международной группы по изучению детского рассеянного склероза для пациентов с указанной симптоматикой, не проводилось.
2.1 Жалобы и анамнез
- У всех пациентов с подозрением на РС рекомендуется подробный сбор анамнеза на предмет наличия признаков острых демиелинизирующих эпизодов в прошлом для определения возможности соответствия критериям диссеминации в пространстве и времени (Приложение А3.1) [5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Оценка данных анамнеза должна проводиться врачом-неврологом для определения соответствия жалоб характерным клиническим проявления обострения РС и соответствия критериям диссеминации в пространстве и времени (Приложение А3.1).
- Всем пациентам с подозрением на РС рекомендуется проводить полную дифференциальную диагностику с другими неврологическими и не неврологическими заболеваниями с целью уменьшения риска диагностической ошибки и нанесения вреда пациенту по причине отложенного или неправильного лечения (План дифференциальной диагностики изложен в Приложении А3.3) [18–20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: Исследование Yamout и соавт. продемонстрировало, что только 70% пациентов, направленных к специалисту по РС, поставили диагноз РС [19]. Из пациентов с другими диагнозами 3,5% полностью соответствовали критериям РИС. Наиболее распространенными альтернативными диагнозами были психические расстройства (16,3%), неспецифические МРТ-поражения белого вещества (14,7%), заболевания спектра оптиконейромиелита (9,5%), мигрень (8,6%) и системные аутоиммунные заболевания (8,6%) [19]. Исследование Solomon с соавт. продемонстрировало, что 33% пациентов наблюдались с неправильным диагнозом в течение более 10 лет. 70% из них получали терапию ПИТРС и 31% имели нежелательные явления, связанные с терапией ПИТРС [20].
- Всем пациентам с наличием оптического неврита на момент осмотра или в анамнезе рекомендуется консультация врача-невролога с целью исключения РС [21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
2.2 Физикальное обследование
- При проведении неврологического осмотра пациентов с подозрением на РС рекомендуется использовать Шкалу функциональных систем по Куртцке (ФС (Приложение Г1) и Расширенную шкалу инвалидизации (EDSS; Приложение Г2) [5,22,23].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
2.3 Лабораторные диагностические исследования
- Всем пациентам с подозрением на РС рекомендуется назначать следующие лабораторные анализы для исключения сопутствующих заболеваний и определения возможности назначения последующей терапии ПИТРС [24,25]:
— Общий (клинический) анализ крови развернутый;
— Анализ крови биохимический общетерапевтический, исследование уровня С-реактивного белка в сыворотке крови, исследование уровня фибриногена в крови, исследование уровня общего кальция в крови;
— Исследование уровня тиреотропного гормона (ТТГ) в крови, исследование уровня свободного тироксина (СТ4) сыворотки крови, определение содержания антител к тиреопероксидазе в крови, исследование уровня тиреоглобулина в крови.
— Общий (клинический) анализ мочи и микроскопическое исследование осадка мочи;
— Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови, определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител к поверхностному антигену (HBsAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител классов к ядерному антигену (HBcAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител к вирусу гепатита C (Hepatitis C virus) в крови, определение антител к бледной трепонеме (Treponema pallidum) в нетрепонемных тестах (RPR, РМП) (качественное и полуколичественное исследование) в сыворотке крови;
— Определение содержания антител к антигенам ядра клетки и ДНК [283].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Данный перечень исследований рассматривается экспертами-членами рабочей группы как достаточный, но не исчерпывающий. План обследования должен исходить из клинической картины заболевания и других данных, полученных при объективных, лабораторных и инструментальных методах обследования.
- Пациентам с подозрением на РС, при наличии признаков, заставляющих включить в дифференциальный диагноз церебральную аутосомно-доминантную артериопатию с субкортикальными инфарктами и лейкоэнцефалопатией (CADASIL), с целью проведения дифференциального диагноза рекомендуется назначать молекулярно-генетическое исследование мутации гена NOTCH3 [26].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1).
- Пациентам с подозрением на РС, при наличии признаков, заставляющих включить в дифференциальный диагноз дефицит витамина В12, с целью проведения дифференциального диагноза рекомендуется назначать определение уровня витамина B12 (цианокобаламин) в крови [27].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
- Пациентам с подозрением на РС, при наличии признаков, заставляющих включить в дифференциальный диагноз прогрессирующую мультифокальную лейкоэнцефалопатию (ПМЛ), с целью проведения дифференциального диагноза рекомендуется назначать анализ спинномозговой жидкости методом полимеразноцепной реакции (ПЦР) на наличие JC-вируса [28].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: ПМЛ развивается в результате реактивации полиомавируса JC у JCV-серопозитивных пациентов. После того, как вирус приобретает нейротропность, он инфицирует клетки олигодендроглии и вызывает литическую инфекцию ЦНС [29]. Определение ДНК вируса в спинномозговой жидкости при наличии соответствующей клинической картины позволяет поставить диагноз ПМЛ [28].
- Пациентам с подозрением на РС, при наличии признаков, заставляющих включить в дифференциальный диагноз заболевания спектра оптиконейромиелита (ЗСОНМ), с целью проведения дифференциального диагноза рекомендуется назначать анализ на антитела к аквапорину-4 в крови [30].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: Антитела к аквапорину-4 являются высокоспецифичным маркером оптиконейромиелита, клиническая специфичность составляет 97 — 98%. Наибольшей чувствительностью и специфичностью обладает методика определения антител к аквапорину-4 в культуре трансфицированных клеток, экспрессирующих аквапорин-4 [30].
- Пациентам с подозрением на РС, при наличии признаков, заставляющих включить в дифференциальный диагноз системные заболевания соединительной ткани, с целью проведения дифференциального диагноза рекомендуется назначать определение содержания антител к антигенам ядра клетки и ДНК и определение содержания антител к экстрагируемым ядерным антигенам в крови [31–33].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарий: Системные заболевания соединительной ткани имеют разнообразные проявления, в том числе, вовлекающие ЦНС. Исследования Leuchten с соавт. и Haga с соавт. показывают, что скрининговое тестирование на антинуклеарный фактор и определение антител к экстрагируемому ядерному антигену IgG имеют высокую чувствительность и специфичность при выявлении таких заболеваний как системная красная волчанка, синдром Шегрена [32,33]. Важной особенностью является высокая отрицательная прогностическая значимость и низкая позитивная прогностическая значимость [31]. Выявление указанных антител не является признаком системного заболевания само по себе, однако в таком случае требуется консультация ревматолога.
- Пациентам с подозрением на РС в качестве дополнительного метода подтверждения диагноза РС рекомендуется назначать парное исследование олигоклональных иммуноглобулинов класса IgG с установлением типа синтеза в сыворотке крови и спинномозговой жидкости [5,34–39].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарий: Чувствительность и специфичность определения олигоклональных иммуноглобулинов класса IgG по данным разных авторов составляет около 90% и 60%, соответственно [34,36,37]. 2-й и 3-й типы синтеза олигоклональных IgG являются наиболее характерными для РС [35]. Исследование может использоваться в качестве дополнительного метода, подтверждающего диссеминацию во времени в соответствии с критериями МакДональда в редакции 2017 года [5,38]. Отсутствие олигоклональных иммуноглобулинов не является подтверждением отсутствия у пациента РС, что встречается с частотой до 13% случаев при РС и до 33% при КИС [34]. Наличие олигоклональных IgG в СМЖ является независимым фактором, повышающим риск конверсии КИС в достоверный РС [39].
- Пациентам с подозрением на РС в качестве дополнительного лабораторного метода подтверждения диагноза РС рекомендуется провести парное исследование концентрации свободных легких цепей иммуноглобулинов каппа (ƙ-СЛЦ) и индекса свободных легких цепей иммуноглобулинов каппа в сыворотке крови и спинномозговой жидкости [40].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: анализ СМЖ и сыворотки крови на концентрацию и индекс ƙ-СЛЦ является количественным биомаркером, отражающим уровень интратекальной продукции иммуноглобулинов [41]. Исследования, посвященные диагностической ценности данного биомаркера, демонстрируют чувствительность и специфичность, сопоставимую с определением олигоклональных иммуноглобулинов [42–44]. В дополнение к исследованию на олигоклональные иммуноглобулины, определение данного биомаркера повышает информативность диагностики и позволяет выявлять воспалительный процесс у пациентов с отрицательным анализом на олигоклональные антитела [41,44]. Исследования разных авторов указывают на прогностическую значимость ƙ-СЛЦ для определения риска прогрессирования РС [45,46].
2.4 Инструментальные диагностические исследования
- Всем пациентам с подозрением на РС не рекомендуется постановка диагноза РС только на основании данных МРТ, с целью снижения риска ошибочного диагноза [47].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: РС устанавливается, прежде всего, на основании характерной клинической картины [5]. МРТ является дополнительным методом исследования, повышающим точность и скорость диагностики.
- Всем пациентам с подозрением на РС рекомендуется проведение МРТ головного мозга с контрастированием для исключения иной природы неврологического заболевания, а также для установления соответствия процесса критериям диссеминации в пространстве и времени [48].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: Протокол первичной магнитно-резонансной томографии головного мозга должен включать в себя следующие обязательные последовательности: 1) Т2-FLAIR и Т2-ВИ/PD в аксиальной плоскости, 2) 2D или 3D Т2-FLAIR в сагиттальной плоскости, 3) 2D или 3D Т1-ВИ с введением КВ. Для получения снимков с контрастным усилением рекомендуется использовать стандартную дозировку КВ (0,1 — 0,2 ммоль/кг в зависимости от концентрации КВ), вводимую на протяжении 30 секунд, минимум за 10 минут до получения постконтрастного Т1-ВИ. При необходимости дополнительно проводятся: 1) 2D или 3D Т1-ВИ без КВ, 2) 2D и/или 3D DIR, 3) ДВИ в аксиальной плоскости. Исследуется весь объём головного мозга, толщина срезов ≤ 5 мм в зависимости от программы [49].
- Пациентам с подозрением на РС и наличием клинических симптомов поражения спинного мозга или радиологических признаков поражения головного мозга, не удовлетворяющих критериям диссеминации в пространстве, рекомендуется дополнительное проведение магнитно-резонансной томографии спинного мозга с внутривенным контрастированием (шейный отдел) с целью снижения риска ошибочного диагноза и критериального подтверждения возможного диагноза РС [50]. Выполнение магнитно-резонансной томографии спинного мозга (грудной и поясничный отделы) рекомендуется при подозрении на локализацию очага в этих областях.
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
Комментарий: Выполнение МРТ спинного мозга (шейный отдел) одновременно с МРТ головного мозга позволяет сократить частоту повторного направления на МРТ и избежать повторного введения контраста. В случае наличия возможности необходимо сразу выполнять оба исследования. Обязательными для включения в протокол МРТ последовательностями являются: 1) Т2-ВИ в импульсной последовательности быстрое «спиновое эхо» и Т2-STIR в сагиттальной плоскости, 2) 2D и/или 3D Т2-ВИ в импульсной последовательности быстрое «спиновое эхо» в аксиальной плоскости. При выявлении очагов на Т2-ВИ обязательно выполняется Т1-ВИ в импульсной последовательности «спиновое эхо» с введением КВ в сагиттальной и аксиальной плоскостях. В качестве альтернативы Т2-STIR могут быть использованы последовательности PSIR или режим протонной плотности (PD) в сагиттальной плоскости. Срезы должны выполняться без промежутков между срезами, толщиной не более 3 мм в сагиттальной плоскости и не более 5 мм в аксиальной плоскости [51] .
- Пациентам с подозрением на РС старше 40 лет с неспецифическими находками на МРТ головного мозга рекомендуется дополнительное проведение магнитно-резонансной томографии спинного мозга с внутривенным контрастированием (шейный отдел) с целью снижения риска ошибочного диагноза и критериального подтверждения возможного диагноза РС [50].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
Комментарий: Выполнение МРТ спинного мозга (шейный отдел) одновременно с МРТ головного мозга позволяет сократить частоту повторного направления на МРТ и избежать повторного введения контрастного препарата. В случае наличия возможности необходимо сразу выполнять оба исследования. Обязательными для включения в протокол МРТ последовательностями являются: 1) Т2-ВИ в импульсной последовательности быстрое «спиновое эхо» и Т2-STIR в сагиттальной плоскости, 2) 2D и/или 3D Т2-ВИ в импульсной последовательности быстрое «спиновое эхо» в аксиальной плоскости. При выявлении очагов на Т2-ВИ обязательно выполняется Т1-ВИ в импульсной последовательности «спиновое эхо» с введением КВ в сагиттальной и аксиальной плоскостях. В качестве альтернативы Т2-STIR могут быть использованы последовательности PSIR или режим протонной плотности (PD) в сагиттальной плоскости. Срезы должны выполняться без промежутков между срезами, толщиной не более 3 мм в сагиттальной плоскости и не более 5 мм в аксиальной плоскости [51].
- Пациентам с подозрением на РС, у которых при однократной магнитно-резонансной томографии головного мозга не удалось установить соответствие критериям диссеминации в пространстве и времени, рекомендуется назначение повторной МРТ головного мозга для оценки динамики и соответствия критериям диагностики РС [51–53].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: В 2016 году группой MAGNIMS предложены дополнения по применению МРТ при установлении диагноза РС по критериям МакДональда 2010 года (Приложение А3.4), однако эти дополнения не полностью соответствуют новым критериям МакДональда 2017 года, поэтому приводятся в качестве справочной информации [54]. В случае обнаружения у пациента с клинической картиной острого демиелинизирующего эпизода на первичной МРТ двух и более очагов, характеристики которых указывают на демиелинизирующий характер поражения при отсутствии признаков контрастного усиления, повторная МРТ головного мозга должна быть выполнена через 3 — 6 месяцев от первичной [52,53]. В случае выявления на МРТ двух и более очагов, характеристики которых указывают на демиелинизирующий характер поражения, у пациента без клиники острого демиелинизирующего эпизода или при неспецифической клинической картине (радиологически изолированный синдром – РИС) повторную МРТ рекомендуется проводить через 12 — 24 месяца [55]. При этом обязательными для включения в протокол повторной МРТ головного мозга последовательностями являются: 3D Т1-ВИ без контрастного усиления, 2D или 3D Т2-FLAIR в сагиттальной и аксиальной плоскости, 2D или 3D Т2-ВИ в аксиальной плоскости, 2D или 3D Т1-ВИ в аксиальной плоскости с введением КВ с толщиной срезов не более 3 мм без промежутков между срезами, а также 2D ДВИ в аксиальной плоскости с толщиной срезов не более 5 мм. При необходимости возможно выполнение последовательностей 2D и/или 3D DIR, SWI (SWAN), T1-ВИ и PD. Покрытие МРТ должно охватывать весь объём головного мозга, разрешение пикселя не должно превышать 1×1 мм на срез [51].
- Пациентам с подозрением на РС при выполнении МРТ исследований рекомендуется оформление структурированного протокола МРТ заключения, в том числе с целью оценки динамики очагов, сопоставления критериям диссеминации в месте и/или во времени (Приложение А3.5) [56,57].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: Экспертами — членами рабочей группы, однозначно рекомендуется оформление структурированного протокола МРТ заключения, включающего описательную часть (локализация, характеристики очагов, отсутствие или наличие патологического накопления КВ очагами), оценку динамики патологического процесса (появление, локализация и количество новых и/или увеличенных старых очагов в режимах Т2-ВИ и Т2FLAIR, накапливающих или не накапливающих КВ) и интерпретацию патологического процесса (типичная, атипичная или нетипичная для РС МРТ картина), на основе которого лечащий врач может принимать решения о дальнейшей тактике ведения пациента. Без оформления структурированного протокола МРТ заключения услуга проведения МРТ исследования считается выполненной некачественно.
2.5 Иные диагностические исследования
- У пациентов с подозрением на РС при наличии симптомов неврита зрительного нерва в настоящий момент или в анамнезе в качестве дополнительного метода исследования рекомендуется использовать дополнительные инструментальные методы диагностики: регистрация вызванных потенциалов коры головного мозга одной модальности (зрительные), магнитно-резонансная томография глазницы для объективизации эпизода зрительных нарушений [58,59].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий: Чувствительность определения очаговых изменений зрительного нерва на МРТ составляет до 93%[58]. Наличие контрастируемого очага демиелинизации в зрительном нерве связано с более тяжелым течением неврита зрительного нерва и менее благоприятным прогнозом восстановления зрения [58]. В исследовании Frederiksen и соавт. чувствительность диагностики замедления проведения вызванных потенциалов при неврите зрительного нерва составила 77%, амплитуда зрительных вызванных потенциалов коррелировали с остротой зрения [59]. Увеличение латентности было связано с наличием подтвержденного диагноза РС [59].
- Пациентам с подозрением на РС, при наличии симптомов неврита зрительного нерва в настоящий момент или в анамнезе, в качестве дополнительного метода исследования рекомендуется назначение оптической когерентной томографии глаза для определения истончения слоя нервных волокон и слоя ганглионарных клеток сетчатки [60].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарий: Наилучшая чувствительность метода достигается приблизительно через 3 месяца после перенесённого неврита зрительного нерва [49]. Атрофия слоя зрительных волокон сетчатки является неблагоприятным прогностическим фактором в отношении прогрессирования инвалидизации [61]. В систематическом обзоре Britze и соавт. показано, что атрофия слоя ганглионарных клеток проявляется раньше, чем атрофия слоя зрительных волокон сетчатки и лучше предсказывает восстановление функции зрения [62].
Лечение
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Терапия РС состоит из трех составляющих компонентов: 1) терапия обострений РС, 2) препараты, изменяющие течение РС (ПИТРС) и 3) симптоматическая терапия (коррекция отдельных симптомов заболевания). В настоящее время препаратов, с доказанным нейропротективным и нейрорепаративным эффектом при РС не зарегистрировано.
3.1 Терапия обострений РС
- При наличии у пациента с РС клинических признаков обострения РС, подтвержденных объективно врачом-неврологом (вне зависимости от факта выполнения МРТ центральной нервной системы и/или при наличии активности по данным МРТ) рекомендуется терапия обострения РС c целью уменьшения выраженности и продолжительности симптомов обострения РС и уменьшения их продолжительности [63,64] (Приложение Б. Алгоритм 2).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
- В качестве терапии обострения РС у пациентов с РС рекомендуется использование глюкокортикоидов (ГК) в высоких дозах с целью уменьшения выраженности и продолжительности симптомов обострения РС [63–65].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: До начала терапии глюкокортикоидами (ГК) следует учитывать возможные побочные эффекты использования ГК.
- При наличии у пациентов с РС обострения РС в ситуации, когда риски терапии обострения РС превышают возможную пользу терапии, рекомендуется воздержаться от терапии обострения РС по совместному решению врача-невролога и пациента с РС с целью предотвращения побочных эффектов терапии обострения РС (критерии оценки тяжести обострения представлены в Приложении А3.12) [63].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Лечащий врач может обсуждать с пациентом возможность не применять глюкокортикоиды для лечения неинвалидизирующих обострений или обострений, с момента начала которых прошел продолжительный период времени (например, больше 3 месяцев). По данным исследования Национального института здравоохранения Великобритании, исследования эффективности глюкокортикоидов по сравнению с плацебо, как правило, имели низкое качество [63]. По данным метаанализа Miller c соавт., разница клинического эффекта глюкокортикоидов составила лишь 0,76 балла EDSS по сравнению с группой плацебо в конце лечения по сравнению с исходным уровнем [64]. Решение о воздержании от терапии обострения должно приниматься только совместно с пациентом. Freedman и соавт. предложена классификация, позволяющая определить степень тяжести обострения с целью дальнейшей маршрутизации помощи пациенту (Приложение А3.12) [66].
- С целью уменьшения выраженности и продолжительности симптомов обострения РС у пациентов с РС с 18 лет включительно в качестве лекарственного препарата первого выбора рекомендуется использовать метилпреднизолон**для внутривенного применения в режиме пульс-терапии в дозе 1000 мг в течение 3 — 5 дней (максимально – 7) [65,67–69].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
- Для пациентов с РС младше 18 лет доза метилпреднизолона**для внутривенного применения в режиме пульс-терапии рассчитывается исходя из веса ребенка: 500 мг при весе 25 — 40 кг, 750 мг при весе 40 — 55 кг, 1000 мг при весе свыше 55 кг [70–72].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Рандомизированное исследование LaMantia и соавт. и систематический обзор с применением метаанализа Citterio с соавт. демонстрируют, что внутривенное введение метилпреднизолона** при обострении РС в режиме пульс-терапии способствовало значимому снижению показателя EDSS через 4 — 5 недель [65,69].
- В случае невозможности использования метилпреднизолона** с целью уменьшения выраженности и продолжительности симптомов обострения РС у пациентов с РС (с 18 лет) рекомендуется использование #дексаметазона** для внутривенного капельного применения по схеме: 8 мг в сутки в течение 7 дней, затем 4 мг в сутки в течение 4 дней, затем 2 мг в сутки в течение 3 дней [69].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: Приведенное РКИ имело малый размер выборки и не продемонстрировало статистически значимых преимуществ терапии #дексаметазоном** перед терапией метилпреднизолоном** при оценке показателя EDSS через 7 и 15 дней после терапии [69]. Количество пациентов без обострений РС через 1 год после терапии обострения РС в группе высокодозного метилпреднизолона** было статистически значимо выше, чем в группе #дексаметазона**.
- В случаях, затрудняющих проведение терапии обострений РС парентеральными глюкокортикоидами, для пациентов с РС (с 18 лет) с обострением РС рекомендуется использование пероральных (таблетированных) глюкокортикоидов в эквивалентных суточных дозах (эквивалентных 1000 мг метилпреднизолона**) в течение 3 — 5 дней с целью уменьшения продолжительности и выраженности симптомов обострения РС [65,68,73–77].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарий: Нет достоверных данных о статистически значимых различиях в эффективности и безопасности парентеральных и пероральных глюкокортикоидов в эквивалентных дозах в качестве терапии обострения РС в течение 5 дней. Однако, мощность исследований, включённых в мета-анализ, была ограниченной, а результаты не везде были согласованными, что не позволяет сделать окончательный вывод об однозначной эквивалентности данных типов терапии [65,68,73–77].
- У пациентов с РС (с 18 лет) при терапии обострений РС с использованием пероральных (таблетированных) глюкокортикоидов альтернативно внутривенному введению метилпреднизолона** не рекомендуется применение длительных курсов пероральных глюкокортикоидов (более 5 дней), в том числе с постепенным снижением дозы, с целью предотвращения развития побочных эффектов длительной терапии пероральными глюкокортикоидами [69,73,74].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: Более длительные курсы терапии глюкокортикоидами не являются более эффективными по сравнению с курсом продолжительностью до 5 дней [69,73,74].
- Пациентам с РС с 18 лет в случае неэффективности курса терапии глюкокортикоидами рекомендуется применение высокообъемного плазмафереза в количестве до 7 сеансов для терапии обострения РС [79, 80].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарий: Эффективность плазмафереза в качестве дополнительной терапии для пациентов, у которых терапия глюкокортикоидами при обострении РС оказалась неэффективной, продемонстрирована в некоторых рандомизированных клинических исследованиях [79,80].
- Пациентам с РС младше 18 лет в случае неэффективности курса терапии глюкокортикоидами рекомендуется применение высокообъемного плазмафереза в количестве до 7 сеансов для терапии обострения РС [78–80].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
- Пациентам с РС младше 18 лет при обострении РС рекомендуется применение #иммуноглобулина человека нормального** для внутривенного приема в курсовой дозе 2 г/кг веса в течение 5 дней с целью уменьшения продолжительности и выраженности симптомов обострения РС при наличии противопоказаний к приему глюкокортикоидов [70,81,82].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: #Иммуноглобулин человека нормальный** для внутривенного введения может рассматриваться как альтернативный метод лечения обострений РС у пациентов младше 18 лет, когда прием глюкокортикоидов противопоказан. Введение иммуноглобулинов может уменьшать выраженность воспаления путем снижения уровня цитокинов и связывания антител против миелина путем блокирования Fc рецепторов, а также стимулировать ремиелинизацию [83,84]. Ряд репортированных случаев лечения детей с демиелинизирующими заболеваниями (РС, ОРЭМ) сообщают о возможной эффективности применения иммуноглобулинов для внутривенного введения, однако контролируемых исследований надлежащего качества не опубликовано [81,82].
3.2 Терапия, изменяющая течение РС
- Всем пациентам с РС перед назначением терапии, изменяющей течение РС, рекомендуется установить тип течения и уровень инвалидизации по шкале EDSS (Приложение Г2) [9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
- Всем пациентам с 18 лет с ремиттирующим РС с уровнем EDSS ≤ 6,5 баллов, не соответствующих критериям быстропрогрессирующего рассеянного склероза, с целью снижения риска подтвержденного прогрессирования инвалидизации и развития ВПРС (Приложение А3.7, Приложение Б. 4.1, 4.2, 4.3, 4.4) при первом назначении терапии ПИТРС рекомендуется максимально раннее назначение ПИТРС первой линии: интерферон бета-1а** (для п/к введения), интерферон бета-1b**, глатирамера ацетат**, диметилфумарат**, терифлуномид**[85–92].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
или
интерферон бета-1а** (для в/м введения) [94]
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
или
пэгинтерферон бета-1a** [93,96].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: Раннее назначение терапии ПИТРС способствует снижению риска прогрессирования инвалидизации и развития ВПРС [92].
- Интерферон бета-1а** 30 мкг для внутримышечного введения 1 раз в неделю рекомендуется пациентам с РРС (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [94].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
- Интерферон бета-1а** 44 мкг подкожно 3 раза в неделю рекомендуется пациентам с РРС (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [88].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
- Интерферон бета-1b** 250 мкг подкожно через день рекомендуются пациентам с РРС (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [86].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
- Пэгинтерферон бета-1а** (пегилированный интерферон) 125 мкг подкожно 1 раз в 14 дней рекомендуется пациентам с РРС (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [93,96].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
- Глатирамера ацетат** 20 мг подкожно ежедневно или глатирамера ацетат** 40 мг подкожно 3 раза в неделю рекомендуется пациентам с РРС (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [86,87,97].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
- Терифлуномид** 14 мг перорально 1 раз в сутки рекомендуется пациентам с РРС (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [89].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
- Диметилфумарат** 240 мг перорально 2 раза в день рекомендуется пациентам с РРС (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [90,91].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
- Всем пациентам с 12 лет с ремитирующим РС с уровнем EDSS ≤ 6,5 баллов, не соответствующих критериям быстропрогрессирующего рассеянного склероза, с целью снижения риска подтвержденного прогрессирования инвалидизации и развития ВПРС (Приложение А3.7, Приложение Б. 4.1, 4.2, 4.3, 4.4) при первом назначении терапии ПИТРС рекомендуется максимально раннее назначение ПИТРС первой линии интерферон бета-1а** 30 мкг для внутримышечного введения 1 раз в неделю [282].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
или
интерферон бета-1а** 44 мкг подкожно 3 раза в неделю [95].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
- Детям с 12 лет рекомендуется интерферон бета-1а** 30 мкг для внутримышечного введения 1 раз в неделю с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [282].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
- Детям с 12 лет рекомендуется Интерферон бета-1а** 44 мкг подкожно 3 раза в неделю с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [95].
Уровень убедительности рекомендаций С (уровень достоверности доказательств –4).
- Рекомендуется регулярно (не реже 1 раза в 6 месяцев) проводить оценку эффективности проводимой терапии ПИТРС. Терапию ПИТРС следует считать эффективной в случае наличия оптимального ответа на терапию (НДАЗ, «нет данных за активность заболевания»). При этом срок наблюдения и оценки эффективности должен соответствовать среднему сроку наступления эффекта для данного лекарственного препарата [98].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Критерий НДАЗ признается большинством экспертов как достоверный маркер ответа на терапию ПИТРС. В исследовании Rotstein и соавт. выполнение критерия НДАЗ через 2 года терапии обладало положительным прогностическим значением в 78,3% в отношении отсутствия прогрессирования инвалидизации через 7 лет [99].
- Для оценки эффективности терапии ПИТРС у пациентов с РС с целью предотвращения отмены терапии ПИТРС до начала развития эффекта терапии ПИТРС рекомендуется использовать следующие сроки начала ожидаемого эффекта от терапии [86,100–102]:
— глатирамера ацетатом** – 9 — 12 месяцев;
— интерферонами бета-1a** и интерфероном бета-1b** – 3 — 6 месяцев;
— терифлуномидом**– 3 — 6 месяцев;
— диметилфумаратом** – 3 — 6 месяцев;
— натализумабом** — 3 — 6 месяцев;
— финголимодом** – 3 — 6 месяцев;
— алемтузумабом** – 24 месяца;
— окрелизумабом** – 12 месяцев;
— кладрибином** – 24 месяцев;
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Исследования, направленные на определение сроков достижения эффективности ПИТРС, за исключением глатирамера ацетата**, не проводились. Для всех ПИТРС, за исключением глатирамера ацетата**, приведено мнение экспертов – членов рабочей группы. Рекомендация основана на данных отдельных РКИ, при этом сроки ожидаемого развития эффекта соответствуют срокам, в которые проводилась оценка эффективности терапии в представленных исследованиях. Исследования высокого методологического качества, в которых бы изучалось именно время наступления оптимального ответа на терапию, не проводились [87,100–102].
- Пациентам с РС, достигшим уровня EDSS ≥ 7,0 баллов, при отсутствии обострений и радиологической активности заболевания по данным МРТ в течение периода не менее 2 лет не рекомендуется продолжать терапию ПИТРС в связи с недоказанностью эффективности терапии в данной когорте пациентов и существенным повышением рисков побочных эффектов с целью предотвращения возможных побочных эффектов, связанных с терапией ПИТРС [25]. Решение о прекращении терапии ПИТРС должно приниматься только совместно с пациентом.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Исследований клинической эффективности ПИТРС в указанной когорте пациентов не проводилось, однако некоторые выводы можно сделать из анализа естественного течения заболевания. В исследовании Ahrweiller и соавт. показано, что частота обострений снижается на 46% каждые 5 лет после конверсии в ВПРС [103]. Похожие данные получены в исследовании Mateo Paz Soldan и соавт., которые показали, что в отобранной ими группе пациентов 91,6% обострений происходило в течение первых 5 лет после конверсии в ВПРС и 95,2% обострений развивалось до достижения возраста 55 лет [104]. При балле EDSS 6,0 и выше риск обострений и/или активности на МРТ ниже на 50%, поэтому отмена ПИТРС может не сопровождаться существенным риском возобновления клинической и радиологической активности РС [25].
- При развитии субоптимального ответа на терапию ПИТРС первой линии у пациента с РРС с уровнем EDSS ≤ 6,5 баллов, при условии высокой комплаентности пациента и достаточного времени для развития эффекта терапии ПИТРС рекомендуется смена терапии ПИТРС в рамках первой линии ПИТРС (Приложение Б, Алгоритм 3, Приложение А3.7) [105–110].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
- При развитии резистентности на терапию ПИТРС первой линии у пациентов с РРС (ВАРС, «высокоактивный РС») с уровнем EDSS ≤ 6,5 баллов, при условии высокой комплаентности пациента, достаточного времени для развития эффекта терапии ПИТРС рекомендуется эскалация терапии на ПИТРС второй линии (Приложение Б, Алгоритм 3, Приложение А3.7) [105–110].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
- При стойком субоптимальном ответе на терапию ПИТРС первой линии у пациентов с РРС (терапия проводилась двумя и более ПИТРС первой линии) рекомендуется эскалация терапии на ПИТРС второй линии (Приложение Б, Алгоритм 3, Приложение А3.7) [105–108].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
- Пациентам с 18 лет с быстропрогрессирующим РРС с уровнем EDSS≤ 6,5 баллов рекомендуются ПИТРС второй линии (Приложение Б, Алгоритм 3, Приложение А3.7):
натализумаб** [117–121]
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
или
финголимод** [122,123]
Уровень убедительности рекомендаций A (уровень достоверности доказательств –1).
или
алемтузумаб** [110,125,126]
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
или
окрелизумаб** [127,128]
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
или
кладрибин** [102,129]
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
или
#митоксантрон** [130].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
- Пациентам с 10 лет с быстропрогрессирующим РРС с уровнем EDSS ≤ 6,5 баллов рекомендуется назначение финголимода** 0,5 мг перорально один раз в день [122,124]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
- Натализумаб** 300 мг внутривенно 1 раз в 28 дней рекомендуется пациентам (с 18 лет) с быстропрогрессирующим РРС или с высокоактивным РРС с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [117–121]. При применении натализумаба** у пациентов с РС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.6).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
- Финголимод** 0,5 мг перорально один раз в день рекомендуется (с 10 лет) пациентам с быстропрогрессирующим РРС или с высокоактивным РС с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [122–124]. При применении финголимода** у пациентов с РС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.7).
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
- Алемтузумаб** 12 мг внутривенно 2 курса терапии (5 инфузий в 1-й год и 3 инфузии во 2-й год) рекомендуется пациентам (с 18 лет) с быстропрогрессирующим РРС или с высокоактивным РРС с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [110,125,126]. При применении алемтузумаба** у пациентов с РС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.8).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
- Окрелизумаб** 600 мг внутривенно 1 раз в 6 месяцев рекомендуется пациентам (с 18 лет) с быстропрогрессирующим РРС или с высокоактивным РРС с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [127,128]. При применении окрелизумаба** у пациентов с РС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.9).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
- Кладрибин** в таблетках 10 мг (3,5 мг/кг массы тела пациента в течение 2 лет: 1,75 мг/кг на 1 курс лечения в год общей продолжительностью не более 10 дней каждый курс без приёма препарата в последующие 2 года) рекомендуется пациентам (с 18 лет) с быстропрогрессирующим РРС или с высокоактивным РРС с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [102,129]. При применении кладрибина** у пациентов с РС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.10).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
- #Митоксантрон** рекомендуется при высокоактивном РРС (с 18 лет) при отсутствии альтернативы в качестве препарата резервной терапии в связи с негативным профилем безопасности (предельная относительно безопасная кумулятивная доза – 80 мг/м2) в дозировке 12 мг/м2 в/в на 200 мл изотонического раствора натрия хлорида** каждые 3 месяца с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [130]. При применении #митоксантрона** у пациентов с РС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.5).
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
- Пациентам с РС с 18 лет с уровнем EDSS ≤ 6,5 баллов при использовании терапии ПИТРС второй линии (натализумаб**, финголимод**, окрелизумаб**, алемтузумаб**, кладрибин**, #митоксантрон**) и оптимальном ответе на терапию, в случае наличия высоких рисков нежелательных побочных реакций (НПР), угрожающих жизни пациента, или при наличии риска развития тяжелой инвалидизации в условиях продолжения данной терапии ПИТРС рекомендуется смена терапии на другой ПИТРС второй линии с соблюдением рекомендованных периодов переходов и планов управления рисками при смене [98].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Рандомизированных клинических исследований, сравнивающих эффективность смены терапии в рамках ПИТРС второй линии, не проводилось. Существует некоторый положительный опыт смены натализумаба**(в основном, из-за рисков ПМЛ) на окрелизумаб**, алемтузумаб**, финголимод** и кладрибин** при соблюдении сроков перевода [131–136].Однако исследование Vollmer и соавт. демонстрирует, что частота обострений может возрастать после смены натализумаба** на финголимод** при более продолжительном интервале переключения [137]. В исследовании Alping и соавт. смена натализумаба** на #ритуксимаб** была более эффективной, чем на финголимод** [138].
- У пациентов с РС с 18 лет с уровнем EDSS ≤ 6,5 баллов при использовании терапии ПИТРС второй линии (натализумаб**, финголимод**, окрелизумаб**, алемтузумаб**, кладрибин**, #митоксантрон**), при условии высокой комплаентности пациента, достаточного времени для развития эффекта терапии ПИТРС, при отсутствии оптимального ответа на терапию ПИТРС рекомендуется смена терапии на другой ПИТРС второй линии с соблюдением рекомендованных периодов переходов и планов управления рисками при смене [98].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Рандомизированных клинических исследований, сравнивающих эффективность смены терапии в рамках ПИТРС второй линии, не проводилось. Эксперты-члены рабочей группы рассматривают смену терапии в рамках ПИТРС второй линии как способ добиться выполнения критерия оптимального ответа на терапию (НДАЗ) у пациентов с резистентностью к одному из ПИТРС второй линии. Выбор другого ПИТРС должен производиться с учетом спектра нежелательных явлений, предыдущего опыта пациента на терапии ПИТРС, сопутствующих заболеваний и текущей активности заболевания.
- Пациентам с 18 лет с ВПРС с обострениями с уровнем EDSS ≤ 6,5 баллов с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями, но не с целью предотвращения прогрессирования РС рекомендуется назначение ПИТРС:
интерферон бета-1а** (для п/к введения) [139],
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
или
интерферон бета-1b** [139],
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 1).
или
окрелизумаб** [127,128],
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
или
#митоксантрон** [130].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: LaMantina и соавт. проанализировали 5 РКИ, в которых 3122 (1829 ИФН и 1293 плацебо) пациента, получавших лечение интерфероном бета-1а** или интерфероном бета-1b**, соответствовали критериям ВПРС. Включенная популяция была гетерогенной с точки зрения исходных клинических характеристик заболевания, в частности доля пациентов с ВПРС с обострениями колебалась от 72% до 44% [139]. Интерфероном бета-1а** или интерфероном бета-1b** не снижали риск прогрессирования, сохранявшегося в течение 6 месяцев после трех лет лечения. Анализ установил достоверное снижение риска прогрессирования заболевания через 3 месяца и риска развития новых обострений через три года. Риск развития новых активных очагов в головном мозге со временем снижался, но эти данные были получены в результате единичных исследований МРТ, выполненных в подгруппах пациентов; несмотря на отсутствие влияния на прогрессирование, рентгенологические данные подтверждали влияние на параметры МРТ [139].
- Интерферон бета-1b** 250 мкг подкожно через день рекомендуется пациентам с ВПРС с обострениями с уровнем EDSS ≤ 6,5 баллов (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями, но не с целью предотвращения прогрессирования РС [139].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1).
Комментарий: Несмотря на снижение частоты обострений у пациентов с ВПРС с активностью, терапия интерфероном бета-1b** не замедляла прогрессирование инвалидизации в течение нескольких лет по сравнению с плацебо, что подтверждено данными крупного метаанализа [139].
- Интерферон бета-1а** 44 мкг подкожно 3 раза в неделю рекомендуется пациентам с ВПРС с обострениями с уровнем EDSS ≤ 6,5 баллов (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями, но не с целью предотвращения прогрессирования РС [139].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1).
Комментарий: Несмотря на снижение частоты обострений у пациентов с ВПРС с активностью, терапия интерфероном бета-1а** не замедляла прогрессирование инвалидизации в течение нескольких лет по сравнению с плацебо, что подтверждено данными крупного мета-анализа [139].
- Окрелизумаб** 600 мг внутривенно 1 раз в 6 месяцев рекомендуется пациентам с ВПРС с обострениями и уровнем EDSS ≤ 6,5 баллов (с 18 лет) с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [127,128]. При применении окрелизумаба** у пациентов с ВПРС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.9).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: Безопасность и эффективность окрелизумаба** не исследовалась у пациентов старше 55 лет. У таких пациентов окрелизумаб** следует использовать с осторожностью.
- #Митоксантрон** рекомендуется пациентам с ВПРС c обострениями с уровнем EDSS ≤ 6,5 баллов (с 18 лет) в качестве препарата резервной терапии при отсутствии альтернативы в связи с негативным профилем безопасности (предельная относительно безопасная кумулятивная доза – 80 мг/м2) в дозировке 12 мг/м2 в/в на 200 мл изотонического раствора натрия хлорида** каждые 3 месяца с целью предотвращения обострений и радиологической активности заболевания по данным МРТ головного/спинного мозга и инвалидизации, вызванной данными событиями [130]. При применении #митоксантрона** у пациентов с РС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.5).
Уровень убедительности рекомендаций A (уровень достоверности доказательств — 1).
- Пациентам с ППРС с 18 лет с уровнем EDSS ≤ 6,5 баллов рекомендуется назначение окрелизумаба**с целью предотвращения прогрессирования РС [140].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: Безопасность и эффективность окрелизумаба** не исследовалась у пациентов младше 18 лет и старше 55 лет. У таких пациентов окрелизумаб** следует использовать с осторожностью. У пациентов с уровнем EDSS ≥ 7,0 баллов эффективность и безопасность окрелизумаба** не исследовалась.
- Окрелизумаб** 600 мг внутривенно 1 раз в 6 месяцев рекомендуется пациентам с ППРС и уровнем EDSS ≤ 6,5 баллов (с 18 лет) с целью предотвращения прогрессирования РС [140]. При применении окрелизумаба** у пациентов с ППРС с целью обеспечения безопасности пациента рекомендуется соблюдение плана управления рисками (Приложение Б. 4.9).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
3.2. Хирургическое лечение
Не предусмотрено
3.3. Иное лечение
Симптоматическая терапия является одной из важнейших составляющих лечения РС, рациональное использование препаратов позволяет существенно улучшить качество жизни пациентов. Симптоматическая терапия назначается любым медицинским специалистом по профилю своей деятельности. Назначение симптоматической терапии не зависит от получения или не получения пациентом ПИТРС, и индивидуально назначается в зависимости от стадии и типа течения заболевания.
Коррекция синдрома хронической усталости
- Пациентам с РС (с 18 лет) для лечения синдрома хронической усталости рекомендуется использование #амантадина** в дозе 200 мг в сутки [141].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: метаанализ Yang и соавт. показал, что амантадин** был наиболее эффективным средством для лечения синдрома хронической усталости, однако исследования высокого качества, подтверждающие это, отсутствуют [136].
- Пациентам с РС (с 18 лет) для лечения синдрома хронической усталости рекомендуется #левокарнитин в дозе 1 г 2 раза в сутки [141].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: метаанализ Yang и соавт. показал, что #левокарнитин был эффективен у некоторых пациентов с синдромом хронической усталости, однако все исследования были низкого качества [136].
Коррекция нарушений мочеиспускания у пациентов с рассеянным склерозом
- У пациента с РС (с 18 лет) с синдромом гиперактивности мочевого пузыря, проявляющегося частыми императивными позывами к мочеиспусканию или недержанием мочи, с целью коррекции расстройств мочеиспускания, рекомендуется использование оксибутинина 5 мг 2 — 3 раза в сутки, или #толтеродина 2 — 4 мг 1 раз в сутки [142, 285].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: М-холиноблокаторы (G04BD средства для лечения учащенного мочеиспускания и недержания мочи) являются наиболее распространенным средством для лечения синдрома гиперактивности мочевого пузыря при РС [142]. Однако, данных по их эффективности при РС пока недостаточно, а Кокрановский обзор с применением мета-анализа демонстрирует отсутствие статистически значимого эффекта в улучшении симптомов гиперактивности мочевого пузыря [143]. Тем не менее, данные отдельных клинических исследований демонстрируют эффективность М-холиноблокаторов в лечении синдрома гиперактивности мочевого пузыря [144–146].
- У пациента с РС (с 18 лет) с синдромом гиперактивности мочевого пузыря, проявляющегося частыми императивными позывами к мочеиспусканию или недержанием мочи, с целью коррекции расстройств мочеиспускания, рекомендуется использование #десмопрессина** 10 — 100 мкг 1 р/сутки [147,148, 285].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарий: #Десмопрессин** показал эффективность в исследовании Valiquette и соавт., уменьшив процент ночей с никтурией с 97% до 66%, а также в исследовании Hilton и соавт., снизив частоту позывов к мочеиспусканию [147,148]. Все исследования были низкого качества.
- У пациента с РС (с 18 лет) с затруднением опорожнения мочевого пузыря вследствие синдрома сфинктерно-детрузорной диссинергии рекомендуется использование альфа-адреноблокаторов (тамсулозин** 0,4 г 1 раз в сутки, доксазозин** 2 — 8 мг в сутки) с целью коррекции расстройств мочеиспускания [149,150].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий: Положительный эффект при задержке мочеиспускания был показан в ряде исследований при рассеянном склерозе и других неврологических заболеваниях [149,150].
- У пациента с РС (с 18 лет) с синдромом гиперактивности мочевого пузыря, проявляющегося частыми императивными позывами к мочеиспусканию или недержанием мочи, и резистентности к пероральным и интраназальным лекарственным препаратам рекомендуется использование препаратов ботулинического токсина типа А** в виде интравезикальных инъекций по назначению врача-уролога с целью коррекции расстройств мочеиспускания [149–153].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: Интравезикальное введение ботулинического токсина типа A** приводило к увеличению максимального объема мочевого пузыря, уменьшению частоты позывов в течения дня и ночи, уменьшению количества эпизодов недержания мочи, а также частоты использования впитывающего белья [152–156]. Большинство исследований были проведены в смешанных группах, включая пациентов с различными причинами нейрогенной дисфункции мочевого пузыря, что осложняет заключение вывода об эффективности метода лечения при рассеянном склерозе.
Коррекция нарушений мышечного тонуса
- У пациента с РС (с 18 лет) с синдромом спастичности с целью снижения мышечного тонуса рекомендуется использование:
баклофена** [159 — 164]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
или
тизанидина** [158]
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 3).
или
толперизона (доза подбирается индивидуально с учетом переносимости и
эффективности) [157].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Систематический обзор клинических исследований сообщает об эффективности использования данных препаратов для коррекции спастического гипертонуса [158].
- В случае непереносимости либо неэффективности терапии баклофеном**, тизанидином** или толперизоном у пациентов с РС (с 18 лет) с синдромом спастичности рекомендуется использование #габапентина (доза подбирается индивидуально с учетом переносимости и эффективности) с целью снижения мышечного тонуса [158,165,166].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
- У пациента с РС (с 18 лет) с локальным спастическим гипертонусом мышц и неэффективности пероральной терапии спастичности рекомендуется применение препаратов ботулинического токсина типа A** внутримышечно обученным специалистом для облегчения передвижения пациента, манипуляций рукой или улучшения возможности обслуживания / самообслуживания [158,167–174].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарий: Клинические исследования Hyman и соавт. и Gusev и соавт. продемонстрировали уменьшение выраженности нижнего спастического парапареза у пациентов с EDSS ≥ 7,0 баллов [168,169]. Введение ботулинического токсина типа A** в приводящие мышцы бедра увеличило объем движений в тазобедренном суставе, уменьшило выраженность спастического гипертонуса, боль в мышцах ног и облегчило проведение гигиенических мероприятий. Исследование Gracies и соавт. на менее инвалидизированной смешанной популяции пациентов (включая РС) с нижним спастическим парапарезом показало, что введение ботулинического токсина типа A** увеличило скорость ходьбы [170]. Ограниченные данные в смешанных популяциях существуют в отношении влияния ботулинического токсина типа A** на гипертонус мышц рук при РС [171–173]. На сегодняшний день не получено данных, что действие и спектр НПР ботулинического токсинатипа А** отличается при лечении спастичности при РС по сравнению с другими нозологиями.
- У пациентов с РС (с 18 лет) с такими симптомами и/или синдромами, как боль, синдром беспокойных ног, бессонница лечение рекомендуется осуществлять в соответствии с общими рекомендациями для таких синдромов и симптомов с целью их коррекции [175–177].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Специальных исследований при РС по данному вопросу не проводилось. В настоящий момент, лечение указанных синдромом подразумевает использование общих рекомендаций, не специализированных для лечения РС.
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Пациентам с РС рекомендуется проводить медицинскую реабилитацию усилиями мультидисциплинарной бригады специалистов с целью снижения уровня инвалидизации, улучшения показателей активности и участия и улучшения качества жизни [178,179].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарий: Клинические исследования с умеренной доказательностью демонстрируют положительный эффект от мультидисциплинарной реабилитации.
- Пациентам с РС с 18 лет рекомендуется проводить медицинскую реабилитацию в рамках специализированного отделения нейрореабилитации в течение 3 — 5 недель с целью снижения уровня инвалидизации, улучшения показателей активности и участия и улучшения качества жизни [179–182].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарий: Клинические исследования применения мультидисциплинарного подхода к реабилитации демонстрируют краткосрочную эффективность (до 12 недель) в рамках стационарного пребывания в течение 3 — 5 недель для показателей активности и участия и уменьшения имеющегося неврологического дефицита [179–181]. Данные исследований подтверждают со слабой силой доказательности, что интенсивная стационарная реабилитация превосходит по эффективности амбулаторную реабилитацию в краткосрочной перспективе (через 3 месяца) [182].
- Пациентам с РС, недавно перенесшим обострение c неполным регрессом симптомов, рекомендуется проведение мультидисциплинарной реабилитации с целью уменьшения неврологического дефицита, ограничений активности и участия [181,183,184].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарий: В систематическом обзоре 3 исследований (включая 1 рандомизированное плацебоконтролируемое исследование) показана эффективность мультидисциплинарной реабилитации в условиях круглосуточного стационара или дневного стационара при давности возникновения симптомов не более 5 месяцев [181,183,184].
- Всем пациентам с РС рекомендуется проводить оценку эффективности реабилитации валидированными объективными методами с использованием тестов, шкал и опросников для оценки ходьбы, баланса, функции рук, повседневной жизнедеятельности и качества жизни. Оценка должна проводиться до начала и после завершения реабилитации [185–187].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4 (сложившаяся клиническая практика)).
Комментарий: Объективные методики оценки могут включать тесты оценки ходьбы (тест 6-минутной или 2-минутной ходьбы, тест 25 шагов, индекс мобильности Ривермид и др.), тесты оценки баланса (шкала баланса Берг, тест «Встань и иди» и др.) [185,186], тест функциональной независимости (FIM), тест 9 колышков и отверстий, тест руки Френчай, опросник оценки качества жизни (SF-36) (Приложения Г3 — Г8). Методы оценки должны применяться в зависимости от клинической ситуации, но целесообразно использование набора тестов для оценки всего спектра нарушений. Исследования по эффективности реабилитации рассеянного склероза с применением оценки до вмешательства и после по сравнению с отсутствием оценок не проводились. Однако, сложившаяся клиническая практика подтверждает важность регулярного тестирования и оценки эффективности реабилитации для врачей, пациентов, страховых компаний и государства [187]. Многим методикам требуется адаптация и валидация в условиях российской клинической практики.
- После курса реабилитации в рамках круглосуточного стационара, пациентам с РС с любым типом течения рекомендуется долгосрочная (до 6 недель) реабилитация в условиях реабилитационного дневного стационара или на дому (до 12 недель) для уменьшения инвалидизации, улучшения показателей активности и участия, а также качества жизни [179,188–190].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: Существуют ограниченные доказательства эффективности высокоинтенсивного реабилитационного вмешательства в течение 6 недель в амбулаторных условиях для улучшения показателей участия и качества жизни через 12 месяцев [179]. Для долгосрочных вмешательств амбулаторно или на дому существуют убедительные доказательства улучшения качества жизни пациентов [188–190].
- Рекомендуется при кодировании реабилитационного диагноза пациентов с РС специалистам по медицинской реабилитации выставлять диагноз в категориях Международной классификации функционирования (МКФ) c целью унифицированного обозначения всех имеющихся нарушений пациента, а также для улучшения междисциплинарного взаимодействия [191–194].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: Постановка реабилитационного диагноза с помощью МКФ занимает центральное место при планировании реабилитации. Опираясь на рекомендации Всемирной Организации Здравоохранения (ВОЗ), специально для РС были разработаны и валидированы ключевые разделы МКФ для РС (ICF Core Set) [191–194]. Их использование помогает объективизировать состояние пациента и сформировать план реабилитации [191].
- Пациентам с РС рекомендуется физическая реабилитация в качестве обязательного компонента реабилитационных программ для снижения инвалидизации, улучшения показателей активности и участия и качества жизни [178,190].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: Существующие данные с высокой степенью доказательности подтверждают эффективность физических методов реабилитации (например, лечебной физкультуры, кинезотерапии, роботизированной механотерапии, гидрокинезотерапии) для улучшения показателей активности и участия, повышения мышечной силы, способность пациента к передвижению, независимости, аэробной выносливости, снижает утомляемость и улучшает показатели качества жизни [178,190]. Никакой из методов не обладает существенным преимуществом перед остальными.
- Пациентам с РС для уменьшения мышечной слабости и утомляемости рекомендуется физическая реабилитация, в особенности, с использованием тренировок на выносливость, силовых тренировок, роботизированной механотерапии, йоги, лечебной физкультуры в бассейне, спортивного скалолазания [178,195–200].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарий: Полученные данные клинических исследований и их мета-анализа указывают на эффект физической реабилитации для уменьшения утомляемости. Наибольшую эффективность продемонстрировали тренировки на выносливость, силовые тренировки, роботизированная механотерапия, йога, тренировки баланса и смешанные методики [178,195]. Механизмом, определяющим эффективность физической реабилитации при утомляемости, является улучшение состояния сердечно-сосудистой и дыхательной систем, прямой нейропротективный эффект реабилитации и нормализация работы гипоталамо-гипофизарной оси, которая, как считается, вовлечена в патогенез утомляемости при РС [195–198]. Исследования по оценке эффекта на утомляемость проводились в основном у пациентов с уровнем EDSS < 6,0 баллов. Эффективность подобных методик у более инвалидизированных пациентов не изучалась, однако, при наличии возможности, физическая реабилитация должна проводиться пациентам с любым уровнем EDSS [178]. Лечебная физкультура в бассейне и гидрокинезотерапия показали эффективность в уменьшении утомляемости, мышечной силы, депрессии и качества жизни [201,202]. Небольшие рандомизированные клинические исследования по спортивному скалолазанию демонстрируют снижение утомляемости и увеличение мышечной силы [203]. Интенсивность и продолжительность вмешательства следует выбирать индивидуально для каждого пациента. Никакой из методов не обладает существенным преимуществом перед остальными.
- Пациентам с РС для уменьшения общей (не мышечной) утомляемости рекомендуется назначение специализированной индивидуальной программы реабилитации с использованием когнитивной поведенческой терапии, обучения принципам сохранения энергии, а также проведение тренингов по формированию режима дня [178,200,204].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарий: Данные исследований с применением метаанализа с высокой достоверностью отмечают эффективность специализированных программ, направленных на борьбу с утомляемостью, включающих когнитивную поведенческую терапию и обучение принципам сохранения энергии [178,200]. Неоднозначные данные существуют в отношении использования охлаждающих жилетов [204].
- Пациентам с РС рекомендуется включение эрготерапии в программы реабилитации с целью уменьшения ограничений активности и участия, улучшения качества жизни [205].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарий: Ряд РКИ низкого качества демонстрирует эффективность некоторых подходов в эрготерапии для улучшения показателей активности и участия, утомляемости и качества жизни. При включении эрготерапии в программы реабилитации следует прежде всего рассматривать такие методы как обучение и консультирование пациентов и программы сохранения энергии, имеющие доказательную базу при РС [205].
- Пациентам с РС рекомендуется мультидисциплинарная холистическая реабилитация верхних конечностей для уменьшения степени нарушений их функций, ограничения активности и участия. Наиболее эффективными вмешательствами могут считаться роботассистированная реабилитация, лечебной физкультуры и эрготерапия [206].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарий: Исследования демонстрируют улучшение показателей реализации и капаситета (в структуре МКФ) верхних конечностей после проведения комплексной мультидисциплинарной и роботассистированной реабилитации [206]. Лечебная физкультура и тренировки на выносливость показали улучшение показателей функций верхних конечностей, но не активности и участия [206].
- Пациентам с РС с 18 лет рекомендуется обучение навыкам самообслуживания, консультирование по адаптации среды, по вопросам трудоустройства с учетом имеющихся ограничений, а также подбор необходимых технических средств реабилитации для уменьшения степени выраженности ограничений, социальной дезадаптации и снижения качества жизни [207]. Консультации рекомендуется проводить эрготерапевтам, врачам по физической и реабилитационной медицине и социальным работникам.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
- В процессе реабилитации рекомендуется проводить консультации и обучение с родственниками пациентов с РС для уменьшения ограничений активности и участия пациента, обучения родственников уходу за инвалидизированным пациентом и профилактики психологического выгорания родственников инвалидизированных пациентов [208].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
- Пациентам с РС с 18 лет для коррекции нарушений баланса и ходьбы, а также профилактики падений рекомендуются баланстерапия, роботизированная механотерапия при заболеваниях центральной нервной системы и головного мозга, тренировка с биологической обратной связью по опорной реакции при заболеваниях центральной нервной системы и головного мозга [202,209–217].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарий: Клинические исследования и данные систематических обзоров выявили слабый или умеренный положительный эффект на показатели баланса при использовании индивидуальных и групповых упражнений для тренировки баланса [209], совмещенных с йогой [210], ЛФК в бассейне [202], упражнениями для зрения [211], сенсорной интеграцией [212], а также при использовании стабилометрических платформ с обратной связью для тренировки баланса [213]. В метаанализе использование виртуальной реальности продемонстрировало эффективность, сопоставимую с традиционными методиками [214]. Клинические исследования с использованием роботассистированной тренировки ходьбы продемонстрировали значимое улучшение некоторых показателей баланса [215]. Клинические исследования умеренного и слабого методологического качества демонстрируют улучшения баланса и ходьбы после применения экзоскелетассистированной реабилитации [216,217]. Ни один из методов не имеет научно-обоснованного предпочтения перед остальными.
- Пациентам с РС с 18 лет с синдромом свисающей стопы рекомендуется применение функциональной электростимуляции для увеличения скорости ходьбы [218].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: Систематический обзор с применением мета-анализа продемонстрировал значимое увеличение скорости ходьбы при применении функциональной электростимуляции мышц передней поверхности голени при синдроме свисающей стопы [218].
- Пациентам с РС с 18 лет с синдромом спастического гипертонуса рекомендуются следующие немедикаментозные методы с целью коррекции спастического гипертонуса, болевого синдрома, профилактики и лечения суставных контрактур: физические упражнения на растяжение и сокращение мышц-агонистов и антагонистов (отдельно или в сочетании с инъекциями ботулинического токсина типа А**), транскраниальная магнитная стимуляция, ношение индивидуальных ортезов покоя, гипсование и обучение стратегиям поведения в повседневной жизни с целью уменьшения спастического гипертонуса мышц, увеличения объема активных и пассивных движений, уменьшения болевого синдрома [219].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: Систематический анализ данных рандомизированных клинических исследований выявил низкое качество проведенных исследований [219]. Тем не менее, ряд исследований демонстрируют краткосрочную (до 1 недели) или среднесрочную (до 6 месяцев) эффективность от проведения лечебной физкультуры (отдельно или в сочетании с инъекциями ботулинического токсина типа А**), транскраниальной магнитной стимуляции[219]. Не показали эффективности методы чрескожной электрической стимуляции нервов, вибрация всего тела, спортивное скалолазание и йога [219]. Исследования демонстрируют недостаточно согласованные данные по эффективности использования индивидуальных ортезов покоя и гипсования при инсульте или при других приобретенных повреждениях головного мозга, однако в большинстве публикаций отмечен значимый положительный эффект от вмешательства в отношении объема активных и пассивных движений, уменьшения болевого синдрома [220–222].
- Пациентам с РС, получающим терапию ботулиническим токсином типа А** для уменьшения спастического гипертонуса мышц верхних и нижних конечностей, рекомендуется дополнительное применение физических методов реабилитации для уменьшения гипертонуса и увеличения объема пассивных и активных движений пораженных конечностей [223].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: Систематический обзор с применением метаанализа демонстрирует с умеренной степенью доказательности эффективность сочетания упражнений на растяжение и терапии, вызванная ограничением движения, с инъекциями ботулинического токсина типа А** [223]. Стоит отметить, что выраженность эффекта от данных мероприятий не высока, но превышает эффект от применения только инъекций ботулинического токсина типа А**.
- Пациентам с РС с 18 лет с нарушениями речи и глотания рекомендуется ранняя комплексная медико-логопедическая процедура при дисфагии, медико-логопедическая процедура при дизартрии, разработка индивидуальной программы логопедической реабилитации, обучение компенсаторным стратегиям и альтернативным способам коммуникации с целью уменьшения выраженности нарушений речи и глотания, улучшения дыхания, профилактики аспирации и снижения ограничений активности и участия [207].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
- Всем пациентам с РС, проходящим реабилитацию на амбулаторном или стационарном этапе, рекомендуется комплексное клинико-психологическое нейропсихологическое обследование с целью выявления нарушений памяти, внимания или других когнитивных функций. В ряде случае может быть рекомендован совместный осмотр эрготерапевта и медицинского психолога (нейропсихолога) [224].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: Большая часть пациентов с РС имеют нарушения когнитивных функций, что снижает качество жизни и влияет на инвалидизацию при РС [224]. Для коррекции нарушений требуется предварительная оценка выраженности нарушений.
- Пациентам с РС при выявлении объективного снижения показателей когнитивных функций по данным стандартизированных тестов рекомендуется нейропсихологическая реабилитация когнитивных функций с использованием холлистического подхода и/или специализированных когнитивных тренингов (в том числе в электронной форме) [224–226].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: Систематический обзор данных исследований с применением метаанализа выявил слабый положительный эффект от проведения нейропсихологической реабилитации, при этом часть исследований имели низкое качество. Результаты некоторых метаанализов конфликтуют с результатами других [224–226]. Исследования демонстрируют значимое улучшение показателей кратковременной и долговременной памяти, внимания, объема памяти и уменьшение депрессии после реабилитации [224,225]. Учитывая отсутствие доказанного эффекта на когнитивные функции от медикаментозной терапии, нейропсихологическую реабилитацию следует рассматривать как единственный доказанный метод улучшения когнитивных функций в настоящий момент. Продолжительность и виды вмешательства могут отличаться. В настоящий момент недостаточно данных, что определить преимущественную эффективность одного метода над другим [226].
- Пациентам с РС с 18 лет, проходящим реабилитацию на амбулаторном или стационарном этапе, рекомендуется консультация медицинского психолога и клинико-психологическое психодиагностическое обследование с целью выявления депрессии, тревожного синдрома, суицидальных наклонностей, нарушений мотивации и других эмоционально-волевых нарушений, а также для принятия решения о необходимости консультации врача-психиатра [227–229].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: Депрессия и тревога являются частыми психологическими нарушениями при РС, приводя к снижению качества жизни, риску суицида и снижению комплаентности [227–229].
- Пациентам с РС при выявлении депрессивного синдрома по данным обследования медицинского психолога, рекомендуется индивидуальное клинико-психологическое консультирование, индивидуальная психотерапия и групповая психотерапия с целью снижения выраженности депрессии и улучшения качества жизни [230–232].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарий: Систематический обзор данных клинических исследований среднего качества (не все первичные конечные точки и выводы согласованы) с применением метаанализа демонстрирует снижение уровня депрессии от применения психологического консультирования и когнитивной поведенческой терапии индивидуально и в группе [232]. Недостаточно данных представлено по эффективности психологического вмешательства для уменьшения тревожного синдрома.
- Пациентам c РС с 18 лет рекомендуется проведение телемедицинской реабилитации для коррекции нарушений функций, улучшения показателей активности и участия (в структуре МКФ), уменьшения выраженности инвалидизации, уменьшения утомляемости и улучшения качества жизни [233].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: Телемедицинская реабилитация может применяться в комплексном оказании помощи пациентам с РС. Очевидным преимуществом телереабилитации является возможность использования этого метода для наблюдения и контроля эффективности реабилитации у пациентов, проживающих удаленно. Исследования демонстрируют низкий уровень доказательности для проведенных вмешательств: в 9 РКИ, включенных в метаанализ, использовали различные виды и продолжительность вмешательств. Реабилитационные телемедицинские мероприятия включали физические упражнения, образование пациентов, поведенческую терапию и программы, направленные на снижение симптомов [233].
- Пациентам с РС при недержании мочи рекомендуются физические методы реабилитации с целью уменьшения выраженности дисфункции мочевого пузыря и улучшения качества жизни [234].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: Рандомизированные клинические исследования выявили положительный эффект на показатели непроизвольного мочеиспускания и качества жизни при использовании физических упражнений для тренировки мышц малого таза, упражнений с применением биологической обратной связи c помощью электронейромиографии, стимуляции большеберцового нерва, стимуляции мышц тазового дна [234], совмещенных с ЛФК.
Прогноз
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
При постановке диагноза рассеянного склероза должны быть исключены все другие заболевания нервной системы, в том числе поражения при инфекционных, токсических, сосудистых и неопластических заболеваниях, а также системные аутоиммунные заболевания с васкулитами и наследственно-дегенеративные заболевания.
При начале и проведении ПИТРС необходимо учитывать соматическое состояние пациента и возможные побочные реакции. Особое внимание нужно уделить следующим состояниям на фоне терапии ПИТРС:
— Интерферонами бета-1a** и интерфероном бета-1b** – возможно усиление депрессии, усиление спастического повышения тонуса, повышение риска припадков при наличии эпилепсии в анамнезе;
— Терифлуномид** – у женщин детородного возраста — тщательная контрацепция, патология поджелудочной железы;
— Диметилфумарат** – гастроинтестинальные проблемы, симпатические реакции («жжение и горение» и др.), лимфопения и риск ПМЛ;
— #Митоксантрон**– существенное повышение риска развития лейкозов, повышение риска развития патологии сердца;
— Натализумаб** – острые инфузионные аллергические реакции на введение, риск ПМЛ в зависимости от наличия JC-инфекции и титра антител к этому вирусу, а также от предшествующей иммуносупрессии и длительности курса терапии препаратом, при отмене препарата – обострения РС, нельзя сочетать с другими ПИТРС;
— Финголимод** – брадикардия и нарушения ритма сердца, нельзя назначать при наличии сердечно-сосудистых заболеваний, особенно с брадикардией, при применении препаратов, замедляющих сердечный ритм, отек макулы (в малой степени), лимфопения и риск ПМЛ и других инфекций, высокий риск развития обострения при отмене препарата;
— Алемтузумаб** – острые инфузионные аллергические реакции на введение, риск оппортунистических инфекций (в том числе листериоза), патология щитовидной железы, иммунная тромбоцитопения (ИТП) и другие вторичные аутоиммунные реакции;
— Окрелизумаб** – острые инфузионные аллергические реакции на введение, риск оппортунистических инфекций;
— Кладрибин** — лимфопения и риск инфекций.
Госпитализация
Организация оказания медицинской помощи
- Для оказания помощи пациентам с РС рекомендуется организовывать отдельные структуры (кабинеты, клинико-диагностические кабинеты, отделения, специализированные неврологические центры по рассеянному склерозу) с целью диагностики, диспансерного наблюдения за данной категорией пациентов [237].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Организация специализированного центра/отделения/кабинета рассматривается экспертами — членами рабочей группы как единственно эффективная мера организации квалифицированной помощи пациентам с РС, а также способ сбора актуальной информации о распространённости заболевания и потребности в терапии ПИТРС, реабилитации и других мероприятиях.
- Диспансерное наблюдение пациентов с РС рекомендуется осуществлять в специализированном клинико-диагностическом кабинете/отделении или специализированном неврологическом центре рассеянного склероза [237].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Организация специализированного центра/отделения/кабинета рассматривается экспертами — членами рабочей группы как единственно эффективная мера организации квалифицированной помощи пациентам с РС, а также способ сбора актуальной информации о распространённости заболевания и потребности в терапии ПИТРС, реабилитации и других мероприятиях.
- Терапию обострений РС легкой степени тяжести рекомендуется проводить в дневном стационаре (Приложение Г14) [272].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: Не все пациенты нуждаются в госпитализации в круглосуточный стационар для проведения терапии обострения РС. Нет достаточных данных для достоверной оценки преимуществ терапии обострения РС в условиях круглосуточного стационара, дневного стационара, домашних условиях. РКИ, проведенное Chataway и соавт., со средним качеством доказательств, включающее 124 пациента, не продемонстрировало различий в клинической эффективности между терапией обострения (внутривенными глюкокортикоидами), проводимой в дневном стационаре и на дому.
- Терапию обострений РС средней и тяжелой степеней тяжести рекомендуется проводить в круглосуточном стационаре (Приложение А3.12) [272].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарий: Не все пациенты нуждаются в госпитализации в круглосуточный стационар для проведения терапии обострения РС. Нет достаточных данных для достоверной оценки преимуществ терапии обострения РС в условиях круглосуточного стационара, дневного стационара, домашних условиях. РКИ, проведенное Chataway и соавт., со средним качеством доказательств, включающее 124 пациента, не продемонстрировало различий в клинической эффективности между терапией обострения (внутривенными глюкокортикоидами), проводимой в дневном стационаре и на дому.
- В случаях, затрудняющих проведение терапии обострений РС средней степени тяжести в круглосуточном стационаре, рекомендуется проводить лечение в дневном стационаре после обсуждения с пациентом [272].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: Не все пациенты нуждаются в госпитализации в круглосуточный стационар для проведения терапии обострения РС. Нет достаточных данных для достоверной оценки преимуществ терапии обострения РС в условиях круглосуточного стационара, дневного стационара, домашних условиях. РКИ, проведенное Chataway и соавт., со средним качеством доказательств, включающее 124 пациента, не продемонстрировало различий в клинической эффективности между терапией обострения (внутривенными глюкокортикоидами), проводимой в дневном стационаре и на дому.
- Пациентам, получающим инфузионные ПИТРС, для проведения внутривенных инфузий рекомендуется организовывать специализированные дневные стационары в структуре неврологических центров РС, клинико-диагностических кабинетов [237,273].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Проведение инфузии ПИТРС в рамках дневного стационара позволит снизить нагрузку на стационарное звено здравоохранения, обеспечив при этом оптимальный контроль за переносимостью и эффективностью терапии.
- В случае отсутствия показаний к назначению ПИТРС или письменного отказа пациента от терапии ПИТРС рекомендуется организация медицинской помощи по принципу доступности и качества (Приложение А3.9) [237].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: В первичную медицинскую документацию помещается документ, обосновывающий неполучение пациентом ПИТРС (решение специализированного центра; отказ пациента от получения ПИТРС). Пациентам, которые могут посещать первичное специализированное ЛПУ, проводится: осмотр лечащего врача-невролога (не реже 1 раза в 6 месяцев); назначение симптоматической терапии. Для пациентов, которые не могут посещать первичное специализированное ЛПУ, должна быть организованна патронажная служба по месту первичного ЛПУ.
- В случае принятия решения пациенткой с РС о планировании беременности рекомендуется направить пациентку в специализированный Центр (отделение, кабинет, клинико-диагностический кабинет) РС для проведения беседы об особенностях течения беременности и послеродового периода при РС. РС не является показанием для прерывания беременности [241–243].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
- Решение вопроса об оказании экстренной и плановой хирургической помощи, в том числе стоматологической, пациенту с РС рекомендуется принимать на основании объемов оперативного вмешательства и состояния пациента [274,275].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарий: РС не является противопоказанием для проведения медицинского вмешательства, необходимого пациенту в связи с возникшим сопутствующим заболеванием. Нет данных о наличии существенных противопоказаний к определенным видам медицинских вмешательств. Систематический обзор данных исследований с применением метаанализа выявил слабое повышение риска развития РС у пациентов, которым проводилась тонзилэктомия или аппендэктомия в возрасте до 20 лет, при этом часть исследований имели низкое качество.
- Решение вопроса об анестезиологическом пособии пациенту с РС в случае оказания хирургической помощи, в том числе стоматологической, рекомендуется принимать на основании объемов оперативного вмешательства и состояния пациента [276].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: РС не является противопоказанием для проведения медицинского вмешательства, необходимого пациенту в связи с возникшим сопутствующим заболеванием. Нет данных о наличии существенных противопоказаний к определенным видам медицинских вмешательств.
- Пациентам с РС рекомендуется телемедицинская консультация с целью обучения пациента использованию ПИТРС, плановой оценки состояния в динамике, выписки рецепта, а также с целью обсуждения вопросов, не требующих присутствия пациента (например, обсуждение диеты, режима дня или рисков передачи РС по наследству) [277,278].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарий: Телемедицинская консультация является вариантом эффективного расходования сил и средств системы здравоохранения и пациента в условиях дефицита времени и ограничений мобильности инвалидизированных пациентов. Широкое введение телемедицинских консультаций позволит пациентам получить от врача информацию, которую, за неимением времени на очном приеме, они задать не смогут.
- Пациентам с РС рекомендуется дистанционное наблюдение с целью оценки динамики лабораторных и инструментальных показателей при выполнении плана управления рисками, оценки рекомендованных и выполненных показателей обследований, оценки качества жизни пациентов [277,278].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3).
Комментарий: Дистанционное наблюдение возможно с применением информационных технологий и систем поддержки принятия решений, которые могут собирать, обрабатывать и фиксировать данные, полученные от пациента и передавать их лечащему врачу в соответствии с действующим законодательством.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Доказательных исследований по методам профилактики рассеянного склероза не проводилось. Вопросы первичной профилактики являются наиболее значимыми для людей, имеющих высокий риск развития РС, а именно – для родственников пациентов РС первой степени родства, пациентов с клинически изолированным синдромом, радиологически изолированным синдромом, носителями генетических маркеров РС (HLA-DR-1.15). Несмотря на отсутствие обширных исследований, отдельные эпидемиологические работы по методу случай-контроль показывают ассоциацию некоторых факторов риска с высокой частотой развития РС. К таким факторам относятся, курение, недостаток витамина Д, вирусные инфекции, хронический психоэмоциональный стресс.
Вторичная профилактика включает в себя профилактику активности РС (клиническую, радиологическую) и прогрессирования, а также управление рисками на ПИТРС, согласно утвержденному плану. Значимым считается правильное ведение беременности и родов, ограничение вакцинирования и инсоляции, диетические рекомендации, своевременная коррекция психоэмоциональных нарушений (особенно депрессии и тревоги) [235,236].
- Пациента с РС рекомендуется взять на диспансерное наблюдение в рамках специализированной амбулаторной неврологической службы, организованной либо в виде специализированного клинико-диагностического кабинета/отделения или специализированного неврологического центра по оказанию помощи пациентам с демиелинизирующими заболеваниями, с целью эффективного наблюдения и сопровождения [237].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Организация специализированного центра/отделения/кабинета рассматривается экспертами — членами рабочей группы как единственно эффективная мера организации квалифицированной помощи пациентам с РС, а также способ сбора актуальной информации о распространённости заболевания и потребности в терапии ПИТРС, реабилитации и других мероприятиях.
- Пациентам с РС рекомендуется плановый диспансерный осмотр проводить не реже чем 1 раз в 6 месяцев, с целью актуализации типа течения и стадии болезни, оценки прогрессирования, оценки эффективности ПИТРС, оценки безопасности терапии ПИТРС, соблюдения плана управления рисками, корректировки тактики ведения [238,239].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: Осмотр у специалиста по РС не реже 1 раза в 6 месяцев рассматривается экспертами-членами рабочей группы как достаточно эффективная мера для контроля эффективности и переносимости терапии, контроля над течением заболевания.
- Пациентам с РС при появлении новой неврологической симптоматики или значимого ухудшения имеющейся симптоматики длительностью свыше 24 часов рекомендуется проведение неврологического осмотра на предмет наличия обострения. При осмотре проводится объективизация имеющихся жалоб, исключение наличия инфекционного заболевания либо иной причины неврологических нарушений [24,240].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Ухудшение симптомов РС может возникать по многим причинам, в том числе, в результате инфекционного заболевания. Только осмотр квалифицированного врача-невролога — специалиста по РС — сможет определить причину появления жалоб, зафиксировать обострение или прогрессирование заболевания, а также сделать выводы об эффективности принимаемой терапии ПИТРС.
- Пациентам с РС при первоначальном назначении ПИТРС, а также при любой смене терапии рекомендуется повторный прием врача-невролога с целью разъяснительной беседы лечащим врачом об ожидаемых результатах терапии, режиме терапии. Пациенту должна быть предоставлена информация о рисках и побочных эффектах терапии [24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Информированность пациента важна для повышения комплаенса. Совместное принятие решения о назначении или смене терапии ПИТРС, информирование пациента о рисках и правилах приема ПИТРС, а также о плане управления рисками является необходимым этапом при начале любой терапии ПИТРС, что требует дополнительного времени и повторного визита именно с целью обсуждения и принятия решения.
- При назначении ПИТРС пациенткам с РС рекомендуется проводить беседу о необходимости применения надежных методов контрацепции в течение всего периода терапии ПИТРС и определенное время после окончания терапии (в случае лечения натализумабом**, алемтузумабом**, окрелизумабом**, терифлуномидом**, #митоксантроном**, финголимодом**, кладрибином**) [241–244].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
- Пациентам с РС рекомендуется проведение МРТ головного мозга с контрастированием по следующим показаниям [51,54]:
— при наличии клинических признаков обострения РС;
— перед началом терапии ПИТРС или при замене ПИТРС;
— после родов;
— при отсутствии корректных данных предыдущего исследования (например, пациент начинает наблюдаться в другой клинике, данные МРТ из предыдущей клиники отсутствуют);
— при сомнении и предполагаемом пересмотре диагноза;
— на фоне терапии ПИТРС (через 6 месяцев после начала терапии, через 12 месяцев после начала терапии, далее каждые 12 месяцев);
— на фоне терапии натализумабом** более 2 лет при наличии высокого риска развития ПМЛ (пациенты с высоким индексом антител к JC-вирусу ≥ 1,5 или предшествующей терапией иммунодепрессантами в анамнезе) каждые 3 — 6 месяцев по сокращенному протоколу [51].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Динамическое наблюдение пациента с использованием методики МРТ на фоне терапии ПИТРС для определения эффективности получаемой терапии. При анализе данных наблюдения следует учитывать, что начало клинического эффекта препарата обычно отсрочено и наступает (в зависимости от препарата) через 3 — 6 месяцев после начала его использования. Поэтому проведение контрольной МРТ при назначении или замене ПИТРС до срока 6 месяцев нецелесообразно. Проведение МРТ головного мозга в случае замены ПИТРС необходимо для обеспечения безопасности новой
терапии и стартовой оценки активности РС.
- Пациентам с РС при выполнении МРТ исследовании рекомендуется оформление структурированного протокола заключения, с целью анализа динамики очагов, оценки эффективности проводимой терапии (Приложение А3.5) [56,245].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: Экспертами — членами рабочей группы однозначно рекомендуется заполнение структурированного протокола заключения, на основе которого лечащий врач может принимать решения о дальнейшей тактике ведения пациента. Без заполнения структурированного протокола заключения услуга проведения МРТ исследования считается не выполненной или выполненной не качественно.
- Выбор тактики ведения беременности и метода родоразрешения у пациенток с РС рекомендуется осуществлять в соответствии с общими рекомендациями ведения беременности и родов по усмотрению лечащего врача-акушера-гинеколога [241,242].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий: при наличии у пациентки с РС нижнего парапареза с выраженной спастичностью целесообразно использовать метод кесарева сечения для предупреждения развития вторичной слабости родовой деятельности [242].
- Пациенткам с РС после родов рекомендуется особое внимание уделять профилактике инфекций и адекватной психокоррекции, наиболее оптимальным сроком возобновления приема ПИТРС является третий месяц послеродового периода при условии полного прекращения грудного вскармливания ребенка (с целью минимизации возможных рисков обострений через 3 месяца после родов) [241,243].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
- Пациентам с РС рекомендуется отказаться от курения, с целью предотвращения ухудшения прогноза течения заболевания [246,247].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Курение связано с большим риском обострений и прогрессирования РС [246,247]. С целью снижения риска прогрессирования инвалидизации рекомендуется информировать пациентов о пользе и способах отказа от курения.
- Пациентам с РС рекомендуется исследование уровня 25-OH витамина Д в крови в сыворотке крови с последующей коррекцией его уровня до нормальных значений с целью снижения риска ухудшения течения заболевания; в случае невозможности контроля уровня витамина Д необходимо рекомендовать безопасную дозу колекальциферола** до 4000 МЕ на постоянный прием; необходимо избегать бесконтрольного приема доз, превышающих 10000 МЕ[248].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Низкий уровень витамина Д связан с повышением риска развития РС [248]. Основным ограничением, препятствующим использованию витамина Д в качестве модифицирующей течение РС добавки, является отсутствие контролируемых рандомизированных исследований [248]. Существуют косвенные данные, указывающие на то, что прием витамина Д может снизить частоту обострений, однако эти данные нуждаются в подтверждении [249,250]. Не известно также влияние приема витамина Д на нейродегенеративный компонент РС и клиническое прогрессирование симптомов.
- При наличии у пациента с РС расстройств мочеиспускания рекомендуется направить пациента к профильному специалисту (врач-уролог, врач-акушер-гинеколог) для исключения сопутствующих заболеваний, приводящий к нарушению тазовых функций и выполнения УЗИ мочевого пузыря с определением объема остаточной мочи, при необходимости проведения уродинамических исследований для обеспечения безопасности терапии расстройств мочеиспускания [142].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Квалифицированное обследование у профильного специалиста позволит провести дифференциальную диагностику состояния, исключить причины, не связанные с поражением ЦНС и назначить адекватную терапию. Предпочтительнее направлять к специалистам, имеющим опыт в работе с пациентами неврологического профиля – врачам-урологам (нейроурологам).
- При остаточном объеме мочи более 100 мл у пациентов с РС с расстройствами мочеиспускания рекомендуется проведение периодической самокатетеризации (после обучения специалистом) с целью коррекции расстройств мочеиспускания [142].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Объем остаточной мочи, требующий периодической самокатетеризации, достоверно не определен. Необходимо учитывать индивидуальные особенности пациентов.
- У пациентов с РС, получающих инъекционную терапию ПИТРС первой линии с целью профилактики появления и контроля местных НПР терапии (покраснение и отек, зуд, уплотнение, дискомфорт, кровоизлияние, липоатрофия, некроз) рекомендуется [251,252]:
— при начале терапии интерферонами бета-1a** и интерфероном бета-1b**–титровать дозу препарата согласно инструкции по медицинскому применению лекарственного препарата;
— при наличии технической возможности использовать автоинжектор;
— проконтролировать асептику и антисептику, технику выполнения инъекций пациентом;
— перед инъекцией выдержать препарат при комнатной температуре в течение 20-30 минут;
— после инъекции приложить пакет охлаждающий к месту инъекции на 2 — 3 минуты;
— не вводить препарат в имеющиеся уплотнения после предыдущих инъекций;
— в случае подозрения на воспалительные изменения в местах инъекций или некроз – срочно проконсультировать у врача-хирурга.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Данные рекомендации по мнению экспертов-членов рабочей группы позволят снизить риск развития НПР. Дополнительное предоставление наглядной информации в виде раздаточных материалов, буклетов или материалов в сети Интернет поможет повысить информированность пациентов, особенно при нарушениях памяти.
- Пациентам с РС (с 18 лет), получающим ПИТРС (интерферон бета-1a** или интерферон бета-1b**), с целью профилактики появления и контроля гриппоподобного синдрома рекомендуется [252]:
— при начале терапии — титровать дозу препарата согласно инструкции по медицинскому применению лекарственного препарата;
— выполнять инъекцию в вечернее время или на ночь, за исключением лекарственного препарата пэгинтерферон бета-1a**, инъекции которого желательно проводить в утренние или дневные часы;
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
- Пациентам с РС (с 12 лет), получающим ПИТРС (интерферон бета-1a** или интерферон бета-1b**), с целью профилактики появления и контроля гриппоподобного синдрома рекомендуется [284]:
— при старте терапии — начинать терапию с половины рекомендуемой дозы для взрослых, достигая полной дозы в течение 1 — 3 месяцев;
— выполнять инъекцию в вечернее время или на ночь;
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Данные рекомендации по мнению экспертов-членов рабочей группы позволят снизить риск развития НПР.
- У пациентов с РС, получающих терапию ПИТРС, с целью контроля функции печени рекомендуется определение уровня печеночных ферментов (определение активности аспартатаминотрансферазы в крови, определение активности аланинаминотрансферазы в крови, при необходимости – определение активности гамма-глютамилтрансферазы в крови и определение активности щелочной фосфатазы в крови), исследование уровня общего билирубина в крови и исследование уровня свободного и связанного билирубина в крови по окончании первого месяца терапии, затем с частотой не менее 1 раза в 3 месяца для пациентов с РС, получающих терапию интерферонами бета-1a**, пэгинтерфероном бета-1a** и интерфероном бета-1b**, глатирамера ацетатом**, диметилфумаратом**, кладрибином**, натализумабом** (для натализумаба** – перед каждым введением препарата), финголимодом**, терифлуномидом** (для терифлуномида** — первые 6 месяцев 1 раз в месяц). Пациентам, получающим терапию окрелизумабом**, рекомендуется контроль анализов каждые 6 месяцев. Пациентам, получающим терапию алемтузумабом**, рекомендуется контроль анализов каждый месяц в течение 4 лет терапии. [251,253]:
— рекомендуется временное приостановление приема препарата с консультацией врача-гастроэнтеролога и направлением в специализированный центр (кабинет) РС в случае, если: [251]
1) уровень АлАТ/АсАТ превышает 8 верхнюю границу нормы (ВГН);
2) уровень АлАТ/АсАТ превышает 5 ВГН на протяжении 2 недель (в 3
последовательных анализах);
3) уровень АлАТ/АсАТ превышает 3 ВГН в сочетании с повышением общего билирубина свыше 2 ВГН;
4) уровень АлАТ/АсАТ превышает 3 ВГН в сочетании с проявлениями тошноты, рвоты, боли и напряжения в правой подреберье, лихорадкой и/или эозинофилией (> 5%);
5) уровень общего билирубина изолированно превышает 2 ВГН в повторных анализах с промежутком 48 часов.
Для терифлуномида** необходимо приостановление приема препарата с консультацией врача-гастроэнтеролога и направлением в специализированный центр (кабинет) РС в случае, если уровень АЛТ/АСТ превышает 3 ВГН, подтвержденный через 2 недели;
— в случае подтверждения лекарственного гепатита на фоне терапии терифлуномидом** рекомендуется проведение ускоренного курса выведения препарата – #активированный уголь 50 г каждые 12 часов в течение 11 дней (при плохой переносимости ежедневный прием необязателен) [286], дальнейшая терапия – согласно клиническим рекомендация по терапии лекарственного гепатита;
— в случае выявления отклонений уровня АлАТ/АсАТ, превышающих 3 ВГН, но не достигающих критериев отмены, рекомендован еженедельный мониторинг до нормализации показателей, возможно снижение дозы препарата до ½ дозы.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Клиническими исследованиями не определена периодичность выполнения анализов крови и тактика действия в каждом конкретном случае приема терапии ПИТРС. Данные рекомендации по мнению экспертов — членов рабочей группы позволят снизить риск развития и выраженность НПР.
- У пациентов с РС, получающих терапию ПИТРС, с целью контроля функции кроветворения рекомендуется проведение развернутого клинического анализа крови (с подсчетом числа лимфоцитов, нейтрофилов) по окончании первого месяца терапии, затем с частотой не менее 1 раза в 3 месяца для пациентов с РС, получающих терапию интерферонами бета-1a**, пэгинтерферон бета-1a** и интерфероном бета-1b**, глатирамера ацетатом**, диметилфумаратом**, натализумабом** (для натализумаба** – перед каждым введением препарата), финголимодом**, терифлуномидом** [254] в связи с повышенным риском развития инфекционных осложнений [254,255]. Пациентам на терапии окрелизумабом** рекомендуется выполнение исследований каждые 6 месяцев, на терапии алемтузумабом** – каждый месяц в течение 4 лет после проведенной терапии. Пациентам на терапии кладрибином** рекомендуется проведение исследований через два и шесть месяцев после начала лечения на первом и втором годах терапии:
— Для оценки риска возникновения осложнений рекомендуется использовать общую шкалу токсичности (Приложение А3.8);
— В случае обнаружения 2 степени токсичности на фоне терапии интерферонами бета-1a**, пэгинтерфероном бета-1a** и интерфероном бета-1b** или глатирамера ацетатом** рекомендуется снизить дозировку препарата до ½ дозы с повторным анализом через 4 недели, либо мониторировать показатели с периодичность в 2 или 4 недели по решению врача-невролога; на фоне терапии диметилфумаратом** или финголимодом** рекомендуется повторить анализ через 4 недели;
— На фоне терапии интерферонами бета-1a**, пэгинтерфероном бета-1a** и интерфероном бета-1b**, глатирамера ацетатом**, терифлуномидом** в случае обнаружения 3 или 4 степени токсичности рекомендуется отменить препарат, повторить анализ крови в кратчайшие сроки и направить пациента в специализированный центр (кабинет) РС для решения вопроса о дальнейшей тактике;
— На фоне терапии диметилфумаратом** в случае обнаружения 3 или 4 степени токсичности по уровню лимфоцитов (уровень менее 0,5х109/л) либо при сохраняющемся уровне лимфоцитов ниже 0,8х109/л в течение 6 месяцев рекомендуется отменить препарат, повторить анализ крови в кратчайшие сроки и направить пациента в специализированный центр (кабинет) РС для решения вопроса о дальнейшей тактике;
— На фоне терапии финголимодом** в случае обнаружения 4 степени токсичности по уровню лимфоцитов (менее 0,2х109/л) или 3 степени токсичности по уровню тромбоцитов (менее 50х109/л) или 2 степени по уровню нейтрофилов (менее 1,0х109/л) рекомендуется временно отменить препарат, повторить анализ крови в кратчайшие сроки и направить пациента в специализированный центр (кабинет) РС для решения вопроса о дальнейшей тактике.
— На фоне терапии кладрибином** в случае обнаружения 3 токсичности по уровню лимфоцитов (менее 0,5х109/л) активный контроль должен проводиться до восстановления числа лимфоцитов. В случае выявления 4 степени токсичности по уровню лимфоцитов (менее 0,2х109/л), целесообразно рассмотреть вопрос о профилактическом назначении противогерпетической терапии на пока сохранения лимфопении 4 степени токсичности. При необходимости 2-й годовой курс лечения может быть отложен на срок до 6 месяцев до восстановления приемлемого числа лимфоцитов (более 0,8х109/л). В случае, если период восстановления числа лимфоцитов занимает более 6 месяцев, прием кладрибина** должен быть прекращен.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Клиническими исследованиями не определена периодичность выполнения анализов крови и тактика действия в каждом конкретном случае приема терапии ПИТРС. Данные рекомендации по мнению экспертов-членов рабочей группы позволят снизить риск развития и выраженность НПР.
- У пациентов с РС, получающих диметилфумарат**, с целью профилактики появления и контроля гастроинтестинальных НПР (тошнота, рвота, боли в животе), рекомендуется [91]:
— при начале терапии — титровать дозу препарата согласно инструкции по медицинскому применению лекарственного препарата;
— принимать препарат вместе с приемом пищи;
— консультация врача-гастроэнтеролога;
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
- У пациентов с РС, получающих финголимод**, с целью профилактики появления и контроля кардиальных НПР(брадикардия, блокады) рекомендуется проводить мониторинг приема первой дозы препарата в условиях специализированного центра (кабинета) РС [123,256]. Перед решением вопроса о назначение лекарственного препарата финголимод** пациент должен быть обязательно консультирован врачом-кардиологом с проведением холтеровского мониторирования сердечного ритма. При благоприятном решении:
— до приема препарата рекомендуется провести измерение артериального давления и пульса, регистрация электрокардиограммы на предмет наличия противопоказаний к приему первой дозы: 1) ЧСС в покое менее 55 ударов/мин); 2)
атриовентрикулярной блокады II и III степени (текущей или в анамнезе), 3) синоатриальной блокады; 4) синдрома слабости синусового узла; 5) удлинения QT (QTc > 470 мс у женщин, QTc > 450 мс у мужчин);
— после приема дозы препарата – каждый час в течение 6 часов необходимо провести измерение артериального давления и пульса; через 6 часов – регистрацию электрокардиограммы;
— пациенты могут быть отпущены домой, если соблюдаются все условия: 1) частота пульса выше минимального значения в ходе 6-часового наблюдения, 2) нет симптомов брадикардии (головокружение, усталость, ощущение сердцебиения и т.д.), 3) на ЭКГ нет удлинения QT ≥ 500 мс, 4) нет признаков впервые выявленной атриовентрикулярной блокады второй или более высокой степени, 5) прошло 6 часов от момента приёма первой дозы финголимода**;
— если ЧСС через 6 часов после приема финголимода** минимальна, то необходимо продлить мониторинг на 2 часа и более, до увеличения ЧСС;
— если у пациента ЧСС < 45, QTc > 500 мс, впервые возникшая АВ-блокада 2 степени или в любое время АВ-блокада 3 степени – продлить мониторинг до 24 часов;
— аналогичный мониторинг необходимо организовать в случае перерыва в приёме препарата свыше 7 дней.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий: Указанные рекомендации помогут предотвратить развитие клинически значимой брадикардии.
- У пациентов с РС, получающих натализумаб**, для профилактики появления оппортунистических инфекций (прогрессирующая мультифокальная энцефалопатия (ПМЛ)) рекомендуется проводить стратификацию пациентов по риску развития ПМЛ и действовать в соответствии с выбранным алгоритмом (Приложение А3.10) [257].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Несмотря на то, что большинство ПМЛ у пациентов с РС возникли на терапии натализумабом**, следует учитывать, что развитие данной оппортунистической инфекции возможно на фоне терапии финголимодом**, терифлуномидом**, диметилфумаратом**, алемтузумабом**, окрелизумабом** [258].
- У пациентов с РС, получающих терапию интерферонами бета-1a** и интерфероном бета-1b**, с целью установления причины субоптимального ответа на терапию ПИТРС рекомендуется исследование титра нейтрализующих антител (НАТ) к препаратам интерферона бета-1a** и интерферона бета-1b** в крови через 12 месяцев от начала терапии. У НАТ-негативных пациентов повторный анализ рекомендуется повторять не реже 1 раза в 12 месяцев. У пациентов со стойким низким титром НАТ рекомендуется исследование активности МхА-протеина, при отсутствии активности которого рекомендуется смена терапии на препарат с другим механизмом действия. У пациентов с высоким титром НАТ, сохраняющимся в повторных анализах, рекомендована смена терапии на препарат ПИТРС с другим механизмом действия [259].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: Определение клинической значимости выявления НАТ является сложным по нескольким причинам: многие исследования этой проблемы не имели достаточного количества участников, за которыми бы наблюдали в течение достаточно длительного времени; забор образцов для анализа проводился в разное время от начала терапии; не были определены единые референтные значения для низкого, среднего и высокого титра, особенно для разных видов интерферона бета [259–261]. Некоторые пациенты из НАТ-позитивных могут со временем стать НАТ-негативными [262]. Исследование Kappos и соавт. показывает, что определение НАТ в высоком титре через 1 год от начала терапии снижает эффективность терапии препаратами интерферона бета-1a** через 4 года [263]. Рекомендации Goodin c соавт. определяют консенсусные значения титров НАТ и тактику терапии в каждом конкретном случае [259].
- У пациентов, получающих окрелизумаб**, алемтузумаб**, с целью профилактики реактивации хронических инфекций рекомендуется определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови,определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови,определение антител к поверхностному антигену (HBsAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител классов к ядерному антигену (HBcAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител к вирусу гепатита C (Hepatitis C virus) в крови, определение антител к бледной трепонеме (Treponema pallidum) в нетрепонемных тестах (RPR, РМП) (качественное и полуколичественное исследование) в сыворотке крови и внутрикожной пробы с туберкулезным аллергеном перед каждым введением препарата [25,264–266].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Введение указанных ПИТРС может приводить к реактивации хронических инфекций, что отражено в инструкции по применению данных препаратов. С целью снижения риска терапии всем пациентам рекомендовано выполнение указанных исследований перед началом терапии.
- Пациентам с ремиттирующим РС, имеющим контакт с пациентами с подтвержденным COVID-19, которым планируется назначение ПИТРС, с целью снижения риска тяжелого течения COVID-19 рекомендуется терапия высокодозным интерфероном бета-1b** 250 мкг; высокодозным интерфероном бета-1а** 44 мкг; интерфероном бета-1а** 30 мкг; пэгинтерфероном бета-1a** 125 мкг; глатирамера ацетатом** 20 мг и 40 мг при соблюдении соотношения польза/риск от рекомендованной терапии [267–271].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Данные рекомендации, по мнению экспертов-членов рабочей группы, позволят снизить риск развития тяжелого течения коронавирусной инфекции SARS-CoV-2 в период эпидемических вспышек. Решение о начале рекомендованной терапии следует принимать совместно с пациентом при соблюдении соотношения польза/риск от рекомендованной терапии.
- Пациентам с быстропрогрессирующим РС, имеющим контакт с пациентами с подтвержденным COVID-19, которым планируется назначение ПИТРС, с целью снижения риска тяжелого течения COVID-19 рекомендуется терапия натализумабом** 300 мг внутривенно 1 раз в 28 дней [267–271].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Данная рекомендация, по мнению экспертов-членов рабочей группы, позволят снизить риск развития тяжелого течения коронавирусной инфекции SARS-CoV-2в период эпидемических вспышек у пациентов с быстропрогрессирующим РС, которым по жизненным показаниям рекомендована терапия ПИТРС второй линии.
- Пациентам с первично-прогрессирующим РС, имеющим контакт с пациентами с подтвержденным COVID-19, которым планируется назначение ПИТРС, с целью снижения риска тяжелого течения COVID-19 рекомендуется отложить терапию окрелизумабом** 600 мг внутривенно капельно на 1 месяц [267–271].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Данная рекомендация, по мнению экспертов-членов рабочей группы, позволят снизить риск развития тяжелого течения коронавирусной инфекции SARS-CoV-2 в период эпидемических вспышек у пациентов с ППРС.
- Пациентам с РС, имеющим контакт с пациентами с подтвержденным COVID-19 и получающим ПИТРС, с целью снижения риска тяжелого течения СOVID-19 рекомендуется в отношении определенных ПИТРС следующая тактика, с целью соблюдения соотношения польза/риск от проводимой терапии:
— натализумаб**: увеличить интервал между инфузиями до 6 недель после 6 месяцев терапии с интервалом 4 недели между инфузиями;
— окрелизумаб**: отложить планируемую инфузию на 1 месяц;
— алемтузумаб**: увеличить интервал между 1-м и 2-м лечебными циклами до 18 месяцев; при запланированном 3-м или 4-м лечебных курсах терапии проведение инфузии отложить до 6 месяцев;
— кладрибин**: отложить начало терапии на 1 месяц [267–271].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Данная рекомендация, по мнению экспертов — членов рабочей группы, позволят снизить риск развития тяжелого течения коронавирусной инфекции SARS-CoV-2 в период эпидемических вспышек.
- Пациентам с РС с подтвержденным COVID-19, получающим ПИТРС, с целью снижения риска тяжелого течения COVID-19 рекомендуется приостановить до реконвалесценции по вирусному заболеванию все ПИТРС, кроме интерферона бета-1b** 250 мкг; интерферона бета-1а** 44 мкг; интерферона бета-1а** 30 мкг; пэгинтерферона бета-1a** 125 мкг; глатирамера ацетата** 20 мг и 40 мг, при соблюдении соотношения польза/риск от проводимой терапии [267–271].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: Данная рекомендация, по мнению экспертов-членов рабочей группы, позволят снизить риск развития тяжелого течения коронавирусной инфекции SARS-CoV-2 в период эпидемических вспышек. Требуются дальнейшие исследования по влиянию терапии ПИТРС на течение коронавирусной инфекции SARS-CoV-2.
Информация
Источники и литература
-
Клинические рекомендации Всероссийского общества неврологов
- 1. Гусев ЕИ, Бойко А, Столяров И. Рассеянный Склероз. Москва: РеалТайм; 2009.
2. Ramagopalan S V., Dobson R, Meier UC, Giovannoni G. Multiple sclerosis: risk factors,
prodromes, and potential causal pathways. Lancet Neurol. 2010;9(7):727-739.
doi:10.1016/S1474-4422(10)70094-6
3. Loma I, Heyman R. Multiple Sclerosis: Pathogenesis and Treatment. Curr
Neuropharmacol. 2011;9(3):409-416. doi:10.2174/157015911796557911
4. Thompson AJ, Baneke P. Multiple Sclerosis International Federation (MSIF) Design and
Editorial Support by Summers Editorial & Design Graphics by Nutmeg Productions
Printed by Modern Colour Solutions.; 2013. www.msif.org. Accessed April 13, 2020.
5. Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017
revisions of the McDonald criteria. Lancet Neurol. 2018;17(2):162-173.
doi:10.1016/S1474-4422(17)30470-2
6. Gusev E, Boiko A, Bikova O, et al. The natural history of early onset multiple sclerosis:
Comparison of data from Moscow and Vancouver. In: Clinical Neurology and
Neurosurgery. Vol 104. Clin Neurol Neurosurg; 2002:203-207. doi:10.1016/S0303-
8467(02)00039-2
7. Simone IL, Carrara D, Tortorella C, et al. Course and prognosis in early-onset MS:
Comparison with adult-onset forms. Neurology. 2002;59(12):1922-1928.
doi:10.1212/01.WNL.0000036907.37650.8E
8. Etemadifar M, Afzali P, Tabrizi N, Hosseini S-A. Pediatric Multiple Sclerosis with
Primary Progressive Course—Report of a Retrospective Cohort Study in Iran.
Neuropediatrics. 2012;44(03):167-170. doi:10.1055/s-0032-1329614
9. Lublin FD, Reingold SC, Cohen JA, et al. Defining the clinical course of multiple
sclerosis: The 2013 revisions. Neurology. 2014;83(3):278-286.
doi:10.1212/WNL.0000000000000560
10. CHMP. Committee for Medicinal Products for Human Use (CHMP) Assessment Report.;
2014. www.ema.europa.eu. Accessed April 13, 2020.
11. Huisman E, Papadimitropoulou K, Jarrett J, et al. Systematic literature review and
network meta-analysis in highly active relapsing-remitting multiple sclerosis and rapidly
evolving severe multiple sclerosis. BMJ Open. 2017;7(3):e013430. doi:10.1136/bmjopen-
2016-013430
12. Van Der Vuurst De Vries RM, Mescheriakova JY, Wong YYM, et al. Application of the 2017 Revised McDonald Criteria for Multiple Sclerosis to Patients with a Typical
Clinically Isolated Syndrome. JAMA Neurol. 2018;75(11):1392-1398.
doi:10.1001/jamaneurol.2018.2160
13. Lee DH, Peschke M, Utz KS, Linker RA. Diagnostic value of the 2017 McDonald criteria
in patients with a first demyelinating event suggestive of relapsing–remitting multiple
sclerosis. Eur J Neurol. 2019;26(3):540-545. doi:10.1111/ene.13853
14. Miclea A, Salmen A, Wiest R, et al. Prediction of conversion to multiple sclerosis using
the 2017 McDonald and 2016 MAGNIMS criteria in patients with clinically isolated
syndrome: a retrospective single-centre study. Ther Adv Neurol Disord. 2019;12.
doi:10.1177/1756286419835652
15. Wong YYM, De Mol CL, Van Der Vuurst De Vries RM, et al. Real-world validation of
the 2017 McDonald criteria for pediatric MS. Neurol Neuroimmunol NeuroInflammation.
2019;6(2). doi:10.1212/NXI.0000000000000528
16. Fadda G, Brown RA, Longoni G, et al. MRI and laboratory features and the performance
of international criteria in the diagnosis of multiple sclerosis in children and adolescents: a
prospective cohort study. Lancet Child Adolesc Heal. 2018;2(3):191-204.
doi:10.1016/S2352-4642(18)30026-9
17. Krupp LB, Tardieu M, Amato MP, et al. International Pediatric Multiple Sclerosis Study
Group criteria for pediatric multiple sclerosis and immune-mediated central nervous
system demyelinating disorders: Revisions to the 2007 definitions. Mult Scler J.
2013;19(10):1261-1267. doi:10.1177/1352458513484547
18. Solomon AJ, Bourdette DN, Cross AH, et al. The contemporary spectrum of multiple
sclerosis misdiagnosis. Neurology. 2016;87(13):1393-1399.
doi:10.1212/WNL.0000000000003152
19. Yamout BI, Khoury SJ, Ayyoubi N, et al. Alternative diagnoses in patients referred to
specialized centers for suspected MS. Mult Scler Relat Disord. 2017;18:85-89.
doi:10.1016/j.msard.2017.09.016
20. Solomon AJ, Klein EP, Bourdette D. ‘Undiagnosing’ multiple sclerosis: The challenge of
misdiagnosis in MS. Neurology. 2012;78(24):1986-1991.
doi:10.1212/WNL.0b013e318259e1b2
21. Ghezzi A, Martinelli V, Torri V, et al. Long-term follow-up of isolated optic neuritis: The
risk of developing multiple sclerosis, its outcome, and the prognostic role of paraclinical
tests. J Neurol. 1999;246(9):770-775. doi:10.1007/s004150050453
22. Meyer-Moock S, Feng YS, Maeurer M, Dippel FW, Kohlmann T. Systematic literature
review and validity evaluation of the Expanded Disability Status Scale (EDSS) and the
Multiple Sclerosis Functional Composite (MSFC) in patients with multiple sclerosis. BMC
Neurol. 2014;14(1):58. doi:10.1186/1471-2377-14-58
23. Bin Sawad A, Seoane-Vazquez E, Rodriguez-Monguio R, Turkistani F. Evaluation of the
Expanded Disability Status Scale and the Multiple Sclerosis Functional Composite as
clinical endpoints in multiple sclerosis clinical trials: quantitative meta-analyses. Curr
Med Res Opin. 2016;32(12):1969-1974. doi:10.1080/03007995.2016.1222516
24. Perry M, Swain S, Kemmis-Betty S, et al. Multiple sclerosis: Summary of NICE
guidance. BMJ. 2014;349. doi:10.1136/bmj.g5701
25. Epstein D. J., Dunn J., Deresinski S. Infectious complications of multiple sclerosis
therapies: implications for screening, prophylaxis, and management //Open forum
infectious diseases. – US : Oxford University Press, 2018; 5 (8):ofy174.
26. Wei LK, Griffiths LR, Irene L, Kooi CW. Association of NOTCH3 gene polymorphisms
with ischemic stroke and its subtypes: A meta-analysis. Med. 2019;55(7).
doi:10.3390/medicina55070351
27. Senol MG, Sonmez G, Ozdag F, Saracoglu M. Reversible myelopathy with vitamin B12
deficiency. Singapore Med J. 2008;49(11):e330-2.
http://www.ncbi.nlm.nih.gov/pubmed/19037544. Accessed April 14, 2020.
28. Hammarin AL, Bogdanovic G, Svedhem V, Pirskanen R, Morfeldt L, Grandien M.
Analysis of PCR as a tool for detection of JC virus DNA in cerebrospinal fluid for
diagnosis of progressive multifocal leukoencephalopathy. J Clin Microbiol.
1996;34(12):2929-2932. doi:10.1128/jcm.34.12.2929-2932.1996
29. Giovannoni G, Marta M, Davis A, Turner B, Gnanapavan S, Schmierer K. Switching
patients at high risk of pml from natalizumab to another disease-modifying therapy. Pract
Neurol. 2016;16(5):389-393. doi:10.1136/practneurol-2015-001355
30. Ruiz-Gaviria R, Baracaldo I, Castañeda C, Ruiz-Patiño A, Acosta-Hernandez A, Rosselli
D. Specificity and sensitivity of aquaporin 4 antibody detection tests in patients with
neuromyelitis optica: A meta-analysis. Mult Scler Relat Disord. 2015;4(4):345-349.
doi:10.1016/j.msard.2015.06.003
31. Slater CA, Davis RB, Shmerling RH. Antinuclear antibody testing: A study of clinical
utility. Arch Intern Med. 1996;156(13):1421-1425. doi:10.1001/archinte.156.13.1421
- 1. Гусев ЕИ, Бойко А, Столяров И. Рассеянный Склероз. Москва: РеалТайм; 2009.
Информация
Список сокращений
АФС – антифосфолипидный синдром
ВАРС – высокоактивный рассеянный склероз
ВГН – верхняя граница нормы
ВИ – взвешенное изображение
ВПРС – вторично-прогрессирующий рассеянный склероз
ГК – глюкокортикоиды
ГГТ – гамма-глутамилтрансфераза
ИТП – иммунная тромбоцитопения
КВ – контрастное вещество
КИС – клинически изолированный синдром
МЗ – Министерство здравоохранения
МРТ – магнитно-резонансная томография
МЭС – медико-экономические стандарты
НДАЗ – нет данных за активность заболевания
НПР – нежелательная побочная реакция
ОНМ – оптиконейромиелит
ЗСОНМ – заболевания спектра оптиконейромиелита
ОРЭМ – острый рассеянный энцефаломиелит
ПИТРС – препараты, изменяющие течение рассеянного склероза
ППРС – первично-прогрессирующий рассеянный склероз
ПЦР – полимеразная цепная реакция
РИС – радиологически изолированный синдром
РКИ – рандомизированное клиническое исследование
РРС – ремиттирующий рассеянный склероз
РС – рассеянный склероз
СКВ – системная красная волчанка
СОЭ – скорость оседания эритроцитов
ТТГ – тиреотропный гормон
ЦНС – центральная нервная система
СМЖ – спинномозговая жидкость
EDSS – Расширенная шкала статуса инвалидизации пациента (РШСИ)
ФС – Функциональные системы (шкала функциональных систем Куртцке)
IgG – иммуноглобулин класса G
IgM– иммуноглобулин класса М
MSIF – Международная Федерация пациентов с рассеянным склерозом
** – жизненно необходимые и важнейшие лекарственные препараты
# – препарат, применяющийся не в соответствии с показаниями к применению и противопоказаниями, способами применения и дозами, содержащимися в инструкции по применению лекарственного препарата (офф-лейбл)
Термины и определения
Активность РС по данным МРТ – состояние, определяемое по данным МРТ, характеризующееся появлением новых и/или увеличением размера старых очагов на Т2-ВИ и/или наличием накапливающих парамагнитный контраст очагов на Т1-ВИ в головном и/или спинном мозге.
Диссеминация в пространстве – классический критерий РС, входящий в состав критериев МакДональда 2010 и 2017 года (Приложения А 3.2 и А 3.1), согласно которому пациент должен иметь клинические признаки поражения не менее двух различных участков центральной системы (ЦНС), либо соответствовать критериям диссеминации в пространстве по данным МРТ, либо комбинацию этих признаков
Диссеминация во времени – классический критерий РС, входящий в состав критериев МакДональда 2010 и 2017 года (Приложения А 3.2 и А 3.1), согласно которому пациент должен иметь не менее двух клинических обострений, либо соответствовать критериям диссеминации во времени по данным МРТ, либо комбинацию этих признаков.
Клинически изолированный синдром (КИС) – первый и единственный клинический эпизод нарушения неврологических функций, вызванный повреждением одного или нескольких отделов центральной нервной системы (ЦНС), длящийся свыше 24 часов, при этом имеющиеся данные клиники и МРТ-картины не удовлетворяют критериям диагностики РС (критерии Мак Дональда 2010 и 2017).
Оптимальный ответ на терапию (нет данных за активность заболевания, НДАЗ) – отсутствие обострений, отсутствие прогрессирования неврологического дефицита в течение периода наблюдения, отсутствие активности по данным МРТ.
Острый демиелинизирующий эпизод – остро возникшая симптоматика, клинически подозрительная на проявления РС или другое демиелинизирующее заболевание.
ПИТРС первой линии – ПИТРС, назначаемые в качестве препаратов первого выбора при РС.
ПИТРС второй линии – ПИТРС, назначаемые в качестве препаратов последующего выбора в случае неэффективности или непереносимости препаратов первой линии, либо в случае наличия быстропрогрессирующего течения РС в качестве препаратов первого выбора. При оценке безопасности терапии требуется проведение дополнительных специальных анализов и консультаций иных специалистов, кроме врача-невролога.
Резистентность к терапии – это клинико-радиологические характеристики течения РС, возникающие на фоне проводимой терапии, на основании которых необходимо принятие решения об эскалации терапии (Приложение А 3.7).
Субоптимальный ответ на терапию – это клинико-радиологические характеристики течения РС и лабораторные показатели на фоне проводимой терапии, на основании которых необходимо принятие решения о смене терапии на препарат с иным механизмом действия в рамках той же линии ПИТРС (Приложение А 3.7).
Критерии оценки качества медицинской помощи
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Все члены рабочей группы заявили об отсутствии финансовой или нематериальной заинтересованности по теме разработанной клинической рекомендации. Член(ы)рабочей группы, сообщившие об обстоятельствах, которые могут повлечь за собой конфликт интересов, был(и) исключен(ы) из обсуждения разделов, связанных с областью конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
1. Главные врачи (начальники) медицинских организаций
2. Заместители руководителя (начальника) медицинских организаций
3. Заведующие (начальники) структурных подразделений
4. Главные медицинские сестры
5. Врачи-специалисты:
— Врачи-неврологи, код специальности 31.08.42
— Врачи-рентгенологи, код специальности 31.08.09
— Врачи-клинические фармакологи, код специальности 31.08.37
— Врачи по лечебной физкультуре и спортивной медицине, код специальности 31.08.39
— Врачи по физической и реабилитационной медицине
— Врачи скорой медицинской помощи, код специальности 31.08.48
— Врачи-терапевты, код специальности 31.08.49
— Врачи-физиотерапевты, код специальности 31.08.50
— Врачи общей врачебной практики, код специальности 31.08.54
— Врачи-офтальмологи, код специальности 31.08.59
— Врачи-урологи, код специальности 31.08.68
— Врачи-организаторы здравоохранения и общественного здоровья, код специальности 31.08.71
6. Медицинские сестры:
— медицинская сестра врача общей практики
— медицинская сестра палатная (постовая)
— медицинская сестра (фельдшер) по приему вызовов скорой медицинской помощи и передаче их выездным бригадам скорой медицинской помощи
— медицинская сестра процедурная
— медицинская сестра по реабилитации
— медицинская сестра участковая
— медицинский регистратор
— медицинский статистик
— рентген-лаборант
— старшая медицинская сестра
— фельдшер
— фельдшер скорой медицинской помощи
7. Заведующие аптечными организациями
8. Провизоры
9. Фармацевты
10. Студенты медицинских вузов, ординаторы, аспиранты;
11. Преподаватели медицинских вузов, научные сотрудники.
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме (таб. П1, таб. П2).
Таблица П1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Таблица П2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
Таблица П3. Шкала оценки уровней убедительности рекомендаций
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.(УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
1) Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 N 323-ФЗ
2) Федеральный закон от 12 апреля 2010 г. N 61-ФЗ «Об обращении лекарственных средств»
3) Федеральный закон «О внесении изменений в статью 40 Федерального закона «Об обязательном медицинском страховании в Российской Федерации» и Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» по вопросам клинических рекомендаций» от 25.12.2018 N 489-ФЗ (последняя редакция)
4) Порядок оказания медицинской помощи взрослому населению при заболеваниях нервной системы (приказ Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. N 926н).
5) Стандарт специализированной медицинской помощи при первом клиническом проявлении рассеянного склероза (клинически изолированном синдроме) Приложение к Приказу Министерства здравоохранения РФ от 20 декабря 2012 г. № 1085н
6) Стандарт первичной медико-санитарной помощи при остром оптиконевромиелите (диагностика) Приложение к Приказу Министерства здравоохранения РФ от 24 декабря 2012 г. № 1533н
7) Стандарт первичной медико-санитарной помощи при рассеянном склерозе в стадии ремиссии Приложение к Приказу Министерства здравоохранения РФ от 24 декабря 2012 г. № 1542н
Федеральный закон от 29.07.2017 N 242-ФЗ «О внесении изменений в отдельные законодательные акты Российской Федерации по вопросам применения информационных технологий в сфере охраны здоровья»
Приложение А 3.1. Критерии диагностики РС МакДональда, модификация 2017 года
При типичной картине РС необходимо пользоваться критериями МакДональда в модификации 2017 года [5].
Диссеминация в пространстве:
— Клиническая – признаки наличия двух и более клинических очагов поражения,
— По данным МРТ — наличие 1 или более Т2-гиперинтенсивных очагов в двух или более областях ЦНС:
1) перивентрикулярно,
2) кортикально и/или юкстакортикально,
3) инфратенториально,
4) в спинном мозге.
Диссеминация во времени:
— Клиническая – очередное обострение с вовлечением нового участка ЦНС, клинические проявления обострения должны продолжаться не менее 24 часов, интервал между клиническими атаками должен быть не менее 1 месяца,
— По данным МРТ:
1) одновременное выявление очагов, накапливающих и ненакапливающих контраст на МРТ, выполненной в любое время от начала заболевания; очаги могут быть как симптомными, так и бессимптомными. При соблюдении других критериев, диагноз РС может быть подтвержден без повторной МРТ;
2) появление новых Т2-гиперинтенсивных или накапливающих контраст очагов на повторной МРТ; при этом интервал между первым и вторым МРТ- исследованиями может быть любым.
В реальной клинической практике рассматривается несколько диагностических вариантов:
— Наличие 2 и более клинических обострений И объективно обнаруживаемые повреждения 2 и более функциональных систем («симптомные» очаги) – дополнительных данных для подтверждения РС не требуется
— Наличие 2 и более клинических обострений И объективно обнаруживаемое повреждение 1 функциональной системы («симптомный» очаг), при этом по данным медицинской документации в анамнезе имеются доказательства наличия еще одного «симптомного» очага другой локализации – дополнительных данных для подтверждения РС не требуется
— Наличие 2 и более клинических обострений И объективно обнаруживаемое повреждение 1 функциональной системы («симптомный» очаг) – требуется доказательство диссеминации в пространстве (новое обострение с другой локализацией очага или диссеминация в пространстве по данным МРТ)
— Наличие 1 клинического обострения И объективно обнаруживаемые повреждения 2 и более функциональных систем («симптомные» очаги) – требуется доказательство диссеминации во времени (новое обострение или данные МРТ или наличие олигоклональных иммуноглобулинов в ЦСЖ)
— Наличие 1 клинического обострения И объективно обнаруживаемое повреждение 1 функциональной системы («симптомный» очаг) – требуется доказательство диссеминации в пространстве и во времени (новое обострение с другой локализацией очага или диссеминация в пространстве по данным МРТ)
Критерии диагностики РС (модификация 2017 года) для пациентов с первично-прогрессирующим течением:
— прогрессирование в течение 1 года, подтвержденное ретроспективно или проспективно, несвязанное с возникновением обострений,
И наличие двух признаков из перечисленных:
— наличие 1 или более Т2-гиперинтенсивных очагов в двух или более областях ЦНС: перивентрикулярно, кортикально и/или юкстакортикально, инфратенториально;
— два или более Т2-гиперинтенсивных очага в спинном мозге;
— наличие олигоклональных иммуноглобулинов в СМЖ.
Приложение А 3.2. Критерии диагностики РС МакДональда, модификация 2010 года
При атипичной клинической картине установление диагноза РС возможно в соответствии с критериями 2010 года [279]:
Диссеминация в пространстве:
— Клиническая – признаки наличия двух и более клинических очагов поражения,
— По данным МРТ выявление >1 Т2-гиперинтенсивного очага в двух из четырех областей, типично поражающихся при РС (контрастного усиления не требуется):
а) перивентрикулярной,
б) юкстакортикальной (вблизи коры головного мозга),
в) инфратенториальной,
г) в спинном мозге (в случае наличия симптомов поражения ствола мозга или спинного мозга, очаги, соответствующие клинической картине, не учитываются).
Диссеминация во времени:
— Клиническая – очередное обострение с вовлечением нового участка ЦНС, клинические проявления обострения должны продолжаться не менее 24 часов, интервал между клиническими атаками должен быть не менее 1 месяца,
— По данным МРТ один из следующих критериев:
а) одновременное выявление бессимптомных очагов, накапливающих и ненакапливающих контраст на МРТ, выполненной в любое время от начала заболевания; в этом случае, при соблюдении других критериев, диагноз РС может быть подтвержден без повторной МРТ;
б) появление новых Т2-гиперинтенсивных и/или накапливающих контраст очагов на повторной МРТ; при этом интервал между первым и вторым МРТ-исследованием может быть любым.
В реальной клинической практике рассматривается несколько диагностических вариантов:
— Наличие 2 и более клинических обострений И объективно обнаруживаемые повреждения 2 и более функциональных систем (2 и более клинических очага) или объективное клиническое подтверждение поражения 1 функциональной системы (1 клинического очага) с анамнестическими объективными доказательствами наличия повреждения еще 1 функциональной системы по данным медицинской документации – при отсутствии объективных данных других неврологических заболеваний дополнительных данных для подтверждения диагноза РС не требуется;
— Наличие 2 и более клинических обострений И объективно обнаруживаемое повреждение 1 функциональной системы (1 клинический очаг) – необходимо доказательство диссеминации в пространстве по данным МРТ либо появление нового клинического обострения с поражением иной функциональной системы;
— Наличие 1 клинического обострения И объективно обнаруживаемые повреждения 2 и более функциональных систем (2 и более клинических очага) – необходимо доказательство диссеминации во времени по данным МРТ либо появление нового клинического обострения;
— Наличие 1 клинического обострения И объективно обнаруживаемое повреждение 1 функциональной системы (1 клинический очаг) – необходимо доказательство диссеминации во времени и в пространстве по данным МРТ либо появление нового клинического обострения с поражением иной функциональной системы;
— Наличие неуклонного прогрессирования, предполагающее РС либо установление диагноза первично-прогрессирующего РС И объективно обнаруживаемые повреждение 1 функциональной системы (1 клинический очаг) – необходимо доказательство диссеминации во времени — неуклонное прогрессирование в течение 1 года и более (+1 балл EDSS за 6 месяцев) и диссеминации в пространстве (2 критерия из 3-х):
- при проведении МРТ головного мозга 1 Т2-очага в не менее, чем одном участке ЦНС, типичном для РС (перивентрикулярно, юкстакортикально, инфратенториально)
- при проведении МРТ спинного мозга 2 Т2-очагов в спинном мозге
- положительный анализ ликвора (олигоклональные группы IgG или повышенный индекс IgG, или оба параметра).
Приложение А 3.3. Дифференциальная диагностика РС
Диагноз РС ставится методом исключения при отсутствии других (лучших) объяснений симптоматики, при этом дифференциальная диагностика проводится с несколькими основными группами заболеваний:
1. Системные воспалительные заболевания с аутоиммунными механизмами
развития:
— Клиническая дифференциальная диагностика основывается на исключении системности поражения:
- Ретинопатия с явлениями васкулита (васкулит).
- Увеит (СКВ, болезнь Бехчета).
- Рецидивирующие язвы слизистых (болезнь Бехчета, СКВ).
- Сухой синдром – сухой кератоконъюктивит (Болезнь Шегрена).
- Вовлечение почек (СКВ, васкулиты).
- Артриты, полиартралгии, миалгии (СКВ).
- Антифосфолипидный синдром (АФС) – диффузное заболевание соединительной ткани, характеризующееся поражением сосудов микроциркуляторного русла вследствие формирования аутоиммунных антител к фосфолипидам мембран клеток, которые включают в себя волчаночный антикоагулянт, антитела к кардиолипину IgG и/или IgM и антитела к бета-2-гликопротеину 1 IgG и/или IgM.
- Сетчатое ливедо (АФС).
- Привычное невынашивание беременности (АФС).
— Параклинические методы исключения ревматических заболеваний.
- Общеклинические – воспалительные изменения в анализах крови (лейкоцитоз, повышение скорости оседания эритроцитов (СОЭ), появление С-реактивного белка), анемия.
- Серологические – поиск диагностически значимых титров антител к фосфолипидам мембран клеток, эндотелию, нейтрофилам, нативной ДНК, париетальным клеткам желудка, слюнной железе, а также циркулирующих иммунных комплексов.
- Нейровизуализационные – множественные мелкие очаги (до 5 мм), наличие ишемических очагов и кист, очаги в сером веществе.
— Основные заболевания, требующие дифференциальной диагностики с РС:
- Первичные системные васкулиты – группа заболеваний, в основе которых лежит различное генерализованное аутоиммунное поражение сосудов с воспалением и некрозом сосудистой стенки, что приводит к ишемическим изменениям органов и тканей, в том числе и мозга, а также повреждение циркулирующими иммунными комплексами, антителами к эндотелию, антителами к цитоплазме нейтрофилов.
- Ревматические заболевания с вторичным васкулитом: синдром Шегрена – хроническое аутоиммунное заболевание; которое характеризуется лимфоцитарной инфильтрацией экзокринных желез, приводящей к развитию ксеростомии и ксерофтальмии, сухости слизистых оболочек носа, гортани, трахеи, бронхов, женских половых органов, атрофическому гастриту; болезнь Бехчета – системный васкулит неустановленной этиологии, характеризующийся преимущественным язвенным поражением слизистой оболочки глаз, полости рта, кожи, половых органов и нервной системы; системная красная волчанка (СКВ) – диффузное заболевание соединительной ткани, характеризующееся системным иммунокомплексным поражением соединительной ткани и её производных, с поражением сосудов микроциркуляторного русла вследствие формирования аутоиммунных антител к ДНК.
- Саркоидоз – мультисистемное гранулематозное заболевание неизвестной этиологии, при этом субстратом являются гранулемы в различных органах и тканях, состоящие из эпителиоидных и гигантских клеток, а также макрофагов, приводящие к периваскулиту или лептоменингиту.
- Изолированные васкулиты ЦНС — Th1-опосредованное гранулематозное воспаление артерий и вен мелкого и среднего калибра, особенно мягких мозговых оболочек и субкортикальных областей, в качестве подтверждения используются данные ангиографии.
2. Инфекционные заболевания (с развитием аутоиммунного компонента):
— Клиническая дифференциальная диагностика основывается на поиске признаков инфекционного процесса:
- данные эпидемиологического анамнеза,
- общесоматический статус (лихорадка, системность поражения),
- неврологический статус (общемозговой синдром, вовлеченность периферической нервной системы, признаки страдания серого вещества, ранний когнитивный дефицит).
— Параклинические методы исключения нейроинфекций:
- Серологические – поиск диагностически значимых титров антител IgM к предполагаемому инфекционному агенту, (в ряде случаев – нарастание титров IgG при динамическом исследовании), при необходимости – уточнение с помощью полимеразной цепной реакции (ПЦР).
- Ликворологические – плеоцитоз, наличие в ликворе антител к предполагаемому инфекционному агенту и/или его обнаружение с помощью ПЦР.
- Нейровизуализационные – очаги различных размеров и локализации в белом веществе полушарий (в том числе субкортикально и перивентрикулярно), очаги в сером веществе, реже — мозжечке, таламусе, базальных ядрах. У большинства – сочетанное поражение нескольких областей головного мозга, очаги накапливают контраст.
— Основные заболевания, требующие дифференциальной диагностики с РС:
- Спирохетозные энцефалиты и энцефаломиелиты (нейроборрелиоз, нейросифилис).
- Иммунодефицитарные энцефалиты и энцефаломиелиты – ретровирусные (ВИЧ-энцефалопатия), паповавирусные (прогрессирующая мультифокальная лейкодистрофия).
- Флавивирусные энцефалиты и энцефаломиелиты (японский комариный, клещевой, Сент-Луис, Западного Нила).
- Герпесвирусные энцефалиты и энцефаломиелиты (простого герпеса, цитомегаловирусный, Эпштейн — Барр).
- Экзантемные энцефалиты и энцефаломиелиты – герпесвирусные (ветряночный); тогавирусные (краснушечный); парамиксовирусные (коревой).
- Нейробруцеллез.
- Тропический спинальный парапарез (HTLV-1-миелопатия).
- Болезнь Уиппла.
3. Сосудистые заболевания с поражением ЦНС:
— Основные заболевания, требующие дифференциальной диагностики с РС.
- Болезнь Бинсвангера (субкортикальная артериосклеротическая энцефалопатия).
- Мигрень.
- Семейная кавернозная гемангиома.
- Синдром Сусака (ретинокохлеоцеребральная аутоиммунная васкулопатия).
4. Наследственные заболевания с поражением ЦНС:
— Основные заболевания, требующие дифференциальной диагностики с РС.
- Адренолейкодистрофия.
- Метахроматическая лейкодистрофия.
- Спиноцеребеллярные атаксии.
- Семейная спастическая параплегия (Штрюмпеля).
- Наследственная атрофия зрительного нерва (Лебера).
- Митохондриальная энцефалопатия (CADASIL, MELAS и пр.).
5. Дисметаболические и токсические заболевания:
— Основные заболевания, требующие дифференциальной диагностики с РС.
- Острая интермиттирующая порфирия.
- Центральный понтинный миелинолиз.
- Фуникулярный миелоз (дефицит витамина В12 – цианкобаламина – и/или В9 – фолиевой кислоты).
- Целиакия (глютеновая недостаточность).
- Токсическая энцефалопатия (в том числе пострадиационная)
6. Метастатические опухоли спинного и головного мозга.
7. Другие формы воспалительных демиелинизирующих заболеваний:
— Острый рассеянный энцефаломиелит (ОРЭМ) [17]:
- впервые развившийся эпизод мультифокального поражения ЦНС предположительно воспалительного демиелинизирующего характера,
- острая энцефалопатия (изменение сознания или поведения, несвязанные с лихорадкой, соматическим заболеванием, постиктальным периодом эпилептического припадка),
- при МРТ-исследовании в течение трех месяцев от начала эпизода выявляются следующие типичные изменения: 1) остро возникшие, 2) множественные (реже возможен один большой очаг), 3) супра- или/и инфратенториальные; 4) обычно имеется хотя бы один большой очаг (1-2 см в диаметре); 5) в очагах имеется накопление контраста (в острый период все очаги накапливают контраст, при более позднем проведении МРТ часть очагов могут уже не накапливать контраст, но это не является подтверждением диссеминации во времени).
- в течение трех месяцев или более после начала эпизода отсутствуют новые клинические или МРТ очаги
- в течение трех месяцев от начала заболевания допускается появление новых симптомов, моно- или мультифокальных, например, оптического неврита, миелита, при условии, что они не отделены периодом полной ремиссии от начальных симптомов (в случае полной ремиссии устанавливается диагноз РС)
- имеется последующее уменьшение или полное восстановление, хотя возможно сохранение резидуального неврологического дефицита.
— ЗСОНМ с наличием антител к аквапорину-4 [280]:
- наличие хотя бы одного основного клинического синдрома: 1) оптический неврит, 2) острый миелит, 3) синдром area postrema (синдром самого заднего поля): эпизод необъяснимой икоты или тошноты и рвоты, 4) остро возникший стволовой синдром, 5) клинически значимая нарколепсия или острый гипоталамический синдром с наличием на МРТ головного мозга очагов в гипоталамической области, типичных для ЗСОНМ, 6) клинически значимый церебральный синдром с наличием очагов в головном мозге, типичных для ЗСОНМ.
- положительный результат исследования сыворотки крови на иммуноглобулины класса G к аквапорину-4 наиболее чувствительным методом (рекомендуется исследование методами с клеточной презентацией антигена, cell-based assay),
- исключение альтернативных заболеваний.
— ЗСОНМ – заболевания спектра оптиконейромиелита без антител к аквапорину-4 или при невозможности определения антител [280]:
- наличие хотя бы двух основных клинических синдромов, появившихся во время одного или более клинических обострений и соответствующих следующим условиям: а) хотя бы один основной клинический синдром – это оптический неврит, острый миелит с продольно-распространенным поперечным миелитом (LETM, longiudinally extensive transverse myelitis) или синдром area postrema, б) диссеминация в пространстве (два или более различных основных клинических синдрома),
- наличие дополнительных МРТ-признаков при остром оптическом неврите: а) отсутствие изменений или неспецифические очаги в белом веществе ИЛИ б) очаг в зрительном нерве гиперинтенсивный на Т2 взвешенном изображении (ВИ) или накапливающий контрастное вещество на Т1-ВИ, распространяется на более чем половину длины зрительного нерва или вовлекает хиазму.
- наличие дополнительных МРТ-признаков при остром миелите: а) интрамедуллярный очаг, длина которого больше или равна длине трех позвоночных сегментов (longiudinally extensive transverse myelitis, продольно-распространенный поперечный миелит) ИЛИ б) наличие участка атрофии спинного мозга, длина которого больше или равна длине трех сегментов спинного мозга, у пациентов с наличием в анамнезе острого миелита соответствующей локализации.
- наличие дополнительных МРТ-признаков при синдроме area postrema: наличие очагов в дорзальной части продолговатого мозга, очагов в области area postrema.
- наличие дополнительных МРТ-признаков при остром стволовом синдроме: наличие периэпендимальных очагов в стволе.
Приложение А 3.4. Дополнения MAGNIMS по применению МРТ при установлении диагноза РС по критериям МакДональда 2010 года
Данные дополнения сформулированы рабочей группой экспертов в 2016 году [54].
Диссеминация в пространстве устанавливается при наличии двух признаков из пяти:
— три или более перивентрикулярных очага
— один или более инфратенториальный очаг
— один или более спинальный очаг
— один очаг или более с локализацией в зрительном нерве
— один очаг или более с кортикальной или юкстакортикальной локализацией (это означает расширение термина «юкстакортикальный» – очаг в белом веществе вблизи коры, очаг с вовлечением коры)
Комментарий: При определении диссеминации в пространстве считаются все очаги, в том числе вызывающие клинические симптомы. Например, если у пациента имеются клинические симптомы поражения ствола, спинного мозга или зрительного нерва, очаги в этих областях нервной системы учитываются (в отличие от предыдущей редакции критериев). Критерии диссеминации во времени остаются без изменений (см. Критерии 2010 года).
Приложение А 3.5. Форма структурированного протокола заключения МРТ
С целью оценки динамики очаговых изменений при оформлении заключения МРТ головного мозга у пациентов при подозрении на РС и у всех пациентов с РС. В полях «Результат» и «Предыдущий результат» рекомендуется указывать точное количество очагов демиелинизации. Форма носит рекомендательный характер, является структурной частью заключения и не заменяет описательной части или репортирования других находок на МРТ.
* Если общее количество очагов превышает более 20 и не поддается подсчету, указывать – более 20 (>20).
** Если пациент выполняет МРТ исследование впервые, то поля Предыдущего результата остаются пустыми.
Приложение А 3.6. Принципы формулировки клинического диагноза
Формулировку клинического диагноза рекомендуется выполнять с учетом МКБ-10 и действующих классификаций заболевания по типу течения, стадии заболевания и выраженности функциональных нарушений [281]:
1) Название болезни – Рассеянный склероз, Код МКБ-10 G 35.0.
2) Течение – ремиттирующее, вторично-прогрессирующее, первично-прогрессирующее.
3) Стадия:
а) при ремиттирующем – ремиссия, обострение, при осмотре пациента в течение одного месяца от начала обострения можно указать дату начала обострения, основные неврологические синдромы в порядке убывания их функциональной значимости с указанием их выраженности (выраженный/глубокий, умеренный, легкий).
б) при вторично-прогрессирующем – прогрессирование, стабилизация, обострение, при осмотре пациента в течение одного месяца от начала обострения можно указать дату начала обострения, основные неврологические синдромы в порядке убывания их функциональной значимости с указанием их выраженности (выраженный/глубокий, умеренный, легкий).
в) при первично-прогрессирующем – прогрессирование, стабилизация, обострение, при осмотре пациента в течение одного месяца от начала обострения можно указать дату начала обострения, основные неврологические синдромы в порядке убывания их функциональной значимости с указанием их выраженности (выраженный/глубокий, умеренный, легкий).
4) оценка по шкале EDSS.
Примеры формулировки клинического диагноза:
— Рассеянный склероз, ремиттирующее течение, стадия обострения (от 01.08.2016), умеренный парез правой ноги, умеренная мозжечковая атаксия. EDSS 4,5.
— Рассеянный склероз, ремиттирующее течение, стадия ремиссии, легкая мозжечковая атаксия. EDSS 2,0.
— Рассеянный склероз, вторично-прогрессирующее течение, стадия стабилизации, умеренный нижний парапарез, умеренная мозжечковая атаксия, легкие проводниковые чувствительные нарушения. EDSS 6,0.
При формулировке диагноза важно указывать функциональные нарушения (в соответствии с данными действующего законодательства (на момент написания рекомендаций — Приказа Министерства труда и социальной защиты РФ от 17 декабря 2015 №1024н «О классификационных критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной защиты»):
— Незначительные нарушения моторики, незначительные нарушения функций тазовых органов; по шкале EDSS в пределах 1 — 2,5 баллов — степень выраженности – 10-30%;
— Умеренные парезы верхних и/или нижних конечностей, умеренные нарушения функций тазовых органов; по шкале EDSS в пределах 3 — 4,5 баллов — степень выраженности – 40 — 60%;
— Выраженные парезы верхних и/или нижних конечностей, выраженные нарушения функций тазовых органов; по шкале EDSS в пределах 5 — 7 баллов — степень выраженности – 70 — 80%;
— Значительно выраженные парезы или параличи верхних и/или нижних конечностей, значительно выраженные нарушения функций тазовых органов (полное недержание мочи и/или кала с полной нечистоплотностью); по шкале EDSS в пределах 7,5 — 9,5 баллов — степень выраженности – 90 — 100%.
Приложение А 3.7. Принципы замены ПИТРС
Ниже представлены рекомендации для определения действий врача в зависимости от ответа на терапию [105 — 114].
Все критерии применимы на продолжительность периода измерения 12 месяцев с момента, когда начал действовать ПИТРС. С последующими годовыми интервалами.
Попадание одного критерия в первые 12 месяцев, а второго критерия во вторые 12 месяцев измерения должны расцениваться как не состоявшиеся.
Данные критерии применимы только к пациентам с РРС (не проводились исследования шкал для пациентов с ППРС и ВПРС).
Характеристики активности по данным МРТ – новый очаг в режиме Т2-ВИ или увеличившийся очаг в режиме Т2-ВИ или очаг, накапливающий контрастный препарат в режиме Т1-ВИ. Новый очаг, накапливающий контрастное вещество, считается как один очаг.
* Вариабельность ситуаций, которые могут попадать под данную категорию очень большая, поэтому лечащий врач принимает решение исходя из конкретной клинической ситуации.
Приложение А 3.8. Общая шкала токсичности
Изменение показателей белой и красной крови является наиболее частым побочным эффектом терапии ПИТРС и оценивается по Общей шкале токсичности
Действия при выявлении токсичности:
• Степень 1 – терапию продолжать
• Степень 2 – терапию продолжать (мониторировать показатели с периодичностью от 2 недель до 1 месяца по решению врача-невролога)
• Степень 3 – отмена терапии до восстановления показателей и направление на комиссию по назначению ПИТРС
• Степень 4 – отмена терапии до восстановления показателей и направление на комиссию по назначению ПИТРС.
Детально рекомендации по наблюдению за пациентами на терапии препаратами первой и второй линии, включая частоту и характер мониторируемых показателей (показатели белой и красной крови, биохимические показатели и др.), а также действия при выявлении токсичности при терапии отдельными ПИТРС, представлены в Приложении Б, разделе 3.3., а также в разделах 3.1.17.3 и 3.1.17.4, посвященных консервативному лечению.
Приложение А 3.9. Форма заявления об отмене ПИТРС
ФОРМА ЗАЯВЛЕНИЯ ОБ ОТМЕНЕ ПИТРС
(оригинал в амбулаторной карте, копия в материалах комиссии)
В региональный центр (кабинет) РС
от гр._____________________________________,
проживающего(ей) по адресу:___________________
_____________________________________
ЗАЯВЛЕНИЕ
Прошу отменить препарат________________________, принимаемый мной по
Федеральной (или региональной) льготе с__________________, по поводу заболевания
рассеянный склероз в связи с (причина)__________________________________________
Я информирован(а) врачами о последствиях прекращения приема препарата. Я
задал все интересующие вопросы и получил на них ответы.
Данное решение принято мной добровольно и осознанно, претензий к органам
здравоохранения и врачам не имею.
Дата Подпись:
______________________
Приложение А 3.10. План управления рисками ПМЛ при терапии натализумабом**
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) — редкая, прогрессирующая, потенциально фатальная инфекция головного мозга, вызывается JC вирусом. Поражаются пациенты со сниженным иммунитетом: пациенты со СПИДом до назначения высокоактивной антиретровирусной терапии (ВААРТ) 1 — 8%, пациенты, перенесшие трансплантацию органов (редко, << 1%), пациенты со злокачественными опухолями кроветворной системы; пациенты, получавшие противоопухолевую или иммуносупрессивную терапию; редкие случаи ПМЛ ассоциированы с применением натализумаба**.
Диагностика ПМЛ: Клиническая картина: неврологический дефицит нарастает в течение нескольких недель. Клиника: изменения личности, поведения, когнитивных функций, афазия, миоклонические судороги, гемипарезы и гемиплегии, корковые нарушения зрения, в конечной стадии — деменция, кома и гибель пациента – необходимо дифференцировать с обострениями и прогрессированием при РС. Течение вариабельно, летальный исход без лечения наступает в течение 6 — 12 месяцев.
МРТ-признаки: крупные гиперинтенсивные очаги на T2-взвешенных или FLAIR изображениях, чаще монофокальные, располагаются в субкортикальном БВ, чаще поражаются U-волокна, типичные очаги не формируют масс-эффекта или отека – дифференцировать с очагами при РС. В 40 — 50% случаев в очагах присутствуют признаки контрастного усиления.
Анализ СМЖ — исследование ДНК JC вируса с помощью ПЦР в реальном времени (примерно у половины пациентов число копий ДНК JCV было небольшим < 500 копий/мл).
При наличии клинической картины ПМЛ рекомендуется немедленная отмена препарата.
Риск ПМЛ при использовании натализумаба**.
Факторы риска развития ПМЛ:
1) присутствие вируса JC (серопозитивность);
2) наличие иммуносупрессии (ИС) в анамнезе;
3) длительность терапии.
К пациентам высокого риска ПМЛ относятся:
— Пациенты с тремя факторами риска ПМЛ:
o Иммуносупрессия (ИС) в анамнезе;
o Длительность терапии натализумабом**> 2 лет;
o Серопозитивный статус;
— Пациенты, получающие натализумаб** более 2 лет и имеющие титр выше 1,5.
Стратификация риска развития ПМЛ и рекомендации по ведению пациента представлены на рисунках Г12.1 и Г12.2
Рисунок А 3.10.1 Обновленная стратификация риска развития ПМЛ
Рисунок А 3.10.2 Рекомендации по ведению пациентов на натализумабе** с учетом рисков ПМЛ
Клиническое обследование пациента с подозрением на ПМЛ включает несколько этапов (рисунок А 3.10.2).
Рисунок А 3.10.3. Клиническое обследование при развитии новых или усугублении имеющихся симптомов, либо при появлении изменений на МРТ, предположительно указывающих на ПМЛ у пациентов, получающих натализумаб**
Приложение А 3.11. Критерии Международной группы по изучению детского рассеянного склероза, 2013 г.
У пациентов младше 18 лет рекомендуется использовать указанные критерии в случаях, определенных соответствующими рекомендациями [16].
Детский рассеянный склероз (любой из следующих):
• Два или более клинических эпизода, разделенные более чем 30 днями, признаки повреждения более чем в одной функциональной сфере центральной нервной системы;
• Одно из клинических событий ассоциировано с изменениями по МРТ, соответствующих критериям ДВП и последующее МРТ показывает, по крайней мере, одно новое поражение в соответствие с критерием ДВВ;
• Через 3 месяца после первых проявлений ОРЭМ-подобной атаки возникает новое клиническое событие, которое связано с новым очагом по МРТ в соответствии с критериями ДВП;
• Клинический изолированный синдром при котором данные МРТ согласуются с критериями ДВП и ДВВ.
Детский клинически изолированный синдром (КИС) (все обязательно):
• Клиническое событие поражения ЦНС с предполагаемой причиной — воспалительная демиелинизация;
• Отсутствие в анамнезе предшествующего демиелинизирующего заболевания ЦНС;
• Нет данных за энцефалопатию (за исключением случаев, когда можно объяснить лихорадкой);
• Нет соответствия критериям ДВП и ДВВ на базовой МРТ.
Детский острый рассеянный энцефаломиелит (ОРЭМ) (все обязательные):
• Первое полифокальное клиническое событие поражения ЦНС с предполагаемой причиной — воспалительная демиелинизация.
• Энцефалопатия, которая не может быть объяснена повышением температуры тела.
• Нет новых клинических или МРТ событий 3 или более месяцев после первых симптомов;
МРТ головного мозга и патологическими изменениями во время острой фазы (3 месяца) с типичными диффузными плохо разграниченными крупными очагами располагающиеся преимущественно в белом веществе головного мозга.
Приложение А 3.12. Критерии оценки тяжести обострений
Представленная классификация адаптирована из Freedman и соавт. [66] и рекомендована к оценке тяжести обострений для принятия решения о тактике ведения пациентов.
Приложение Б. Алгоритмы действий врача
1. Алгоритм диагностики рассеянного склероза
1.1. Алгоритм установления диагноза РС
1.2. Алгоритм постановки диагноз РС, первично-прогрессирующий тип течения
2. Алгоритм ведения пациента с обострением РС
3. Алгоритм: Принципы замены ПИТРС [105–114]
4. Планы наблюдения за пациентами на терапии ПИТРС
4.1. Рекомендации по наблюдению за пациентами на терапии интерферонами бета-1a** и интерферонами бета-1b**
4.2. Рекомендации по наблюдению за пациентами на терапии глатирамера ацетатом**
4.3. Рекомендации по наблюдению за пациентами на терапии терифлуномидом**
4.4. Рекомендации по наблюдению за пациентами на терапии диметилфумаратом**
4.5. Рекомендации по наблюдению за пациентами на терапии #митоксантроном**
4.6. Рекомендации по наблюдению за пациентами на терапии натализумабом**
4.7. Рекомендации по наблюдению за пациентами на терапии финголимодом**
4.8. Рекомендации по наблюдению за пациентами на терапии алемтузумабом**
4.9. Рекомендации по наблюдению за пациентами на терапии окрелизумабом**
4.10. Рекомендации по наблюдению за пациентами на терапии кладрибином**.
Приложение В. Информация для пациента
1. Информация для пациента на этапе диагностики:
1.1. Информация о природе неврологического дефицита при демиелинизирующих заболеваниях, а также о возможных проявлениях РС;
1.2. Информация об этиологии РС, факторах риска развития РС;
1.3. Информация о риске передачи РС по наследству;
1.4. Информация о неблагоприятных прогностических факторах, повышающих риск конверсии в РС после первого обострения и факторах более быстрой инвалидизации
1.5. Информацию о профилактике коморбидности и здоровом образе жизни, мотивация отказа от вредных привычек;
1.6. Информация о работе локального центра/кабинета РС;
1.7. Информация о возможности получить психологическую поддержку, группах поддержки для пациентов, сообществах пациентов, информационных школах для пациентов по вопросам лечения;
2. Информация для пациента на этапе лечения и диспансерного наблюдения:
2.1. Информация о возможностях терапии РС с помощью ПИТРС, зарегистрированных на территории Российской Федерации и подходящих для лечения конкретного пациента в соответствии с его типом течения РС (представляется индивидуально для каждого пациента);
2.2. Информация о профиле эффективности и безопасности ПИТРС, выбранного для терапии, а также об альтернативных ПИТРС, профиль их эффективности и безопасности;
2.3. Рекомендации по наблюдению в рамках плана управления рисками: кратность визитов, сдачи лабораторных анализов, выполнения МРТ, вакцинации и других профилактических и лечебно-диагностических мероприятий;
2.4. Информация о возможности получения медицинской и социальной реабилитации;
2.5. Информация о возможности получения инвалидности;
2.6. В случае необходимости смены терапии – предоставить информацию о критериях смены терапии, возможности смены терапии, профиле безопасности и эффективности предложенных для смены ПИТРС;
3. На этапе медицинской реабилитации:
3.1. Предоставить информацию о целях реабилитации;
3.2. Предоставить информацию о природе ограничений повседневной жизнедеятельности пациента;
3.3. Индивидуальная программа реабилитации для выполнения в домашних условиях;
3.4. Информация о необходимости использования технических средств реабилитации и возможности их получения.
Приложение Г1 — ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Шкала повреждения функциональных систем (ФС) по J.F.Kurtzke
Название на русском: Шкала повреждения функциональных систем (ФС) по J.F.Kurtzke
Оригинальное название: Kurtzke Functional Systems Scores
Источник (официальный сайт разработчиков, публикация с валидацией): Kurtzke JF. Rating neurologic impairment in multiple sclerosis: An expanded disability status scale (EDSS). Neurology. 1983;33(11):1444-1452. doi:10.1212/wnl.33.11.1444
Тип: шкала оценки
Назначение: оценка типа и тяжести неврологического дефицита ц пациентов с рассеянным склерозом.
Содержание (шаблон):
1. Поражение зрительного нерва (необходимы данные осмотра офтальмолога):
0 баллов – нет изменений.
1 балл:
бледность диска ЗН;
«маленькая» скотома (о ней пациент не знает = отрицательная);
острота зрения (с коррекцией) худшего глаза меньше 1,0, но лучше, чем
0,67.
2 балла:
худший глаз с «большой» скотомой (пациент жалуется на наличие скотомы);
острота зрения (с коррекцией) худшего глаза 0,67 — 0,34.
3 балла (для расчета EDSS конвертируется в 2 балла):
худший глаз с «большой» скотомой;
умеренное сужение полей зрения (= пациент замечает сужение полей
зрения, но гемианопсия неполная);
острота зрения худшего глаза (с коррекцией) 0,33 — 0,2.
4 балла (для расчета EDSS конвертируется в 3 балла):
худший глаз с выраженным сужением полей зрения (= полная гомонимная гемианопсия);
острота зрения худшего глаза (с коррекцией) 0,2 — 0,1;
изменения, соответствующие 3 баллам, но острота зрения лучшего глаза 0,3 и меньше.
5 баллов (для расчета EDSS конвертируется в 3 балла):
острота зрения худшего глаза (с коррекцией) меньше 0,1;
изменения, соответствующие 4 баллам, но острота зрения лучшего глаза 0,3 и меньше.
6 баллов (для расчета EDSS конвертируется в 4 балла):
изменения, соответствующие 5 баллам, но острота зрения лучшего глаза 0,3 и меньше.
2. Нарушение функции других черепных нервов (функция глазодвигателей, жевательная и мимическая мускулатура лица, бульбарная группа нервов):
0 баллов – нет изменений.
1 балл — симптомы без нарушений функций:
легкие нарушения, выявляемые при неврологическом осмотре, у пациента жалоб нет;
нистагм в крайних отведениях;
симптомы нарушения функции со стороны тройничного, лицевого нервов.
2 балла – легкие нарушения – у пациента есть жалобы на нарушение функции, есть изменения легкой степени выраженности (в некоторых случаях умеренной степени) при неврологическом осмотре:
умеренно выраженный нистагм (=постоянный нистагм при отведении глаз по горизонтали или вертикали на 30 градусов, отсутствие нистагма при взгляде прямо);
легкое нарушение движений глаз, пациент жалуется на двоение;
парез какой-либо одной наружной мышцы глаза, у пациента жалоб нет;
снижение чувствительности на лице, пациент жалуется на онемение;
пациент жалуется на асимметрию лица, она заметна при осмотре;
пациент жалуется на нечеткость речи, дизартрия заметна при беседе;
трудности при проглатывании жидкости.
3 балла – умеренные нарушения:
выраженный нистагм:
— постоянный нистагм при взгляде прямо;
— крупноразмашистый нистагм в любом направлении, снижающий остроту зрения;
— полная межъядерная офтальмоплегия с постоянным нистагмом при отведении глаза;
— осциллопсия (ощущение покачивания перед глазами окружающего пространства).
умеренное нарушение движений глаз:
— парез какой-либо одной наружной мышцы глаза, у пациента есть жалобы на двоение;
— паралич взора в одном направлении;
— снижена поверхностная чувствительность на лице с одной стороны;
— тригеминальная невралгия (хотя бы один приступ за последние 24 часа).
парез половины лица (слабость круговой мышцы глаза, на ночь требуется повязка на глаз; слабость круговой мышцы рта со слюнотечением);
снижение слуха (не слышит несколько слов при проверке различения шепотной речи);
дизартрия заметна при беседе, речь пациента трудно понять;
трудности при глотании жидкой и твердой пищи.
4 балла – выраженные нарушения:
паралич взора в одном или более направлениях;
полная потеря чувствительности на лице с одной или обеих сторон;
паралич мышц лица с одной или обеих сторон (есть лагофтальм, вытекание жидкой пищи изо рта);
не слышит шепотную речь;
речь пациента неразборчива из-за дизартрии;
постоянные трудности при глотании, может глотать только кашицеобразную пищу.
5 баллов — невозможность глотать или говорить.
3. Симптомы поражения пирамидного пути:
0 баллов – нет изменений.
1 балл — патологические пирамидные рефлексы без снижения силы.
2 балла – легкие нарушения:
пациент жалуется на утомляемость;
нарушение выполнения функциональных проб (проба Барре для рук и для ног, 10 прыжков на одной ноге);
снижение силы до 4 баллов в одной-двух мышечных группах.
3 балла:
легкий или умеренный пара- или гемипарез:
cнижение силы до 4 баллов в трех мышечных группах и более
cнижение силы в одной-двух группах до 3 баллов
глубокий монопарез (снижение силы в одной группе мышц до 2 баллов)
4 балла:
глубокий пара- или гемипарез (снижение силы до 2 баллов в двух конечностях);
умеренный тетрапарез (снижение силы до 3 баллов в трех или четырех конечностях);
моноплегия (снижение силы до 0 — 1 баллов в одной конечности).
5 баллов:
параплегия;
гемиплегия;
глубокий тетрапарез (сила 2 балла и меньше в трех или четырех конечностях).
6 баллов:
тетраплегия (сила 0 — 1 балл в руках и ногах).
4. Симптомы нарушения координаторной сферы (дополнительно отмечается, если у пациента есть снижение силы до 3 баллов, влияющее на выполнение координаторных проб):
0 баллов – нет изменений.
1 балл — неврологические симптомы без нарушения функции.
2 балла – легкая атаксия:
пошатывание в позе Ромберга и в положении сидя при закрытых глазах;
тремор и неловкость заметны, немного затрудняют движения;
ходьба по одной линии затруднена.
3 балла — умеренная атаксия:
неустойчив в позе Ромберга при закрытых глазах;
покачивание сидя при открытых глазах;
тремор и неловкость значительно затрудняют движения;
атаксия при обычной ходьбе;
требуется поддержка при ходьбе.
4 балла – выраженная атаксия:
не может сидеть без поддержки;
выполнение координаторных проб затруднено в трех-четырех конечностях;
неустойчив в позе Ромберга при открытых глазах.
5 баллов — координированные движения невозможны из-за атаксии.
5. Симптомы нарушения чувствительности:
0 баллов – нет изменений.
1 балл – легкие нарушения — в одной или двух конечностях следующие изменения;
вибрационная чувствительность – ощущает вибрацию больше 10 секунд, но хуже, чем врач (снижение до 5/8 – 7/8 по градуированному камертону);
снижение температурной чувствительности;
снижение двумерно-пространственного чувства;
легкое снижение мышечно-суставного чувства (1 — 2 неверных ответа при проверке в дистальных суставах).
2 балла –
в одной или двух конечностях отмечаются следующие изменения:
легкое нарушение поверхностной чувствительности (пациент ощущает снижение чувствительности, но различает «острое-тупое»);
умеренное нарушение вибрационной (ощущает вибрацию 2 — 10 секунд; 1/8 — 4/8 по градуированному камертону);
в трех-четырех конечностях отмечаются следующие изменения:
легкое снижение вибрационной или двумерно-пространственного чувства, или температурной чувствительности.
3 балла –
в одной или двух конечностях отмечаются следующие изменения:
— плохо различает «острое-тупое»;
— много неверных ответов при проверке мышечно-суставного чувства, есть нарушения в проксимальных суставах;
— потеря вибрационной чувствительности.
в трех-четырех конечностях отмечаются следующие изменения:
— легкое нарушение поверхностной чувствительности (пациент ощущает снижение чувствительности, но различает «острое-тупое»);
— много неверных ответов при проверке мышечно-суставного чувства, есть нарушения в проксимальных суставах;
— умеренное нарушение вибрационной (ощущает вибрацию 2 — 10 секунд; 1/8 — 4/8 по градуированному камертону).
4 балла –
в одной-двух конечностях отмечаются следующие изменения:
— не различает «острое-тупое»;
— потеря мышечно-суставного чувства.
в трех-четырех конечностях отмечаются следующие изменения:
— плохо различает «острое-тупое»;
— потеря мышечно-суставного чувства.
5 баллов –
в одной-двух конечностях утрата всех видов чувствительности;
в трех-четырех конечностях:
— плохо различает «острое-тупое»;
— потеря мышечно-суставного чувства.
6 баллов — утрата всех видов чувствительности во всех конечностях и на туловище.
6. Симптомы нарушения функций тазовых органов:
0 баллов – нет изменений.
1 балл — незначительные нарушения мочеиспускания: императивные позывы, задержки мочеиспускания, запоры, не влияющие на повседневный распорядок жизни.
2 балла –
умеренно выраженные задержки;
частые инфекции мочевых путей;
частые императивные позывы;
эпизоды недержания не более 1 раза в неделю, необходимы прокладки.
3 балла –
частые эпизоды недержания мочи (от нескольких раз в неделю до одного и более в день);
пользуется памперсами или мочеприемником;
иногда требуется самокатетеризация;
для опорожнения кишечника требуется клизма.
4 балла — необходимость в постоянной катетеризации и постоянных дополнительных мероприятий для опорожнения кишечника (для расчета EDSS конвертируется в 3)
5 баллов – потеря контроля за функцией мочевого пузыря или кишечника, требуется постоянный катетер (для расчета EDSS конвертируется в 4).
6 баллов — полное недержание мочи и кала (для расчета EDSS конвертируется в 5).
0 баллов – нет изменений.
1 балл –
изменения настроения (только депрессия или только эйфория, не влияет на EDSS):
легкая утомляемость (не влияет на работоспособность) (учитывается при подсчете EDSS);
минимальное снижение когнитивных функций (незаметны для пациента и окружающих, выявляются только при тестах) (учитывается при подсчете EDSS).
2 – легкое снижение когнитивных функций:
пациент или окружающие замечают наличие расстройств;
снижение скорости принятия решений;
легкие ошибки при решении сложных задач;
справляется с повседневными делами, но возникают трудности в стрессовых ситуациях;
снижение производительности;
небрежность в делах, объясняемая усталостью или забывчивостью;
умеренная утомляемость (снижает повседневную активность не более чем на 50%);
выраженная утомляемость (снижает повседневную активность более чем на 50%).
3 — умеренное снижение когнитивных функций:
ориентирован в месте, времени, собственной личности, имеются явные нарушения при скрининговом тестировании.
4 – выраженное снижение когнитивных функций:
потеря ориентации по одному или двум параметрам (место, время, собственная личность);
снижение повседневной активности.
5 – деменция.
Приложение Г2. Расширенная шкала статуса инвалидизации пациента (EDSS)
Название на русском: Расширенная шкала статуса инвалидизации пациента (EDSS)
Оригинальное название: An expanded disability status scale (EDSS)
Источник (официальный сайт разработчиков, публикация с валидацией): Kurtzke JF. Rating neurologic impairment in multiple sclerosis: An expanded disability status scale (EDSS). Neurology. 1983;33(11):1444-1452. doi:10.1212/wnl.33.11.1444
Тип: шкала оценки
Назначение: оценка типа и тяжести неврологического дефицита ц пациентов с рассеянным склерозом.
Приложение Г3. Шкала баланса Берг
Название на русском: Шкала баланса Берг
Оригинальное название: Berg Balance Scale (BBS)
Источник (официальный сайт разработчиков, публикация с валидацией): Berg K, Wood-Dauphine S, Williams J, Gayton D. Measuring balance in the elderly: preliminary development of an instrument. Physiother Can 1989;41(6):304–11.
Тип: шкала оценки
Назначение: оценка способностей человека к статическому и динамическому равновесию
Если у больного выраженный когнитивный дефицит или речевые нарушения, препятствующие пониманию команд, следует использовать альтернативные источники коммуникации.
Если пациент находится без сознания, то он получает 0 баллов. Если у пациента ампутирована одна нога, то тест выполняется с протезом отсутствующей части. В случае если протез отсутствует — тест не проводится.
1. Задание: встать со стула
Инструкция: попросите пациента встать со стула. Если при исполнении пациент держится за подлокотники, попросите повторить задание, не используя руки. Следите за тем, чтобы ноги не упирались в край стула. Используйте стул с подлокотниками.
Оценка:
4 – встает самостоятельно без помощи рук и самостоятельно удерживает равновесие;
3 – встает самостоятельно с первой попытки, использует руки, самостоятельно удерживает равновесие;
2 – встает самостоятельно при помощи рук, требуется несколько попыток, чтобы встать;
1 – требуется минимальная помощь для того, чтобы встать со стула или принять устойчивое положение стоя;
0 – для того, чтобы встать требуется помощь (умеренная или значительная).
2. Задание: стоять без поддержки
Инструкция: попросите пациента самостоятельно стоять в течение 2х минут.
Пациент не должен касаться ногами стула (отодвиньте стул от пациента). Следите за пациентом, будьте готовы, если он будет терять равновесие.
Оценка:
4 – уверенно стоит в течение 2 мин;
3 – стоит в течение 2 мин с вашим контролем (без мануального контакта с пациентом, вы стоите ближе, чем этого требует выполнение задания на 4 балла);
2 – стоит без поддержки 30 сек;
1 – требуется несколько попыток для того, чтобы стоять в течение 30 сек;
0 – не может стоять 30 сек без поддержки.
Если пациент стоит уверенно 2 минуты, отметьте высший балл для пункта 3 (выполнять проверку не нужно). Приступайте к пункту 4.
3. Задание: сидеть на стуле, ноги на полу, руки скрещены на груди
Инструкция: сидеть без опоры на спину, руки скрещены на груди, ноги стоят на полу, в коленях 90°, стопы на комфортном расстоянии для пациента в течение 2-х мин. Используйте стул без подлокотников и секундомер.
Оценка:
4 – уверенно сидит в течение 2 мин;
3 – сидит в течение 2 мин с контролем со стороны (без мануального контакта с пациентом, вы стоите ближе, чем этого требует выполнение задания на 4 балла, также для 2 и 1 баллов);
2 – сидит 30 сек под контролем со стороны;
1 – сидит 10 сек под контролем со стороны;
0 – не может сидеть 10 сек без поддержки.
4. Задание: перейти из положения стоя в положение сидя
Инструкция: попросить пациента сесть на стул, не используя руки. Тщательно наблюдайте за контактом ног и стула. Отодвиньте стул на 5 — 8 см от стены, чтобы контакт был очевиден (например, стул сдвинется). Используйте стул с подлокотниками.
Оценка:
4 – уверенно садиться, минимально использует руки;
3 – контролирует посадку при помощи рук;
2– для контроля посадки опирается задней поверхностью ног на стул;
1 – садится самостоятельно, но посадка не контролируется (плюхается на стул) ;
0 – для посадки требуется помощь.
5. Задание: пересесть со стула с подлокотниками на стул без подлокотников и обратно
Инструкция: перемещаться от стула с подлокотниками к стулу без подлокотников и обратно. Поставьте стулья под углом 90°, расстояние между стульями до 10 см. Инструкция дается перед выполнением задания, можно продемонстрировать. Помощь рук означает, что пациент переносит вес на руки. Используйте стул с подлокотниками и стул без подлокотников.
Оценка:
4 – уверенное перемещение с минимальным использованием рук;
3 – уверенное перемещение с некоторым использованием рук (использует руки при вставании и при посадке);
2 – требуются устные подсказки и/или контроль со стороны;
1 – требуется помощь одного человека;
0 – требуется помощь/контроль двумя людьми.
6. Задание: стоять без поддержки с закрытыми глазами
Инструкция: закрыть глаза и стоять неподвижно в течение 10 сек. Ноги на ширине плеч, руки по бокам. Используйте секундомер.
Оценка:
4 – уверенно стоит в течение 10 сек;
3 – уверенно стоит в течение 10 сек при наблюдении (без мануального контакта с пациентом, вы стоите ближе, чем этого требует выполнение задания на 4 балла);
2 – стоит в течение 3 сек;
1 – не может держать глаза закрытыми в течение 3 сек, но стоит уверенно;
0 – нужна поддержка для того, чтобы избежать падения.
7. Задание: стоять без поддержки, ноги вместе
Инструкция: попросите пациента поставить ноги вместе (пятки и носки соприкасаются) и стоять 1 мин. Используйте секундомер.
Оценка:
4 – ноги вместе, может независимо стоять в течение 1 мин;
3 – ноги вместе, может независимо стоять в течение 1 мин при наблюдении (без мануального контакта с пациентом, вы стоите ближе, чем этого требует выполнение задания на 4 балла);
2 – может поставить ноги вместе, но не может продержаться 30 сек;
1 – нужна помощь для принятия позиции (соединить ноги), но может стоять в течение 15 сек. (0) нужна помощь для принятия позиции (соединить ноги), не может стоять в течение 15 сек.
Если пациент не в состоянии сдвинуть ноги вместе по причинам, не связанным с равновесием (т.е. из-за ожирения или Х-образной формы ног), и не снимайте баллы. В таких случаях отметьте положение ног в качестве контрольного для проведения оценивания в будущем.
8. Задание: наклониться вперед с вытянутыми руками
Инструкция: попросите пациента поднять руку на 90°, распрямить/вытянуть пальцы вперед насколько возможно, ноги на ширине плеч, стопы параллельно. Экзаменатор помещает линейку у кончиков пальцев пациента, не касаясь линейкой пальцев пациента. Далее попросите пациента наклониться вперед с вытянутой рукой вдоль линейки, насколько это возможно, не перемещая ноги. Оценивается расстояние, на которое перемещаются пальцы при максимальном наклоне вперед. По достижении максимального наклона, пациент должен вернуться в исходное положение. Если для малейшего наклона требуется контроль со стороны — это 3 балла. Для выполнения задания потребуется линейка.
Оценка:
4 – уверенно наклоняется вперед на 25 см;
3 – наклоняется вперед от 24 см до 12 см;
2 – наклоняется вперед от 11 см до 5 см;
1 – наклоняется вперед, но нужно наблюдение (без мануального контакта с пациентом, вы стоите ближе, чем этого требует выполнение задания на 4 балла);
0 – нужна поддержка для того, чтобы избежать падения (теряет равновесие).
9. Задание: поднять предмет с пола
Инструкция: попросите пациента поднять с пола ботинок, который следует положить перед пациентом по средней линии. Отведите пациента от стула, чтобы он не упирался в него ягодицами. Пациент может ставить ноги в любом удобном для него положении.
Оценка:
4 – легко и уверенно поднимает тапочек;
3 – поднимает тапочек, но нужно наблюдение;
2 – не может поднять, но самостоятельно наклоняется на 2-4 см от ботинка, удерживает равновесие;
1 – не может поднять, требуется помощь при попытке выполнить задание;
0 – не получается поднять и нужна поддержка для того, чтобы избежать падения
Если пациент не может выполнить задание из-за избыточного веса, предложите пациенту «присесть» и выполнить задание (в этом случае оценивать выполнение задания следует по предложенным баллам). Если не получается «присесть», задание пропускается. В обоих случаях необходимо сделать пометку о том, как было выполнено или почему было не выполнено задание, для возможности оценке в динамике.
10. Задание: обернуться и посмотреть через левое и правое плечо
Инструкция: попросите пациента обернуться и посмотреть через левое плечо и вернуться в исходное положение. Затем после небольшой паузы повторить через поворот правое плечо. Перемещать ноги нельзя. Стойте напротив пациента, чтобы наблюдать за симметрией поворота головы и шеи и переносом веса тела. Поворот влево или вправо подразумевает поворот приблизительно на 90°. Можно попросить пациента визуально определить какие –то объекты сзади них, чтобы отметить полный разворот.
Оценка:
4 – смотрит по обе стороны, вес тела переносит хорошо;
3 – смотрит только через одно плечо, на другой стороне вес тела переносит хуже;
2 – поворачивается только в сторону, но удерживает равновесие;
1 – при повороте требуется контроль со стороны;
0 – нужна поддержка для того, чтобы избежать падения.
11. Задание: обернуться на 360°
Инструкция: попросите пациента обернуться вокруг себя, затем остановиться и обернуться полный круг в другую сторону. Продемонстрируйте пациенту, как следует выполнять задание. Засекайте время каждого поворота отдельно. Повторите попытку, если пациент прикоснулся к стулу. Площадь поверхности пола, которая требуется пациенту для совершения разворота, не имеет значения.
Оценка:
4 – может обернуться в обе стороны на 360°, менее чем за 4 сек;
3 – может обернуться в одну сторону на 360°, менее чем за 4 сек;
2 – может обернуться на 360°, но медленно;
1 – требуется наблюдение или устные подсказки;
0 – в процессе поворота требуется помощь.
12. Задание: попеременные шаги на подставку
Инструкция: попросите пациента поочередно ступать на подставку, по 4 шага каждой ногой. Поставьте ступеньку перед пациентом, высота ступеньки. Продемонстрируйте пациенту, как следует выполнять задание. Если для выполнения задания потребовалась посторонняя помощь, выберите оценку не более 2 баллов.
Оценка:
4 – стоит без поддержки и уверенно, может выполнить 8 шагов за 20 сек;
3 – стоит без поддержки, может выполнить 8 шагов больше, чем за 20 сек;
2 – совершает 4 шага без помощи под наблюдением;
1 – может выполнить меньше шагов (2-3), нужна минимальная помощь ;
0 – нужна поддержка для того, чтобы избежать падения/ не в состоянии совершить попытку.
13. Задание: устоять в положении «стопы друг перед другом на одной линии»
Инструкция: попросите пациента поставить одну ногу прямо перед второй (пятка одной ноги касается носка другой ноги). Если не получается поставить стопы четко одну перед другой, то возможны варианты расположения стоп относительно друг друга.
Оценка:
4 – получается поставить одну ногу прямо перед второй (пятка одной ноги касается носка другой ноги) и держать равновесие в течение 30 сек;
3 – получается, поставить одну ногу перед второй на расстоянии и держать равновесие в течение 30 сек;
2 – делает небольшой шаг вперед, удерживает равновесие 30 сек;
1 – нужна помощь чтобы сделать шаг вперед, но удерживает равновесие 15 сек;
0 – теряет равновесие при положении стоя или при шаге вперед/не в состоянии совершить попытку.
В случае если не получились поставить одну ногу прямо перед второй (пятка одной ноги касается носка другой ноги) и задание выполнялось в другой позиции стоп, не забудьте отметить и учесть при выполнении повторного тестирования.
14. Задание: стоять на одной ноге
Инструкция: попросите пациента постоять на одной ноге столько, сколько он/она может, не пользуясь посторонней помощью. Ногу необходимо поднимать на заметную высоту, следите за тем, чтобы ноги пациента не касались друг друга. Если потребовалась посторонняя помощь, выберите оценку не более 1 балла. На какой ноге стоять пациент выбирает сам.
Оценка:
4 – может поднять ногу и держаться > 10 сек;
3 – может поднять ногу и держаться 5 — 10 сек;
2 – может поднять ногу и держаться 3 сек;
1 – попытка поднять ногу, но не может держать равновесие в течение 3 секунд, но стоит независимо;
0 – нужна поддержка для того, чтобы избежать падения.
— Если пациент выполнил два пункта подряд на оценку ноль, то дальше тестирование не продолжается.
— Когда пациент получает 4 балла за выполненное задание, экзаменатор должен находиться недалеко, но не настолько близко, чтобы пациент чувствовал поддержку от присутствия экзаменатора рядом. Если Вы стоите очень близко к пациенту, то это оценка не более 3-х баллов.
— Если Вы не уверены, как правильно оценить выполнение задания, например пациент, выполнил задание вроде на 3 балла, но с погрешностями, ставьте балл 2. То есть, если есть сомнения, всегда выбирайте меньший балл.
— Любое задание может быть продемонстрировано вами пациенту, перед его выполнением — Если пациент перемещается с дополнительными средствами опоры (ходунки, трость), то задания из шкалы следует выполнять без дополнительной опоры.
Ключ (интерпретация): менее 43 баллов из 56 – высокий риск падения.
Приложение Г4. Тест функциональной независимости (FIM)
Название на русском: Тест функциональной независимости (FIM)
Оригинальное название: Functional Independence Measure (FIM)
Источник (официальный сайт разработчиков, публикация с валидацией): Kidd D, Stewart G, Baldry J et al. The Functional Independence Measure: A comparative validity and reliability study. Disabil Rehabil. 1995;17(1):10-14. doi:10.3109/09638289509166622
Тип: шкала оценки
Назначение: оценка функциональной независимости пациента.
Оценка проводится специалистом, наблюдающим пациента постоянно или несколькими специалистами и медсестрами. Шкала заполняется по результатам совокупных наблюдений за пациентом в течение 2 — 4 дней. Специалисты, проводящие оценку, могут заполнить шкалу в процессе наблюдений поочередно или в процессе консилиума. Шкала функциональной независимости FIM включает 18 пунктов, при этом пункты 1 — 13 отражают состояние двигательных функций, а пункты 14 — 18 — состояние интеллектуальных функций.
Семибалльная градация оценки:
7 – полная независимость в выполнении соответствующей функции (все действия выполняются самостоятельно, в общепринятой манере и с разумными затратами времени);
6 – ограниченная независимость (больной выполняет все действия самостоятельно, но медленнее, чем обычно, либо нуждается в постороннем совете);
5 – минимальная зависимость (при выполнении действий требуется наблюдение персонала, либо помощь при надевании протеза/ортеза);
4 – незначительная зависимость (при выполнении действий нуждается в посторонней помощи, однако более 75% задания выполняет самостоятельно);
3 – умеренная зависимость (самостоятельно выполняет 50 — 75 % необходимых для исполнения задания действий);
2 – значительная зависимость (самостоятельно выполняет 25 — 50% действий)
1 — полная зависимость от окружающих (самостоятельно может выполнить менее 25% необходимых действий).
Ключ (интерпретация): каждая из указанных функций оценивается по семибальной шкале. Таким образом, суммарная оценка по шкале FIM может составлять от 18 до 126 баллов: чем ниже суммарная оценка FIM, тем в большей степени пациент зависим от окружающих в повседневной жизни.
Приложение Г5. Тест 9 колышков и отверстий
Название на русском: Тест 9 колышков и отверстий
Оригинальное название: The Nine-Hole Peg Test
Источник (официальный сайт разработчиков, публикация с валидацией): Feys P, Lamers I, Francis G et al. The Nine-Hole Peg Test as a manual dexterity performance measure for multiple sclerosis. Multiple Sclerosis Journal. 2017;23(5):711-720. doi:10.1177/1352458517690824
Тип: шкала оценки
Назначение: оценка моторики рук.
Пациент сидит за столом. Контейнер с отверстиями располагается на столе перед пациентом таким образом, чтобы углубление в контейнере для сбора колышков находилось с той же стороны, что и проверяемая рука. Исследование всегда начинается с доминирующей руки. Пациент должен вставить колышки в отверстия и вынуть их по одному одной рукой. Регистрируется время от начала перемещения первого колышка в одно из 9 отверстий и до складывания последнего колышка в углубление контейнера. Затем нужно повторить все действия другой рукой. Время выполнения теста каждой рукой фиксируется с помощью секундомера.
Если во время выполнения задания колышек падает на стол, тестируемый должен его поднять и продолжить задание; если колышек падает на пол, его поднимает не пациент, а лицо, проводящее обследование.
Ключ (интерпретация): снижение скорости выполнения при повторном тестировании более чем на 20% расценивается как клинически значимое ухудшение.
Приложение Г6. Тест для руки Френчай
Название на русском: Тест для руки Френчай
Оригинальное название: The Frenchay Arm Test
Источник (официальный сайт разработчиков, публикация с валидацией): Heller A, Wade D, Wood V, Sunderland A, Hewer R, Ward E. Arm function after stroke: measurement and recovery over the first three months. Journal of Neurology, Neurosurgery & Psychiatry. 1987;50(6):714-719. doi:10.1136/jnnp.50.6.714
Тип: шкала оценки
Назначение: оценка функции поражённой руки.
Если у больного выраженный когнитивный дефицит или речевые нарушения, препятствующие пониманию команд, следует использовать альтернативные источники коммуникации. Если пациент находится без сознания, то он получает 0 баллов.
Инструкция:
• Исходное положение для каждого задания: сидя за столом, руки лежат на коленях
• Все задания выполняются пораженной рукой
• За каждое успешно выполненное задание больной получает 1 балл (максимум 5 балл)
• За невыполненное – 0 баллов
Задания:
1. Удержать линейку паретичной рукой и с ее помощью начертить линию, держа карандаш в другой (непораженной) руке. Задание считается выполненным успешно, если линейка удерживается стабильно.
2. Взять в руку цилиндр диаметром 1,2 и длиной 5 см, поставленный вертикально на расстоянии 15 – 30 см от края стола, поднять на высоту около 30 см и затем опустить на место, не уронив при этом.
3. Взять стакан, наполовину наполненный водой и поставленный на расстоянии 15 – 30 см от края стола, отпить воды и поставить стакан на место, не расплескав при этом воду.
4. Снять, а затем установить на прежнее место бельевую прищепку, укрепленную на вертикальном колышке длиной 15 и диаметром 1 см. Колышек укреплен на квадратной дощечке (длина стороны 10 см), расположенной на расстоянии 15 – 30 см от края стола. Пациент не должен уронить прищепку или колышек
5. Причесать волосы (или имитировать причесывание). Пациент должен расчесать волосы на макушке, на затылке, с правой и левой стороны.
Приложение Г7. Индекс мобильности Ривермид
Название на русском: Индекс мобильности Ривермид
Оригинальное название: Rivermead Mobility Index
Источник (официальный сайт разработчиков, публикация с валидацией): Whiting S, Lincoln N, Bhavnani G, Cockburn J. Rivermead Perceptual Assessment Battery. Occup Ther Health Care. 1986;3(3-4):209-210. doi:10.1080/j003v03n03_18
Тип: шкала оценки
Назначение: методика для клинической оценки мобильности пациента.
Если пациент с афазией или иными проблемами с коммуникацией (Интубация, ИВЛ) тест не проводится.
Если пациент находится в лежачем состоянии тест не проводится.
Если больной не говорит, но способен перемещаться, тест проводится с визуальной подсказкой, по результатам наблюдения за его действиями либо при помощи карточек альтернативной коммуникации (обозначения действия).
Если пациент находится без сознания тест не проводится.
Если у пациента выраженный когнитивный дефицит тест проводится по результатам наблюдения за его деятельностью.
Если пациент не способен понять вопрос и (или) выполнить действие – выставляется оценка 1.
Если у пациента нет когнитивного дефицита и он способен отвечать на вопросы, оценка проводится со слов пациента, либо пациент сам заполняет опросник при помощи опрашивающего специалиста.
Начисляется следующее количество баллов:
1 — зависим от посторонней помощи (то есть самостоятельное выполнение действия невозможно, или небезопасно, или требует неразумных затрат времени);
2 — требуется присмотр (вербальная помощь и подсказка);
3 — независим (может использовать вспомогательные приспособления).
Приложение Г8. Опросник оценки качества жизни SF-36
Название на русском: Опросник оценки качества жизни SF-36
Оригинальное название: The 36-Item Short Form Health Survey questionnaire
Источник (официальный сайт разработчиков, публикация с валидацией): Saris-Baglama RN, Dewey CJ, Chisholm GB, et al. Quality Metric health outcomes™ scoring software 4.0. Lincoln, RI: Quality Metric Incorporated, 2010, p. 138.
Тип: шкала оценки
Назначение: опросник для оценки качества жизни пациента.
Пожалуйста, ответьте на 36 вопросов обследования состояния здоровья полностью, честно и не прерываясь.
ОБЩЕЕ СОСТОЯНИЕ ЗДОРОВЬЯ:
В целом Вы бы оценили состояние здоровья как:
⬜ Отличное ⬜ Очень хорошее ⬜ Хорошее ⬜ Посредственное ⬜Плохое
Как бы вы оценили свое здоровье сейчас по сравнению с тем, что было год назад?
⬜ Значительно лучше, чем год назад
⬜ Несколько лучше, чем год назад
⬜ Примерно так же
⬜ Несколько хуже, чем год назад
⬜ Намного хуже, чем год назад
ОГРАНИЧЕНИЕ ФИЗИЧЕСКИХ НАГРУЗОК:
Следующие вопросы касаются физических нагрузок, с которыми Вы, возможно, сталкиваетесь в течение своего обычного дня. Ограничивает ли Вас состояние Вашего здоровья в настоящее время в выполнении этих физических нагрузок? Если да, то в какой степени?
Тяжелые физические нагрузки, такие как бег, поднятие тяжестей, занятие силовыми видами спорта
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Умеренные физические нагрузки, такие как передвинуть стол, пропылесосить, боулинг или игра в гольф
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Поднять или нести сумку с продуктами
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Подняться пешком по лестнице на несколько пролетов
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Подняться пешком по лестнице на один пролет
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Наклониться, встать на колени, согнуться
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Пройти расстояние более одного километра
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Пройти расстояние в несколько кварталов
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Пройти расстояние в один квартал
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
Самостоятельно вымыться, одеться
⬜ Да, значительно ограничивает ⬜ Да, немного ограничивает ⬜ Нет, совсем не ограничивает
ПРОБЛЕМЫ С ФИЗИЧЕСКИМ ЗДОРОВЬЕМ:
Бывало ли у Вас в течение последних 4 недель, что Ваше физическое состояние вызывало затруднения в Вашей работе или другой обычной повседневной деятельности, вследствие чего:
Пришлось сократить количество времени, затрачиваемого на работу или другие дела
⬜ Да ⬜ Нет
Вы выполнили меньше, чем хотели
⬜ Да ⬜ Нет
Вы были ограничены в выполнении какого-либо определенного вида работы или другой деятельности
⬜ Да ⬜ Нет
Были трудности при выполнении работы или других дел (например, они потребовали дополнительных усилий)
⬜ Да ⬜ Нет
ПРОБЛЕМЫ С ЭМОЦИОНАЛЬНЫМ ЗДОРОВЬЕМ:
Бывало ли у Вас в течение последних 4 недель, что какие-либо из перечисленных ниже проблем вызывали затруднения на работе или другой обычной повседневной деятельности в результате каких-либо эмоциональных проблем (таких как чувство депрессии или беспокойства)?
Пришлось сократить количество времени, затрачиваемого на работу или другие дела
⬜ Да ⬜ Нет
Вы выполнили меньше, чем хотели
⬜ Да ⬜ Нет
Выполняли свою работу или другие дела не так аккуратно, как обычно
⬜ Да ⬜ Нет
ОБЩЕСТВЕННАЯ ДЕЯТЕЛЬНОСТЬ (ДОСУГ):
Насколько Ваши эмоциональные проблемы мешали Вам проводить совместное время с семьей, друзьями, соседями или в коллективе?
⬜ Совсем не мешало ⬜ Немного ⬜ Умеренно ⬜ Сильно ⬜ Очень сильно
Насколько сильную физическую боль Вы испытывали за последние 4 недели?
⬜ Совсем не испытывал(а) ⬜ Очень слабую ⬜ Слабую ⬜ Умеренную ⬜ Сильную ⬜ Очень сильную
В какой степени боль в течение последних 4 недель мешала Вам заниматься Вашей нормальной работой (включая работу вне дома и по дому)?
⬜ Совсем не мешало ⬜ Немного ⬜ Умеренно ⬜ Сильно ⬜ Очень сильно
ЭНЕРГИЯ И ЭМОЦИИ
Эти вопросы касаются того, как Вы себя чувствовали и каким было Ваше настроение в течение последних 4 недель. Пожалуйста, на каждый вопрос дайте ответ, который наиболее соответствует Вашим ощущениям.
Вы чувствовали себя полным(ой) бодрости?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
Вы чувствовали себя таким подавленным(ой), что ничто не могло Вас взбодрить?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
Вы чувствовали себя спокойным(ой), и умиротворенным(ой)?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
Вы чувствовали себя полным(ой) сил и энергии?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
Вы чувствовали себя упавшим(ой) духом и печальным?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
Вы чувствовали себя измученным(ой)?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
Вы чувствовали себя счастливым(ой)?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
Вы чувствовали себя уставшим(ой)?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
ОБЩЕСТВЕННАЯ ДЕЯТЕЛЬНОСТЬ (ДОСУГ):
Как часто за последние 4 недели Ваше физическое или эмоциональное состояние мешало Вам активно общаться с людьми (например, навещать друзей, родственников и т.п.)?
⬜ Все время
⬜ Большую часть времени
⬜ Часто
⬜ Иногда
⬜ Редко
⬜ Ни разу
ОБЩЕЕ СОСТОЯНИЕ ЗДОРОВЬЯ:
Насколько верным или неверным представляется по отношению к Вам каждое из нижеперечисленных утверждений?
Мне кажется, что я более склонен(на) к болезням, чем другие люди
⬜ Определенно верно
⬜ В основном верно
⬜ Не знаю
⬜ В основном не верно
⬜ Определенно неверно
Мое здоровье не хуже, чем у большинства моих знакомых
⬜ Определенно верно
⬜ В основном верно
⬜ Не знаю
⬜ В основном не верно
⬜ Определенно неверно
Я ожидаю, что мое здоровье ухудшится
⬜ Определенно верно
⬜ В основном верно
⬜ Не знаю
⬜ В основном не верно
⬜ Определенно неверно
⬜ Определенно верно
⬜ В основном верно
⬜ Не знаю
⬜ В основном не верно
⬜ Определенно неверно
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Примечание Лахта Клиники. Ежегодно с 1 марта в мире проводится Месяц осведомленности о рассеянном склерозе (Multiple Sclerosis Awareness Month, причем многозначное слово «Awareness» в данном контексте можно понимать и как «бдительность», и как «узнавание», «осознание» и т.п.). На момент публикации данного материала очередная кампания подходит к концу, и мы считаем целесообразным дополнить статью «Рассеянный склероз», размещенную на нашем сайте, анализом некоторых ложных представлений об этом тяжелом заболевании.
Рассеянный склероз (множественный склероз) – хроническое заболевание центральной нервной системы, при котором поражается как головной, так и спинной мозг. На сегодняшний день не существует способов обратить процесс или, тем более, обернуть его вспять, поэтому применяется эффективное паллиативное лечение, задачей которого является замедление развития болезни, смягчение ее многочисленных неврологических симптомов, отдаление сроков инвалидизации.
По данным на 2016 год, как сообщал ведущий медицинский журнал мира The Lancet, рассеянный склерозом страдали на земном шаре 2.2 миллиона человек. Известно, что это иммуно-опосредованный процесс, и большинство экспертов относят его к аутоиммунным заболеваниям. С другой стороны, рассеянный склероз относится к рубрике демиелинизирующих заболеваний, поскольку разрушается защитная и электроизолирующая белковая (миелиновая) оболочка нервных волокон. Это приводит к нарушениям связей между центральной нервной системой и прочими системами организма.
Поэтому клинические проявления рассеянного склероза могут обнаруживаться где угодно и, в частности, включать:
— онемения, покалывания и другие парестезии;
— проблемы со зрением;
— мышечные спазмы и слабость;
— хроническую усталость;
— тревожные и/или депрессивные расстройства;
— боли различного характера;
— ограничения подвижности;
— нарушения речи и глотания, и т.д.
В некоторых случаях симптоматика с течением времени медленно нарастает, что называют первичным прогрессирующим рассеянным склерозом. Другие пациенты переживают приступы, «атаки», обострения, в ходе которых имевшиеся проявления болезни усугубляются или появляются новые симптомы. Этот тип течения называют возвратно-ремиттирующим.
Общее состояние некоторых пациентов с возвратно-ремиттирующей формой постепенно ухудшается, что определяется как вторичный прогрессирующий рассеянный склероз.
К настоящему времени остается неясным, почему у одних людей это заболевание развивается, а у других нет. Предполагается, что патогенетическую роль могут играть средовые (экологические) и наследственные факторы. А поскольку механизмы развития неизвестны, то в отношении рассеянного склероза (и многих других этиопатогенетически неясных болезней) существует масса устойчивых мифов и заблуждений. В данной статье рассмотрим девять основных из них.
- Любой человек с рассеянным склерозом нуждается в инвалидном кресле-каталке
Это именно миф. В действительности, как разъясняет Общество изучения рассеянного склероза, все наоборот: большинство пациентов обходятся без инвалидного кресла.
По данным PubMed Central (база данных Институтов здравоохранения США. – прим. Лахта Клиники), через 15 лет от момента установления диагноза лишь 20% больных рассеянным склерозом вынуждены пользоваться креслом-каталкой, костылями или подпоркой для хоьбы. Этим медико-статистическим исследованием занималась, в частности, врач-невролог Лорен А. Ролак.
В материалах Общества изучения рассеянного склероза отмечается: «Когда болезнь начинает ограничивать вашу подвижность, возможно, будет трудно решиться на использование палочки для ходьбы, специального скутера или кресла-каталки. Но когда вы начнете пользоваться чем-то из этих средств, то быстро убедитесь, – как убедились многие люди до вас, – насколько это просто и насколько это помогает сохранить свою независимость».
- При рассеянном склерозе невозможно работать
И это – миф. Многие пациенты с рассеянным склерозом годами остаются незаменимыми членами своих рабочих коллективов и команд. Да, проблемы возможны, и некоторые люди могут столкнуться с необходимостью пересмотра дальнейших карьерных путей и планов. Однако это вовсе не является неизбежным для каждого. Сегодня «…люди с диагностированным рассеянным склерозом продолжают работать в течение длительного времени». Национальное общество изучения рассеянного склероза допускает, однако, что «некоторые заболевшие сразу решают оставить работу, услышав диагноз или пережив первое серьезное обострение; к такому решению человека нередко подталкивает семья либо лечащий врач».
Вместе с тем, этот выбор во многих случаях оказывается слишком поспешным: решение нельзя принимать на высоте симптоматики. Существует масса вариантов паллиативной терапии, постоянно разрабатываются новые технологии, стратегии контроля болезни, а также ресурсы правовой защиты и общественной поддержки. В совокупности все это поможет вам сохранять за собой рабочее место как можно дольше.
Действительно, привычная работа идет больным на пользу, что также было подтверждено специальными исследованиями: «Вдобавок к обеспечению финансовой безопасности, трудоустройство способно внести значительный вклад в физическое и психическое благополучие людей, страдающих рассеянным склерозом, поскольку является источником социального взаимодействия и поддержки, чувства идентичности, наличия целей и перспектив».
Прим. Лахта Клиники. С 2019 года в Российской Федерации реализуется проект «Неограниченные возможности», задачей которого выступает обеспечение трудоустройства пациентов с рассеянным склерозом. Программу осуществляет Межрегиональное Московское общество рассеянного склероза при активном участии ряда общественных и коммерческих организаций.
- Рассеянный склероз развивается только у пожилых людей
В действительности у большинства пациентов с рассеянным склерозом первые симптомы появились в возрасте от 20 до 40 лет. И хотя процесс может начаться на любом этапе жизни, случаи манифестации после 50 лет являются сравнительно редкими. Вместе с тем, авторы одного из исследований обращают внимание на то, что дифференцировать начало рассеянного склероза от других подобных заболеваний у людей пожилого возраста может быть очень непросто, поэтому такие случаи на самом деле могут оказаться гораздо более частым явлением, чем принято считать.
- Людям с рассеянным склерозом нельзя выполнять физические упражнения
Неправда. Физическая активность помогает контролировать симптомы, продлевая баланс и силу.
Миф о том, что при рассеянном склерозе любые упражнения невозможны или противопоказаны, очень распространен. В базе PubMed есть публикации, авторы которых отмечают: некоторые больные с диагностированным рассеянным склерозом сворачивают всякую физическую активность, опасаясь, что она может спровоцировать усугубление симптоматики. На самом же деле: «Физические упражнения должны рассматриваться как безопасное и эффективное средство реабилитации больных рассеянным склерозом. Полученные доказательства свидетельствуют о том, что индивидуализированные и контролируемые врачом комплексы упражнений позволяют поддерживать и улучшать форму, функциональные возможности и качество жизни в целом, равно как и редуцировать те симптомы, которые при данном заболевании поддаются редукции».
В прошлом году Национальное общество изучения рассеянного склероза в сотрудничестве с группой экспертов опубликовало подробные рекомендации для пациентов, касающиеся физической активности. Кроме прочего, в рекомендациях подчеркивается:
«Работники здравоохранения должны разъяснять больным необходимость уделять [как минимум] 150 минут в неделю физическим упражнениям, и столько же – активному отдыху. […] Выходить на этот уровень следует постепенно, отталкиваясь от индивидуальных возможностей, предпочтений и безопасности пациента».
Совершенно необходимо проконсультироваться с врачом, прежде чем приступать к новому образу жизни и осваивать системы упражнений.
- Если мои симптомы минимальны, никакие лекарства мне не нужны
Согласно современным публикациям экспертов, лечение при рассеянном склерозе должно проводиться даже в тех случаях, когда болезнь протекает малосимптомно.
На ранних этапах развития заболевания симптоматика и в самом деле может не причинять ощутимых проблем. Однако безотлагательное начало лечения под долгосрочным постоянным наблюдением врача способно замедлить прогрессирование симптомов.
Этот эффект также был специально исследован, и в 2016 году были опубликованы данные, согласно которым «Имеются статистические ассоциации между ранним начало лечения и более благоприятным клиническим исходом».
- Женщины с рассеянным склерозом должны избегать беременности
Еще одно распространенное заблуждение заключается в том, что рассеянный склероз может снижать фертильность и создавать проблемы с вынашиванием беременности. Это именно заблуждение.
Как поясняют специалисты Multiple Sclerosis Trust, «беременность не должна связываться с высоким риском на том лишь основании, что у будущей матери выявлен рассеянный склероз. Если вы страдаете этим заболеванием, вероятность выкидыша или врожденных аномалий не отличается от среднестатистического уровня в общей популяции».
Более того, при возвратно-ремиттирующем типе течения беременные пациентки переживают рецидивы и обострения реже, чем обычно. Риск обострения возвращается к исходному уровню лишь полгода спустя после родов.
В 2019 году Association of British Neurologists опубликовала консенсусное руководство по ведению беременности у женщин с рассеянным склерозом, – на всем протяжении, начиная от консультирования на этапе планирования семьи и до послеродового сопровождения. Кроме прочего, авторы рекомендуют не прерывать поддерживающую медикаментозную терапию в связи с тем, что планируется деторождение в будущем.
- Если у меня рассеянный склероз, он будет и у моих детей
Наследственный фактор имеет определенное значение, однако рассеянный склероз не является собственно генетической болезнью и не передается напрямую, сколько-нибудь предсказуемым образом, от родителей к детям.
Накопленные наблюдения показывают, что если у одного из гомозиготных близнецов начинается рассеянный склероз, риск развития той же болезни у второго близнеца варьирует в пределах 20-40%. Для гетерозиготных близнецов риск и того меньше: 3-5%.
Иными словами, гены как-то вовлечены в развитие болезни, однако главный пусковой механизм все же не в них.
Согласно актуальным данным Общества по изучению рассеянного склероза, при наличии этого заболевания у одного из родителей ребенок тоже заболевает в 1 случае из 67. Для детей со здоровыми обоими родителями аналогичный показатель составляет примерно 1:500.
Таким образом, риск действительно выше, однако это никоим образом не является абсолютным противопоказанием.
- Люди с рассеянным склерозом должны исключить все источники стресса и тревоги
Да, жизнь в т.н. «ситуации хронического стресса» в некоторых случаях может утяжелять течение болезни. Правда и то, что люди с рассеянным склерозом более предрасположены к повышенной тревожности.
Однако полностью исключить стрессы с тревогами невозможно.
Специалисты рекомендуют искать более эффективные способы совладания и преодоления стрессов. В недавно опубликованной брошюре говорится о том, что «Стрессов нельзя, – и не нужно, – панически избегать. Другое дело, что хорошее овладение способами снижать интенсивность переживаний будет работать на нас, а не против».
Похожий миф состоит в том, что стрессогенная жизнь может увеличить риск развития рассеянного склероза. До сих не получено никаких подтверждений этого.
- Рассеянный склероз всегда фатален
Этот вопрос также изучался специалистами.
Рассеянный склероз – хроническое, пожизненное заболевание. Средняя продолжительность жизни у заболевших меньше примерно на 7 лет, чем популяционный показатель. Но сама по себе эта болезнь не является летальной. Более того, в выборках людей, заболевших много десятилетий назад, средняя продолжительность жизни меньше, чем в когортах заболевших в более поздние годы. Это говорит о том, что продолжительность жизни у больных рассеянным склерозом, в среднем, постепенно увеличивается.
И она все меньше будет отличаться от среднестатистического уровня – по мере появления новых научных данных и разработки новых терапевтических стратегий.
По материалам сайта Medical News Today
Кафедра неврологии и нейрохирургии Ярославской государственной медицинской академии
Синдром Шегрена и рассеянный склероз: сходство и различия
Журнал:
Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2012;112(2‑2): 69‑74
Как цитировать:
Пизова Н.В.
Синдром Шегрена и рассеянный склероз: сходство и различия. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски.
2012;112(2‑2):69‑74.
Pizova NV. The Sjögren’s syndrome and multiple sclerosis: similarity and differences. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2012;112(2‑2):69‑74. (In Russ.).

?>
В клинической практике часто появляются затруднения в проведении дифференциального диагноза рассеянного склероза (РС) и других заболеваний с поражением центральной нервной системы, при которых наблюдается сходство клинических и томографических признаков, особенно в дебюте заболевания [1, 28, 49]. Так, S. Watanabe и соавт. [53] длительно наблюдали женщину, у которой в 38 лет постепенно развился медленно прогрессирующий спастический монопарез левой ноги, и ей было трудно ходить; в 40 лет при клиническом осмотре были выявлены замедление речи, вертикальный нистагм, спастичность в руках и ногах и монопарез левой ноги, повышенный нижнечелюстной рефлекс, гиперрефлексия сухожильных рефлексов и положительные двусторонние рефлексы Гофмана и Бабинского. При лабораторном обследовании определялись положительные титры антинуклеарных антител и anti-SS-A/Ro-антитела. В цереброспинальной жидкости (ЦСЖ) отмечались наличие олигоклональных полос и повышенный показатель IgG. На МРТ определялись множественные бляшки в белом веществе головного мозга и стволе, которые не накапливали гадолиний. Дополнительно наблюдалась сухость глаз, и только после проведенной биопсии пациентке был выставлен диагноз синдрома Шегрена (СШ), хотя течение заболевания у этой пациентки очень напоминало хронический прогрессирующий РС и требовало проведения дифференциального диагноза. Ошибочный диагноз РС, к сожалению, выставляется в 5-10% случаев [50].
СШ и РС — это хронические иммуноопосредованные заболевания с обострениями и ремиссиями, развивающиеся у лиц молодого возраста, патогенез которых до сих пор недостаточно известен. Эти нозологические формы имеют сходство этиологических, патогенетических, клинических и нейровизуализационных показателей. Для них характерны мультифакториальная этиология; аутоиммунный, воспалительный и нейродегенеративный процессы в качестве основных патогенетических механизмов; выраженная вариабельность клинической картины и часто непредсказуемый прогноз.
Аутоиммунные механизмы имеют большое значение в патогенезе СШ и РС (табл. 1).

СШ и РС — хронические воспалительные заболевания, причем РС характеризуется Th1-типом иммунного ответа, а СШ — Th1- и Th2-опосредованным типом иммунного ответа [2, 16, 22-25, 31, 40, 48] (Th1 — ИЛ-2, ИЛ-3, лимфотоксин, ИФ-γ, ГМ-КСФ, фактор некроза опухолей α (ФНО-α); Th2 — ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-9, ИЛ-10, ИЛ-13, ИЛ-3, ИФ-γ, ГМ-КСФ, ФНО-α)[1].
СШ — системное аутоиммунное заболевание неизвестной этиологии, характеризующееся лимфоплазмоклеточной инфильтрацией секретирующих эпителиальных желез с наиболее частым поражением слюнных и слезных желез [2, 28]. У больных c первичным СШ в сыворотках обнаруживаются различные антитела. Неврологические проявления при СШ очень часто схожи с клинической картиной РС. При обоих заболеваниях у пациентов могут выявляться гипестезия, спастичность, гиперрефлексия, атаксия, корешковые нарушения, гемипарезы или гемиплегия, дизартрия, мозжечковые нарушения речи, нистагм, межъядерная офтальмоплегия и др. У пациентов с СШ с поражением спинного мозга могут развиться нижний парапарез, тетрапарезы, острая или подострая поперечная миелопатия, хроническая прогрессирующая миелопатия, нейрогенный мочевой пузырь, нарушения функции тазовых органов, синдром Броун-Секара. Если у больных с СШ в патологический процесс будет вовлечен зрительный нерв, то может быть монокулярная или бинокулярная потеря зрения или неврит/нейропатия зрительного нерва. Некоторые симптомы поражения ЦНС представлены как при РС, так и при СШ (табл. 2).

У большинства больных с СШ преобладают нефокальные нейропсихологические нарушения [37]. Так, по данным J. Anaya и соавт. [6], при наблюдении 120 пациентов с первичным СШ согласно Европейским критериям у 3 из них поражение ЦНС было схожим с другими неврологическими заболеваниями — РС, оптическим невритом и осложненной мигренью. У всех этих больных выявлялись повышенный уровень anti-Ro-антител. В литературе [9] описан случай развития оптиконейромиелита Девика у пациентки с первичным СШ, в другом наблюдении [20] у пациентки в 10-летнем возрасте отмечался неврит правого зрительного нерва, в последующие годы в патологический процесс были вовлечены оба зрительных нерва и продолговатый мозг, а диагноз СШ был выставлен позднее, когда появился сухой синдром. Схожесть в клинической картине отметили и C. Iñiguez и соавт. [26], которые среди 100 пациентов с РС выявили 2 больных женского пола, имеющих ксерофтальмию и ксеростомию и позитивные Ro-антитела. У одной из этих женщин регистрировались периодически возникающие эпизоды слабости в левых конечностях и атаксия, а на МРТ головного мозга — гиперинтенсивные очаги в перивентрикулярном белом веществе. У второй пациентки с диагнозом РС (выставлен в 53 года) определялись множественные гиперинтенсивные очаги на МРТ головного мозга и сухой синдром.
МРТ головного мозга у пациентов с СШ и поражением ЦНС могут иметь схожую с РС нейровизуализационную картину (табл. 3).

B. Thong и N. Venketasubramanian [47] наблюдали 40-летнюю пациентку с множественной неврологической симптоматикой со стороны спинного и головного мозга, у которой на МРТ головного и спинного мозга во время обострения выявлялись гиперинтенсивный сигнал и отек спинного мозга. Позднее у нее стали определяться антинуклеарные антитела и anti-Ro-антитела, а затем сухой синдром, что позволило выставить диагноз СШ. Также наличие повреждения головного мозга по данным МРТ показано [37] у неврологически асимптомных пациентов с СШ в виде мелких очагов в белом веществе головного мозга.
При СШ в патологический процесс может вовлекаться и спинной мозг (табл. 4), что проявляется развитием поперечной миелопатии, часто рецидивирующей или хронической прогрессирующей, нарушениями функции тазовых органов, реже встречаются синдром Броун-Секара.

Некоторые авторы полагают, что эти антитела представляют результат перекрестных реакций антител против миелина или вирусных антигенов с Ro/-SSA-молекулами и другими аутоантигенами. Если анти-Ro, антинуклеарные антитела, анти-н-ДНК и антитела к кардиолипинам обнаруживаются у пациентов с РС, то эти пациенты должны быть повторно обследованы на предмет ревматического заболевания, которое должно быть пролечено иммуносупрессивной терапией (цитостатики, глюкокортикостероиды).
У пациентов с СШ при иммунологическом исследовании в сыворотке выявляют повышенные титры ревматоидного фактора (РФ), антитела к растворимым ядерным антигенам Ro(SS-A), La(SS-B), причем антитела к Ro(SS-A)-антигену отмечаются у 50% пациентов, а антитела к La(SS-B)-антигену — у 40-50% [43]. Однако анти-Ro-антитела могут выявляться в 2-15% случаев и у больных РС (табл. 5) [12].

Олигоклональные полосы в ЦСЖ относятся к характерным признакам РС, они выявляются в 95% случаев и включены в диагностические критерии этого заболевания. Однако эти изменения в ЦСЖ могут наблюдаться и при СШ (табл. 6), но различия заключаются в том, что у пациентов с РС имеются многочисленные полосы, в то время как при СШ только 1 или 2 полосы.

Исследование ЦСЖ у 17 пациентов с первичным СШ [19, 51] показало, что у 6 из 8 пациентов с клиническими проявлениями поражения нервной системы и у 5 из 9 пациентов без вовлечения нервной системы был выявлен интратекальный синтез олигоклональных полос IgG. Интратекальный синтез противовирусных IgG-антител к вирусам кори, эпидемического паротита, вирусу простого герпеса наблюдался у 8 из 17 пациентов с СШ и у 7 из 12 с РС. В ЦСЖ IgG-антитела к миелину были обнаружены у 3 из 12 больных РС и ни у кого с СШ.
В недавнем исследовании, проведенном в Швеции методом свободной выборки, были отобраны 30 пациентов с РС и исследованы на наличие СШ согласно Копенгагенским критериям. У 5 из этих больных регистрировался сухой кератоконъюнктивит, у 1 — ксеростомия и у 3 — гистологически подтвержденный сиалоаденит со снижением выработки слюны, однако ни у одного из этих больных не был диагностирован СШ [42]. В другом исследовании [52] среди 12 пациентов с ремиттирующим РС, проживающих в Азии, были выявлены 6 лиц, полностью соответствующих диагнозу первичного СШ. В то же время J. de Seze и соавт. [15], изучая частоту СШ у 60 пациентов с первично-прогрессирующим РС согласно клиническим, лабораторным, инструментальным диагностическим критериям и результатам биопсии, выявили у 10 (16,6%) наличие 4 и более критериев диагноза СШ. Выявленная частота превышает общепопуляционную (1-5%). В другой работе [39] при обследовании пациентов с диагнозом первично прогрессирующего РС на наличие у них диагностических критериев СШ с использованием Европейских критериев СШ, теста Schirme, сцинтиграфии слюнных желез, биопсии слюнных желез и серологических тестов (антитела Ro/SS-A, La/SS-B и антинуклеарные) у 9 больных РС был диагностирован СШ (не менее 4 классификационных критериев). Все эти пациенты — женщины, средний возраст которых на момент появления симптомов составил 46,6 года. Спастический парапарез наблюдался у всех из них, а на МРТ спинного мозга у большинства выявлялись изменения, однако anti-Ro- и anti-La-антитела были негативными в большинстве случаев. Другие авторы [17, 35, 36] среди пациентов с РС также определяли как отдельные симптомы, характерные для СШ, так и диагностировали СШ как нозологическую форму, в то время как в крупном исследовании, проведенном J. Noseworthy и соавт. [38], среди 192 пациентов с РС не было выявлено ни одного больного, имеющего клинические проявления СШ.
В настоящее время в литературе дискутируется вопрос о влиянии патогенетической терапии на течение заболевания [50]. Так, L. de Santi и соавт. [13] наблюдали 48-летнюю женщину с ремиттирующим РС, с хорошим ответом на интерферон 1а-бета и развившимся через 29 лет после постановки диагноза РС сухим синдромом, который был подтвержден инструментально и по данным биопсии.
Таким образом, у пациентов с СШ и РС достаточно часто определяются схожие данные клинических, нейровизуализационных и лабораторных исследований, что нередко создает трудности в проведении дифференциального диагноза между этими нозологическими формами.
[1]Использованы следующие сокращения: ИЛ — интерлейкин, ИФ — интерферон, Th — T-лимфоциты хелперы, ГМ-КСФ — гранулоцитарно-макрофагальный колониестимулирующий фактор.