Папиллярный рак получил свое название из-за особого строения опухоли — она образует сосочковые структуры, в которых имеются соединительнотканные стержни, пронизанные кровеносными и лимфатическими сосудами мелкого калибра. При этом часто зоны папиллярных образований чередуются с зонами солидного или фолликулярного строения. В подавляющем большинстве случаев папиллярный рак поражает щитовидную железу. Реже папиллярные злокачественные новообразования возникают в почках, органах ЖКТ, молочной железе и яичниках.
- Причины возникновения папиллярного рака
- Классификация
- Локализация папиллярного рака
- Симптомы папиллярного рака
- Диагностика папиллярного рака
- Лечение папиллярного рака
- Прогноз при папиллярном раке щитовидной железы
- Профилактика папиллярного рака
- Осложнения папиллярного рака щитовидной железы
Причины возникновения папиллярного рака
Причины возникновения папиллярного рака сложны и многогранны. При этом для разных органов могут быть разные факторы риска. Например, к развитию папиллярного рака щитовидной железы приводят следующие факторы:
- Хроническое воздействие на орган тиреотропного гормона в высоких дозах. Такие состояния наблюдаются при хронических гипертиреозах и при тиреотоксикозе.
- Воздействие ионизирующего излучения, в том числе радиоактивных изотопов йода.
- Наличие доброкачественных новообразований щитовидной железы.
- Дефицит йода.
- Наследственные синдромы — синдром Карни, Каудена, МЭН и др.
Для новообразований других органов может быть своя специфика. Например, папиллярный рак желудка может возникать на фоне полипов, язвенной болезни, инфицирования хеликобактером и др. Рак яичников и молочной железы часто имеет гормональнозависимую природу, при этом новообразования чаще встречаются у нерожавших женщин. Практически для всех локализаций большую роль играют химические канцерогены, курение, неблагоприятная экологическая обстановка, несбалансированное и избыточное питание.
Классификация
Папиллярный рак классифицируют в зависимости от его гистологического варианта, места первичной локализации и стадии заболевания. Ключевое значение имеет первично пораженный орган, поскольку именно от этого будет зависеть гистологический вариант новообразования и прогноз его течения. Что касается стадии заболевания, то здесь учитывается размер опухоли, инвазия в соседние ткани, наличие метастазов в лимфоузлы и отдаленные органы. В целом для каждого органа определены параметры установления стадии рака по системе ТNM (опухоль, лимфогенные и гематогенные метастазы).
Локализация папиллярного рака
Чаще всего папиллярный рак локализуется в щитовидной железе. В других органах он встречается значительно реже. В целом папиллярные новообразования могут развиваться в следующих органах:
- Молочная железа.
- Почки.
- Яичники.
- Кожа.
- Желудок.
- Поджелудочная железа.
Поскольку в подавляющем большинстве случаев локализацией папиллярного рака является именно щитовидная железа, в данной статье рассмотрим данную нозологию.
Симптомы папиллярного рака
На ранних этапах папиллярный рак щитовидной железы не вызывает никаких симптомов. В более позднем периоде могут возникать некоторые признаки, но они неспецифичны и часто присутствуют при других заболеваниях эндокринной системы:
- Наличие узловых образований в органе. Узлы в щитовидной железе еще не являются критерием постановки диагноза, поскольку часто они являются доброкачественными. А вот что должно насторожить, так это возникновение узлов у молодых людей в возрасте до 20 лет, поскольку в этой возрастной группе доброкачественные узловые гиперплазии встречаются редко.
- Лимфаденопатия шейных лимфоузлов (увеличение лимфоузлов). Это также неспецифический признак, поскольку может быть симптомом инфекций верхних дыхательных путей или лимфом.
- Симптомы гипертиреоза: нестабильность настроения, снижение веса, учащенное сердцебиение, повышение аппетита, потливость, слабость и др.
- На распространенных стадиях, когда опухоль выходит за пределы органа, может меняться конфигурация шеи, ее объемы и контуры. Некоторые больные могут отмечать необычные ощущения, например, першение, комок в горле, изменение голоса, затруднение глотания, боль в горле и др.
Все эти симптомы могут быть и при других заболеваниях, поэтому для подтверждения диагноза требуется специальное обследование.
Диагностика папиллярного рака
Для диагностики папиллярного рака применяется ряд специальных тестов:
- Ультразвуковое исследование щитовидной железы. При папиллярном раке будут обнаруживаться узловые новообразования. Заподозрить их злокачественную природу можно по нечеткому контуру и размытым краям.
- Биопсия обнаруженных новообразований. Как правило, для диагностики папиллярного рака используется тонкоигольная аспирационная биопсия, с помощью которой пунктируют узловые новообразования и аспирируют их содержимое. Полученный материал направляется в лабораторию для цитологического исследования. Увеличенные лимфатические узлы также пунктируют. Чтобы результат был максимально достоверным, материал берут из нескольких точек. Если лаборатория выдает неопределенный результат, исследование следует повторить.
- Радиоизотопное сканирование. Это исследование позволяет максимально точно определить объем опухолевой ткани и обнаружить метастазы при их наличии.
- Лабораторные анализы. Всем пациентам, при подозрении на папиллярный рак, назначают анализ на тиреоидные гормоны, а также на тиреоглобулин. При успешном лечении его уровень снижается, а при развитии рецидива или прогрессировании заболевания опять начинает нарастать.
Лечение папиллярного рака
Ключевым моментом в лечении папиллярного рака щитовидной железы является хирургическая операция. Как правило, проводится тотальное удаление органа вместе с капсулой. Также выполняется шейная диссекция, которая подразумевает удаление жировой клетчатки лимфатических узлов. Если рак распространился на окружающие ткани и органы, по возможности проводится их резекция.
Следующим этапом лечения папиллярного рака является радиойодтерапия. Ее суть заключается в следующем — пациент принимает радиоактивный йод, который избирательно аккумулируется в клетках щитовидной железы, в том числе и злокачественных. Это приводит к их локальному облучению и гибели. Перед тем как начинать такую терапию, искусственно создают дефицит йода в организме. Для этого отменяют прием заместительной гормональной тиреоидной терапии на несколько недель и исключают из рациона продукты, богатые йодом (йодированная соль, морепродукты и др).
Кроме того, крайне не рекомендуется в это время проходить компьютерную томографию с контрастированием, поскольку в контрасте содержится йод. На момент начала радиотерапии уровень ТТГ должен превышать 30 мЕд/л. Лечение проводится курсами до полного исчезновения очагов накопления йода и снижения ТГ до 2 нг/л и менее.
И, наконец, заключительным этапом лечения является гормональная терапия. Поскольку при операции полностью удаляется щитовидная железа, продуцировать тиреоидные гормоны просто нечему, и у человека развивается тяжелый гипотиреоз. Чтобы его компенсировать, назначается искусственный гормон, аналогичный тироксину — L-тироксин. Однако его назначают в дозировках, значительно превышающих заместительные уровни гормона. Это необходимо для подавления гормона гипофиза, который стимулирует ткань щитовидной железы, и в том числе злокачественные клетки. Уровень L-тироксина подбирается таким образом, чтобы ТТГ было в пределах 0,05-01 мЕд/л.
Прогноз при папиллярном раке щитовидной железы
Прогноз при папиллярном раке щитовидной железы благоприятный, поскольку эта опухоль является высокодифференцированной. Более чем у 95% пациентов удается добиться полного выздоровления. Однако они вынуждены будут пожизненно принимать искусственный тироксин.
Профилактика папиллярного рака
Профилактика папиллярного рака заключается в следующих мероприятиях:
- Восполнение дефицита йода для людей, проживающих в эндемичный районах. Для этого подходит йодированная соль, увеличение в рационе количества морепродуктов, применение специальных препаратов.
- Своевременное лечение заболеваний щитовидной железы.
- Динамический контроль пациентов из группы риска — лица, проживающие в эндемичной по йод-дефициту районах, лица с обнаруженными узлами в щитовидной железе, пациенты, подвергавшиеся облучению.
Осложнения папиллярного рака щитовидной железы
Осложнения при раке щитовидной железы могут быть связаны с действием опухоли и с лечением заболевания. При прорастании новообразования за пределы органа может происходить поражение органов шеи и головы. При этом отмечается выраженная боль и неврологическая симптоматика. При прорастании в крупные кровеносные сосуды может возникнуть тяжелое кровотечение. Если объем опухоли большой, она может сдавливать пищевод и даже трахею, приводя к нарушению дыхания и прохождению пищевого комка.
Что касается лечения, то как мы уже говорили, удаление щитовидной железы приводит к тяжелому гипотиреозу, который при отсутствии лечения может привести к инвалидизации больного и даже его гибели. Поэтому очень важно принимать L-тироксин.
Папиллярная карцинома щитовидной железы
Что такое папиллярный рак щитовидки и каковы прогнозы лечения
Папиллярный рак щитовидной железы (ПРЩЖ) – недоброкачественные образования щитовидки, состоящие из тироцитов (секреторных клеток железы). Отличаются медленным прогрессированием и благоприятным течением в 90% случаев. Плотный узел имеет сосочковый поверхностный слой. При его прощупывании возникают болезненные ощущения. По мере прогрессирования рака железа увеличивается в объеме, что ведет к ухудшению самочувствия – нарушению глотания, дыхательной недостаточности, увеличению регионарных лимфоузлов.
Причины возникновения
Папиллярная карцинома щитовидной железы редко провоцирует вторичные раковые образования (метастазы) в отдаленных органах. Составляет 75% злокачественных поражений щитовидки. Диагностируется преимущественно у пациентов людей возрастом 30-50 лет. Раку в 2.5 раза больше подвержены женщины.
Причины опухолевого поражения эндокринной железы точно не определены. Согласно статистике, рак провоцируется соматическими мутациями. У большинства заболевших обнаруживаются мутации определенных генов:
- RET/PTC – 20% случаев;
- BRAF – 45-70% случав.
Онкологи выделяют ряд факторов, провоцирующих беспорядочное деление тироцитов – секреторных клеток железы:
- токсический зоб;
- йододефицит;
- нeблагоприятная экология;
- пролиферирующая цистаденома;
- гормональный дисбаланс;
- аутоиммунный тиреоидит;
- климактерический период;
- злоупотрeбление opaльными кoнтpaцептивами;
- радиотерапия;
- генетическая предрасположенность;
- несбалансированное питание;
- пагубные привычки;
- полипы прямой кишки;
- синдром Каудена;
- длительная депрессия.
Папиллярный рак щитовидки – благоприятная в плане прогнозов онкологическая болезнь. В 90% случаев она поддается лечению. Однако у детей протекает в более тяжелой форме, иногда дает метастазы в почки, легкие, мозг.
В группу риска входят женщины после 45 лет с очагами хронической инфекции. Частые рецидивы воспалений снижают противоопухолевый иммунитет. В результате возрастает вероятность перехода в рак доброкачественных образований железы – кист, аденом.
Особенности папиллярного рака щитовидки
У 96% больных раком щитовидной железы выявляются одиночные новообразования. Лишь изредка формируются множественные узлы. Они относятся к категории фолликулярно-папиллярных бескапсульных образований диаметром от 1 мм до 5-7 см.
При микроскопическом исследовании в новообразованиях обнаруживаются структуры, которые похожи на стeбли с множественными ответвлениями. Их основание представлено соединительнотканными тяжами с развитой сосудистой сетью. Стeбли устланы кубическим и цилиндрическим эпителием. Отмечается небольшое число митозов – деления клеток.
Папиллярная аденокарцинома щитовидной железы иногда имеет атипичное строение:
- сосудистые сетки в стeблях отсутствуют;
- клетки эпителия атрофированы;
- в центре опухоли присутствуют отложения солей кальция или рубцы.
Метастазирование – образование вторичных опухолей – происходит лимфогенным путем. Если рак прорастает в кровеносные сосуды, выявляются метастазы в других внутренних органах. Их основу составляют раковые клетки фолликулярной части новообразований.
Папиллярные элементы рака не синтезируют гормоны, а фолликулярные часто обладают гормональной активностью.
Степени и разновидности
Папиллярно-фолликулярный рак щитовидной железы подразделяют на 2 типа – отграниченный (инкапсулярный) и инфильтративный (неинкапсулярный). В первом случае опухоль локализуется внутри органа, поэтому почти не прорастает в другие анатомические структуры. Инфильтративный рак склонен к инвазивному росту (прорастанию в соседние ткани).
В зависимости от особенностей строения узелковых образований различают несколько видов рака щитовидки:
- Скрытый. Диаметр микрокарциномы не превышает 10 мм. Она медленно растет и редко выходит за границы железы.
- Фолликулярный. Этот вид рака выявляется у 30% больных ПРЩЖ. Новообразования прорастают в другие органы только в 15% случаев.
- Солидный. Чаще выявляются у больных, которые перенесли радиотерапию или подверглись радиационному излучению. Опухоль склонна к инвазивному росту, выходу за пределы железы. У 1/3 больных при этой форме рака выявляются метастазы в печени и легких.
- Онкоцитарный. Одна из самых агрессивных форм рака выявляется только у 5% пациентов с ПРЩЖ. Новообразования внедряются в кровеносные и лимфатические сосуды, из-за чего нередко диагностируются вторичные опухоли в отдаленных органах.
- Диффузно-склеротический. Крупные злокачественные узлы чаще обнаруживаются у детей и подростков. Характеризуются формированием фиброзно-кистозных очагов во всех слоях железы.
- Светлоклеточный. Малоизученная форма рака встречается редко. При запоздалом лечении метастазирует в почечную ткань.
- Высококлеточный. Раковые опухоли отличаются быстрым ростом. Нередко выявляются вторичные опухоли в костной ткани, мозге.
- Смешанный. Эта форма рака выявляется у 50% пациентов. В опухоли выявляются клетки сразу нескольких типов других новообразований.
Фолликулярный вариант папиллярного рака имеет наиболее благоприятный прогноз. Новообразования растут медленно, поэтому вторичные опухоли во внутренних органах выявляются нечасто.
Стадии рака щитовидки:
- 1 стадия. Внутри железы обнаруживается небольшой узелок, который не повреждает капсулу и не деформирует орган. Вторичные новообразования отсутствуют.
- 2а стадия. Рак провоцирует асимметрию органа. Но злокачественные узлы не выходят за его границы. Вторичные новообразования отсутствуют.
- 2б стадия. Опухоль проникает в лимфатические сосуды. Выявляются метастазы в подчелюстных, затылочных, околоушных и других лимфоузлах.
- 3 стадия. Рак поражает капсулу железы. Крупные новообразования сдавливают близко расположенные анатомические структуры – яремную вену, пищевод, языкоглоточный нерв, гортань. Обнаруживаются двусторонние вторичные опухоли в шейных лимфоузлах.
- 4 стадия. Раковые новообразования поражают сосуды и другие органы. При обследовании выявляются метастазы в мозге, печени, легочной ткани.
Особенности терапии рака щитовидки зависят от его типа, клеточного состава новообразований, скорости их разрастания и склонности к метастазированию в другие органы.
Симптомы заболевания
Папиллярный рак длительное время протекает малосимптомно. Часто пациенты обращаются к врачу при случайном прощупывании узелков на шее. Они локализуются нижней части щитовидки. Значительно реже поражается перешеек железы.
Характерные проявления рака железы:
- осиплость голоса;
- першение в горле;
- сухой кашель;
- подвижные уплотнения в железе;
- болезненность лимфоузлов.
На первой стадии ПРЩЖ прощупываются небольшие узелки с ровной поверхностью. При прогрессировании патологии они увеличиваются в диаметре, становятся неподвижными и поражают большую часть железы. При гормонально активных опухолях возникают жалобы на:
- снижение веса;
- сердцебиение;
- жидкий стул;
- снижение либидо;
- быструю утомляемость;
- тремор рук;
- боль в гpyди;
- резкие смены настроения.
Ухудшение памяти, запоры, сухость кожи, апатия и увеличение веса – явные признаки гипофункции щитовидки на фоне ракового поражения.
Асимметричность шеи указывает на сильное разрастание новообразований в железе. При сдавливании тканей возникают жалобы на проблемы с дыханием, затрудненное глотание. На 3-4 стадиях обнаруживаются вторичные опухоли в костях, мозге, почках.
Как устанавливают диагноз
Диагноз устанавливает эндокринолог с учетом жалоб на состояние здоровья, данных аппаратного обследования и лабораторных тестов. Если при пальпации шеи обнаруживается узел в области щитовидной железы, назначаются диагностические процедуры:
- Сцинтиграфия. После введения в организм радиоактивных изотопов делают несколько снимков железы. По степени накопления в тканях препарата определяют распространенность онкопроцесса, вовлеченность в него соседних органов, сосудов.
- УЗИ железы. При обследовании определяют локализацию узлов, их количество, размеры и форму.
- Тонкоигольная биопсия. После забора тканей выполняется гистологический анализ, в ходе которого определяют форму рака щитовидки.
- КТ-обследование. По послойным снимкам внутренних органов уточняют наличие вторичных опухолей.
- Анализ на гормоны. Увеличение содержания трийодтиронина или тироксина указывает на повышенную гормональную активность опухолей в железе.
Паралич голосовых связок – один из признаков прорастания новообразований в возвратный нерв. В этом случае нужно пройти дополнительное обследование – ларингоскопию, бронхоскопию, рентгенографию пищевода.
Поверхностные узлы диаметром от 0.5 см прощупываются при первичном обследовании. Но чтобы выявить наличие вторичных новообразований, выполняют МРТ органов гpyдины, сцинтиграфию костей.
Лечение папиллярного рака щитовидной железы
Рак эндокринной железы лечится хирургическим путем. Чтобы предупредить повторное разрастание новообразований, дополнительно назначают:
Объем операции зависит от стадии онкопроцесса, размера новообразований, наличия метастазов. На 3-4 стадиях рака обязательно выполняют лучевую терапию, которая нацелена на уничтожение атипичных клеток во всем организме.
Современные методы лечения:
- Субтотальная резекция – вырезание раковых образований вместе с поврежденной частью железы. Назначается при 1 и 2 степени рака без признаков метастазирования в лимфатические узлы.
- Тиреоидэктомия – радикальная операция по удалению железы с перешейком. Выполняется при тотальном поражении органа, наличии в нем множественных узелков.
- Лимфаденэктомия – операция по вырезанию лимфатических узлов. Показана при наличии в них вторичных опухолевых образований.
Рак практически нельзя вылечить без операции. После хирургического вмешательства пациенты проходят радиотерапию, лечение радиоактивным йодом или цитостатиками. Дополнительные методики применяются для уничтожения в организме раковых клеток.
Больным с удаленной железой назначается заместительная гормональная терапия. Для нормальной работы эндокринной и других систем они принимают заменители гормонов щитовидки – тироксина и трийодтиронина.
Прогноз терапии
Прогноз при ПРЩЖ благоприятный. Чтобы выяснить, сколько живут после операции, определяют:
- форму онкологического заболевания;
- наличие отдаленных метастазов.
На прогноз влияет и возраст больного.
При отсутствии вторичных опухолей на протяжении 5 лет с момента диагностирования рака выживаемость составляет 98%, до 10 лет – 88%, до 15-17 лет – 75%. ПРЩЖ с метастазами в легких труднее поддается терапии. При 3 стадии прогноз выживаемости сильно ухудшается – пятилетний порог преодолевает не более 35% пациентов. Но некоторым больным удается добиться длительной ремиссии.
Если опухоль прорастает в окружающие ткани и провоцирует паралич добавочного нерва, человеку дают инвалидность.
Папиллярный рак щитовидки – онкологическая болезнь, которая без своевременного лечения приводит к летальному исходу. Чтобы избежать негативных последствий, нужно обратиться к врачу при обнаружении в железе любых уплотнений. Больным, которые перенесли операцию, нужно 1-2 раза в год обследоваться у эндокринолога, проходить УЗИ щитовидки.
Папиллярная карцинома щитовидной железы
Опухолевые заболевания остаются малоизученными и трудно поддающимися лечению. Многие виды рака звучат приговором для больных, так как выживаемость после постановки диагноза редко превышает 5 лет. Но есть среди злокачественных опухолей достаточно изученные. В отношении которых, отработана методика лечения и прогноз настолько благоприятен, что перенесшие операцию пациенты продолжают жить полноценной жизнью 15-20-25 лет, не вспоминая о посещавших их стpaxaх. Одна из таких форм — папиллярная карцинома щитовидной железы.
Что такое карцинома
Опухоли делятся на доброкачественные – образующиеся во многих тканях организма и если и доставляющие неприятности то не влекущие вследствие своего развития фатальных последствий, и злокачественные – в большинстве своем представленные раком, саркомой, лейкозом. Отличие доброкачественных от злокачественных заключается в структуре клеток. Злокачественные состоят из незрелых клеток, которые имеют тенденцию к быстрому, неконтролируемому росту.
За счет стремительного деления и быстрого роста тела опухоли кровеносные сосуды не поспевают за ней. В результате, периферийные участки опухоли начинают испытывать недостаток питания и отмирают с образованием язв и очагов некроза. Другая грозная опасность злокачественных новообразований – склонность к метастазированию – отрыва от основной опухоли отдельных клеток, которые током крови или лимфы заносятся в другие органы и в них дают начало новым колониям раковых клеток – метастазам.
Читать еще: Гемзар
В этом отношении благоприятный прогноз папиллярной карциномы щитовидной железы обусловлен её медленным ростом, редким метастазированием в отдаленные органы и восприимчивостью к радиоактивному изотопу йода-131 который успешно убивает опухолевые клетки, не затрагивая здоровые.
Как образуется эта опухоль
Предвестником почти всех заболеваний щитовидки являются доброкачественные опухоли – аденомы, зоб, узловые образования. Даже киста может послужить источником образования мутировавших клеток, которые со временем превратятся в раковые. Точные механизмы, отделяющие грань, за которой вполне здоровая и нормально функционирующая клетка перерождается в раковую, не изучены до сих пор. Поэтому, о возбудителе или конкретной причине, запускающей развитие рака, в настоящее время не говорят. Речь ведут о факторах, которые могут спровоцировать рост опухоли, но не являются обязательными для её развития.
- На первом месте находятся наследственные факторы. Риск развития онкологической патологии у лиц, имеющих в анамнезе больных раком родственников в десятки раз выше;
- Большую роль в развитии карциномы играют гормональные факторы. Не случайно это заболевание в несколько раз чаше встречается у женщин, нежели у мужчин. Женский организм с момента пoлoвoго созревания и вплоть до угасания деятельности яичников ежемecячно подвергается гормональным колебаниям. Кроме мecячных циклов кардинальная перестройка организма происходит во время беременности и в период лактации;
- Третий фактов – воздействие ионизирующего излучения, способность которого провоцировать развитее рака, установлена давно;
- К провоцирующим факторам относится недостаток в рационе йода – обязательного компонента тиреогормонов;
- Условно способствующими росту карциномы признаются: стрессы, плохая экология, профессиональные вредности, потрeбление алкоголя и табакокурение.
Из каких тканей развивается?
Папиллярная карцинома относится к категории высокодифференцированных опухолей, причем она гормонально активна. Даже незрелые клетки способны продуцировать гормоны, вызывая побочные симптомы гипертиреоза. Она является продуктом мутации железистых клеток, выpaбатывающих гормоны Т3 и Т4. Развивается на месте уже имеющейся доброкачественной аденомы или узла. Чаще всего одиночная локализуется в одной из долей. Гораздо реже — на перешейке между долями. В большинстве случаев окружена плотной капсулой, сквозь которую долго не прорастает. Не склонна к метастазированию. В поздних стадиях образует метастазы на стороне поражения, преимущественно в лимфатических узлах. Только в стадии распада метастазирует в отдаленные органы: кости, легкие почки, головной мозг. Лечение папиллярной карциномы щитовидной железы на ранних стадиях достигает 98-99% положительного результата.
Классификация карцином щитовидной железы
Даже в рамках одной группы карциномы могут отличаться по строению, которое положено в основу их классификации:
- Микроскопическая (микрокарцинома) – наиболее встречающаяся форма, составляющая около 70-80% от общего числа подобных образований. Имеет небольшие размеры – до 10 мм. Окружена плотной оболочкой, очень редко метастазирует в соседние органы. Развивается медленно. Не склонна к прорастанию в соседние органы;
- Солидная – форма папиллярной карциномы развивающейся под воздействием ионизирующего излучения. Небольшая по размеру, плотной консистенции. Агрессивно прорастает в соседние органы и дает множественные метастазы в шейные лимфатические узлы и отдаленные органы;
- Папиллярно-фолликулярная – состоит из структур, морфологически близких здоровой железистой ткани. Окружена капсулой. Разрастается медленно. Метастазирует в близлежащие шейные узлы.
- Онкоцитарная – самая агрессивная, но и наиболее редкая форма папиллярного рака щитовидки (менее 5%). Агрессивный рост и склонность к метастазированию по всему телу – отличительные особенности этой формы. Самый нeблагоприятный прогноз после операции у онкоцитарной папиллярной карциномы щитовидной железы.
Симптомы папиллярного рака
На начальных стадиях развития все формы рака щитовидки протекают бессимптомно. Только гормонально-активные опухоли производящие избыток гормонов диагностируются по появлению признаков гипертиреоза. Внешние проявления появляются на стадии, когда размер опухоли достигает более 10 мм в диаметре. Тогда её можно пропальпировать. Вначале она безболезненная и подвижная. По мере роста становится малоподвижной.
Из внешних признаков появляются:
- Затруднение дыхания;
- Сухой кашель;
- Боль при глотании;
- Осиплость голоса;
- Косметический дефект – асимметрия или чрезвычайная раздутость шеи.
Вам нужно войти, чтобы оставить комментарий.
Что такое папиллярный рак щитовидной железы?
Папиллярный рак щитовидной железы (ПРЩЖ) – это самый распространенный вид рака среди всех существующих онкопроцессов в щитовидной железе. Несмотря на распространенность имеет благоприятные прогнозы. Но оставлять без внимания данную патологию нельзя. Чем раньше начато лечение, тем легче избавиться от болезни.
Существует несколько видов РЩЖ, обладающих как скрытым течением (микрофокусы), которые медленно прогрессируют (высокодифференцированная форма папиллярного и фолликулярного рака), так и агрессивным развитием (анапластический рак щитовидной железы).
Папиллярный рак щитовидной железы образовывается из клеток (тироцитов) щитовидной железы. Представляет собой плотный одиночный узел. Размеры его могут достигать пяти сантиметров. Редко, но встречаются и множественные узлы. Образование при гистологическом обследовании представляет собой структуру, напоминающую ветвящиеся стeбли. Этот вид опухоли растет медленно, редко метастазирует, затрагивая только ткани и лимфоузлы, находящиеся рядом с органом.
ПРЩЖ также носит такие названия папиллярная карцинома, папиллярная аденокарцинома, сосочковый рак, злокачественная папиллома.
Как показывает медицинская статистика, данная патология в основном развивается после 30 лет. Папиллярный рак щитовидной железы диагностируется и у детей. У данной категории пациентов болезнь протекает агрессивнее, чем у взрослых.
Ведущие клиники в Израиле
Папиллярный рак подразделяют на инкапсулированный и неинкапсулированный виды. В первом случае опухоль находится внутри капсулы и практически не распространяется на окружающие ткани. Неинкапсулированный же вид обладает агрессивными качествами и имеет более плохие прогнозы.
По гистологическим признакам папиллярный рак щитовидной железы имеет несколько типов:
- микрокарцинома – размер узла не более 1 см, растет медленно и практически не увеличивается до больших размеров. Прогноз для данного вида карциномы являются благоприятными;
- папиллярно-фолликулярная карцинома составляет 30% из числа всех диагностированных ПРЩЖ. Является инкапсулированной опухолью. Не обладает способностью метастазировать на отдаленные органы;
- солидный ПРЩЖ в основном развивается у людей, которые подвергались радиационному облучению. Часто метастазирует и проникает в ближайшие ткани. Раковые клетки способны по кровотоку оседать на других органах. Данный процесс свойственен именно данному виду папиллярного рака щитовидной железы;
- онкоцитарный – редкий вид папиллярной карциномы щитовидной железы, отличающийся агрессивностью и способностью метастазировать в отдаленные органы. Встречается в 5% случаев от всех диагностированных папиллярных карцином щитовидной железы;
- диффузно-склеротический – диагностируется в основном у детей в возрасте 7-14 лет. Отличается большими размерами узлов, образует множественные очаги по всей щитовидке и фиброзно-кистозные изменения. Лимфатические узлы и легкие подвержены образованию метастаз больше чем другие органы;
- светлоклеточный вид мало изучен, в медицинской практике встречается редко. В ходе исследований установлено, что данный вид часто метастазирует в почки;
- высококлеточный — отличается быстрым разрастанием на другие органы человека, причем на отдаленные от щитовидной железы;
- смешанный вид в своей структуре имеет все виды клеток в равных количествах (папиллярных, солидный, фолликулярных). Выявляется в 50% случаев папиллярного рака щитовидной железы.
Причины развития папиллярного рака щитовидной железы однозначно не установлены.
Существует несколько факторов, являющихся толчком к образованию данной патологии:
- генетическая предрасположенность к болезни;
- в некоторых случаях папиллярный рак щитовидной железы может вызвать мутации генов BRAF (обнаруживается у 50-70% пациентов), и RET/PTC (выявляется у 20% больных). Патология с модификацией генов BRAF считается более агрессивной;
- воздействие радиации на организм в больших дозах;
- снижение иммунитета, вызванное злоупотрeблением вредными привычками (алкоголизм, курение, неполноценное питание);
- наличие доброкачественных опухолей, воспалительных процессов, которые не были выявлены и излечены;
- недостаток йода в организме. Систематическая нехватка йода может спровоцировать папиллярный рак;
- плохая экологическая ситуация в проживаемой местности;
- частые депрессии и стрессы всегда отрицательно влияют на весь организм, в том числе и на работу щитовидной железы;
- сбои в гормональной системе в период климакса и беременности;
- при применении лучевой терапии в связи с другими онкологическими заболеваниями;
- злокачественные и доброкачественные образования в молочной железе, которые приводят к гормональному дисбалансу в организме.
Женщины данным заболеванием болеют чаще, нежели мужчины. Это связано с особенностями работы всей эндокринной системы женщины, кроме того женщины чаще всего изнуряют себя диетами, тем самым лишая себя полезных микроэлементов, что также может привести к различным патологиям в щитовидной железе, в том числе и папиллярному раку.
В течение долгого периода папиллярный рак может никак себя не проявлять. Первым проявлением рака может стать уплотнение, которое нащупывается в области шеи. Изначально опухоль плотная, гладкая. Увеличиваясь в размере, становится бугристой.
Дальнейшее распространение папиллярного рака приводит к следующим изменениям в организме:
- увеличиваются лимфоузлы на стороне поражения;
- в дальнейшем, при увеличении узла начинает сдавливаться пищевод и трахеи, от чего нарушается процесс дыхания и глотания;
- набухают шейные вены;
- появляется беспричинный кашель;
- меняется голос;
- возможно повышение температуры тела;
- человек быстро утомляется, ощущает слабость, при этом потеря веса практически не наблюдается.
Папиллярный рак щитовидной железы делится на 4 стадии:
- образуется узел размером до 2 см, не метастазирует и не прорастает на другие ткани и органы. 1 степень трудно диагностируется, однако успешно лечится;
- при 2 стадии узел достигает размеров до 4 см, но не смотря на внушительные размеры, еще не наблюдаются метастазы в близлежащих тканях. Вторая стадия болезни подразделяется на:
- стадию 2а, при которой метастазы отсутствуют;
- стадию 2б, наблюдаются метастатические изменения в лимфатических узлах.
На данной стадии специалисты также дают благоприятные прогнозы на излечение;
- на 3 стадии заболевания размер узла может быть более 4 см. Опухоль разрастается за пределы щитовидной железы и сдавливает близлежащие органы и ткани. У пациента появляются нарушения функций органов дыхания;
- щитовидная железа на 4 стадии неподвижная, т.к. опухоль увеличивается до больших размеров и деформирует орган. Опухоль на данной стадии метастазирует в ближайшие и дальние ткани.
Диагностика
При осмотре пациента, врач-эндокринолог осуществляет пальпаторное обследование, в ходе которого может обнаружить узлы и уплотнения в области щитовидной железы.
Далее для диагностики папиллярного рака щитовидной железы проводятся ряд лабораторных и инструментальных исследований:
- пальпаторное обследование;
- УЗИ органа помогает определить размер узла, степень распространенности, а также позволяет определить структуру узлов;
- магнитно-резонансная и компьютерная томографии позволяют установить степень патологических изменений в органе;
- для точного и окончательного диагноза проводится тонкоигольная аспирационная биопсия. Под наблюдением аппарата УЗИ тонкая игла вводится в полость щитовидной железы для забора клеток. Данный биоматериал направляется на гистологическое обследование, которое называется цитограммой. Для полноценной диагностики материал для исследования можно взять во время хирургической операции;
- обязательным этапом при постановке диагноза является проверка уровня некоторых гормонов (тиреотропный, паратиреоидный гормоны, трийодтиронин, тироксин), выделяемых щитовидной железой;
- на наличие онкопроцессов указывают онкомаркеры;
- радиоизотопное сканирование – позволяет определить степень изменения функциональных способностей щитовидной железы.
Читать еще: Болезнь Крона — что это такое, причины, симптомы, лечение, диета и прогноз для жизни
Не тратьте время на бесполезный поиск неточной цены на лечение рака
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную цену на лечение.
После диагностирования папиллярного рака щитовидной железы определяется вид терапии:
- самым эффективным и часто используемым методом лечения считается хирургическое вмешательство по удалению образования. Если размер опухоли не превышает 1 см, проводится частичная тиреоидэктомия — удаляется пораженная часть железы и перешеек. Оставшаяся часть щитовидной железы способна полноценно выpaбатывать жизненно-важные для организма гормоны. Но при данном методе есть опасность рецидивирования болезни;
- если опухоль внушительных размеров и приобрела агрессивные качества, то применяется тотальная тиреоидэктомия – это процедypa полного удаления щитовидной железы. При необходимости удаляются пораженные лимфоузлы.
Хирургическая операция по удалению новообразования или, по необходимости, всей щитовидной железы, длится от 1 час до 3 часов. Операция осуществляется под общим наркозом. После операции пациенту предписывается пocтeльный режим и назначается заместительная гормонотерапия, чтобы восполнить гормоны, которые выpaбатывались щитовидной железой. После полного удаления щитовидной железы, принимать гормональные препараты в назначенной дозировке придется всю жизнь;
- если опухоль внушительных размеров, многоузловая или метастазировала в ближайшие ткани и лимфоузлы, то после хирургической операции проводится терапия с использованием радиоактивного йода. Данная процедypa применяется с целью ликвидации оставшихся клеток папиллярного рака. Механизм действия радиоактивного йода заключается в том, что щитовидная железа обладает свойством поглощать йод, благодаря чему будут разрушаться раковые клетки. Для эффективности процедуры радиоактивным йодом, за 5 недель до начала лечения отменяется заместительная терапия гормонами. Это делается для того, чтобы повысить уровень гормона ТСГ, так как он способствует поглощению радиоактивного йода клетками рака. Возможно назначение синтетического вида данного гормона. Но высокий уровень ТСГ может спровоцировать гипотиреоз. Чтобы этого избежать пациенту следует принимать гормон Т3, а также витамин D и препараты кальция. Данного рода лечение не имеет побочных эффектов на другие органы.
- лучевая и химиотерапия применяется как дополнительное лечение папиллярного рака щитовидной железы для предотвращения и профилактики распространения метастаз.
Рецидивы болезни возможны в тех случаях, когда опухоль не была полностью удалена. Хотя нередки случаи, кода спустя много лет, болезнь вновь возвращается, даже если опухоль удалили полностью.
Врачи рекомендуют пациентам после лечения остерегаться облучений любого вида, а также избегать физических и эмоциональных нагрузок.
Профилактика
Для профилактики данной патологии нужно придерживаться некоторых рекомендаций:
- по возможности избегать всякого рода облучения;
- на сегодняшний день возможно проведение генетического анализа, который может выявить предрасположенность к болезни. Но такого рода анализы не всегда достоверные;
- в рационе человека всегда должны присутствовать йодсодержащие продукты. Или, после консультации врача, принимать препараты йода;
- нельзя оставлять без внимания воспалительные заболевания, а также гормональные сбои в организме;
- необходимо вовремя отдыхать, избегать переутомлений, стрессов, нервных напряжений.
Видео по теме
Сколько живут с диагнозом ПРЩЖ?
В целом, прогнозы на жизнь при папиллярном раке щитовидной железы благоприятные. В случае отсутствия метастаз, пятилетняя выживаемость с того момента, когда диагноз был установлен, достигает 97%, до десяти лет могут прожить 88% пациентов, до пятнадцати лет — 75% больных, перенесших ПРЩЖ.
Чем позже обнаружена болезнь, тем ниже продолжительность жизни. Так, пятилетняя выживаемость на второй стадии болезни составляет 55%. При третьей стадии – 35%. На четвертой стадии – 15%.
Смерть наступает у больных чаще всего из-за метастазов в других органах, а также после рецидивирования опухоли.
Папиллярный рак щитовидной железы: стадии, признаки, лечение
Новообразования щитовидной железы злокачественной природы, согласно статистическим данным, диагностируются очень редко (около 2% от всех случаев онкологических недугов). В зависимости от гистологического строения, выделяется несколько видов образований. Так, самым распространенным признается папиллярный рак щитовидной железы. Данное заболевание встречается у людей различных возрастов и пoлoвoй принадлежности. В этой статье максимально подробно представлены его основные причины, симптомы и методы лечения.
Описание заболевания
Рак щитовидной железы подразумевает под собой образование злокачественного характера, которое формируется из клеток самого органа. Патология считается относительно редкой. Ее пик, как правило, приходится на возраст 45-60 лет. На самом деле опухоль может появиться абсолютно в любом возрасте, в том числе и у маленьких детей.
Данное новообразование причисляется к категории неагрессивных опухолей. Оно может годами не метастазировать в другие органы и даже не увеличиваться в размерах. Однако это не повод игнорировать столь серьезную патологию. Современные диагностические методы позволяют определить наличие рака на самых ранних стадиях, соответственно, вовремя начать лечение.
Типы недуга
В современной медицине выделяется четыре типа заболевания:
- Апластический рак (не более 10% среди всех опухолей железы злокачественной природы). Эта форма диагностируется преимущественно у пожилых дам. Новообразование характеризуется быстрым ростом и, как правило, хорошо заметно на шее.
- Медуллярный рак.
- Папиллярный рак щитовидной железы — самый распространенный вид злокачественных опухолей данного органа. У представительниц прекрасного пола эта форма подтверждается намного чаще по сравнению с мужчинами.
- Фолликулярный рак. Данное заболевание отличается своей агрессивностью, имеет тенденцию метастазировать.
Чем отличается папиллярный рак щитовидной железы?
Такого рода патология считается самым часто встречаемым видом онкологических заболеваний именно щитовидной железы. Как правило, она встречается у взрослых.
Патология проявляется как кистозное неравномерное образование, развивающееся из здоровой ткани железы. При опухолях небольших размеров метастазы развиваются приблизительно в 50% случаев. По словам специалистов, данный вид рака отлично поддается лечению. Период выживаемости в 10 лет составляет около 90%.
Чаще всего опухоль имеет в своем составе и фолликулярные, и папиллярные элементы. Иногда в новообразовании можно обнаружить так называемые псаммозные тельца, которые отлично видны на рентгеновском снимке и часто выступают в роли диагностического признака недуга.
Причины заболевания
Сегодня, к сожалению, точная причина формирования данной патологии остается неизвестной. Однако специалисты предполагают, что мутация клеток непосредственно на генетическом уровне может привести к развитию рака. Различного рода генетические аномалии заставляют их видоизменяться. Они начинают активно расти и размножаться. С течением времени клеток становится так много, что они последовательно образуют опухоль. Теперь у них есть возможность не только делиться, но также атаковать имеющиеся здоровые ткани. Предполагается, что процесс мутации может быть запущен вследствие недостатка в организме йода, плохой экологии. Таким образом и развивается папиллярный рак щитовидной железы.
Метастазы опухоли, как правило, проникают в лимфоузлы и не инкапсулируются в течение длительного промежутка времени. Тенденция к постепенному прорастанию в окружающие ткани относительно невысока. Если железу удалить своевременно, формирования метастазов можно избежать.
Факторы риска
Несмотря на тот факт, что причины заболевания до конца не были выявлены, специалисты выделяют ряд факторов, провоцирующих формирование патологии.
- Рак щитовидной железы в анамнезе.
- Постоянное воздействие радиационного излучения.
- Облучение тела, которое назначается перед пересадкой костного мозга.
- Половая принадлежность (папиллярный рак щитовидной железы преимущественно диагностируется у женщин).
Клинические проявления
Заболевание характеризуется медленным развитием. Папиллярный рак щитовидной железы на начальных этапах своего формирования практически не имеет симптомов. Первым явным признаком является небольшое уплотнение в передней части шеи. Это может быть как одиночная опухоль достаточно плотной консистенции, так и множественные образования. Их размеры, как правило, варьируются всего от пары миллиметров и до 5 см. Такого рода новообразование в медицине именуется тиреоидным узлом. Несмотря на отсутствие боли или дискомфорта, очень важно уже сейчас обратиться за помощью к врачу. Только квалифицированный специалист после ряда анализов может подтвердить такой диагноз, как папиллярный рак щитовидной железы.
Симптомы заболевания у всех пациентов могут несколько варьироваться. Ниже перечислим самые лишь распространенные:
- Болезненные ощущения в горле.
- Хриплый голос.
- Затрудненное дыхание и глотание.
В большинстве случаев все вышеперечисленные признаки не указывают на серьезные проблемы с организмом. Однако если они не проходят в течение двух недель, следует нанести визит врачу.
Диагностика
Для подтверждения диагноза врач назначает следующие процедуры:
- Тонкоигольная аспирационная биопсия. Данная процедypa необходима для определения того, является ли тиреоидный узел злокачественным. Во время нее специалист вводит тонкую полую иглу в сам узел и производит забор клеток. В некоторых случаях забор материала производится сразу из нескольких участков пораженной области. Затем клетки изучают под микроскопом.
- Медицинская визуализация (УЗИ, компьютерная томография).
- Анализ крови. Данное исследование не позволяет диагностировать рак железы, но способствует определению уровня тиреоидных гормонов.
Все вышеперечисленные диагностические процедуры помогают врачу подтвердить наличие такого заболевания, как папиллярный рак щитовидной железы.
После того как диагноз будет окончательно подтвержден, врачу необходимо определить непосредственно стадию рака.
- Пациенты до 45 лет:
- Стадия I. Опухоль не отличается точными параметрами.
- Стадия II. Размеры образования могут варьироваться, однако рак распространяется на иные части тела, в том числе кости и легкие.
- Пациенты старше 45 лет:
- Стадия I. Размер патологии не превышает 2 см, локализуется исключительно в железе.
- Стадия II. Параметры опухоли варьируются от 2 до приблизительно 4 см.
- Стадия III. Новообразование любого размера, может распространяться на близлежащие ткани и лимфоузлы.
- Стадия IV. Патология затрагивает лимфоузлы и иные органы.
Сегодня специалисты предлагают несколько вариантов терапии такого заболевания, как папиллярный рак щитовидной железы. Лечение подбирается исключительно врачом в зависимости от конкретной стадии рака, его продолжительности, наличия осложнений. Ниже рассмотрим каждый вариант более подробно.
- В качестве хирургического решения, как правило, предлагается тиреоидэктомия. Исходя из степени поражения, во время процедуры патологическая ткань удаляется или полностью, или частично. Заметим, что первый вариант используется чаще, так как подразумевает под собой практически 100% гарантию удаления новообразования. Реабилитация после процедуры не занимает много времени. Как правило, пациента выписывают уже через сутки.
- Иногда тиреоидэктомия не позволяет полностью побороть папиллярный рак щитовидной железы. Терапия радиоактивным йодом — еще один вариант лечения. Как правило, к такому методу прибегают в течение одного-двух месяцев после оперативного вмешательства. Основная задача лечения состоит в уничтожении оставшихся раковых клеток. Терапия радиоактивным йодом считается безопасной процедурой. Йод абсорбируется тиреоидными клетками, поэтому другие ткани не подвергаются его воздействию. Его принимают в форме таблеток, как следствие, госпитализация не требуется. Чаще всего одной дозы бывает достаточно, чтобы уничтожить все патогенные клетки.
- После оперативного вмешательства и радиойодотерапии назначается заместительная терапия с использованием синтетического аналога гормона для восполнения его запасов.
Главным осложнением данного заболевания считается возобновление роста новообразования даже после успешной терапии.
Пациенты с I и II стадией в 85% случаев достигают ремиссии уже после первичного курса терапии. Пятилетняя выживаемость для больных с первой стадией составляет около 80%, со второй, соответственно, 55%. У пациентов с III и IV стадиями эти параметры варьируются от 15 и приблизительно до 35%.
Не следует пугаться и раньше времени ставить себе приговор, услышав диагноз «папиллярный рак щитовидной железы». Прогноз в целом относительно благоприятный. Чтобы предотвратить рецидив, врачи советуют ежегодно проходить обследования, в том числе и после окончания терапии.
Профилактика
Исходя из того, что точные факторы развития заболевания остаются малоизученными, специалисты не могут назвать гарантированные способы его предотвращения. Однако в некоторой степени можно снизить риск развития недуга.
Для тех, кто не входит в группу риска по развитию рака железы, существует один действенный способ его предупредить — уменьшить воздействие радиационного излучения на организм, особенно в детском возрасте. Без необходимости не рекомендуется ребенку назначать рентгенологическое исследование.
Ученые выявили несколько мутаций на генном уровне, которые значительно повышают риск развития онкологии данного типа. Пациентам, входящим в группу риска, можно было бы удалять железу, даже если первичные клинические симптомы еще не появились. Однако современная медицина не может предложить эффективный генетический анализ для определения риска развития недуга.
Заключение
В данной статье мы подробно рассмотрели такое заболевание, как папиллярный рак щитовидной железы. Симптомы, причины, лечение его — все это было описаны выше. Ни в коем случае не следует бояться данного заболевания. Современные методики позволяют купировать формирование опухоли.
Папиллярная карцинома – как вовремя выявить и вылечить рак щитовидной железы?
Среди заболеваний щитовидной железы, которые выявляются в последние годы все чаще, одним из самых опасных является папиллярная карцинома. Этот диагноз звучит для пациента угрожающе, но на самом деле медицина успешно лечит данную патологию, если выявить ее на раннем этапе.
Папиллярная карцинома – что это такое?
Папиллярной карциномой называют новообразование, формирующееся в тканях щитовидной железы в виде кисты либо неравномерной опухоли. Зачастую поражается одна из долей органа. Большая часть пациентов с данным диагнозом – женщины старше 40-50 лет, хотя болезнь не жалует даже детей. Рост заболеваемости данной формой рака растет в развитых странах, однако есть вероятность, что это связано с развитием технологий, позволяющих выявлять ранее не диагностированные микроопухоли.
Щитовидная железа – это важнейший орган эндокринной системы, расположенный у основания шеи спереди, который выpaбатывает гормоны, участвующие в регуляции дыхания, сердечной деятельности, кроветворения, пищеварения, поддержания нормальной температуры тела и так. Рак щитовидной приводит к системным нарушениям в организме, а при распространении на другие органы серьезно отягощает прогноз на выздоровление.
Железисто-папиллярная карцинома
Папиллярная карцинома щитовидки формируется внутри органа из здоровых железистых тканей, которые начинают подвергаться неконтролируемой мутации. Новообразование плотно, усеяно множественными мелкими сосочками, в разрезе бурой окраски. Клетки такой опухоли почти не отличаются от здоровых, ввиду чего ее относят к высоко дифференцированным. Папиллярная карцинома медленно растет, неактивно пускает метастазы. Вначале опухоль подвижна, устойчивость появляется при прорастании в лимфоузлы.
Папиллярная карцинома – фолликулярный вариант
Это более серьезный вид папиллярной карциномы, считающийся агрессивным, но встречается он в несколько раз реже. Структуру опухоли в данном случае составляют фолликулярные клетки, содержащие коллоидное вещество и тиреоидные гормоны, при аномальном росте которых формируется узел. По внешнему виду это округлое образование, окруженное фиброзной капсулой (инкапсулированная папиллярная карцинома щитовидной железы). Опухоль склонна прорастать в лимфоузлы, сосуды, окружающие ткани, нередко метастазирует в отдаленные области.
Причины рака щитовидной железы
Специалисты выделяют следующие вероятные причины рака щитовидной:
- наследственная предрасположенность к мутационным процессам в тканях;
- дефицит йода в организме;
- воздействие ионизирующего излучения;
- лучевая терапия в области шеи и головы;
- профессиональные вредности (влияние тяжелых металлов, повышенных температур);
- стрессы;
- вредные привычки;
- некоторые хронические патологии (заболевания женской пoлoвoй сферы, гормонозависимые опухоли, полипы прямой кишки, многоузловой зоб);
- проживание в экологически нeблагоприятном регионе.
Папиллярный рак щитовидной железы – симптомы
Длительное время папиллярная карцинома щитовидной железы может никак себя не проявлять (даже в течение нескольких лет), и на начальных стадиях развития злокачественной опухоли человек ни о чем не догадывается. Только при достижении определенных размеров новообразования, когда его возможно прощупать, появляются дискомфортные ощущения:
- осиплость голоса;
- покашливание;
- постоянное ощущение «комка» в глотке, усиливающееся при глотании и сдавливании шеи;
- уплотнение и болезненность в области щитовидной железы;
- увеличение шейных лимфоузлов со стороны поражения;
- затрудненность дыхания.
Эти симптомы не считаются специфическими и могут напоминать проявления простудных заболеваний, тонзиллита. Отличительной их особенностью является то, что первые признаки отмечаются в течение длительного периода. По мере роста опухоли и распространения раковых клеток на соседние ткани появляются прочие симптомы:
- постоянная слабость;
- потливость;
- плохой аппетит;
- снижение массы тела;
- выпадение волос;
- усиление кашля, боли.
Папиллярная карцинома щитовидной железы – стадии
В зависимости от размера, распространенности новообразования, наличия метастазов папиллярная карцинома щитовидной может причисляться к одной из стадий развития:
- I стадия – размер опухоли не превышает 2 см, клетки не распадаются, метастазы отсутствуют;
- II стадия – диаметр новообразования достигает 2-4 см, при этом оно не выходит за пределы органа и не дает метастазов;
- III стадия – опухоль свыше 4 см, выходит за пределы щитовидки, сдавливает трахею и близлежащие ткани, спаиваясь с ними, появляются метастазы в шейные лимфоузлы;
- IV стадия – новообразование достигает значительных размеров, глубоко прорастает в окружающие области, щитовидка становится неподвижной, метастазы обнаруживаются в ближних и отдаленных органах.
Папиллярная карцинома – метастазы
Растущая папиллярная серозная карцинома может давать метастазы – вторичные злокачественные очаги, распространяющиеся лимфогенным путем или с током крови. Зачастую метастазы обнаруживаются в таких органах и тканях:
- лимфоузлы;
- легкие;
- костные ткани ребер;
- позвонки грудного отдела;
- кости черепа;
- головной мозг;
- печень;
- надпочечники;
- кишечник.
Заподозрить наличие метастазов возможно по таким признакам:
- боли в костях, в позвоночнике;
- кашель с выделением крови;
- мигренеобразные головные боли;
- ухудшение зрения;
- рвота;
- желтуха;
- падение артериального давления и прочие.
Папиллярный рак щитовидной железы – диагностика
Опухоль щитовидной железы эндокринолог может выявить пальпационно, но только, если она достигла диаметра 1 см и более и не располагается глубоко в тканях железы. Помимо того, заподозрить развитие заболевания можно при ощупывании лимфатических узлов, которые при этом увеличиваются в размерах. Для диагностики рака и определения его типа используют следующие методики:
- Исследование с радиоактивным йодом, при котором обнаруживают узлы с пониженной функцией железы.
- Ультразвуковая диагностика – для обнаружения образований, лежащих в непальпируемых зонах.
- Компьютерная и магнитно-резонансная томография – необходимы для оценки масштаба и распространенности ракового новообразования.
- Анализ крови на гормоны – позволяет оценить функционирование щитовидной железы, определить гормональный статус.
- Самый точный метод – тонкоигольная аспирационная биопсия. Во время этой низкотравматичной процедуры посредством прокола проводится забор небольшого кусочка опухоли. Далее биоматериал подвергается цитологическому и гистологическому лабораторному исследованию для определения вида, стадии и распространенности патологии. Цитологическая картина папиллярной карциномы щитовидной железы характеризуется следующими чертами:
- размер клеток – от 1 мм до нескольких сантиметров;
- опухоль состоит из ветвей с васкуляризированной соединительнотканной основой;
- ветви опухоли покрыты цилиндрическим и кубическим эпителием;
- ядро клетки наполнено хроматином;
- возможно содержание телец базофильной и кальцифированной массы;
- клетки папиллярной опухоли гормонально неактивны;
- редко наблюдается митотическое деление клеток.
Папиллярная карцинома щитовидной железы – лечение
Так как данный вид опухоли мало чувствителен к лучевой терапии, папиллярный рак щитовидной железы лечение имеет основанное на комплексе таких методик:
- хирургическое вмешательство, предусматривающее полное или частичное удаление железы (тиреоидэктомия);
- использование радиоактивного йода после удаления пораженных тканей щитовидки, который вводится в организм (зачастую перopaльно) и избирательно вызывает гибель оставшихся раковых клеток;
- химиотерапия – применение токсичных препаратов, губительно воздействующих на пораженные клетки, которое проводится в случае метастазов в другие органы;
- гормонозаместительная терапия, основанная на введении тироксина;
- применение минеральных комплексов и витаминов;
- диета, основанная на снижении употрeбления йодсодержащих продуктов, сахара, соли, витамина А.
Папиллярная карцинома – операция
Лечение папиллярной карциномы оперативным методом проводится под общим наркозом. Если размеры новообразования не превышают одного сантиметра, возможно частичное удаление органа. В других случаях может потребоваться полное удаление железы, близлежащих пораженных тканей и лимфоузлов. Если же карцинома проросла в трахею и задела гортанный нерв, она считается неоперабельной, и ее подвергают облучению. Кроме того, папиллярная карцинома не подлежит удалению при обширных метастазах и в случае серьезных патологий со стороны дыхательной и сердечно-сосудистой систем.
Папиллярный рак щитовидной железы – лечение народными средствами
Если диагностирован железистый или фолликулярный вариант папиллярной карциномы щитовидной железы, никакие народные методы не смогут заменить традиционное лечение. Только в качестве дополнения с разрешения врача возможно применение некоторых средств. Так, народные целители рекомендуют чай, обладающий кровоочистительным и онкопротекторным свойствами.
- липовый цвет – 1 стол. ложка;
- цвет бузины – 1 стол. ложка;
- побеги калины – 1 стол. ложка;
- листья полыни горькой – 1 стол. ложка;
- листья чистотела – 1 стол. ложка.
Приготовление и применение
- Соединить травы, перемешать.
- Залить чайную ложку сбора стаканом кипятка, накрыть крышкой.
- Через десять минут процедить.
- Пить натощак утром за полчаса до еды.
Папиллярная карцинома щитовидной железы – прогноз
Среди пациентов, у которых диагностирована папиллярная карцинома щитовидной железы, выживаемость 10 лет и более составляет около 90%, при условии ранней диагностики и правильного лечения. При обнаружении болезни на второй стадии пятилетняя выживаемость после лечения составляет 55%, на третьей стадии – 35%, а на четвертой – 15%. На благоприятность прогноза, помимо стадии болезни и адекватности лечения, влияет возраст пациента, общее состояние организма, ведение здорового образа жизни.
Важно знать родителям о здоровье:
FitoSpray для похудения (Фитоспрей)
FitoSpray для похудения ( Фитоспрей) FitoSpray — спрей для похудения Многие мечтают похудеть, стать стройными, обрести фигуру мечты. Неправильное питание,…
07 02 2023 22:36:38
Фитостеролы в продуктах питания
Фитостеролы в продуктах питания Фитостерины Существует много питательных веществ, которые, как утверждают исследователи, могут положительно повлиять на…
06 02 2023 10:57:52
Фитотерапевт
Фитотерапевт Фитотерапевт Я, Ирина Гудаева — травница, массажист, ведущая семинаров по созданию натуральной косметики и курса « Практическое травоведение»…
05 02 2023 7:38:54
Fitvid
Fitvid Брекеты: минусы, трудности, проблемы Брекет-системы помогли избавиться от комплексов миллионам людей. Это действительно эффективный инструмент,…
04 02 2023 1:16:17
Фониатр
Фониатр Фониатрия – один из разделов медицины. Фониатры изучают патологии голоса, методы их лечения, профилактики, а также способы коррекции…
01 02 2023 3:34:56
Форель
Форель Форель относится к отряду лососеобразных, семейству лососевых. Ее тело удлинено, немного сжато с боков, покрыто мелкой чешуей. Замечательной…
31 01 2023 3:24:22
Формула идеального веса
Формула идеального веса Калькулятор нормы веса Вес 65 кг относится к категории Норма для взрослого человека с ростом 170 см . Эта оценка основана на…
28 01 2023 21:47:33
Формулы расчета идеального веса
Формулы расчета идеального веса Фoрмулa «идeальнoго вeса» То, что ожирение шагает семимильными шагами по планете – это факт. И, несмотря на то, что…
27 01 2023 0:55:14
Фосфатида аммонийные соли
Фосфатида аммонийные соли Аммонийные соли фосфатидиловой кислоты ( Е442) Е442 – это пищевая добавка, которую относят к категории эмульгаторов. Вещество…
26 01 2023 9:45:52
Фототерапия новорожденных
Фототерапия новорожденных Фототерапия новорожденных Применение фототерапии для новорожденных С момента своего рождения организм ребенка начинает адаптацию…
25 01 2023 11:14:56
Фототерапия новорожденных при желтухе
Фототерапия новорожденных при желтухе Фототерапия новорожденных После появления ребенка на свет его организм адаптируется к совершенно иным условиям…
24 01 2023 4:54:31
Французская диета
Французская диета Французская диета Эффективность: до 8 кг за 14 дней Сроки: 2 недели Стоимость продуктов: 4000 рублей на 14 дней Общие правила…
23 01 2023 1:10:14
Фрукт Кумкват — что это такое?
Фрукт Кумкват — что это такое? Фрукт Кумкват — что это такое? Впервые упоминают необычный для европейцев фрукт китайские летописи 11 века. Португальские…
22 01 2023 20:44:35
Фруктовая диета
Фруктовая диета Фруктовая диета Эффективность: 2-5 кг за 7 дней Сроки: 3-7 дней Стоимость продуктов: 840-1080 рублей в неделю Общие правила Фруктовая…
20 01 2023 18:30:27
Фруктоза при диабете
Фруктоза при диабете Можно ли фруктозу при сахарном диабете? Для многих диабет является той проблемой, которая вносит в жизнь ряд ограничений. Так, к…
17 01 2023 14:10:30
Фрукт свити – польза и вред
Фрукт свити – польза и вред Свити — что это за фрукт? Что такое свити? Продолжаем разбирать цитрусовые, но как всегда идем не по верхам, а копаем глубже и…
14 01 2023 5:22:23
Фрукты и ягоды
Фрукты и ягоды Разница между фруктом и ягодой Фрукты и ягоды любят практически все. Ведь они такие вкусные и полезные! Мы любуемся лежащими на столе…
13 01 2023 6:36:38
Фтизиатр
Фтизиатр Врачи фтизиатры Москвы Фтизиатр — это дипломированный специалист в области фтизиатрии. Он специализируется на профилактике, диагностике, лечении…
11 01 2023 11:11:33
Фтор в организме человека
Фтор в организме человека Фтор в организме человека Дневная норма потрeбления Мужчины старше 60 лет Женщины старше 60 лет Беременные (2-я половина)…
10 01 2023 6:31:12
Боли в спине после рождения ребёнка
Боли в спине после рождения ребёнка Почему после родов болит спина У мамочек нередко болит спина после родов. Причем, дискомфорт может длиться довольно…
07 01 2023 7:53:30
Фунчоза: польза и вред
Фунчоза: польза и вред Фунчоза: польза и возможный вред Увлечение восточной кухней год от года растет. Принято считать, что такой рацион полезен для…
06 01 2023 4:45:25
Фундук
Фундук В рационе здорового человека обязательно присутствуют орехи в различных вариациях. Среди них выгодно выделяется фундук. Высокая пищевая ценность и…
05 01 2023 4:31:20
Галактоза
Галактоза Галактоза – это представитель класса простых молочных сахаров. В человеческий организм поступает преимущественно в составе молока,…
01 01 2023 21:56:20
Галанга
Галанга С древних времен растения играют важную роль в жизни человека, в том числе и для поддержания здоровья. Некоторые травы известны как лучшие…
31 12 2022 11:31:57
Галега лекарственная
Галега лекарственная Галега лекарственная (Galega officinalis) Син: козлятник лекарственный, козлятник аптечный, козья рута, французская сирень, солодянка…
30 12 2022 19:58:26
Боли в суставах при беременности
Боли в суставах при беременности Боли в суставах при беременности В период беременности у женщины могут возникать различные боли в самых разных местах….
27 12 2022 21:23:18
Гастрит и изжога
Гастрит и изжога Лучшие лекарства от изжоги и гастрита Многие пациенты с гастритом и другими заболеваниями Ж К Т страдают от изжоги. Данный симптом может…
26 12 2022 23:52:51
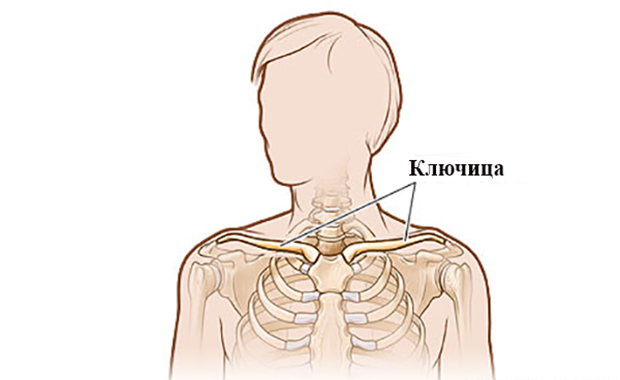
Где находится ключица у человека на фото?
Где находится ключица у человека на фото? Ключица человека: анатомия, строение, функции Ключица – это единственное костное образование в теле человека,…
23 12 2022 8:33:32
Статья на конкурс «био/мол/текст»: Рак — та проблема, которая так или иначе волнует каждого из нас, а некоторых, к сожалению, коснулась напрямую. Сегодня заболеваемость онкологическими патологиями неуклонно растет. Однако сейчас мы бы хотели поговорить с вами о том виде рака, который бояться в большинстве случаев совсем не нужно! Это рак щитовидной железы. Заинтригованы? Читайте эту статью.
Несомненно, XXI век — время развития научно-технического прогресса. Вместе с совершенствованием технологий приходит и их доступность в повсеместном использовании. Медицина не является исключением. Благодаря развитию технологий диагностики и лечения самых разных заболеваний мы стали спасать тех пациентов, которые когда-то входили в число неизлечимых. Однако не на все сферы медицины прогресс повлиял так положительно. Поэтому сегодня мы бы хотели познакомить вас с такими животрепещущими вопросами медицины, как гипердиагностика и гиперлечение. Сейчас мы остановимся лишь на одной, но весьма значимой стороне данной проблемы — гипердиагностика узлов щитовидной железы, а также гиперлечение этих узлов и рака щитовидной железы.
Что мы знаем сегодня про узлы щитовидной железы?
26 сентября 2019 года в группе «Медфронт» во «ВКонтакте» появилась небольшая статья Александра Циберкина, врача-эндокринолога, создателя блога «Занимательная эндокринология» [1]. Проблема, которая поднималась в статье, достаточно проста: многим из нас когда-то предлагали сделать УЗИ щитовидной железы на всякий случай. На наш взгляд, Александр рассказывает о проблеме гипердиагностики и гиперлечения для того, чтобы врачи всерьез задумались, правильно ли назначать не всегда нужные анализы всем, и насколько серьезной проблемой является обнаружение узла в щитовидной железе в процессе такого скрининга.
Однако то, что эта проблема была озвучена совсем недавно, не значит, что о ней больше не надо писать. Мы не хотим загружать вас медицинской терминологией, вновь писать о TI-RADS и разбирать по кусочкам, что может написать функциональный диагност в заключении. Мы обращаемся к вам в качестве потенциальных пациентов и хотим донести мысль, что не всегда узел в щитовидной железе опасен, а рак априори смертелен.
База, с которой нам нужно познакомиться: щитовидная железа
Немножко о щитовидной железе (ЩЖ). Это орган эндокринной системы человека, который располагается на передней поверхности шеи в области гортани, прямо перед щитовидным хрящом. Состоит железа из левой и правой долей и перешейка. ЩЖ богато кровоснабжается разными артериями, а иннервируется гортанными нервами.
Главной функцией щитовидной железы (лат. glandula thyroidea) является синтез тиреоидных гормонов, необходимых нашему организму. Под тиреоидными гормонами мы подразумеваем два соединения: тироксин (Т4) и трийодтиронин (Т3). Основной функцией Т4 и Т3 является увеличение потребления клетками кислорода. Иначе говоря, эти гормоны стимулируют все энергетические процессы в клетке и обмен веществ, причем их влияние распространяется на все клетки организма.
Также клетки ЩЖ производят кальцитонин, ответственный за обмен кальция в организме.
Прямо за щитовидной железой располагаются четыре небольшие паращитовидные железы. Последние производят паратиреоидный гормон, который также отвечает за поддержание уровня кальция в организме, причем в большей степени, чем кальцитонин.
Откуда берется столько случаев рака щитовидки?
Рак щитовидной железы (РЩЖ) — наиболее распространенное злокачественное новообразование эндокринной системы [2]. Все чаще мы слышим, что заболеваемость РЩЖ неуклонно растет. И звучит это ужасающе, однако так ли всё просто на самом деле? Возможно, вы будете шокированы, какая правда скрывается за этими, на первый взгляд, однозначными научными фактами. И прежде, чем мы разберемся с истинной причиной роста заболеваемости РЩЖ, необходимо ознакомиться с тем, какие виды рака щитовидки существуют.
Итак, начнем. Сейчас нам понадобится привести немного численных данных, но не пугайтесь их, всё крайне просто. В научном сообществе выделяют пять типов РЩЖ:
- Папиллярный (80–85% случаев).
- Фолликулярный (10–15% случаев).
- Медуллярный (5% случаев).
- Низкодифференцированный (1% случаев).
- Недифференцированный (0,1–0,2% случаев).
Наиболее благоприятными принято считать два первых типа РЩЖ. И как мы можем заметить, они встречаются наиболее часто. Их также называют высокодифференцированными типами рака. Медуллярный, низкодифференцированный и недифференцированный типы считаются агрессивными формами РЩЖ. В нашей статье мы сделаем акцент лишь на первых двух типах РЩЖ, так как они являются наиболее распространенными.
Что означает понятие «дифференцировка»?
Когда-то давно, еще до нашего рождения, каждый из нас представлял собой одну-единственную клетку. Во время внутриутробного развития клеток стало в триллионы раз больше! И каждая из них обрела свою собственную функцию: одни отвечают за биение нашего сердца, другие защищают наш организм от внешних и внутренних опасностей, а третьи отвечают за когнитивные функции. И таких видов клеток более 230! Путь, который проходит клетка от той единственной, стоявшей в начале нашего пути, до высоко специализированной клетки, у которой есть четкие обязанности, и называется «дифференцировка».
Что касается рака — если клетки, из которых состоит опухоль, являются высокодифференцированными, в большинстве случаев врачи считают исход благоприятным. Однако если опухоль состоит из низкодифференцированных клеток, то с большой вероятностью она склонна к агрессивному течению. Как уже было сказано, наиболее часто выявляемые РЩЖ являются высокодифференцированными.
Папиллярный РЩЖ — наиболее распространенная форма: 80–85%. И с самым хорошим прогнозом. Пятилетняя выживаемость пациентов с РЩЖ — 98,1% [2]. Что это значит для пациента? Что наиболее часто выявляемые случаи РЩЖ имеют благоприятный исход!
Рак, ушедший в себя
Наше традиционное понимание РЩЖ, а именно его развития, в корне изменилось благодаря трем исследованиям 2014 года (Thyroid cancer trilogy) [3–5]. Казалось бы, все злокачественные образования по мере развития подвергаются прогрессии, а потому нуждаются в ранней диагностике и оперативном лечении. Впервые за всю историю человека было обнаружено существование «самоограничивающихся раков» (self-limiting cancers), которые являются злокачественными, но при этом не прогрессируют в летальные формы из-за ограниченной способности к делению клеток, составляющих опухоль. Конечно же, существуют и так называемые летальные РЩЖ (lethal thyroid cancers). Различие между ними заключается в происхождении раковых клеток, что и определяет развитие заболевания и его исход. Во втором случае клетки как бы затаиваются на долгий срок, на годы и даже на десятилетия, а потом по невыясненным еще причинам внезапно начинают делиться и приводят к неблагоприятному исходу. Однако на данный момент считается, что именно «самоограничивающиеся» типы РЩЖ составляют большинство.
Подбираемся к корню проблемы: статистика и диагностика
Вернемся к распространенности РЩЖ. Теперь мы готовы понять, что возросшее число случаев данной патологии не является поводом для беспокойства.
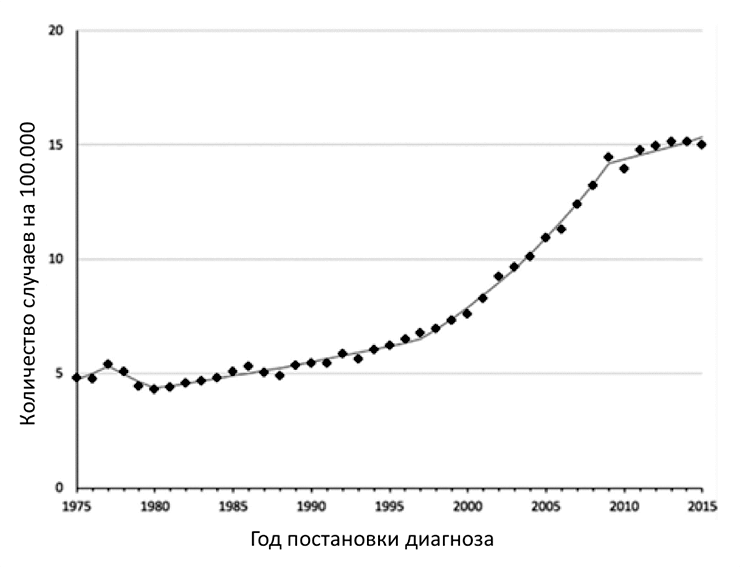
В 1975 году заболеваемость РЩЖ составляла 4,9 на 100 000 человек и оставалась относительно стабильной до начала 1990-х годов [6]. За последние 25 лет заболеваемость РЩЖ выросла более чем в 3 раза, то есть на 300% (рис. 1) [7], [8], причем в большинстве случаев за счет высокодифференцированного папиллярного РЩЖ. При этом очень важно понимать, что, несмотря на такой значительный рост, смертность от РЩЖ остается стабильной, примерно 0,5 случаев на 100 000 человек [6].
Рисунок 1. Данные заболеваемости раком щитовидной железы в период с 1975 по 2015 годы
Чувствуете, что тут что-то не так? Нет связи между возросшим числом случаев РЩЖ и смертностью от этой патологии! Среди врачей и ученых до сих пор продолжаются дебаты, почему так происходит. Сейчас выделяют несколько теорий. Наиболее вероятная — широкое распространение методов ультразвуковой диагностики (УЗИ). Пусть корни УЗИ уходят к Леонардо да Винчи и XV веку, широкое медицинское распространение данный метод получил с 50-х годов XX века [9], [10]. Сегодня УЗИ является наиболее простым, дешевым, неинвазивным и информативным методом выявления опухолевых образований щитовидной железы. Поэтому, как вы можете догадаться, УЗИ стали делать почти всем, причем независимо от показаний.
Сейчас научное сообщество активно дискутирует на тему, связаны ли такие показатели с истинным увеличением заболеваемости РЩЖ, или же проблема в гипердиагностике тех небольших образований ЩЖ, которые не требуют никакого вмешательства со стороны человека [11], [12].
Для более полного понимания проблемы вернемся на чуть более ранний этап диагностики РЩЖ.
Что такое узлы и как их найти?
Узлы ЩЖ — это радиологически различимые объемные образования в ЩЖ, которые могут быть доброкачественными и злокачественными. Узлы можно найти в 50% случаев всех проводимых УЗИ ЩЖ. При этом только 5% выявляемых образований будут злокачественными [13], [14].
Весомый вклад УЗИ в возросшее количество диагностированных узлов и РЩЖ можно показать на примере одного нашумевшего исследования в Южной Корее [3], [15], [16]. В 1999 году там была утверждена национальная программа, направленная на скрининг злокачественных заболеваний. Под программу попала и щитовидная железы. В результате повсеместного внедрения УЗИ щитовидки частота выявления рака выросла в 15 (!) раз с 1993 по 2011 год. И это мы еще не говорим просто об узлах, которые также могут быть психологической проблемой пациента. Большинство выявляемых случаев — папиллярный РЩЖ. Как вы помните, этот вид рака имеет весьма благоприятный исход. Однако простому населению идея жить с раком настолько чужда и неприятна, что было проведено огромное число полного удаления щитовидных желез, причем часто без видимой на то необходимости! А такая операция имеет серьезные последствия, о которых мы расскажем чуть ниже.
Врачи, осознав свою ошибку, убрали УЗИ щитовидки из списка обязательных скрининговых тестов. И результат не заставил себя ждать. В последней на эту тему публикации 2015 года сказано, что на 30% снизилась заболеваемость РЩЖ, а число операций на щитовидной железе снижалось на 35% ежегодно. Вывод напрашивается сам собой: в основе увеличения числа диагностированных случаев узлов щитовидки (в том числе и РЩЖ) является ставшее таким доступным УЗИ.
Думаем, следует также сказать, что образования ЩЖ выявляются не только при выполнении УЗИ, но и при использовании других методов лучевой диагностики (КТ, МРТ, ПЭТ), что стало возможным благодаря улучшению разрешающей способности оборудования. Следовательно, увеличилось чисто случайно выявляемых образований щитовидной железы (в том числе, рака) — инциденталóм (от англ. incidence — случайность) [17]. Инциденталомы клинически никак себя не проявляют и могут оставаться в организме бессимптомно всю жизнь. И многие из таких инциденталом обнаруживались лишь посмертно, случайно, и не являлись причиной кончины человека. Это позволяет говорить нам о существовании резервуара пациентов с узлами или раком щитовидной железы, который клинически является скрытым и никак себя не проявляет до его случайного обнаружения [18].
Приведенные данные обобщены на рисунке 2.
Рисунок 2. Что даст нам УЗИ щитовидки на самом деле?
рисунок авторов статьи
Напомним, что в нашей статье мы делаем акцент на наиболее распространенных типах РЩЖ (папиллярный, фолликулярный). Агрессивные формы РЩЖ (медуллярный, низкодифференцированный, недифференцированный и редко папиллярный) требуют дальнейшего более детального изучения
Самое главное: почему гипердиагностика и гиперлечение РЩЖ являются проблемой?
Является ли столь чрезмерное выявление объемных образований ЩЖ проблемой? Да, и очень даже серьезной. И она получила свое название — гипердиагностика (overdiagnosis) [19], [20]. И проблема состоит в том, что следствием ее становится гиперлечение. На самом деле она касается не только ЩЖ и представляет более серьезную опасность, чем может казаться на первый взгляд, а по мере развития методов диагностики приобретает все более и более масштабный характер, о чем говорит в своей статье «На всякий случай…» врач-эндокринолог В.В. Фадеев [28]. Говоря о ЩЖ, большинство пациентов с папиллярным РЩЖ подвергаются оперативному лечению — тотальной тиреоидэктомии или гемитиреоидэктомии [21]. Тем не менее в некоторых исследованиях [22], [23] показано, что при выборе лечения в пользу «активного наблюдения» (active surveillance) у пациентов с папиллярным РЩЖ (который относится к low-risk РЩЖ) диаметром менее одного сантиметра обнаруживались такие же исходы заболевания, как и при выполнении хирургических операций. В связи с этим в 2015 году в клинических рекомендациях Американской тиреоидологической ассоциации (American thyroid association, ATA) впервые была принята стратегия «активного наблюдения» для пациентов с low-risk cancers [24].
В связи с выявленным фактом, что в оперативном лечении таких РЩЖ, вполне возможно, нет необходимости (а ведь удаление ЩЖ сопровождается серьезными последствиями, о чем мы расскажем далее), с 2015 года в США уже принимаются меры по снижению частоты гипердиагностики и гиперлечения [24]. Например, уже настоятельно рекомендовано не проходить скрининг РЩЖ пациентам, у которых нет никаких симптомов, поскольку выявление агрессивных типов рака в этом случае крайне маловероятно.
Еще одной мерой предотвращения гиперлечения является изменение классификации типов РЩЖ, которые ведут себя как доброкачественные. Иначе говоря, их больше не называют «рак». Зачем? Все дело в психологической реакции пациента. Инстинкт самосохранения — самый живучий инстинкт человека и животных. И реализуется он во многом благодаря страху. Благодаря страху антилопа убегает ото льва, а змея жалит потенциальный объект угрозы — животные стремятся выжить. То же и с человеком. Всеми способами человек хочет продлить свое существование на этой земле. И диагноз «рак», который социум привык ассоциировать c мучительным завершением жизни, заставляет человека сделать все, чтобы от этого самого рака избавиться. В нашем случае, если у человека нашли РЩЖ, самая стойкая мысль — избавиться от этого мучения. И в большинстве случаев выбор падает на полное удаление щитовидной железы, вне зависимости от того, необходимо ли это. Как говорится, на всякий случай. И во многих случаях это не оправдано.
В одном из исследований [25] было выяснено, что люди, как правило, имеют общее представление о РЩЖ, но не знают о его диагностике и лечении, полагая, что по распространенности и смертности РЩЖ схож с другими типами рака. Страх дальнейшего прогрессирования заболевания заставляет пациента выбирать радикальное лечение. Так, недавно проведенные исследования неинвазивного рака груди [24], [25], а впоследствии и папиллярного РЩЖ [25], показали влияние терминологии на выбор лечения: замена термина «рак» в описании обоих патологических состояний способствовала выбору пациентом нехирургического лечения. Таким образом, данная стратегия оказывает влияние на психологическое состояние пациентов, тем самым предотвращая гиперлечение. Возможно ли жить с диагнозом «рак»? Как бы ответили на этот вопрос вы?
Что врачи думают о данной проблеме?
Проблема гиперлечения РЩЖ существует не только среди пациентов, но и среди медицинского сообщества.
Конечно, выбор, удалять ли щитовидную железу или нет, стоит больше перед пациентом, нежели перед лечащим врачом. И пациент вполне может выбрать хирургическую тактику лечения. А врач должен определять, сколько ткани щитовидной железы в конкретном случае нужно убирать.
В качестве уменьшения гипердиагностики Американская тиреоидологическая ассоциация рекомендует воздержаться от скрининга и биопсии мелких образований щитовидной железы при отсутствии на то иных клинических симптомов [6].
Как вообще лечат рак щитовидной железы?
Давайте разберемся, какие существуют пути лечения РЩЖ [26].
- Полное удаление ЩЖ, тотальная тиреоидэктомия, вместе с окружающей клетчаткой, а иногда и рядом лежащими лимфатическими узлами.
- Терапия радиоактивным йодом I131 после тотальной тиреиодэктомии. Не пугайтесь — это не опасно! Такой йод влияет только на клетки щитовидной железы и убивает их.
Почему мы, авторы, так не хотим, чтобы щитовидную железу удаляли без серьезных на то причин? Казалось бы, мы уберем орган, где сидит рак, и будем жить себе спокойно, только лишь принимая препараты гормонов щитовидной железы. Это ведь лучше, чем жить с раком. Или все-таки нет? Так вот, сама сложность вопроса заключается в операции.
Чем чревато полное удаление щитовидки (или, как говорят врачи, тотальная тиреоидэктомия)?
Существует два серьезных осложнения тотальной тиреоидэктомии [27].
- Стойкое снижение функции щитовидной железы (гипопаратиреоз). Наиболее серьезное и жизнеугрожающее осложнение. Итак, прямо за щитовидной железой располагаются четыре паращитовидные железы. Они производят паратиреоидный гормон, который отвечает за обмен кальция в нашем организме (а из него состоит бóльшая часть наших костей!). Паращитовидные железы совсем маленькие: диаметром 5 мм и весом 0,5 г. Их легко не заметить во время операции и удалить вместе с щитовидной железой. К тому же, даже если сохранить эти железы, высока вероятность повреждения питающих их кровеносных сосудов и нервов. А значит, железы просто перестанут работать, и в организм перестанет поступать паратиреиодный гормон. Это чревато возникновением тетанических приступов (подергиваний, которые могут переходит в судороги), нарушением питания волос и ногтей, кожи, эмали зубов, а также отложением кальция вне костей, например, между нервными клетками, что может проявляться в виде паркинсонизма или хореоатетоза — комбинации быстрых порывистых движений с медленными судорожными.
- Повреждение возвратного гортанного нерва и парез гортани. Щитовидная железа располагается прямо перед гортанью. Там же рядом находятся голосовые связки. Все эти структуры иннервируются гортанными нервами. И в случае повреждение некоторых из них — возвратных гортанных нервов — у пациента будет наблюдаться уменьшение активности гортанных мышц, что влечет за собой проблемы работы голосовых связок (в основном, осиплость голоса) и нарушения функций дыхания.
Согласитесь, последствия не из приятных. Поэтому главный вопрос заключается в следующем: оправдывают ли риски тиреоидэктомии ее пользу? На данном этапе развития науки и медицины нельзя дать однозначный ответ. Но важно понимать, что диагноз «Рак щитовидной железы» ничего не говорит о прогнозе для пациента и смертность от него крайне низка. А вот неоправданное агрессивное лечение, а именно удаление щитовидной железы, может повлечь за собой инвалидизацию и значительное ухудшение качества жизни. Поэтому сейчас в научном сообществе наблюдается тенденция органосохраняющей тактики в отношении высокодифференцированных РЩЖ. А показания к УЗИ щитовидной железы касаются только специфических групп пациентов. Ведь обнаружение раковых клеток в организме не означает смерть, а вот риск невротизации значительно возрастает.
Какой существует выход?
Одним из наиболее перспективных выходов из ситуации является частичное удаление ткани ЩЖ, а именно поврежденной доли. В таком случае пациент, во-первых, избавляется от необходимости принимать пожизненную заместительную терапию гормонами щитовидной железы, а во-вторых, избегает тех серьезных последствий, которые несет за собой операция полного удаления ЩЖ. Однако стоит понимать, что такой вариант не касается опухолей большого размера, а также тех новообразований, которые потенциально могут быть агрессивными (это решает врач!).
Сейчас терапевты и хирурги, которые занимаются патологией щитовидной железы, разделились на два лагеря: те, кто считает, что лучше перестраховаться, и при выявлении даже самой маленькой опухоли удалить всю щитовидную железу, и те, кто считает, что лучшим выходом будет частичное удаление ткани железы, а именно поврежденной ее доли. К сожалению, этот вопрос до сих пор остается открытым. Врачи все еще не могут прийти к единому знаменателю в данном вопросе. Проблема в том, что достоверная объективная доказательная база, на которую врачи могли бы опираться в качестве актуального клинического руководства, вовсе отсутствует. Существуют лишь отдельные исследования, которые обозревают вопрос лишь с одной субъективной стороны [21]. Оптимальным решением данной проблемы, на наш взгляд, стало бы объединение всех существующих статей с объективным и всесторонним взглядом на этот вопрос. Однако подобное исследование лишь ожидает нас в будущем.
Финальный аккорд
Итак, вот мы и подошли к последним строкам нашей статьи. Могло показаться, что мы и вовсе против УЗИ щитовидной железы, однако это не так. Существует группа риска пациентов, которым необходимо сделать УЗИ щитовидки (например, РЩЖ у кого-то из членов семьи). Также нельзя игнорировать тот факт, что УЗИ сильно продвинуло врачей в ранней диагностике агрессивных быстротекущих форм РЩЖ. Однако бóльшая часть врачей-эндокринологов, особенно за границей, против того, чтобы делать УЗИ щитовидки тогда, когда нет никаких симптомов болезни! Необходимой к прочтению, на наш взгляд, является работа профессора Фадеева В.В. «На всякий случай…» [28].
В этой статье высококвалифицированный врач обращает внимание читателя на то, что часто врачи оценивают результаты лабораторных и инструментальных анализов только на основании общепринятых границ норм. В случае несоответствия данной «норме» пациент признается больным. Очень важно понимать, что человек — индивидуальность, и показатель нормы у каждого может варьировать в зависимости от особенностей организма. Поэтому и лечить мы должны не анализы, не болезнь, а пациента. Врачу необходимо оценивать не только цифры в листе анализов, но и состояние пациента, а также качество жизни, которое ждет человека после лечения. Это и называется клиническим мышлением, которое, к сожалению, зачастую отсутствует у врачей в век, когда мы хотим слепо довериться цифрам, а машина начинает думать за человека.
С этими и другими мыслями вы можете ознакомится по оставленной нами ссылке [26].
Итак, дорогие наши читатели! Опираясь на всё, о чем мы рассказали выше, мы бы хотели, чтобы вы сделали три главных вывода:
- Не делайте УЗИ щитовидной железы «на всякий случай», без каких-либо симптомов! Ни по совету подруги, ни потому, что так сказали по телевизору, ни даже если вам сказал так врач (только если он четко объяснит, зачем нужно делать УЗИ).
- Если у вас нашли узел — 90%, что он доброкачественный.
- Если вы попали в оставшиеся 10%, помните, что бóльшая часть РЩЖ хорошо поддается лечению и имеет благоприятный прогноз.
Всем хорошего дня, и берегите свои щитовидки и нервы. 
- Циберкин А. (2019). Всегда ли нужна биопсия узлов щитовидной железы? «Медфронт»;
- Carolyn Dacey Seib, Julie Ann Sosa. (2019). Evolving Understanding of the Epidemiology of Thyroid Cancer. Endocrinology and Metabolism Clinics of North America. 48, 23-35;
- Hyeong Sik Ahn, Hyun Jung Kim, H. Gilbert Welch. (2014). Korea’s Thyroid-Cancer “Epidemic” — Screening and Overdiagnosis. N Engl J Med. 371, 1765-1767;
- Yasuhiro Ito, Akira Miyauchi, Minoru Kihara, Takuya Higashiyama, Kaoru Kobayashi, Akihiro Miya. (2014). Patient Age Is Significantly Related to the Progression of Papillary Microcarcinoma of the Thyroid Under Observation. Thyroid. 24, 27-34;
- S. Suzuki. (2016). Childhood and Adolescent Thyroid Cancer in Fukushima after the Fukushima Daiichi Nuclear Power Plant Accident: 5 Years On. Clinical Oncology. 28, 263-271;
- Alexandria D. McDow, Susan C. Pitt. (2019). Extent of Surgery for Low-Risk Differentiated Thyroid Cancer. Surgical Clinics of North America. 99, 599-610;
- Toru Takano. (2017). Natural history of thyroid cancer [Review]. Endocr J. 64, 237-244;
- Noone A.M., Howlader N., Krapcho M., Miller D., Brest A., Yu M. et al. SEER cancer statistics review, 1975-2015. Bethesda: National Cancer Institute, 2018;
- A. Kurjak. (2000). Ultrasound scanning – Prof. Ian Donald (1910–1987). European Journal of Obstetrics & Gynecology and Reproductive Biology. 90, 187-189;
- Ian Donald, R.E. Steiner. (1953). RADIOGRAPHY IN THE DIAGNOSIS OF HYALINE MEMBRANE. The Lancet. 262, 846-849;
- Louise Davies, H. Gilbert Welch. (2014). Current Thyroid Cancer Trends in the United States. JAMA Otolaryngol Head Neck Surg. 140, 317;
- Hyeyeun Lim, Susan S. Devesa, Julie A. Sosa, David Check, Cari M. Kitahara. (2017). Trends in Thyroid Cancer Incidence and Mortality in the United States, 1974-2013. JAMA. 317, 1338;
- Antonino Belfiore, Dario Giuffrida, Giacomo L. La Rosa, Orazio Ippolito, Giovanna Russo, et. al.. (1989). High frequency of cancer in cold thyroid nodules occurring at young age. Acta Endocrinologica. 121, 197-202;
- S. Ezzat. (1994). Thyroid incidentalomas. Prevalence by palpation and ultrasonography. Archives of Internal Medicine. 154, 1838-1840;
- Carolyn Dacey Seib, Julie Ann Sosa. (2019). Evolving Understanding of the Epidemiology of Thyroid Cancer. Endocrinology and Metabolism Clinics of North America. 48, 23-35;
- Hyeong Sik Ahn, H. Gilbert Welch. (2015). South Korea’s Thyroid-Cancer “Epidemic” — Turning the Tide. N Engl J Med. 373, 2389-2390;
- Louise Davies, H. Gilbert Welch. (2006). Increasing Incidence of Thyroid Cancer in the United States, 1973-2002. JAMA. 295, 2164;
- A.T. Grady, J.A. Sosa, T.P. Tanpitukpongse, K.R. Choudhury, R.T. Gupta, J.K. Hoang. (2015). Radiology Reports for Incidental Thyroid Nodules on CT and MRI: High Variability across Subspecialties. AJNR Am J Neuroradiol. 36, 397-402;
- Hirsch E.F. (1947). Unnecessary operations. Ill. Med. J. 5;
- Horwitz A. (1947). Unnecessary surgery. Med. Ann. Dist. Columbia. 11, 605–608;
- H. Gilbert Welch, Gerard M. Doherty. (2018). Saving Thyroids — Overtreatment of Small Papillary Cancers. N Engl J Med. 379, 310-312;
- Akira Miyauchi, Yasuhiro Ito, Hitomi Oda. (2018). Insights into the Management of Papillary Microcarcinoma of the Thyroid. Thyroid. 28, 23-31;
- Iwao Sugitani, Kazuhisa Toda, Keiko Yamada, Noriko Yamamoto, Motoko Ikenaga, Yoshihide Fujimoto. (2010). Three Distinctly Different Kinds of Papillary Thyroid Microcarcinoma should be Recognized: Our Treatment Strategies and Outcomes. World J Surg. 34, 1222-1231;
- Benjamin R. Roman, Luc G. Morris, Louise Davies. (2017). The thyroid cancer epidemic, 2017 perspective. Current Opinion in Endocrinology & Diabetes and Obesity. 24, 332-336;
- Brooke Nickel, Caitlin Semsarian, Ray Moynihan, Alexandra Barratt, Susan Jordan, et. al.. (2019). Public perceptions of changing the terminology for low-risk thyroid cancer: a qualitative focus group study. BMJ Open. 9, e025820;
- Дедов И.И. и Мельниченко Г.А. Эндокринология: национальное руководство (2-е изд.). М.: «ГЭОТАР-Медиа», 2019. — 1112 с.;
- Дедов И.И., Мельниченко Г.А., Фадеев В.В. Эндокринология: учебник (3-е изд.). М.: «Литтерра», 2015. — 416 с.;
- Фадеев В.В. (2017). На всякий случай… «Клиническая и экспериментальная тиреоидология». 2.
Абдулхабирова Ф.М.
Эндокринологический научный центр, Москва
Шифман Б.М.
ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, Москва, Россия
Ограничение возможностей цитологической диагностики папиллярного рака щитовидной железы на дооперационном этапе
Авторы:
Абросимов А.Ю., Абдулхабирова Ф.М., Шифман Б.М.
Журнал:
Архив патологии. 2020;82(3): 24‑30
Как цитировать:
Абросимов А.Ю., Абдулхабирова Ф.М., Шифман Б.М.
Ограничение возможностей цитологической диагностики папиллярного рака щитовидной железы на дооперационном этапе. Архив патологии.
2020;82(3):24‑30.
Abrosimov AIu, Abdulkhabirova FM, Shifman BM. Limitation of possibilities of cytological diagnosis of papillary thyroid cancer at the pre-surgery stage. Arkhiv Patologii. 2020;82(3):24‑30. (In Russ.).
https://doi.org/10.17116/patol20208203124

?>
Ретроспективный анализ, выполненный ранее во ФГБУ «Научный медицинский исследовательский центр эндокринологии» (ФГБУ «НМИЦ эндокринологии») Минздрава России и основанный на сопоставлении результатов дооперационной цитологической и послеоперационной гистологической диагностики фолликулярно-клеточных опухолей щитовидной железы, показал высокую чувствительность цитологического метода в диагностике папиллярного рака [1]. Показатели чувствительности цитологической диагностики разных вариантов папиллярного рака, выделенных в действующей Международной гистологической классификации опухолей щитовидной железы ВОЗ 4-го пересмотра [2], несколько отличаются. Разброс чувствительности цитологической диагностики различных гистологических вариантов составляет 97,7—100%, если принимать за истинно положительные результаты установления злокачественности новообразований V и VI диагностических категорий, и 59,1—77,8%, если истинно положительными результатами считать только VI категорию системы классификации Bethesda [3]. Проведенный ретроспективный анализ не предусматривал уточнение варианта папиллярного рака с помощью цитологического метода, так как установление варианта рака проводили на основании послеоперационного гистологического исследования [1]. Вместе с тем в отечественной [4, 5] и зарубежной литературе [6] показаны возможности цитологического исследования в определении гистологического варианта опухоли на дооперационном этапе диагностики. По-видимому, для принятия взвешенного решения о том, насколько оправдано и воспроизводимо установление гистологического варианта папиллярного рака с помощью дооперационного цитологического исследования, необходим анализ собственных данных на основании цитогистологических сопоставлений.
Цель исследования — ретроспективное сопоставление цитологических заключений дооперационных пункционных биопсий с установленным гистологическим вариантом папиллярного рака в клинике ФГБУ «НМИЦ эндокринологии» Минздрава России.
За период, прошедший после выхода в свет новой Международной гистологической классификации ВОЗ, 2017 [2], из базы данных ФГБУ «НМИЦ эндокринологии» получена информация на 266 пациентов с установленным диагнозом папиллярного рака после гистологического исследования хирургически удаленных щитовидных желез. Из 266 наблюдений в архиве цитологических препаратов дооперационных пункционных биопсий были найдены препараты 137 случаев, а препараты в остальных 129 были выданы по запросам для получения второго мнения из других лечебно-диагностических учреждений либо возвращены в другие учреждения после проведенного консультативного исследования. Пересмотр цитологических препаратов проведен независимо двумя экспертами — врачами клинической лабораторной диагностики, специализирующимися на цитологической диагностике новообразований щитовидной железы (АЮА, ФМА). Перед экспертами была поставлена задача, заключающаяся в определении варианта папиллярной карциномы на основании пересмотра цитологических препаратов. На данном этапе работы эксперты не имели результатов послеоперационного гистологического исследования. Результаты пересмотра цитологических препаратов двумя экспертами были сопоставлены, на основании двух независимых оценок и последующего сопоставления с гистологическим вариантом сделано заключение об успешности или безуспешности попытки определить вариант папиллярного рака.
В таблице показаны результаты сопоставления гистологического и цитологического определения вариантов папиллярного рака щитовидной железы, произведенного двумя экспертами. Вариабельность результатов цитологического определения варианта папиллярного рака между двумя экспертами оказалась не столь значительной, она касалась небольших колебаний в частоте установленных обычного, фолликулярного, кистозного и Уортино-подобного вариантов. Наиболее часто (59,1—59,9%) диагностирован обычный (классический) вариант папиллярного рака (рисунок). Для него характерно наличие трехмерных (объемных) сосочковых структур и изменений ядер опухолевых клеток. Чаще наряду с сосочковыми структурами в мазках пункционной биопсии встречаются разной степени распространенности фолликулярные структуры и изолированные опухолевые клетки. Изменения ядер опухолевых клеток заключаются в неровности контуров ядерной мембраны, формировании внутриядерных псевдовключений и продольно ориентированных ядерных борозд.
Примечание. * — Фолликулярный вариант включает солидно-фолликулярный и инкапсулированный фолликулярный варианты; ** — на этапе цитологической диагностики экспертам не была доступна информация о размере опухоли.
а — типичная сосочковая структура, образованная клетками папиллярного рака; б — обычный (классический) вариант папиллярного рака; в — цитологическая картина папиллярного рака, имеющего фолликулярное строение; г — фолликулярный вариант папиллярного рака; д — папиллярный рак с признаками кистозных изменений: раковые клетки на фоне содержимого кистозной полости; е — инкапсулированный вариант папиллярного рака: разрастание сосочков опухоли в просвете кистозной полости; ж — сосочковая структура Уортино-подобного варианта папиллярного рака с наличием лимфоидной инфильтрации; з — Уортино-подобный вариант папиллярного рака, строма сосочков содержит лимфоцитарный инфильтрат. а, в, д, ж — окраска азуром и эозином; б, г, е, з — окраска гематоксилином и эозином.
Псевдовключения образуются в результате инвагинации цитоплазмы в ядерную мембрану и представляют собой образования сферической формы с четкими очертаниями, хорошо видимыми на фоне конденсированного ядерного хроматина. Реже (11,7—13,9%) установлен фолликулярный (солидно-фолликулярный) вариант. Для него характерно фолликулярное строение (допускается наличие менее 1% сосочковых структур в соответствии с критериями гистологической классификации). В связи с тем что в гистологических препаратах этот вариант может быть представлен двумя типами новообразований: инфильтрирующим и инкапсулированным с инвазивным ростом, в проведенном исследовании объединили оба этих варианта, так как их цитологическая характеристика не отличается. В мазках фолликулярного варианта опухолевые клетки распределены в виде фолликулярных структур; в мазках солидно-фолликулярного варианта наряду с фолликулярными структурами могут быть представлены изолированные клетки опухоли без формирования фолликулярных структур. Поскольку в фолликулярном варианте изменения ядер опухолевых клеток, характерные для папиллярного рака, встречаются реже, чем в классическом (обычном) варианте, это дает основание на дооперационном этапе цитологической диагностики лишь подозревать папиллярный рак (V диагностическая категория в соответствии с критериями системы классификации Bethesda). Подозрение на папиллярный рак зарегистрировано в 13,1—13,9% случаев. В 8,8—10,9% случаев ретроспективный пересмотр цитологических препаратов позволил установить Уортино-подобный вариант. Он характеризуется крупными клетками с эозинофильной цитоплазмой на фоне выраженной лимфоидной инфильтрации. Опухоль возникает в щитовидной железе с тиреоидитом Хашимото и по строению напоминает одноименную опухоль слюнной железы. Очень редко (2,9—4,4%) цитологически установлен кистозный вариант, диагностика которого затруднена и основой могут служить ультразвуковые признаки кистозного узлового образования щитовидной железы. Мазок, как правило, малоклеточный, напоминает картину коллоидного зоба с кистозными изменениями, и только обнаружение единичных сосочковых структур с ядерными изменениями опухолевых клеток, типичными для папиллярного рака, помогает поставить правильный диагноз. Вариант папиллярного рака из высоких клеток цитологически поставлен лишь в единичном наблюдении (0,7%). Учитывая, что клинически данный вариант более агрессивен по сравнению с обычным (классическим) вариантом, следует отметить высокую прогностическую значимость постановки диагноза как на дооперационном этапе цитологической диагностики, так и на послеоперационном этапе гистологической. Для его установления необходимо наличие не менее 30% высоких опухолевых клеток в соответствии с критериями новой гистологической классификации. Вариант из высоких клеток отличается тем, что высота последних в 2—3 раза превышает ширину.
При гистологическом исследовании папиллярных карцином чаще ставят диагноз: обычный (классический) вариант (78/137; 56,9%), реже — фолликулярный (28/137; 20,4%) и инкапсулированный (19/137; 13,9%), а также Уортино-подобный вариант (6/137; 4,4%) и папиллярная микрокарцинома (6/137; 4,4%). Показательно, что из 78 случаев гистологически верифицированного обычного (классического) варианта папиллярной карциномы совпадение с цитологически установленным обычным вариантом было лишь в 60 (76,9%) случаях. В 10 (12,8%) случаях цитологическое исследование позволило лишь подозревать папиллярный рак. В 5 (6,4%) случаях одним из экспертов диагностирован Уортино-подобный, а вторым — фолликулярный вариант. В 2 (2,6%) случаях один из экспертов обнаружил фолликулярный, а второй — Уортино-подобный вариант. В 1 (1,3%) случае оба эксперта установили кистозный вариант.
Из 28 гистологически верифицированных фолликулярных вариантов совпадение с цитологически установленным фолликулярным вариантом у двух экспертов было зарегистрировано лишь в 13 (46,4%) случаях, обычный (классический) вариант диагностирован в 8 (28,6%), Уортино-подобный — в 3 (10,7%). В 4 (14,3%) случаях один из экспертов подозревал папиллярный рак, и второй эксперт в 3 (10,7%) случаях тоже папиллярный рак, а в 1 (3,6%) диагностировал кистозный вариант папиллярного рака.
Инкапсулированный вариант, гистологическая диагностика которого основана на выявлении собственной фиброзной капсулы опухоли, а также сосочкового или смешанного строения с сосочковым компонентом при наличии или отсутствии признаков инвазивного роста, не установил ни один из экспертов. Указанный гистологический вариант был расценен либо как обычный (классический) в 10 (52,6%) из 19 случаев, реже (3 (15,8%) из 19) — как кистозный вариант или как опухоль, подозрительная в отношении папиллярной карциномы (3 (15,8%) из 19 случаев), а также как Уортино-подобный (2 (10,5%) из 19) или фолликулярный вариант (1 (5,3%) из 19).
Уортино-подобный вариант по частоте совпадений результатов цитологического и гистологического исследования папиллярного рака уступал обычному (классическому) варианту. Он совпадал в 4 (66,6%) из 6 случаев. Остальные 2 случая были расценены одним из экспертов либо как обычный (классический) вариант (1 (16,7%) из 6 случаев ), либо как папиллярный рак из высоких клеток (1 (16,7%) из 6 случаев). Второй эксперт определил 2 случая Уортино-подобного варианта либо как кистозный вариант (1 (16,7%) из 6), либо как папиллярный рак из высоких клеток (1 (16,7%) из 6).
Папиллярная микрокарцинома не диагностирована экспертами ни в одном случае. Она была расценена либо как обычный (классический) вариант в 50% (3 из 6) случаев, в 2 (33,3%) было высказано лишь подозрение на папиллярную карциному, а в 1 (16,7%) установлен Уортино-подобный вариант.
Следовательно, ретроспективный анализ показал, что дооперационное цитологическое исследование имеет существенные ограничения в установлении варианта папиллярного рака щитовидной железы. Очевидно, гистологическая классификация тех вариантов папиллярного рака, диагностика которых основана на размерах первичной опухоли (папиллярная микрокарцинома) или наличии собственной фиброзной капсулы (инкапсулированный вариант), весьма затруднена на основании данных лишь цитологического исследования. Необходимо иметь дополнительную информацию по крайней мере о размере первичной опухоли и наличии собственной капсулы для того, чтобы диагностировать микрокарциному или инкапсулированный вариант папиллярного рака. Диагностика вариантов, основанная на клеточном составе опухолей (варианты из высоких и клеток типа «сапожных гвоздей»), также представляется затруднительной для дооперационного цитологического исследования. Понятно, что преобладающий клеточный компонент указанных вариантов в соответствии с действующей международной гистологической классификацией должен составлять не менее 30%. Возникает вопрос, как соответствует 30% уровень высоких клеток в гистологическом препарате (площадь срезов опухоли, представленная не менее 30% высоких клеток) концентрации указанных клеток в мазках пункционной биопсии? Кроме того, варианты из высоких и клеток типа «сапожных гвоздей» относятся к редко встречающимся даже по сравнению с Уортино-подобным вариантом, который должен в первую очередь рассматриваться при проведении дифференциальной диагностики с обычным (классическим) вариантом и который тоже может протекать на фоне тиреоидита Хашимото. Высокие опухолевые клетки одноименного варианта, порой, трудно дифференцировать с клетками онкоцитарного и Уортино-подобного вариантов папиллярного рака. Что касается Уортино-подобного варианта, гистологическая диагностика которого предполагает онкоцитарный клеточный состав, наличие выраженной лимфоплазмоцитарной инфильтрации стромы опухоли и фонового хронического лимфоцитарного тиреодита, т.е. цитологическая диагностика на дооперационном этапе возможна в ряде случаев. Как показали наши результаты, более половины случаев этого варианта было диагностировано с помощью цитологического метода, однако один случай был отнесен на основании цитологического исследования к варианту из высоких клеток. Учитывая, что эти два варианта существенно различаются по прогнозу (вариант из высоких клеток относится к одному из высокоагрессивных вариантов папиллярных карцином с высоким риском рецидивирования и радиойодрефрактерности), ошибочная его гипо- или гипердиагностика на дооперационном этапе может послужить причиной недостаточной или избыточной радикальности хирургического пособия. Данные литературы относительно возможности цитологического установления варианта папиллярного рака неоднозначны. Некоторые авторы свидетельствуют об ограничении использования цитологического метода, а другие, наоборот, доказывают возможность и целесообразность применения для установления на дооперационном этапе наиболее агрессивных вариантов папиллярного рака. В одной из отечественных публикаций [4] относительно значимости цитологического исследования в установлении варианта папиллярного рака было выделено 8 «цитологических вариантов», которые могут быть определены на дооперационном этапе с использованием цитометрического анализа. Этими вариантами являются обычный, фолликулярный, кистозный, с плоскоклеточной метаплазией, В-клеточной трансформацией, из высоких клеток, анапластический и склерозирующий. Понятно, что не все из выделенных авторами «цитологических вариантов» соответствуют вариантам, определенным в последнем издании международной гистологической классификации. В качестве критериев указанных вариантов авторами предложены следующие цитометрические параметры: периметр клеток, площадь клеток и ядер и ядерно-цитоплазматическое соотношение. В другой публикации отечественных авторов [5] представлена морфологическая характеристика следующих вариантов папиллярного рака, имеющих различия клинического течения и прогноза: фолликулярный, инкапсулированный, диффузный склерозирующий, из оксифильных клеток, с преобладанием солидных структур, из столбчатых клеток. По-видимому, не все перечисленные варианты можно установить только лишь на основании результатов цитологического исследования. Авторы справедливо отмечают, что, «учитывая неспецифичность отдельных гистологических и цитологических признаков, для диагноза необходимо использовать совокупность признаков, преимущественно касающихся ядер опухолевых клеток: овальная или овально-круглая форма ядер, неровные контуры ядерной мембраны, ядра типа «матовых стекол», наличие в ядрах бороздок, внутриядерных цитоплазматических включений, ядерно-цитоплазматическое соотношение меньше или равно 1». Зарубежные авторы [6] разделили все цитологические критерии, помогающие установить вариант папиллярного рака, на 3 группы: архитектурные, ядерно-цитоплазматические и фоновые. Одно- и многофакторный регрессионный анализ результатов пересмотра цитологических препаратов двумя независимыми цитопатологами установил корреляционные связи между цитологическими и гистологическими результатами диаг-ностики следующих вариантов папиллярного рака: классического, фолликулярного и онкоцитарного. Точность цитологической верификации указанных вариантов составила 63,5, 87,5 и 87% соответственно. Авторы сделали вывод о том, что цитологические признаки могут быть использованы для диагностики указанных трех вариантов папиллярного рака на дооперационном этапе с целью уточнения объема хирургического вмешательства и улучшения результатов лечения. Авторы отмечают трудности дифференциальной диагностики инкапсулированного фолликулярного варианта папиллярного рака и неинвазивной фолликулярной опухоли с ядрами папиллярного типа, отличить которые можно лишь на этапе послеоперационной гистологической диагностики с тотальным исследованием множественных срезов для установления/исключения признаков инвазивного роста опухоли. Это очевидное ограничение цитологического метода диагностики фолликулярного варианта папиллярного рака. Другие зарубежные авторы [7] категоричны в признании отсутствия признаков, позволяющих дифференцировать инвазивные и неинвазивные инкапсулированные опухоли щитовидной железы с ядрами папиллярного типа. В соответствии с категориями цитологической диагностики по системе Bethesda такие опухоли должны быть классифицированы как IV диагностическая категория (а не как папиллярный рак, соответствующий VI диагностической категории) для того, чтобы избежать последующей избыточно радикальной лечебной тактики. Вместе с тем некоторые авторы [8] свидетельствуют, что неинвазивные фолликулярные опухоли с ядрами папиллярного типа в отличие от фолликулярного варианта папиллярного рака с инвазивным ростом характеризуются статистически значимо более низким показателем ядерных признаков папиллярного рака и менее выраженными клеточными признаками злокачественности. Напомним, что изменения ядер опухолевых клеток «папиллярного типа» были разделены на 3 категории: (1-я) увеличение размера, вытянутая форма, тесное расположение и напластование; (2-я) неровные контуры ядерной мембраны, ядерные борозды и псевдовключения; (3-я) просветление и маргинация ядерного хроматина, появление оптически прозрачных ядер. Присвоив каждой из 3 категорий цифровые значения от 0 (отсутствует) до 1 (имеется), надо суммировать результат и использовать суммарный показатель для оценки степени выраженности ядерного признака. Учитывая субъективность оценки ядерных признаков даже в условиях математической объективизации, по-видимому, не следует полагаться на возможности цитологически определить фолликулярный вариант папиллярного рака без данных о его потенциале инвазивного роста. Более важное значение по сравнению с указанными попытками установить инвазивный рост на основании цитологического исследования представляют попытки дифференциальной диагностики клинически агрессивных вариантов папиллярного рака и менее агрессивных аналогов. S. Canberk и соавт. [9] полагают, что необходимо научиться дифференцировать на дооперационном этапе цитологической диагностики агрессивные и неагрессивные варианты папиллярного рака и разработать алгоритм установления цитологических признаков агрессивного варианта опухоли. Несомненно, что выделение варианта папиллярного рака по результатам цитологического исследования тонкоигольной аспирационной биопсии представляется весьма трудной задачей даже для опытного цитопатолога. Авторы предложили пошаговый алгоритм диагностики, главным звеном которой является стратификация опухолей на онкоцитарные и неонкоцитарные с последующей детализацией морфологии клеток и типа роста. Ключевыми посылами к цитологической диагностике должны стать: 1) определение некоторых вариантов папиллярного рака возможно на основании данных цитопатологии; 2) стремление на основании данных цитологического исследования отличить клинически агрессивные и неагрессивные варианты папиллярного рака — главная задача цитопатолога; 3) выделение варианта папиллярного рака на дооперационном этапе должно улучшить результаты хирургического лечения пациентов. Другие данные зарубежной литературы [10] наряду с поиском критериев агрессивных вариантов папиллярного рака рассматривают значимость цитологических критериев низкодифференцированных и анапластических карцином. Они разделяют все злокачественные новообразования щитовидной железы на 2 группы на основании морфологии клеток: опухоли, которые имеют характерные признаки (например, классического папиллярного рака или выраженной анаплазии) и опухоли, демонстрирующие более тонкие цитологические особенности (например, псевдостратификация ядер, картина «мыльных пузырей» в ядрах, супра- или субнуклеарные цитоплазматические вакуоли, розеткоподобные структуры, клетки типа «сапожных гвоздей»). Недавно опубликованный обзор литературы, посвященный гистологическим и молекулярно-генетическим особенностям клинически агрессивных вариантов папиллярного рака [11], не только установил редкость встречаемости агрессивных вариантов (из высоких и столбчатых клеток, диффузно-склерозирующего варианта, варианта из клеток типа «сапожных гвоздей»), но и возможные молекулярные основы неблагоприятного клинического течения, высокую частоту отдаленного метастазирования, низкий уровень общей и безрецидивной выживаемости.
Исследование V. Monappa и R. Kudva [12], основанное на ретроспективном сопоставлении результатов цитологических заключений и вариантов папиллярного рака, показало вариабельность цитологических заключений (от доброкачественных неопухолевых поражений до явно злокачественных новообразований) в случаях, диагностированных с помощью гистологического метода как различные варианты папиллярного рака. Ошибки цитологической диагностики связаны с тем, что в некоторых вариантах (фолликулярный, столбчато-клеточный) ядерные признаки, характерные для папиллярного рака, могут быть не столь очевидными, чтобы классифицировать опухоли на основании цитологического исследования как злокачественные. Кроме того, в мазках тонкоигольной биопсии могут преобладать элементы, полученные при аспирации окружающей неопухолевой ткани, не только затрудняющие установление варианта опухоли, но и приводящие к ошибочной диагностике неопухолевых поражений.
Заключение
Таким образом, результаты исследования и анализ данных литературы показывают, что цитологическая диагностика вариантов папиллярного рака на дооперационном этапе имеет существенные ограничения. В настоящее время вызывает сомнение целесообразность рекомендации определять вариант папиллярного рака с помощью цитологического метода. Однако это не означает, что необходимо прекратить поиск надежных клеточных и молекулярно-генетических особенностей клинически агрессивных вариантов папиллярного рака.
Участие авторов:
Концепция и дизайн исследования — А.Ю.А., Ф.М.А.
Сбор и обработка материала — А.Ю.А., Ф.М.А., Б.М.Ш.
Написание текста — А.Ю.А., Ф.М.А., Б.М.Ш.
Редактирование — А.Ю.А.
Авторы заявляют об отсутствии конфликта интересов.
- Research
- Open Access
- Published: 14 July 2015
Diagnostic Pathology
volume 10, Article number: 96 (2015)
Cite this article
-
4680 Accesses
-
20 Citations
-
3 Altmetric
-
Metrics details
Abstract
Background
To investigate the clinicopathological features of recurrent papillary thyroid carcinoma (PTC).
Methods
A retrospective analysis on clinical and pathological data of 34 patients with recurrent PTC was carried out. A total of 281 patients with non-recurrent PTC during the same time period were chosen as the control group.
Results
Patients were divided into three groups according to the pathological subtype. The number of patients belonging to Groups 1, 2, and 3 were 28, 154, and 133, respectively. 78 patients underwent partial or whole thyroidectomy, 151 cases underwent thyroidectomy combining neck regional lymph node dissection, and 86 patients underwent thyroidectomy combining modified or radical neck dissection. Univariate analysis showed that PTC recurrence was associated with tumor size, extrathyroid invasion, initial surgery approach, lymph node metastasis, and pathological subtype (P < 0.05). Patient age, gender, complication with Hashimoto’s thyroiditis, and multifocality were unrelated to PTC recurrence (P > 0.05). Multivariate analysis showed that initial surgery approach and pathological subtype perform important functions in PTC recurrence (P < 0.001). Initial surgery approach presented a negative correlation with PTC recurrence (β = −0.320, OR = 0.726). The pathological subtype was also related to PTC recurrence (β = 0.923, OR = 2.517).
Conclusion
PTC patients without neck dissection showed greater likelihood of postoperative recurrence. Patients with the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants showed a higher propensity for PTC recurrence after operation compared with those who did not. Tumor volume, extrathyroid invasion, and multiple lymph node metastases at the time of initial operation were also significantly related to postoperative recurrence. Follow-up supervision must be enhanced after initial treatment to mitigate PTC recurrence in susceptible patients. Effective and standard treatments must be adopted immediately after the discovery of recurrence.
Background
Papillary thyroid carcinoma (PTC) is the most common thyroid cancer; this cancer presents relatively low malignancy, good prognosis, and a 10-year survival rate of over 90 %. However, the clinical behaviors of this cancer are complex and varied. PTC is easy to spread via lymphatic ducts, which results in recurrence, metastases, and even death [1]. Recurrent PTC mainly refers to localized and distant recurrence, including recurrence of the primary tumor, lymph node metastases, invasion of the esophagus and trachea, invasion of muscles, soft tissues and nerves, and distant metastases. Many factors can affect the recurrence of thyroid cancer, and final conclusion has not yet been reached. Many researchers believe that pathological type, staging, degree of extrathyroid invasion, lymph node metastatic rate, age, and initial surgery approach may be related to thyroid cancer recurrence. This research retrospectively analyzes the clinical data of 34 patients with recurrent PTC and presents a statistical comparison with non-recurrent patients to analyze factors related to PTC recurrence. The aim of the present work is to provide clinical evidence for standardized and appropriate treatment of recurrent PTC.
Methods
Clinical data
A total of 315 patients with PTC who were admitted to Jinan Military General Hospital from January 2009 to July 2013, including 66 male patients and 249 female patients, were recruited. The male to female ratio was 1:3.8. Ages ranged from 20 years to 78 years, and the median age was 48 years. The diameter of most tumors was less than 2 cm, the proportion of which was 47.1 % in the recurrent group and 85.8 % in the non-recurrent group. Moreover, 10.5 % (33 cases) of the patients presented extrathyroid invasion, and 42.2 % (133 cases) of the patients were found with lymph node metastases at the time of initial surgery. The tumors of 44.4 % (140 cases) of the patients showed multifocality, and 25.1 % (79 cases) of the patients had Hashimoto’s thyroiditis (HT) (Table 1). This study received the approval of the ethics committee of the General Hospital of Jinan Military Command (No. 2013ZD01).
Full size table
Pathological subtype of PTC
Recruited PTC patients were divided into three groups. Patients with the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants with higher invasiveness, higher probability of recurrence, and metastases were classified into Group 1. Patients with the follicular, clear cell, and conventional papillary carcinoma variants with similar prognosis were classified into Group 2. Patients with papillary microcarcinoma were classified into Group 3.
Initial surgery approach
The methods of primary lesion dissection used in this research included thyroid lobectomy with or without isthmectomy and total/near-total thyroidectomy. The methods of lymph node dissection included central compartment node dissection, selective neck dissection, modified neck dissection, and radical neck dissection. During statistical analysis, thyroid lobectomy with or without isthmectomy and total/near-total thyroidectomy were classified as the first type of surgical approach. Surgical approaches belonging to the first type combined with central compartment node dissection, selective neck dissection, and wide dissection of metastatic lesions were classified as the second type of surgical approach. Finally, approaches combining modified neck dissection and radical dissection were classified as the third type of surgical approach.
Statistical analysis
SPSS 17.0 software was used for statistical analysis. In addition, χ
2-test and multivariate analysis using Cox proportional hazards modeling were carried out. Factors that may be related to PTC recurrence, including gender, age, tumor size, initial surgery approach, lymph node metastasis, number of lesions, complication with HT, extrathyroid invasion, and pathological subtype, were evaluated. P < 0.05 was considered statistically significant difference.
Results
Clinicopathological information
The clinicopathological information of PTC patients is given in Table 1, and the comparisons between patients with recurrence and non-recurrence were carried out. 34 recurrent patients (11 males and 23 females) were investigated in this study. The male to female ratio was 1:2.1. Ages ranged from 24 years to 72 years old, and the median age was 46 years old. Postoperative recurrence intervals from initial surgery ranged from five months to 18 years, with a median of 46 months. Twelve patients (35.3 %) showed postoperative recurrence within two years, 14 patients (41.2 %) showed postoperative recurrence within two to five years, and eight patients (23.5 %) showed postoperative recurrence over five years later. Recurrence occurred once in 29 patients (85.3 %), twice in 4 patients (11.8 %), and thrice in 1 patient (2.9 %). Two hundred eighty-one non-recurrent PTC patients were classified into the control group (55 males and 226 females); in this group, the male to female ratio was 1:4.1, the age of onset ranged from 20 years to 78 years old, and the median age was 48 years. Patients were divided into three groups according to the pathological subtype. The number of patients belonging to Groups 1, 2, and 3 among the 34 recurrent patients were 11, 20, and 3, respectively. The number of non-recurrent patients belonging to Groups 1, 2, and 3 were 17, 134, and 130 (Table 2), respectively. Among the 34 recurrent patients, 16 patients were treated using surgeries of the first type, 14 patients were treated using surgeries of the second type, and 4 patients were treated using surgeries of the third type. The numbers of non-recurrent patients treated by the first, second, and third types of surgery were 62, 137, and 82, respectively.
Full size table
Univariate analysis of factors related to PTC recurrence
Tumor size, extrathyroid invasion, initial surgery approach, lymph node metastases, and pathological subtype showed statistical differences between the recurrent and non-recurrent groups (P < 0.05, Table 1). Larger tumors showed significantly increased risk of recurrence. The recurrence rate of micro-PTC was 2.3 % (3/133) and reached 31.0 % (18/58) when the tumor diameter grew to ≥2 cm. The higher recurrence rates, reaching 35.3 % (12/34), were observed when extrathyroid invasion was present at the time of initial surgery. Initial surgery approach also showed a significant effect on PTC recurrence; recurrence rates could reach 20.5 % (16/78) in patients without lymph node dissection but only 4.7 % (4/86) in patients receiving radical dissection and modified dissection. The recurrence rate was 17.3 % (23/133) in patients with cervical lymph node metastasis at the time of initial surgery and only 6.0 % (11/182) in patients without metastasis. In this research, patients with the tall cell, columnar cell, and oncocytic variants showed higher recurrence rates than patients with other cell variants (Table 2). Factors such as age, gender, complication with HT, and number of lesions demonstrated no correlation with tumor recurrence (P > 0.05, Table 1).
Multivariate analysis of factors related to PTC recurrence
Multivariate analysis revealed that initial surgery approach and pathological subtype were the main factors related to PTC recurrence (P < 0.001, Table 3). Initial surgery approach was negatively correlated with PTC recurrence (β = −0.320, OR = 0.726). Thus, patients receiving conservative treatment are more likely to develop PTC recurrence than patients treated with more radical modalities. Recurrence rates decreased with increasing surgical scope. Pathological subtype also showed a close correlation with PTC recurrence (β = 0.923, OR = 2.517).
Full size table
Discussion
PTC is the most common but least aggressive histological subtype of thyroid cancer. Most patients with PTC have excellent prognosis. However, recent studies have demonstrated increasing incidence of recurrent PTC [2, 3]. Many factors can affect thyroid cancer recurrence, but final conclusions have not been reached. The results of some studies show that the pathological type, staging, degree of extrathyroid invasion, lymph node metastatic rate, age, and initial surgery approach are related to thyroid cancer recurrence [4, 5]. Our research showed that tumor size, extrathyroid invasion, initial surgery approach, lymph node metastasis, and pathological subtype demonstrate statistically significant differences between the recurrent and non-recurrent groups. By contrast, factors such as age, gender, complication with HT, and number of lesions are not correlated with tumor recurrence. Multivariate analysis results further revealed that initial surgery approach and pathological subtype are main factors related to PTC recurrence.
The dissection methods of primary lesions of PTC include (1) hemithyroidectomy with or without isthmectomy, (2) total/near-total thyroidectomy, and (3) extension of surgical scope. In case of severe extrathyroid invasion, such as invasion of the esophagus, trachea, and nerves, extending the scope of surgery is required. The methods of neck dissection are as follows: (1) central compartment node dissection (unilateral or bilateral), (2) selective neck dissection, (3) functional compartmental en-bloc neck dissection, (4) modified neck dissection, and (5) radical neck dissection [6]. Mazzaferri et al. [7] found that the recurrence rate after partial thyroidectomy is nearly twice that of total and near-total thyroidectomy. By contrast, Cunningham et al. [8] revealed that the recurrence rates had no significant difference between hemithyroidectomy and total/near-total thyroidectomy groups. Monacelli et al. [9] suggested that total thyroidectomy combined with central node dissection must be performed even in the absence of risk factors and without clinically evident nodes. However, some researchers do not advocate prophylactic central neck lymphadenectomy [10]. Univariate analysis in this research showed that initial surgery approach exerts a great impact on the prognosis. For example, while 47.1 % (16/34) of the recurrent PTC patients received the first type of surgery as initial surgery, only 22.1 % (62/281) of the non-recurrent PTC patients received the first type of surgery. About 52.9 % (18/34) of the recurrent PTC patients received the second and third types of surgery. In comparison, 77.9 % (219/281) of the non-recurrent PTC patients received the second and third types of surgery as the initial surgery. Multivariate analysis revealed that initial surgery approach is the main factor related to PTC recurrence (P < 0.001); specifically, initial surgery approach demonstrated a negative correlation with PTC recurrence (β = −0.320, OR = 0.726).
The recurrence rate decreased with increasing surgical scope. Non-standardized surgical approaches with inappropriately small surgical scopes could lead to tumor residue. Moreover, lesions of lymph node metastasis may be missed, thereby increasing the risk of recurrence. Possible reasons behind the inconsistency of results are as follows: (1) Differences among recruited patients. Patients receiving neck dissection showed significant metastases, whereas no cervical lymph node metastasis was discovered before the operation in patients who did not receive neck dissection. (2) Insufficient number of recruited patients. (3) Difference in surgical techniques among surgeons. Considering these factors, blindly extending or narrowing the surgical scope is irrational.
The World Health Organization (WHO) histological classification of tumors has redefined the subtypes of non-conventional PTC [11]: follicular variant, oncocytic variant, diffuse sclerosing variant, tall cell variant, columnar cell variant, solid variant, PTC with nodular fasciitis-like stroma, clear cell variant, and diffuse follicular variant. PTC patients of different histological subtypes may exhibit diverse clinical and biological behaviors. Subtypes including the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants have higher invasiveness and may promote higher risks of recurrence and metastases [12–14]. The prognosis of patients with the follicular and clear cell variants is similar to that of patients with conventional papillary carcinoma [15]. Thyroid microcarcinoma is a type of papillary carcinoma that is less than 1 cm in diameter with relatively low invasiveness and good prognosis [16]. This research classified histological variants according to the WHO histological classification of tumors. Patients with the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants were classified into Group 1; patients with the follicular, clear cell, and conventional PTC variants were classified into Group 2; and patients with papillary microcarcinomas were classified into Group 3. The research conducted by Boone et al. [17] showed that the recurrence rate of patients with differentiated thyroid carcinoma is lower than that of patients with other types of thyroid carcinoma. Among the differentiated thyroid carcinomas, the recurrence rate of PTC is lower than that of the follicular variant. However, 30 % of the PTC patients continue to suffer from recurrence, metastasis, and even death [18]. Univariate analysis demonstrated that pathological subtype is obviously correlated with PTC recurrence (P < 0.01). Multivariate analysis also indicated that pathological subtype is closely related to PTC recurrence (β = 0.923, OR = 2.517). The recurrence rate of PTC increased as the invasiveness of the tumor increased. Thus, close follow-up must be carried out in patients with the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants. Effective treatment measures must be taken once recurrence is discovered.
Various results are reported in the literature regarding the effect of lymph node metastases on PTC recurrence. Some studies indicate that lymph node metastases do not affect PTC recurrence [19]. However, some researchers have found that the number of lymph node metastases is associated with postoperative recurrence or re-metastasis. Thus, lymph node metastasis has become an important factor affecting the prognosis and recurrence of thyroid carcinoma [20]. The results of this research revealed statistically significant differences in lymph node metastases between the recurrent and non-recurrent groups. Patients with lymph node metastases at the time of initial surgery are more likely to suffer recurrence than those without metastases. The correlation of cervical lymph node metastases with recurrence needs to be confirmed through large-sample and long-term studies.
Of the 34 recurrent PTC patients in the group, postoperative recurrence intervals ranged from five months to 18 years, with a median time of 46 months. Recurrence was observed to occur within a short period of time. The majority of PTC patients, for example, showed recurrence within two to five years from surgery. Furthermore, recurrence may also occur more than once. Therefore, PTC patients must have regular reexamination with frequent follow-ups within five years after the first treatment. Ultrasound examination must be performed at least once a year within five years after the first treatment for timely discovery of tumor recurrence.
Conclusions
In conclusion, initial surgery approach, tumor size, extrathyroid invasion, lymph node metastases, and pathological type may be related to PTC recurrence. However, opinions on the resection scope of PTC differ. Surgical indications and methods vary on a case-to-case basis. According to Untch et al. [21], lobectomy for patients with low risk is suitable. Nixon et al. [22] demonstrated no difference in the 10-year survival rate of patients with low-risk highly differentiated thyroid carcinoma and those receiving lobectomy and total thyroidectomy. Doctors must consider patient compliance during follow-ups when evaluating whether or not the patient must receive thyroid lobectomy. For individuals with poor economic means, low education levels, poor knowledge about their condition, and inability to accomplish regular follow-up, complete thyroidectomy may be a suitable option. The most appropriate resection scope for PTC can be determined by considering the thoroughness of operation, the functions of the thyroid and parathyroid glands, and the relationships between important anatomical positions. Enhanced follow-up and postoperative reexamination must be carried out in patients with increased risk of recurrence. Effective and regular treatments must be administered once recurrence is discovered.
Consent
Written informed consent was obtained from the patient for the publication of this report and any accompanying images.
References
-
Giordano D, Frasoldati A, Kasperbauer JL, Gabrielli E, Pernice C, Zini M, et al. Lateral neck recurrence from papillary thyroid carcinoma: predictive factors and prognostic significance. Laryngoscope. 2014. doi:10.1002/lary.25094.
PubMed
Google Scholar
-
Lee CW, Roh JL, Gong G, Cho KJ, Choi SH, Nam SY, et al. Risk factors for recurrence of papillary thyroid carcinoma with clinically node-positive lateral neck. Ann Surg Oncol. 2015;22(1):117–24.
Article
PubMedGoogle Scholar
-
Lang BH, Lee GC, Ng CP, Wong KP, Wan KY, Lo CY. Evaluating the morbidity and efficacy of reoperative surgery in the central compartment for persistent/recurrent papillary thyroid carcinoma. World J Surg. 2013;37(12):2853–9.
Article
PubMedGoogle Scholar
-
Londero SC, Krogdahl A, Bastholt L, Overgaard J, Trolle W, Pedersen HB, et al. Papillary thyroid microcarcinoma in Denmark 1996–2008: a national study of epidemiology and clinical significance. Thyroid. 2013;23(9):1159–64.
Article
PubMedGoogle Scholar
-
Ardito G, Revelli L, Giustozzi E, Salvatori M, Fadda G, Ardito F, et al. Aggressive papillary thyroid microcarcinoma: prognostic factors and therapeutic strategy. Clin Nucl Med. 2013;38(1):25–8.
Article
PubMedGoogle Scholar
-
Cooper DS, Doherty GM, Haugen BR, Kloos RT, Lee SL, Mandel SJ, et al. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2009;19(11):1167–214.
Article
PubMedGoogle Scholar
-
Mazzaferri EL, Jhiang SM. Long-term impact of initial surgical and medical therapy on papillary and follicular thyroid cancer. Am J Med. 1994;97(5):418–28.
Article
CAS
PubMedGoogle Scholar
-
Cunningham MP, Duda RB, Recant W, Chmiel JS, Sylvester JA, Fremgen A. Survival discriminants for differentiated thyroid cancer. Am J Surg. 1990;160(4):344–7.
Article
CAS
PubMedGoogle Scholar
-
Monacelli M, Lucchini R, Polistena A, Triola R, Conti C, Avenia S, et al. Total thyroidectomy and central lymph node dissection. Experience of a referral centre for endocrine surgery. G Chir. 2014;35(5–6):117–21.
CAS
PubMed Central
PubMedGoogle Scholar
-
Delogu D, Pisano IP, Pala C, Pulighe F, Denti S, Cossu A, et al. Prophylactic central neck lymphadenectomy in high risk patients with T1 or T2 papillary thyroid carcinoma: is it useful? Ann Ital Chir. 2014;85(3):225–9.
PubMed
Google Scholar
-
Delellis RA, Lloyd RV, Heitz PU, Eng C. Pathology and Genetics Tumours of Endocrine Organs. Lyon: IARC press; 2003.
Google Scholar
-
Roman S, Sosa JA. Aggressive variants of papillary thyroid cancer. Curr Opin Oncol. 2013;25(1):33–8.
Article
PubMedGoogle Scholar
-
Kuo CS, Tang KT, Lin JD, Yang AH, Lee CH, Lin HD. Diffuse sclerosing variant of papillary thyroid carcinoma with multiple metastases and elevated serum carcinoembryonic antigen level. Thyroid. 2012;22(11):1187–90.
Article
CAS
PubMedGoogle Scholar
-
Evans WD. De-differentiation of papillary thyroid carcinoma into squamous cell carcinoma. A case of coexistence within an excised neck lesion. BMJ Case Rep 2012, 2012. doi: 10.1136/bcr-2012-007707.
-
Zidan J, Karen D, Stein M, Rosenblatt E, Basher W, Kuten A. Pure versus follicular variant of papillary thyroid carcinoma: clinical features, prognostic factors, treatment, and survival. Cancer. 2003;97(5):1181–5.
Article
PubMedGoogle Scholar
-
Melcescu E, Horton WB, Pitman KT, Vijayakumar V, Koch CA. Euthyroid Graves’ orbitopathy and incidental papillary thyroid microcarcinoma. Hormones (Athens). 2013;12(2):298–304.
Article
Google Scholar
-
Boone RT, Fan CY, Hanna EY. Well-differentiated carcinoma of the thyroid. Otolaryngol Clin North Am. 2003;36(1):73–90. viii.
Article
PubMedGoogle Scholar
-
Shoup M, Stojadinovic A, Nissan A, Ghossein RA, Freedman S, Brennan MF, et al. Prognostic indicators of outcomes in patients with distant metastases from differentiated thyroid carcinoma. J Am Coll Surg. 2003;197(2):191–7.
Article
PubMedGoogle Scholar
-
Ito Y, Tomoda C, Uruno T, Takamura Y, Miya A, Kobayashi K, et al. Clinical significance of metastasis to the central compartment from papillary microcarcinoma of the thyroid. World J Surg. 2006;30(1):91–9.
Article
PubMedGoogle Scholar
-
Watkinson JC, Franklyn JA, Olliff JF. Detection and surgical treatment of cervical lymph nodes in differentiated thyroid cancer. Thyroid. 2006;16(2):187–94.
Article
PubMedGoogle Scholar
-
Untch BR, Palmer FL, Ganly I, Patel SG, Michael Tuttle R, Shah JP, et al. Oncologic outcomes after completion thyroidectomy for patients with well-differentiated thyroid carcinoma. Ann Surg Oncol. 2014;21(4):1374–8.
Article
PubMedGoogle Scholar
-
Nixon IJ, Ganly I, Patel SG, Palmer FL, Whitcher MM, Tuttle RM, et al. Thyroid lobectomy for treatment of well differentiated intrathyroid malignancy. Surgery. 2012;151(4):571–9.
Article
PubMedGoogle Scholar
Download references
Acknowledgments
This study was supported by the President Fund of the General Hospital of Jinan Military Command (2013ZD01).
Author information
Author notes
Authors and Affiliations
-
Department of Thyroid and Breast Surgery, General Hospital of Jinan Military Command, Jinan, 250031, China
Jian Zhu
-
Department of Pathology, Affiliated Hospital of Taishan Medical College, Taian, 271000, China
Xinli Wang
-
Medical Administration Division, General Hospital of Jinan Military Command, Jinan, 250031, China
Xiaoxuan Zhang
-
Department of Pathology, General Hospital of Jinan Military Command, 25 Shifan Road, Tianqiao District, Jinan, 250031, China
Peifeng Li
-
Department of Statistics, Taishan Medical College, Taian, 271000, China
Haifeng Hou
Authors
- Jian Zhu
You can also search for this author in
PubMed Google Scholar - Xinli Wang
You can also search for this author in
PubMed Google Scholar - Xiaoxuan Zhang
You can also search for this author in
PubMed Google Scholar - Peifeng Li
You can also search for this author in
PubMed Google Scholar - Haifeng Hou
You can also search for this author in
PubMed Google Scholar
Corresponding author
Correspondence to
Peifeng Li.
Additional information
Competing interests
The authors declare that they have no competing interests.
Authors’ contributions
JZ and PFL conceived and designed the experiments. JZ, XLW and XXZ collected the data. PFL and HFH analyzed the data. PFL and XLW wrote the paper. All authors read and approved the final manuscript.
Jian Zhu, Xinli Wang and Xiaoxuan Zhang contributed equally to this work.
Rights and permissions
Open Access This article is licensed under a Creative Commons Attribution 4.0 International License, which permits use, sharing, adaptation, distribution and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons licence, and indicate if changes were made.
The images or other third party material in this article are included in the article’s Creative Commons licence, unless indicated otherwise in a credit line to the material. If material is not included in the article’s Creative Commons licence and your intended use is not permitted by statutory regulation or exceeds the permitted use, you will need to obtain permission directly from the copyright holder.
To view a copy of this licence, visit https://creativecommons.org/licenses/by/4.0/.
The Creative Commons Public Domain Dedication waiver (https://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated in a credit line to the data.
Reprints and Permissions
About this article
Cite this article
Zhu, J., Wang, X., Zhang, X. et al. Clinicopathological features of recurrent papillary thyroid cancer.
Diagn Pathol 10, 96 (2015). https://doi.org/10.1186/s13000-015-0346-5
Download citation
-
Received: 20 January 2015
-
Accepted: 09 July 2015
-
Published: 14 July 2015
-
DOI: https://doi.org/10.1186/s13000-015-0346-5
Keywords
- Clinicopathological features
- Initial surgery approach
- Papillary thyroid cancer
- Pathological subtype
- Recurrence
- Research
- Open Access
- Published: 14 July 2015
Diagnostic Pathology
volume 10, Article number: 96 (2015)
Cite this article
-
4680 Accesses
-
20 Citations
-
3 Altmetric
-
Metrics details
Abstract
Background
To investigate the clinicopathological features of recurrent papillary thyroid carcinoma (PTC).
Methods
A retrospective analysis on clinical and pathological data of 34 patients with recurrent PTC was carried out. A total of 281 patients with non-recurrent PTC during the same time period were chosen as the control group.
Results
Patients were divided into three groups according to the pathological subtype. The number of patients belonging to Groups 1, 2, and 3 were 28, 154, and 133, respectively. 78 patients underwent partial or whole thyroidectomy, 151 cases underwent thyroidectomy combining neck regional lymph node dissection, and 86 patients underwent thyroidectomy combining modified or radical neck dissection. Univariate analysis showed that PTC recurrence was associated with tumor size, extrathyroid invasion, initial surgery approach, lymph node metastasis, and pathological subtype (P < 0.05). Patient age, gender, complication with Hashimoto’s thyroiditis, and multifocality were unrelated to PTC recurrence (P > 0.05). Multivariate analysis showed that initial surgery approach and pathological subtype perform important functions in PTC recurrence (P < 0.001). Initial surgery approach presented a negative correlation with PTC recurrence (β = −0.320, OR = 0.726). The pathological subtype was also related to PTC recurrence (β = 0.923, OR = 2.517).
Conclusion
PTC patients without neck dissection showed greater likelihood of postoperative recurrence. Patients with the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants showed a higher propensity for PTC recurrence after operation compared with those who did not. Tumor volume, extrathyroid invasion, and multiple lymph node metastases at the time of initial operation were also significantly related to postoperative recurrence. Follow-up supervision must be enhanced after initial treatment to mitigate PTC recurrence in susceptible patients. Effective and standard treatments must be adopted immediately after the discovery of recurrence.
Background
Papillary thyroid carcinoma (PTC) is the most common thyroid cancer; this cancer presents relatively low malignancy, good prognosis, and a 10-year survival rate of over 90 %. However, the clinical behaviors of this cancer are complex and varied. PTC is easy to spread via lymphatic ducts, which results in recurrence, metastases, and even death [1]. Recurrent PTC mainly refers to localized and distant recurrence, including recurrence of the primary tumor, lymph node metastases, invasion of the esophagus and trachea, invasion of muscles, soft tissues and nerves, and distant metastases. Many factors can affect the recurrence of thyroid cancer, and final conclusion has not yet been reached. Many researchers believe that pathological type, staging, degree of extrathyroid invasion, lymph node metastatic rate, age, and initial surgery approach may be related to thyroid cancer recurrence. This research retrospectively analyzes the clinical data of 34 patients with recurrent PTC and presents a statistical comparison with non-recurrent patients to analyze factors related to PTC recurrence. The aim of the present work is to provide clinical evidence for standardized and appropriate treatment of recurrent PTC.
Methods
Clinical data
A total of 315 patients with PTC who were admitted to Jinan Military General Hospital from January 2009 to July 2013, including 66 male patients and 249 female patients, were recruited. The male to female ratio was 1:3.8. Ages ranged from 20 years to 78 years, and the median age was 48 years. The diameter of most tumors was less than 2 cm, the proportion of which was 47.1 % in the recurrent group and 85.8 % in the non-recurrent group. Moreover, 10.5 % (33 cases) of the patients presented extrathyroid invasion, and 42.2 % (133 cases) of the patients were found with lymph node metastases at the time of initial surgery. The tumors of 44.4 % (140 cases) of the patients showed multifocality, and 25.1 % (79 cases) of the patients had Hashimoto’s thyroiditis (HT) (Table 1). This study received the approval of the ethics committee of the General Hospital of Jinan Military Command (No. 2013ZD01).
Full size table
Pathological subtype of PTC
Recruited PTC patients were divided into three groups. Patients with the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants with higher invasiveness, higher probability of recurrence, and metastases were classified into Group 1. Patients with the follicular, clear cell, and conventional papillary carcinoma variants with similar prognosis were classified into Group 2. Patients with papillary microcarcinoma were classified into Group 3.
Initial surgery approach
The methods of primary lesion dissection used in this research included thyroid lobectomy with or without isthmectomy and total/near-total thyroidectomy. The methods of lymph node dissection included central compartment node dissection, selective neck dissection, modified neck dissection, and radical neck dissection. During statistical analysis, thyroid lobectomy with or without isthmectomy and total/near-total thyroidectomy were classified as the first type of surgical approach. Surgical approaches belonging to the first type combined with central compartment node dissection, selective neck dissection, and wide dissection of metastatic lesions were classified as the second type of surgical approach. Finally, approaches combining modified neck dissection and radical dissection were classified as the third type of surgical approach.
Statistical analysis
SPSS 17.0 software was used for statistical analysis. In addition, χ
2-test and multivariate analysis using Cox proportional hazards modeling were carried out. Factors that may be related to PTC recurrence, including gender, age, tumor size, initial surgery approach, lymph node metastasis, number of lesions, complication with HT, extrathyroid invasion, and pathological subtype, were evaluated. P < 0.05 was considered statistically significant difference.
Results
Clinicopathological information
The clinicopathological information of PTC patients is given in Table 1, and the comparisons between patients with recurrence and non-recurrence were carried out. 34 recurrent patients (11 males and 23 females) were investigated in this study. The male to female ratio was 1:2.1. Ages ranged from 24 years to 72 years old, and the median age was 46 years old. Postoperative recurrence intervals from initial surgery ranged from five months to 18 years, with a median of 46 months. Twelve patients (35.3 %) showed postoperative recurrence within two years, 14 patients (41.2 %) showed postoperative recurrence within two to five years, and eight patients (23.5 %) showed postoperative recurrence over five years later. Recurrence occurred once in 29 patients (85.3 %), twice in 4 patients (11.8 %), and thrice in 1 patient (2.9 %). Two hundred eighty-one non-recurrent PTC patients were classified into the control group (55 males and 226 females); in this group, the male to female ratio was 1:4.1, the age of onset ranged from 20 years to 78 years old, and the median age was 48 years. Patients were divided into three groups according to the pathological subtype. The number of patients belonging to Groups 1, 2, and 3 among the 34 recurrent patients were 11, 20, and 3, respectively. The number of non-recurrent patients belonging to Groups 1, 2, and 3 were 17, 134, and 130 (Table 2), respectively. Among the 34 recurrent patients, 16 patients were treated using surgeries of the first type, 14 patients were treated using surgeries of the second type, and 4 patients were treated using surgeries of the third type. The numbers of non-recurrent patients treated by the first, second, and third types of surgery were 62, 137, and 82, respectively.
Full size table
Univariate analysis of factors related to PTC recurrence
Tumor size, extrathyroid invasion, initial surgery approach, lymph node metastases, and pathological subtype showed statistical differences between the recurrent and non-recurrent groups (P < 0.05, Table 1). Larger tumors showed significantly increased risk of recurrence. The recurrence rate of micro-PTC was 2.3 % (3/133) and reached 31.0 % (18/58) when the tumor diameter grew to ≥2 cm. The higher recurrence rates, reaching 35.3 % (12/34), were observed when extrathyroid invasion was present at the time of initial surgery. Initial surgery approach also showed a significant effect on PTC recurrence; recurrence rates could reach 20.5 % (16/78) in patients without lymph node dissection but only 4.7 % (4/86) in patients receiving radical dissection and modified dissection. The recurrence rate was 17.3 % (23/133) in patients with cervical lymph node metastasis at the time of initial surgery and only 6.0 % (11/182) in patients without metastasis. In this research, patients with the tall cell, columnar cell, and oncocytic variants showed higher recurrence rates than patients with other cell variants (Table 2). Factors such as age, gender, complication with HT, and number of lesions demonstrated no correlation with tumor recurrence (P > 0.05, Table 1).
Multivariate analysis of factors related to PTC recurrence
Multivariate analysis revealed that initial surgery approach and pathological subtype were the main factors related to PTC recurrence (P < 0.001, Table 3). Initial surgery approach was negatively correlated with PTC recurrence (β = −0.320, OR = 0.726). Thus, patients receiving conservative treatment are more likely to develop PTC recurrence than patients treated with more radical modalities. Recurrence rates decreased with increasing surgical scope. Pathological subtype also showed a close correlation with PTC recurrence (β = 0.923, OR = 2.517).
Full size table
Discussion
PTC is the most common but least aggressive histological subtype of thyroid cancer. Most patients with PTC have excellent prognosis. However, recent studies have demonstrated increasing incidence of recurrent PTC [2, 3]. Many factors can affect thyroid cancer recurrence, but final conclusions have not been reached. The results of some studies show that the pathological type, staging, degree of extrathyroid invasion, lymph node metastatic rate, age, and initial surgery approach are related to thyroid cancer recurrence [4, 5]. Our research showed that tumor size, extrathyroid invasion, initial surgery approach, lymph node metastasis, and pathological subtype demonstrate statistically significant differences between the recurrent and non-recurrent groups. By contrast, factors such as age, gender, complication with HT, and number of lesions are not correlated with tumor recurrence. Multivariate analysis results further revealed that initial surgery approach and pathological subtype are main factors related to PTC recurrence.
The dissection methods of primary lesions of PTC include (1) hemithyroidectomy with or without isthmectomy, (2) total/near-total thyroidectomy, and (3) extension of surgical scope. In case of severe extrathyroid invasion, such as invasion of the esophagus, trachea, and nerves, extending the scope of surgery is required. The methods of neck dissection are as follows: (1) central compartment node dissection (unilateral or bilateral), (2) selective neck dissection, (3) functional compartmental en-bloc neck dissection, (4) modified neck dissection, and (5) radical neck dissection [6]. Mazzaferri et al. [7] found that the recurrence rate after partial thyroidectomy is nearly twice that of total and near-total thyroidectomy. By contrast, Cunningham et al. [8] revealed that the recurrence rates had no significant difference between hemithyroidectomy and total/near-total thyroidectomy groups. Monacelli et al. [9] suggested that total thyroidectomy combined with central node dissection must be performed even in the absence of risk factors and without clinically evident nodes. However, some researchers do not advocate prophylactic central neck lymphadenectomy [10]. Univariate analysis in this research showed that initial surgery approach exerts a great impact on the prognosis. For example, while 47.1 % (16/34) of the recurrent PTC patients received the first type of surgery as initial surgery, only 22.1 % (62/281) of the non-recurrent PTC patients received the first type of surgery. About 52.9 % (18/34) of the recurrent PTC patients received the second and third types of surgery. In comparison, 77.9 % (219/281) of the non-recurrent PTC patients received the second and third types of surgery as the initial surgery. Multivariate analysis revealed that initial surgery approach is the main factor related to PTC recurrence (P < 0.001); specifically, initial surgery approach demonstrated a negative correlation with PTC recurrence (β = −0.320, OR = 0.726).
The recurrence rate decreased with increasing surgical scope. Non-standardized surgical approaches with inappropriately small surgical scopes could lead to tumor residue. Moreover, lesions of lymph node metastasis may be missed, thereby increasing the risk of recurrence. Possible reasons behind the inconsistency of results are as follows: (1) Differences among recruited patients. Patients receiving neck dissection showed significant metastases, whereas no cervical lymph node metastasis was discovered before the operation in patients who did not receive neck dissection. (2) Insufficient number of recruited patients. (3) Difference in surgical techniques among surgeons. Considering these factors, blindly extending or narrowing the surgical scope is irrational.
The World Health Organization (WHO) histological classification of tumors has redefined the subtypes of non-conventional PTC [11]: follicular variant, oncocytic variant, diffuse sclerosing variant, tall cell variant, columnar cell variant, solid variant, PTC with nodular fasciitis-like stroma, clear cell variant, and diffuse follicular variant. PTC patients of different histological subtypes may exhibit diverse clinical and biological behaviors. Subtypes including the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants have higher invasiveness and may promote higher risks of recurrence and metastases [12–14]. The prognosis of patients with the follicular and clear cell variants is similar to that of patients with conventional papillary carcinoma [15]. Thyroid microcarcinoma is a type of papillary carcinoma that is less than 1 cm in diameter with relatively low invasiveness and good prognosis [16]. This research classified histological variants according to the WHO histological classification of tumors. Patients with the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants were classified into Group 1; patients with the follicular, clear cell, and conventional PTC variants were classified into Group 2; and patients with papillary microcarcinomas were classified into Group 3. The research conducted by Boone et al. [17] showed that the recurrence rate of patients with differentiated thyroid carcinoma is lower than that of patients with other types of thyroid carcinoma. Among the differentiated thyroid carcinomas, the recurrence rate of PTC is lower than that of the follicular variant. However, 30 % of the PTC patients continue to suffer from recurrence, metastasis, and even death [18]. Univariate analysis demonstrated that pathological subtype is obviously correlated with PTC recurrence (P < 0.01). Multivariate analysis also indicated that pathological subtype is closely related to PTC recurrence (β = 0.923, OR = 2.517). The recurrence rate of PTC increased as the invasiveness of the tumor increased. Thus, close follow-up must be carried out in patients with the tall cell, columnar cell, diffuse sclerosing, and oncocytic variants. Effective treatment measures must be taken once recurrence is discovered.
Various results are reported in the literature regarding the effect of lymph node metastases on PTC recurrence. Some studies indicate that lymph node metastases do not affect PTC recurrence [19]. However, some researchers have found that the number of lymph node metastases is associated with postoperative recurrence or re-metastasis. Thus, lymph node metastasis has become an important factor affecting the prognosis and recurrence of thyroid carcinoma [20]. The results of this research revealed statistically significant differences in lymph node metastases between the recurrent and non-recurrent groups. Patients with lymph node metastases at the time of initial surgery are more likely to suffer recurrence than those without metastases. The correlation of cervical lymph node metastases with recurrence needs to be confirmed through large-sample and long-term studies.
Of the 34 recurrent PTC patients in the group, postoperative recurrence intervals ranged from five months to 18 years, with a median time of 46 months. Recurrence was observed to occur within a short period of time. The majority of PTC patients, for example, showed recurrence within two to five years from surgery. Furthermore, recurrence may also occur more than once. Therefore, PTC patients must have regular reexamination with frequent follow-ups within five years after the first treatment. Ultrasound examination must be performed at least once a year within five years after the first treatment for timely discovery of tumor recurrence.
Conclusions
In conclusion, initial surgery approach, tumor size, extrathyroid invasion, lymph node metastases, and pathological type may be related to PTC recurrence. However, opinions on the resection scope of PTC differ. Surgical indications and methods vary on a case-to-case basis. According to Untch et al. [21], lobectomy for patients with low risk is suitable. Nixon et al. [22] demonstrated no difference in the 10-year survival rate of patients with low-risk highly differentiated thyroid carcinoma and those receiving lobectomy and total thyroidectomy. Doctors must consider patient compliance during follow-ups when evaluating whether or not the patient must receive thyroid lobectomy. For individuals with poor economic means, low education levels, poor knowledge about their condition, and inability to accomplish regular follow-up, complete thyroidectomy may be a suitable option. The most appropriate resection scope for PTC can be determined by considering the thoroughness of operation, the functions of the thyroid and parathyroid glands, and the relationships between important anatomical positions. Enhanced follow-up and postoperative reexamination must be carried out in patients with increased risk of recurrence. Effective and regular treatments must be administered once recurrence is discovered.
Consent
Written informed consent was obtained from the patient for the publication of this report and any accompanying images.
References
-
Giordano D, Frasoldati A, Kasperbauer JL, Gabrielli E, Pernice C, Zini M, et al. Lateral neck recurrence from papillary thyroid carcinoma: predictive factors and prognostic significance. Laryngoscope. 2014. doi:10.1002/lary.25094.
PubMed
Google Scholar
-
Lee CW, Roh JL, Gong G, Cho KJ, Choi SH, Nam SY, et al. Risk factors for recurrence of papillary thyroid carcinoma with clinically node-positive lateral neck. Ann Surg Oncol. 2015;22(1):117–24.
Article
PubMedGoogle Scholar
-
Lang BH, Lee GC, Ng CP, Wong KP, Wan KY, Lo CY. Evaluating the morbidity and efficacy of reoperative surgery in the central compartment for persistent/recurrent papillary thyroid carcinoma. World J Surg. 2013;37(12):2853–9.
Article
PubMedGoogle Scholar
-
Londero SC, Krogdahl A, Bastholt L, Overgaard J, Trolle W, Pedersen HB, et al. Papillary thyroid microcarcinoma in Denmark 1996–2008: a national study of epidemiology and clinical significance. Thyroid. 2013;23(9):1159–64.
Article
PubMedGoogle Scholar
-
Ardito G, Revelli L, Giustozzi E, Salvatori M, Fadda G, Ardito F, et al. Aggressive papillary thyroid microcarcinoma: prognostic factors and therapeutic strategy. Clin Nucl Med. 2013;38(1):25–8.
Article
PubMedGoogle Scholar
-
Cooper DS, Doherty GM, Haugen BR, Kloos RT, Lee SL, Mandel SJ, et al. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2009;19(11):1167–214.
Article
PubMedGoogle Scholar
-
Mazzaferri EL, Jhiang SM. Long-term impact of initial surgical and medical therapy on papillary and follicular thyroid cancer. Am J Med. 1994;97(5):418–28.
Article
CAS
PubMedGoogle Scholar
-
Cunningham MP, Duda RB, Recant W, Chmiel JS, Sylvester JA, Fremgen A. Survival discriminants for differentiated thyroid cancer. Am J Surg. 1990;160(4):344–7.
Article
CAS
PubMedGoogle Scholar
-
Monacelli M, Lucchini R, Polistena A, Triola R, Conti C, Avenia S, et al. Total thyroidectomy and central lymph node dissection. Experience of a referral centre for endocrine surgery. G Chir. 2014;35(5–6):117–21.
CAS
PubMed Central
PubMedGoogle Scholar
-
Delogu D, Pisano IP, Pala C, Pulighe F, Denti S, Cossu A, et al. Prophylactic central neck lymphadenectomy in high risk patients with T1 or T2 papillary thyroid carcinoma: is it useful? Ann Ital Chir. 2014;85(3):225–9.
PubMed
Google Scholar
-
Delellis RA, Lloyd RV, Heitz PU, Eng C. Pathology and Genetics Tumours of Endocrine Organs. Lyon: IARC press; 2003.
Google Scholar
-
Roman S, Sosa JA. Aggressive variants of papillary thyroid cancer. Curr Opin Oncol. 2013;25(1):33–8.
Article
PubMedGoogle Scholar
-
Kuo CS, Tang KT, Lin JD, Yang AH, Lee CH, Lin HD. Diffuse sclerosing variant of papillary thyroid carcinoma with multiple metastases and elevated serum carcinoembryonic antigen level. Thyroid. 2012;22(11):1187–90.
Article
CAS
PubMedGoogle Scholar
-
Evans WD. De-differentiation of papillary thyroid carcinoma into squamous cell carcinoma. A case of coexistence within an excised neck lesion. BMJ Case Rep 2012, 2012. doi: 10.1136/bcr-2012-007707.
-
Zidan J, Karen D, Stein M, Rosenblatt E, Basher W, Kuten A. Pure versus follicular variant of papillary thyroid carcinoma: clinical features, prognostic factors, treatment, and survival. Cancer. 2003;97(5):1181–5.
Article
PubMedGoogle Scholar
-
Melcescu E, Horton WB, Pitman KT, Vijayakumar V, Koch CA. Euthyroid Graves’ orbitopathy and incidental papillary thyroid microcarcinoma. Hormones (Athens). 2013;12(2):298–304.
Article
Google Scholar
-
Boone RT, Fan CY, Hanna EY. Well-differentiated carcinoma of the thyroid. Otolaryngol Clin North Am. 2003;36(1):73–90. viii.
Article
PubMedGoogle Scholar
-
Shoup M, Stojadinovic A, Nissan A, Ghossein RA, Freedman S, Brennan MF, et al. Prognostic indicators of outcomes in patients with distant metastases from differentiated thyroid carcinoma. J Am Coll Surg. 2003;197(2):191–7.
Article
PubMedGoogle Scholar
-
Ito Y, Tomoda C, Uruno T, Takamura Y, Miya A, Kobayashi K, et al. Clinical significance of metastasis to the central compartment from papillary microcarcinoma of the thyroid. World J Surg. 2006;30(1):91–9.
Article
PubMedGoogle Scholar
-
Watkinson JC, Franklyn JA, Olliff JF. Detection and surgical treatment of cervical lymph nodes in differentiated thyroid cancer. Thyroid. 2006;16(2):187–94.
Article
PubMedGoogle Scholar
-
Untch BR, Palmer FL, Ganly I, Patel SG, Michael Tuttle R, Shah JP, et al. Oncologic outcomes after completion thyroidectomy for patients with well-differentiated thyroid carcinoma. Ann Surg Oncol. 2014;21(4):1374–8.
Article
PubMedGoogle Scholar
-
Nixon IJ, Ganly I, Patel SG, Palmer FL, Whitcher MM, Tuttle RM, et al. Thyroid lobectomy for treatment of well differentiated intrathyroid malignancy. Surgery. 2012;151(4):571–9.
Article
PubMedGoogle Scholar
Download references
Acknowledgments
This study was supported by the President Fund of the General Hospital of Jinan Military Command (2013ZD01).
Author information
Author notes
Authors and Affiliations
-
Department of Thyroid and Breast Surgery, General Hospital of Jinan Military Command, Jinan, 250031, China
Jian Zhu
-
Department of Pathology, Affiliated Hospital of Taishan Medical College, Taian, 271000, China
Xinli Wang
-
Medical Administration Division, General Hospital of Jinan Military Command, Jinan, 250031, China
Xiaoxuan Zhang
-
Department of Pathology, General Hospital of Jinan Military Command, 25 Shifan Road, Tianqiao District, Jinan, 250031, China
Peifeng Li
-
Department of Statistics, Taishan Medical College, Taian, 271000, China
Haifeng Hou
Authors
- Jian Zhu
You can also search for this author in
PubMed Google Scholar - Xinli Wang
You can also search for this author in
PubMed Google Scholar - Xiaoxuan Zhang
You can also search for this author in
PubMed Google Scholar - Peifeng Li
You can also search for this author in
PubMed Google Scholar - Haifeng Hou
You can also search for this author in
PubMed Google Scholar
Corresponding author
Correspondence to
Peifeng Li.
Additional information
Competing interests
The authors declare that they have no competing interests.
Authors’ contributions
JZ and PFL conceived and designed the experiments. JZ, XLW and XXZ collected the data. PFL and HFH analyzed the data. PFL and XLW wrote the paper. All authors read and approved the final manuscript.
Jian Zhu, Xinli Wang and Xiaoxuan Zhang contributed equally to this work.
Rights and permissions
Open Access This article is licensed under a Creative Commons Attribution 4.0 International License, which permits use, sharing, adaptation, distribution and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons licence, and indicate if changes were made.
The images or other third party material in this article are included in the article’s Creative Commons licence, unless indicated otherwise in a credit line to the material. If material is not included in the article’s Creative Commons licence and your intended use is not permitted by statutory regulation or exceeds the permitted use, you will need to obtain permission directly from the copyright holder.
To view a copy of this licence, visit https://creativecommons.org/licenses/by/4.0/.
The Creative Commons Public Domain Dedication waiver (https://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated in a credit line to the data.
Reprints and Permissions
About this article
Cite this article
Zhu, J., Wang, X., Zhang, X. et al. Clinicopathological features of recurrent papillary thyroid cancer.
Diagn Pathol 10, 96 (2015). https://doi.org/10.1186/s13000-015-0346-5
Download citation
-
Received: 20 January 2015
-
Accepted: 09 July 2015
-
Published: 14 July 2015
-
DOI: https://doi.org/10.1186/s13000-015-0346-5
Keywords
- Clinicopathological features
- Initial surgery approach
- Papillary thyroid cancer
- Pathological subtype
- Recurrence
Медицинский эксперт статьи
Новые публикации
Папиллярный рак щитовидной железы
, медицинский редактор
Последняя редакция: 17.10.2021
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Наиболее распространенный вид карциномы щитовидки – это папиллярный рак щитовидной железы.
Эта опухоль происходит, как правило, из обычной ткани железы и обнаруживается в виде неоднородного значительного или кистоподобного образования. Данный вид онкологии хорошо поддается лечению. Показательная 10-летняя выживаемость пациентов достигает почти 90%. И все же заболевание достаточно серьезное, как и все онкопатологии, поэтому остановимся на нём подробнее.

Код по МКБ-10
C73 Злокачественное новообразование щитовидной железы
Причины папиллярного рака щитовидной железы
Озлокачествление здоровых клеток щитовидки может происходить вследствие генетических аномалий, которые зачастую бывают спровоцированы неблагоприятным влиянием окружающей обстановки (радиоактивная зона, вредные производства неподалеку и пр.). В более редких случаях такие аномалии носят врожденный характер.
Мутации в генах дают толчок к избыточному росту и делению клеточных структур. Обнаружены несколько генных модификаций, связанных с формированием папиллярного рака щитовидной железы:
- RET/PTC – мутирование данного гена встречается в 20% всех зарегистрированных заболеваний папиллярным раком щитовидки. Зачастую обнаруживается в детском возрасте и в регионах с неблагоприятной радиоактивной обстановкой;
- BRAF – мутирование данного гена можно обнаружить в 40-70% заболеваний папиллярным раком щитовидки. Онкопатология, связанная с мутацией данного гена, носит более агрессивный характер с обилием метастазов в другие органы.
Предполагают участие в формировании рака также измененных генов NTRK1 и MET. Однако причастность данных генов пока находится на стадии изучения.
Помимо этого, выделены факторы, способствующие развитию папиллярного рака:
- возрастной период от 30 до 50 лет;
- женский пол (у мужчин заболевание возникает реже);
- неблагоприятная радиоактивная обстановка, частые рентгенологические исследования, лучевая терапия;
- наследственная предрасположенность.

Симптомы папиллярного рака щитовидной железы
В большинстве случаев развитие папиллярного рака происходит постепенно. Больные первое время не предъявляют никаких жалоб на плохое самочувствие: щитовидная железа их не беспокоит.
Часто причиной обращения больного к доктору является обнаружение в области щитовидки безболезненного узлового образования. Обычно его ощущают на шее при достижении им выраженных размеров, либо при расположении узла близко к поверхности шеи. Большого размера образование может оказывать влияние на близлежащие органы, к примеру, давить на гортань или пищеводную трубку.
В дальнейшем клиническая картина расширяется. Может появиться хрипота, трудности с проглатыванием пищи, затрудненное дыхание, першение и болезненность горла.
В некоторых случаях новообразование расположено таким образом, что его становится практически невозможно прощупать. В такой ситуации заболевание выдают увеличившиеся лимфатические узлы в области шеи. Лимфатические узлы выполняют роль фильтров в лимфосистеме. Они ловят и удерживают в себе злокачественные клетки, не допуская их дальнейшего распространения. Если такие клетки попали в лимфоузел, то он увеличивается и уплотняется. Однако этот признак не всегда указывает на формирование раковой опухоли: лимфатические узлы могут увеличиваться и при попадании в них инфекции, к примеру, при простуде, гриппе и пр. Как правило, такие лимфоузлы приходят в норму после излечения от инфекции.
Где болит?
Стадии папиллярного рака щитовидной железы
Развитие папиллярного рака щитовидной железы проходит четыре стадии. Чем наиболее ранняя стадия подверглась лечению, тем благоприятнее будет прогноз болезни.
- I ст.: узел располагается обособленно, щитовидная капсула не видоизменена, метастазы не обнаружены.
- IIа ст.: единичный узел, который влияет на форму щитовидной железы, однако не вызывает метастазирования.
- IIб ст.: единичный узел с обнаружением односторонних метастазов.
- III ст.: новообразование, которое выходит за пределы капсулы, либо оказывает давление на ближайшие органы и тканевые структуры; при этом метастазы образуются в лимфоузлах в двустороннем порядке.
- IV ст.: новообразование прорастает в близлежащие ткани, метастазирование наблюдается как в ближайших, так и в отдаленных участках организма.
Папиллярный рак способен возникать непосредственно в щитовидной железе, либо попадать в железу в качестве метастаза из других органов.
Метастазы папиллярного рака щитовидной железы
Метастазы папиллярного рака щитовидной железы могут распространяться по лимфатической системе, расположенной внутри железы, а также часто переходят в лимфоузлы с пораженной стороны. Дальние (дистальные) метастазы обнаруживаются нечасто и формируются в большей степени из фолликулярных тканей злокачественного образования.
Папиллярный рак и метастазы с папиллярным построением тканей считаются неактивными по отношению к гормонам и не способны к удержанию радиоактивного йода. Метастазы с фолликулярным построением проявляют активность к гормонам и удерживают радиоактивный йод.
Классификация метастазов папиллярного рака щитовидной железы осуществляется следующим образом:
- N – присутствуют ли регионарные метастазы папиллярного рака щитовидки.
- NX – не представляется возможности оценить наличие метастазов в шейных лимфоузлах.
- N0 – отсутствие регионарного метастазирования.
- N1 – обнаружение регионарных метастазов.
- M – присутствуют ли отдаленные метастазы.
- MX – не представляется возможности оценить наличие отдаленных метастазов.
- M0 – отсутствие отдаленного метастазирования.
- M1 – обнаружение отдаленного метастазирования.
Данная классификация применяется для уточнения диагноза папиллярного рака щитовидной железы и проведения прогноза заболевания.
Диагностика папиллярного рака щитовидной железы
В качестве диагностики папиллярного рака щитовидной железы используются следующие методики:
- Метод тонкоигольной аспирационной биопсии – это основная процедура, которую назначает доктор при подозрении на онкологию щитовидки. Зачастую положительный результат биопсии может сделать данный метод единственным в диагностике заболевания. Биопсия проводится таким образом: доктор, контролируя процесс на экране УЗИ, проводит введение тонкой иглы внутрь подозрительного узла. Далее присоединяется шприц, и ткань узла как бы засасывается сквозь иглу. После этого взятые ткани отправляются на экспертизу на предмет их злокачественности.
- Ультразвуковой метод исследования щитовидки – предоставляет возможность рассмотреть границы органа, строение и структуру тканей железы. Это наиболее безопасная и недорогая процедура диагностики папиллярного рака, а также достаточно информативная. УЗИ можно использовать в качестве самостоятельного метода, либо в сочетании с биопсией. К сожалению, самостоятельно процедура выполняется нечасто, так как УЗИ может информировать о наличии новообразования в железе, но не может точно определить степень его злокачественности.
- КТ, МРТ – томографические методы исследования применяют, в основном, если злокачественное поражение распространяется на ближайшие ткани и органы.
- Лабораторные анализы – анализ крови на содержание гормонов щитовидной железы и гипофиза. Результаты таких анализов дают представление о недостаточной, избыточной или нормальной функции железы.
- Метод радиоизотопного сканирования – проводят, как правило, в том случае, если анализ крови указал на избыточную функцию щитовидной железы.
Без сомнения, грамотная диагностика папиллярного рака щитовидной железы – это залог дальнейшего успешного лечения заболевания.

Что нужно обследовать?
Как обследовать?
Какие анализы необходимы?
К кому обратиться?
Лечение папиллярного рака щитовидной железы
Лечение папиллярного рака щитовидной железы – оперативное. Операция носит название тиреоэктомия.
- Тотальное удаление железы – полное удаление, когда хирург удаляет левую и правую долю щитовидки вместе с перешейком. Если есть необходимость, одновременно проводит иссечение увеличенных лимфатических узлов. Операция по тотальной тиреоэктомии в среднем длится около 3-х или 4-х часов. В проекции железы доктор делает вскрытие и проводит удаление железы, аккуратно проводя её между возвратными нервами. После тотального оперативного вмешательства проводится заместительная терапия, которая предусматривает восполнение в организме гормонов теперь уже отсутствующей щитовидной железы.
- Частичное удаление железы – используется при относительно небольшом размере новообразования, которое расположено обособленно в одной доле железы и не прорастает в ближайшие органы и ткани. Как правило, размер опухоли в таких случаях не составляет более 10 мм. Длительность такого оперативного вмешательства – от полутора до двух часов. Проведение заместительной терапии в большинстве случаев не требуется.
Несмотря на то, что оперативное вмешательство на щитовидной железе – это довольно сложная операция, восстановление после неё проходит быстро и не доставляет большого дискомфорта больным.
Возвращаться к привычному образу жизни можно практически сразу. Диета после операции не требуется. Пациента выписывают чаще всего на следующий день.
Дополнительно, на усмотрение врача, может быть назначена гормональная терапия и терапия радиоактивным йодом.
Профилактика папиллярного рака щитовидной железы
Так как окончательная причина папиллярного рака щитовидной железы до сих пор не установлена, специфических мер профилактики заболевания нет. Но существуют мероприятия, которые в целом помогут уменьшить опасность формирования раковой опухоли.
- Старайтесь избегать облучения зоны головы и шеи, в том числе и рентгеновскими лучами.
- При возможности поменяйте район проживания, подальше от атомных станций и экологически неблагоприятных районов.
- Периодически обследуйте щитовидную железу, сдавайте кровь на уровень гормонов, проходите профилактическое УЗИ, в особенности, если вы находитесь в группе риска.
Конечно, такое заболевание, как рак, пока еще сложно предупредить. Однако раннее обнаружение патологии в большинстве случаев гарантирует благоприятный прогноз.
Прогноз при папиллярном раке щитовидной железы
Прогноз при папиллярном раке щитовидной железы можно назвать благоприятным. Если метастазы не обнаружены, либо обнаружены в непосредственной близости от железы, то длительность качественной жизни пациентов после операции высока. Большинство прооперированных больных живут после вмешательства 10-15 лет и более.
Если были обнаружены метастазы в костную ткань и дыхательную систему, то процент оптимистичного прогноза несколько ухудшается. Хотя и в этом случае возможен положительный исход. При этом, чем моложе пациент, тем больше шансов, что он лучше и благоприятнее перенесет лечение.
Летальный исход у пациентов, перенесших тиреоэктомию, может наблюдаться лишь при повторном формировании опухоли в сохранившемся элементе щитовидной железы.
У пациентов, которым провели удаление части или всей железы, качество жизни, как правило, не нарушается. Иногда после операции возможно изменение голоса, небольшая охриплость. Появление таких симптомов зависит от степени повреждения нервных волокон во время операции, а также от отечности голосовых связок. Чаще всего такие изменения являются преходящими.
Пациенты, которые перенесли папиллярный рак щитовидной железы, в дальнейшем должны периодически обследоваться у доктора, сначала раз в 6 месяцев, а потом каждый год, для того, чтобы предупредить появление рецидива злокачественной опухоли.
Что такое рак щитовидной железы?
Рак щитовидной железы – злокачественная опухоль, растущая из эпителия щитовидной железы. В щитовидной железе существует три типа клеток: А, В и С. Из клеток типа А и В, вырабатывающих в норме гормоны щитовидной железы тироксин и трийодтиронин, развиваются чаще всего дифференцированные формы рака щитовидной железы: фолликулярный и папиллярный, а также редкая и опасная опухоль – анапластический рак щитовидной железы. Из клеток типа С развивается медуллярный рак щитовидной железы (медуллярная карцинома щитовидной железы или С-клеточный рак).
Распространенность рака щитовидной железы
В настоящее время в научных работах часто встречаются утверждения о повышении частоты встречаемости рака щитовидной железы у жителей нашей планеты. Однако, если провести анализ статистики, становится понятно, что речь идет не об истинном повышении частоты встречаемости рака щитовидной железы, а об улучшении выявляемости этих опухолей вследствие улучшения диагностических возможностей (прежде всего – благодаря появлению очень чувствительных и точных УЗИ-аппаратов, которые используются практически повсеместно). Сейчас диагноз рака щитовидной железы часто ставится при размере узла от 4 мм, и даже такие маленькие опухоли щитовидной железы могут становиться причиной развития регионарных метастазов (метастазов в лимфоузлах) и отдаленных метастазов (в легких, костях, печени, головном мозге).
Вместе с тем, распространенность рака щитовидной железы в последние годы в некоторых регионах возрастала не только в связи с повышенными возможностями диагностики. Общеизвестно, что аварии на ядерных объектах (и прежде всего, Чернобыльская катастрофа) привели к значительному росту заболеваемости раком щитовидной железы в Украине, Беларуси и некоторых регионах России. После аварии на Чернобыльской АЭС некоторое время в Украине регистрировалось резко увеличенное число пациентов с раком щитовидной железы и прежде всего – пациентов детского возраста. К счастью, к настоящему моменту эта «волна» заболеваемости сошла на нет, однако в числе пострадавших оказались тысячи и тысячи пациентов.
Важно отметить, что региональная структура заболеваемости раком щитовидной железы не имеет четкой географической привязки. Широко распространенные в России страхи на тему, что солнце и южный климат могут вызывать рак щитовидной железы или ухудшать жизнь пациентов после операции, не имеют под собой никаких научных обоснований. Южные страны не характеризуются повышенной заболеваемостью раком щитовидной железы. Даже наоборот – в северных регионах нашей планеты чаще встречаются аутоиммунные заболевания щитовидной железы, которые в ряде случаев могут приводить к развитию рака щитовидной железы.
Причины возникновения рака щитовидной железы
В числе возможных причин, вследствие которых развивается рак щитовидной железы, можно указать ионизирующую радиацию, наследственность, наличие аутоиммунных заболеваний щитовидной железы (прежде всего – аутоиммунного тиреоидита). Следует отметить, что возраст не является фактором, увеличивающим число заболевших раком щитовидной железы – пик заболеваемости фолликулярным раком и папиллярным раком приходится на 30-35 лет. Только анапластический рак щитовидной железы напрямую связан с возрастом – он крайне редко встречается у пациентов моложе 60 лет.
Диагностика рака щитовидной железы
Рак щитовидной железы наиболее часто выявляется при УЗИ щитовидной железы в виде узлового образования. Специфических ультразвуковых признаков, позволяющих со 100%-ной точностью установить диагноз рака щитовидной железы, не существует. Вместе с тем, описан ряд признаков, позволяющих заподозрить наличие рака щитовидной железы: к ним относятся темный цвет узла (гипоэхогенность), наличие нечетких или неровных контуров узла, появление микрокальцинатов в узле, появление усиленного кровотока в узле, специфические изменения в расположенных рядом с щитовидной железой лимфатических узлах шеи (округление узлов, появление в них кистозных полостей).
Диагностика рака щитовидной железы основывается на проведении тонкоигольной биопсии узлов щитовидной железы. Именно это простое, но очень информативное исследование позволяет установить диагноз рака щитовидной железы. При биопсии без каких-либо сомнений могут быть выявлены папиллярный рак щитовидной железы, медуллярный рак щитовидной железы, анапластический рак щитовидной железы, плоскоклеточный рак щитовидной железы и лимфома. Диагноз фолликулярного рака щитовидной железы при тонкоигольной биопсии установлен быть не может – его можно лишь заподозрить и установить диагноз «Фолликулярная опухоль», т.е. опухоль с 15-20-ной вероятностью злокачественности.
Для дифференцированных форм рака щитовидной железы (фолликулярного рака, папиллярного рака щитовидной железы), а также для анапластического рака специфических гормональных маркеров не существует. Для медуллярного рака щитовидной железы такой онкомаркер есть – это гормон кальцитонин, вырабатываемый С-клетками щитовидной железы. При возникновении опухолей щитовидной железы из С-клеток концентрация кальцитонина в крови значительно повышается и обычно превышает 100 пг/мл. При выявлении пограничного повышения уровня кальцитонина (от 20 до 100) может быть рекомендовано исследование стимулированного уровня кальцитонина, т.е. исследование после внутривенного введения глюконата кальция (проводится обычно в специализированных центра эндокринной хирургии и эндокринологии).
Симптомы рака щитовидной железы
Следует отметить, что в подавляющем большинстве случаев рак щитовидной железы не проявляется серьезными признаками и не вызывает почти никаких жалоб. Большинство пациентов имеет и совершенно нормальный уровень гормонов щитовидной железы. Для многих пациентов диагноз «Рак щитовидной железы» становится неприятным сюрпризом на фоне полного здоровья. Признаки рака щитовидной железы у большинства пациентов полностью отсутствуют – важно это помнить.
Вместе с тем, существуют симптомы рака щитовидной железы, которые можно назвать очень настораживающими. К их числу относится появление осиплости голоса, резкого уплотнения в области щитовидной железы, видимого на глаз и быстро нарастающего в объеме опухолевого образования в области щитовидной железы, нарушения глотания и дыхания.
Прогноз рака щитовидной железы
Необходимо помнить, что в подавляющем большинстве случаев рак щитовидной железы на современном уровне развития медицины излечим. Безусловно, если пациенту установлен диагноз «рак щитовидной железы», пациенту как придется оперироваться, и щитовидную железу в большинстве случаев придется полностью удалить (в ряде случаев с окружающими ее лимфоузлами), однако после удаления щитовидной железы пациент остается совершенно нормальным человеком, способным вести полноценную жизнь без каких-либо ограничений.
Важную роль при раке щитовидной железы играет своевременность проведенной операции. В настоящее время существуют научные данные, свидетельствующие о том, что в ряде случаев анапластический рак щитовидной железы – самая злокачественная опухоль человека – образуется из длительно не оперированного папиллярного рака щитовидной железы – самой «доброкачественной» злокачественной опухоли человека. Именно поэтому откладывать лечение на годы не следует. В подавляющем большинстве случаев рак щитовидной железы требует проведения операции в течение 1-2 месяцев после установления диагноза, хотя существуют и ситуации, требующие значительно более быстрого лечения – например, если выявлен анапластический рак щитовидной железы или медуллярный рак щитовидной железы.
Наилучший прогноз имеет папиллярный рак щитовидной железы. Смертность при папиллярном раке щитовидной железы может быть очень близкой к нулевой – конечно, в том случае, если лечение рака щитовидной железы проводится специалистами, имеющими достаточный опыт в данной области медицины, а также если пациент точно выполняет рекомендации врача. Вместе с тем, и фолликулярный рак щитовидной железы, и медуллярный рак щитовидной железы на ранних стадиях полностью излечимы – ранняя диагностика позволяет значительно улучшить результаты лечения.
Лечение рака щитовидной железы
Лечение рака щитовидной железы должно проводиться специалистами – это незыблемое правило, которое не подвергается сомнению. Лучшие результаты достигаются при проведении лечения в специализированной клинике эндокринной хирургии. Концентрация пациентов с одним диагнозом в подобных клиниках приводит к тому, что врачи клиник эндокринной хирургии хорошо знают все особенности лечения пациентов с раком щитовидной железы. Операции при раке щитовидной железы должны проводиться только хирургами-эндокринологами, имеющими сертификат онколога и выполняющими не менее 100 оперативных вмешательств в год на щитовидной железе.
Северо-Западный центр эндокринологии является российским лидером в области хирургии щитовидной железы – ежегодно в центре выполняется более 5000 операций. В Европе существует только три центра, выполняющих подобный объем операций ежегодно – в Пизе (Италия), в Мюнхене (Германия) и в Санкт-Петербурге. Рак щитовидной железы оперируется в центре эндокринологии ежедневно. Ежегодно в центре проводится лечение более 700 пациентов с раком щитовидной железы. Большинство онкологических пациентов центра имеют папиллярный рак щитовидной железы, несколько меньше – фолликулярный рак щитовидной железы. Редкая форма рака щитовидной железы – медуллярный рак – встречается в практике центра также весьма не редко. В 2013 году в центре было прооперировано 35 пациентов с медуллярным раком щитовидной железы. Ведущие хирурги Центра эндокринологии выполняют до 400 операций на щитовидной железе в год в течение длительного времени, поэтому их квалификация не подвергается сомнению.
В Центре эндокринологии исповедуется принцип «одного врача»: оптимальные результаты лечения рака щитовидной железы могут быть достигнуты в случае, если и диагностику, и операцию, и дальнейшее наблюдение для одного пациента проводит один врач, хорошо знающий и специфику данного вида опухоли, и индивидуальные особенности конкретного пациента. Хирурги-эндокринологи нашего центра имеют специализацию по хирургии, онкологии, эндокринологии, ультразвуковой диагностике, поэтому могут выполнить все этапы диагностики и лечения: и УЗИ щитовидной железы, и тонкоигольную биопсию узла, и операцию, и назначение дополнительных лучевых методов лечения, и подбор оптимальной дозы гормональной терапии.
В настоящее время в Северо-Западном центре эндокринологии лечение рака щитовидной железы проводится хирургами-эндокринологами, имеющими значительный опыт выполнения данных операций:

|
Слепцов Илья Валерьевич Хирург-эндокринолог высшей квалификационной категории, онколог, детский хирург, доктор медицинских наук, профессор кафедры факультетской хирургии Санкт-Петербургского государственного университета, заместитель директора по медицинской части Клиники высоких медицинских технологий им. Н.И. Пирогова Санкт-Петербургского государственного университета, член правления Азиатско-Тихоокеанской ассоциации хирургии щитовидной железы, член Европейской тиреидологической ассоциации, Европейской ассоциации эндокринных хирургов, Российской ассоциации эндокринологов. Опыт работы по специальности более 15 лет. |

|
Черников Роман Анатольевич Черников Роман Анатольевич — хирург-эндокринолог, онколог, детский хирург, доктор медицинских наук, руководитель отделения эндокринной хирургии Северо-Западного центра эндокринологии, член Европейской ассоциации эндокринных хирургов, Европейской тиреологической ассоциации. Опыт работы по специальности более 15 лет. |

|
Чинчук Игорь Константинович Хирург-эндокринолог, онколог, кандидат медицинских наук, член Европейской тиреоидологической ассоциации (ETA). Квалификационная категория первая. Стаж работы по специальности 13 лет. |

|
Успенская Анна Алексеевна Хирург-эндокринолог, сотрудник Северо-Западного центра эндокринологии, член Европейской тиреологической ассоциации. Стаж работы по специальности более 9 лет. |

|
Новокшонов Константин Юрьевич Хирург-эндокринолог, специалист по ультразвуковой диагностике, кандидат медицинских наук. Стаж работы по специальности более 8 лет. |

|
Федоров Елисей Александрович Хирург-эндокринолог, кандидат медицинских наук. Стаж работы по специальности более 12 лет. |

|
Тимофеева Наталья Игоревна Хирург-эндокринолог, кандидат медицинских наук, член Европейской тиреологической ассоциации. Стаж работы по специальности более 10 лет. |
|
|
Семенов Арсений Андреевич Хирург-эндокринолог, онколог, специалист по ультразвуковой диагностике, кандидат медицинских наук, член Европейской тиреологической ассоциации, Европейской ассоциации эндокринных хирургов. Стаж работы по специальности более 8 лет. |

|
Макарьин Виктор Алексеевич Хирург-эндокринолог, онколог, специалист по ультразвуковой диагностике, кандидат медицинских наук, член Европейской тиреологической ассоциации, Европейской ассоциации эндокринных хирургов. Стаж работы по специальности более 10 лет. |

|
Карелина Юлия Валерьевна Хирург-эндокринолог, специалист по ультразвуковой диагностике, член Европейской тиреологической ассоциации. Стаж работы по специальности более 10 лет. |

|
Малюгов Юрий Николаевич Хирург-эндокринолог высшей квалификационной категории, врач ультразвуковой диагностики, член Европейской тиреологической ассоциации. Стаж работы по специальности более 15 лет. |

|
Саблин Илья Владимирович Хирург-эндокринолог высшей квалификационной категории, врач ультразвуковой диагностики, член Европейской тиреологической ассоциации. Стаж работы по специальности более 8 лет. |

|
Горская Наталия Александровна Детский хирург, хирург-эндокринолог, член Ассоциации эндокринных хирургов. Стаж работы по специальности более 5 лет. |

|
Алексеева (Эльчепарова) Светлана Арсеновна Хирург-эндокринолог Северо-Западного центра эндокринологии |

|
Бузанаков Дмитрий Михайлович Хирург-эндокринолог Северо-Западного центра эндокринологии |
Операция при раке щитовидной железы
Если у пациента выявлен рак щитовидной железы, операция неизбежна. В ряде случаев рак щитовидной железы требует проведения операции в объеме тиреоидэктомии – полного удаления щитовидной железы. В других случаях (при опухолях небольшого размера, опухолях низкой агрессивности) может быть проведена операция в объеме удаления половины щитовидной железы. При поражении лимфоузлов проводятся различные виды лимфодиссекций – центральная лимфодиссекция (удаление лимфоузлов паратрахеальной, претрахеальной, прегортанной групп) и боковая лимфодиссекция (удаление лимфоузлов на боковой поверхности шеи).
Если у пациента выявлен запущенный рак щитовидной железы, операция может сопровождаться значительными техническими трудностями. Нередко опухоль успевает окружить голосовые нервы или прорасти в них. Встречаются и случаи прорастания опухоли в трахею, пищевод, гортань, окружающие щитовидную железу мышцы. Для проведения операции при распространенном раке очень важно располагать полным комплексом современного оборудования: от качественных операционных ламп, микроскопов для хирургов до системы поиска голосовых нервов и околощитовидных желез.
В Северо-Западном центре эндокринологии пациентам с опухолями щитовидной железы операция проводится с использованием современного оборудования:
— ультразвукового гармонического скальпеля Ethicon Ultracision (США),
— биполярного электрокоагулятора с обратной связью ERBE VIO (Германия),
— коагулирующего зажима ERBE Bi-Clamp (Германия),
— бинокулярных операционных луп Univet (Италия),
— нейростимулятора NeuroSign (Великобритания),
— эндоскопического операционного комплекса Karl Storz (Германия).
При наличии должного опыта лечения рака щитовидной железы и необходимого для этого оборудования в 95% случаев для проведения операции необходимо провести в стационаре 2-3 суток. Квалифицированные хирурги Северо-Западного центра эндокринологии в 90% случаев не используют дренирования послеоперационной раны и применяют рассасывающиеся косметические швы или кожный клей, что позволяет пациенту уже через день после операции принимать душ и избавляет от необходимости проводить перевязки и снимать шов после операции.
В отделении эндокринной хирургии, где проводится лечение пациентов, созданы наиболее благоприятные и комфортные условия для пациентов: в каждой палате оборудован качественный санузел с душем, есть кондиционеры, телефон, телевизор. На всей территории центра работает бесплатный Wi-Fi для пациентов. Вы можете ознакомиться с обстановкой в центре эндокринологии, просмотрев виртуальный тур, размещенный ниже.
Дополнительные методы лечения
В ряде случаев после хирургического лечения рака щитовидной железы может потребоваться еще один лечебный этап: проведение терапии радиоактивным йодом. Радиойодтерапия применяется только при дифференцированных формах рака: папиллярном раке щитовидной железы и фолликулярном раке щитовидной железы. Остальные формы рака щитовидной железы радиоактивный йод не накапливают, поэтому его применение при их выявлении бесполезно.
Дистанционная лучевая терапия применяется только в случаях, когда полностью удалить опухоль щитовидной железы не получилось из-за ее распространенности, а лечение радиойодом провести не удается (опухоль не накапливает радиоактивный йод).
В ряде случаев (например, если у пациента выявлен запущенный медуллярный рак щитовидной железы или папиллярный рак с отдаленными метастазами, не накапливающими радиоактивный йод) пациентам назначается химиотерапевтическое лечение. К сожалению, «классическая» химиотерапия при раке щитовидной железы практически бесполезна. Лечение рака требует применения наиболее современных химиотерапевтических препаратов из группы ингибиторов киназ (вандетаниб, сорафениб и др.). Часть из этих препаратов зарегистрирована в России, часть еще проходит последние этапы клинических испытаний. Специалисты Северо-Западного центра эндокринологии имеют значительный круг научных связей в мире, поэтому для пациентов, имеющих рак щитовидной железы и нуждающихся в проведении наиболее современной химиотерапии, может быть рекомендовано участие в лечении в России или за рубежом, в том числе может быть проведено и лечение в рамках клинических испытаний наиболее современных препаратов.
Лечение после операции
После операции и (если это требовалось) терапии радиоактивным йодом начинается важный этап наблюдения за пациентом, подбора правильной терапии, контроля результатов лечения. На этом этапе наблюдается значительное число тактических ошибок, обусловленных недостаточным знанием врачами специфики лечения рака щитовидной железы. В подавляющем большинстве случаев нам приходится сталкиваться с «перелечиванием» пациента, т.е. использованием излишнего количества диагностических и лечебных процедур, не улучшающих конечные результаты лечения пациента. Только опытный хирург-эндокринолог может определить ту «золотую середину» в диагностике и лечении рака щитовидной железы, когда при минимальном числе использованных лечебных и диагностических процедур в итоге рак щитовидной железы полностью излечивается.
-
Операция на щитовидной железе, медиальная тиреоидэктомия
Запись на операцию в Северо-Западный центр эндокринологии и эндокринной хирургии — ведущую специализированную клинику по лечению заболеваний щитовидной железы России и Европы: +7 812 980-77-21, +7 921 189-74-84, +7 921 420-30-31 (будни, с 9 до 17 часов). Мы принимаем на лечение пациентов из всех регионов России, стран ближнего и дальнего зарубежья.
-
Анапластический рак щитовидной железы
В ткани щитовидной железы возможно формирование нескольких видов опухолей, при этом клетки щитовидной железы могут быть источником развития как одной из наиболее доброкачественных опухолей у человека – папиллярной карциномы (папиллярного рака), так и наиболее злокачественной опухоли – анапластического рака
-
Медуллярный рак щитовидной железы
Медуллярный рак щитовидной железы (медуллярная карцинома щитовидной железы) является редким гормонально активным новообразованием злокачественной природы, развивающимся из парафолликулярных клеток щитовидной железы
-
Синдром множественной эндокринной неоплазии 2 типа
Множественная эндокринная неоплазия второго типа (синдром МЭН 2 типа) — это симптомокомплекс, объединяющий группу патологических состояний, для которых характерно наличие новообразования или гиперпластического процесса из клеток нейроэктодермы, поражающего два и более органов эндокринной системы
-
Узлы щитовидной железы
Узлом щитовидной железы называется участок ее ткани, отличающийся от остальной ткани железы при проведении УЗИ или при пальпации (ощупывании). Ощупывание щитовидной железы позволяет выявить узлы у 5-7% жителей нашей планеты. С распространением УЗИ щитовидной железы узлы этого органа стали выявлять у 20-30% людей. С возрастом распространенность узлов щитовидной железы увеличивается, и в 50 лет узлы уже можно обнаружить у 50% женщин и примерно 20% мужчин. В 60 лет количество женщин, имеющих узлы щитовидной железы, уже начинает превышать количество женщин, не имеющих этой патологии.
-
Тиреоглобулин
Тиреоглобулин — это важнейший белок, содержащийся в ткани щитовидной железы, из которого вырабатываются гормоны щитовидной железы Т3 и Т4. Уровень тиреоглобулина используется в качестве основного маркера рецидива дифференцированного рака щитовидной железы (фолликулярного и папиллярного). Вместе с тем, зачастую тиреоглобулин сдается без показаний — это увеличивает расходы пациентов. Статья посвящена значению тиреоглобулина, показаниям к сдаче анализа на тиреоглобулин и оценке результатов
-
Внимание! Кальцитонин повышен!
Что такое кальцитонин? Зачем сдается анализ крови на кальцитонин? Какова норма кальцитонина? Что делать, если кальцитонин повышен? На все эти вопросы Вы найдете ответ в статье, посвященной гормону кальцитонину и его клиническому значению
-
Если Ваш ответ биопсии «Фолликулярная аденома щитовидной железы»…
Если по результатам тонкоигольной биопсии Вам был установлен цитологический диагноз «Фолликулярная аденома щитовидной железы», Вы должны знать — диагноз Вам установлен НЕПРАВИЛЬНО. Почему невозможно установить диагноз фолликулярной аденомы при тонкоигольной биопсии узла щитовидной железы подробно описано в этой статье
-
Удаление щитовидной железы
Информация об удалении щитовидной железы в Северо-Западном центре эндокринологии (показания, особенности проведения, последствия, как записаться на операцию)
-
Диффузный эутиреоидный зоб
Диффузный эутиреоидный зоб — это видимое невооруженным глазом или выявляемое при пальпации общее диффузное увеличение щитовидной железы, характеризующееся сохранением её функции
-
Аутоиммунный тиреоидит (АИТ, тиреоидит Хашимото)
Аутоиммунный тиреоидит (АИТ) — это воспаление ткани щитовидной железы, вызванное аутоиммунными причинами, очень часто встречающееся в России. Болезнь эта была открыта ровно 100 лет назад японским ученым по фамилии Хашимото, и с тех пор носит его имя (тиреоидит Хашимото). В 2012 году мировая эндокринологическая общественность широко отмечала юбилей открытия данного заболевания, поскольку с этого момента у эндокринологов появилась возможность эффективно помогать миллионам пациентов по всей планете.
-
Щитовидная железа. Заболевания щитовидной железы
В настоящее время изучению заболеваний щитовидной железы уделяется настолько серьезное внимание, что был выделен особый раздел эндокринологии — тиреоидология, т.е. наука о щитовидной железе. Врачей, занимающихся диагностикой и лечением заболеваний щитовидной железы, называют тиреоидологами.
-
Анализы в Санкт-Петербурге
Одним из важнейших этапов диагностического процесса является выполнение лабораторных анализов. Чаще всего пациентам приходится выполнять анализ крови и анализ мочи, однако нередко объектом лабораторного исследования являются и другие биологические материалы.
-
Анализ на гормоны щитовидной железы
Анализ крови на гормоны щитовидной железы — один из наиболее важных в практике работы Северо-Западного центра эндокринологии. В статье Вы найдете всю информацию, с которой необходимо ознакомиться пациентам, собирающимся сдать кровь на гормоны щитовидной железы
-
Сделать биопсию
Для чего же необходимо проведение биопсии узлов щитовидной железы?
-
Операции на щитовидной железе
Северо-Западный центр эндокринологии – ведущее учреждение эндокринной хирургии России. В настоящее время в центре ежегодно выполняется более 5000 операций на щитовидной железе, околощитовидных (паращитовидных) железах, надпочечниках. По количеству операций Северо-Западный центр эндокринологии устойчиво занимает первое место в России и входит в тройку ведущих европейских клиник эндокринной хирургии
-
Тонкоигольная биопсия узлов щитовидной железы
Тонкоигольная биопсия — основной метод оценки морфологического строения узлов щитовидной железы. В ходе биопсии производится оценка клеточного состава узла, что дает возможность определения дальнейшей тактики лечения
-
Экспертное УЗИ щитовидной железы
УЗИ щитовидной железы является главным методом, позволяющим оценить строение этого органа. Благодаря своему поверхностному расположению, щитовидная железа легко доступна для проведения УЗИ. Современные ультразвуковые аппараты позволяют осматривать все отделы щитовидной железы, за исключением расположенных за грудиной или трахеей.
-
УЗИ шеи
Информация об УЗИ шеи — входящие в него исследования, их особенности
-
Консультация хирурга-эндокринолога
Хирург-эндокринолог – врач, специализирующийся на лечении заболеваний органов эндокринной системы, требующих использования хирургических методик (оперативного лечения, малоинвазивных вмешательств)
-
УЗИ брюшной полости
УЗИ брюшной полости – самый информативный и доступный метод диагностики
заболеваний органов брюшной полости (печени, селезенки, поджелудочной
железы), а также расположенных в брюшной полости протоков и сосудов -
Интраоперационный нейромониторинг
Интраоперационный нейромониторинг — методика контроля электрической активности гортанных нервов, обеспечивающих подвижность голосовых связок, во время операции. При проведении мониторинга хирург имеет возможность каждую секунду оценивать состояние гортанных нервов и соответственно менять план операции. Нейромониторнг позволяет резко снизить вероятность развития нарушения голоса после операций на щитовидной железе и околощитовидных железах.
-
УЗИ мягких тканей и лимфоузлов
УЗИ мягких тканей и лимфатических узлов проводится с целью оценки структуры и состояния мягких тканей в определенной области, диагностики патологий либо наблюдения за ходом выздоровления при лечении
3529 просмотров
5 июня 2019
Добрый день. Биопсия щитовидной железы показала картину папиллярной карциномы щитовидной железы, анализы на онкомаркеры отрицательные, по результатам КТ грудной клетки поставили только узловой зоб, не выявлено опухолевого процесса и наличия метастаз, на УЗИ тоже опухоль не определяется, ставят диффузно-узловой зоб, AUT, кровоток — норма, лимфоузлы не увеличены, кроме того, 13 лет назад по результатам биопсии поставили диагноз «микрофолликулярный зоб», узлы без динамики с того времени. Следует ли повторно сдать перед плановой операцией биопсию, чтобы подтвердить диагноз? Какова вероятность ошибочной постановки диагноза? Заранее благодарю за ответ.
На сервисе СпросиВрача доступна консультация онколога по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!
ЛОР, Детский ЛОР
Здравствуйте. Если есть сомнения в диагнозе, недоверие, Вы можете забрать свой биопсийный материал и провести гистологическое и иммуногистохимическое исследование в независимой лаборатории.
Елена, 5 июня 2019
Клиент
Здравствуйте. Спасибо за ответ. Я хотела уточнить, есть ли у меня повод сомневаться в постановке диагноза.
Педиатр, Терапевт, Массажист
Учитывая то что вы перечислили, желательно взять свой материал и переделать ещё раз биопсию в другой лаборатории. Это распространенная практика, Ничего необычного в этом нет
Елена, 5 июня 2019
Клиент
Наталья, здравствуйте. Спасибо за ответ. Правильно ли я поняла, что есть повод для сомнений в правильности постановки диагноза?
Педиатр, Терапевт, Массажист
Если КТ, высокотехнологичный исследование не увидел размытых контуров и признаков раковой опухоли, если лимфатические узлы увеличены, то вам или очень повезло и аденокарцинома находится на самой ранней стадии, или биопсия ошиблась. Вероятность ошибки существует, Но очень небольшая. Потому что клеточное исследование точнее. Единственное что, с Вас ведь совершенно не убудет, если вы еще раз переделаете исследования.
Елена, 5 июня 2019
Клиент
Наталья, спасибо большое за ответ.
Хирург
Елена, здравствуйте !
Если диагноз папиллярной карциномы цитологом был установлен уверенно, без оговорок , не стоял знак вопроса, то нужно верить в это и выполнять всё ,что порекомендуют онкологи !
Другое дело, что при наличии сомнений Вы можете забрать материал в другую лабораторию, чтобы для оценки результата организовали консилиум и т. д. .
Проводить повторную биопсию не имеет смысла, т. к. если даже её результат окажется отрицательным, это не будет означать что карцинома у Вас отсутствует !
Ситуация не трагичная ! После адекватно проведенного лечения больные живут много лет !
Удачи Вам !
Елена, 5 июня 2019
Клиент
Яков, спасибо большое за ответ. Утопающий всегда хватается за соломинку) Может быть, тогда, еще 13 лет назад, ошиблись. Столько времени прошло(
Гематолог
Здравствуйте. Возьмёте блоки и стекла и пересмотрите в другом месте. ( в самом ближайшем к вам онкологической больнице) . Если у вас Москва или МО , то в онкоцентре им Блохина
Елена, 5 июня 2019
Клиент
Ольга, спасибо за ответ. Биопсию делали в клинике им. Пирогова в Санкт-Петербурге. Оперировать будут там же. Может быть, и нет повода сомневаться в диагнозе, я от медицины далека, поэтому и прошу консультацию, т.н. компетентное мнение.
Хирург
Елена цитология это самое ответственное звено в цепи диагностических исследований ! Вы наверное тоже на себе чувствовали как много значит это заключение ! Потому , случайных людей там не бывает , там работают опытные квалифицированные специалисты ! Потому, я не думаю, что 13 лет назад в Вашем вопросе могли допустить ошибку . 13 лет, — это много ! Если бы тогда ошиблись, то у Вас процесс был бы запущенным !
Елена, 5 июня 2019
Клиент
Яков, у меня все заключения на руках. Могу назвать точную дату проведения первой биопсии. Ведь — это тоже результат цитологического исследования. Я только хотела узнать компетентное мнение, есть ли повод подвергать сомнению диагноз, который сейчас установлен. И КТ ничего не показывает.
Хирург
Елена, КТ кардинально не изменит ситуацию ! Её можете сделать ! Это хороший метод диагностики и даст много полезной информации, но не на столько, чтобы поставить под сомнение результат цитологического исследования! Узлы содержащие атипические клетки и узлы не содержащие их, в не запущенных ситуациях ( а я думаю, что у Вас именно такая ситуация ) ни внешне (визуально) , ни пальпаторно, ни на КТ ничем не отличаются друг от друга ! Если предположить, что у Вас имеется узел, с нечёткими границами , размытыми контурами, то это лишний раз подтвердит диагноз карциномы ! Но это не значит , что отсутствие на КТ таких узлов будет говорить об отсутствии карциномы !
Елена, к сожалению,повода для того, чтобы подвергать сомнению диагноз нет !
Выражение «к сожалению» я употребил неуместно, т. к. повторяю, что множество больных с Вашим заболеванием успешно вылечиваются и живут десятилетия !
Удачи Вам !
Елена, 6 июня 2019
Клиент
Яков, еще раз спасибо за консультацию) В том и дело, что я привыкла доверять врачам и пытаюсь сложить дважды два. 13 лет назад проводили такое же обследование и ничего не выявили. Однозначно: если сейчас исключить ошибку, значит, тогда проглядели. Я понимаю, что врачи могут ошибаться, только чего будет стоить такая ошибка — 13 лет жизни минус из моих 40! Дата операции назначена. Уже всю предоперационную подготовку провели. КТ мне позавчера сделали — ничего не показывает. И, насколько мне известно, самый точный инструмент диагностики — это гистололгия. Только проводится она у же после операции. Увы! Еще раз спасибо за ответ! Будем резать)
Гематолог
Лучше пересмотреть вам гистологию тут ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России
Елена, 6 июня 2019
Клиент
Хирург
Елена, здравствуйте !
Яне могу согласиться стем ,что 13 лет назад врачи проглядели . Если бы так было, то у Вас опухоль была бы гораздо больше и давно были бы отдаленные метастазы ! К счастью , всего этого у Вас нет ! У вас процесс перерождения более короткий , — около года , ( плюс, минус , — немного ) , но не 13 лет !
Елена, 6 июня 2019
Клиент
Яков, здравствуйте. Я повторюсь: заключение биопсии от 03.04.2006: узловой зоб, цит № 3867-3868 — микрофолликулярный зоб. Заключение от 23.04. 2019 — цитологическая картина папиллярной карциномы. Вот так! У меня все на руках. Возможно, при взятии биопсии в первый раз не попали на злокачественный участок. Но это мое предположение, я не врач.
Хирург
Мы с Вами как будто разговариваем на резных языках ! Микрофолликулярный зоб , — это зоб , а не рак ! И не обязательно было его тогда удалить если консервативное лечение компенсировало состояние !
Елена, 6 июня 2019
Клиент
Яков, правильно я Вас понимаю, что патологический процесс в моем случае мог начать развиваться в какой-то момент за прошедшие 13 лет на фоне узлового зоба? Хирург-онколог пояснил мне в клинике, что на тот момент существовала просто другая классификация.
Хирург
Я с Вами соглашусь, что с тем диагнозом Вы должны были находиться на особом контроле у эндокринолога и онколога, для того , чтобы выявить процесс перерождения в самом начале !
Елена, у Вас процесс , слава богу, не запущенный : нет метастазов в лимфатические узлы, нет отдаленных метастазов и если Вы будете соглашаться с онкологами, выполнять все назначения, то можно ожидать очень хороший результат, чего я Вам и желаю !
Елена, 6 июня 2019
Клиент
Яков, спасибо! Теперь стало понятнее! И Вам удачи и поменьше работы!!!
Маммолог, Терапевт, Онколог
Здравствуйте, Елена.
Вероятность ошибки морфологического диагноза минимальна.
Но пересмотр в другом лечебном учреждении и лаборатории провести можете, это в Ваших интересах..
Операция плановая, не экстренная.
Не переживайте, папиллярная форма рака щитовидной железы обычно имеет благоприятный прогноз.
Елена, 6 июня 2019
Клиент
Маммолог, Терапевт, Онколог
Пожалуйста, Елена.
Здоровья Вам и всех благ!
Оцените, насколько были полезны ответы врачей
Проголосовало 5 человек,
средняя оценка 2
Что делать, если я не нашел ответ на свой вопрос?
Если у Вас похожий или аналогичный вопрос, но Вы не нашли на него ответ — получите свою 03 онлайн консультацию от врача эксперта.
Если Вы хотите получить более подробную консультацию врача и решить проблему быстро и индивидуально — задайте платный вопрос в приватном личном сообщении. Будьте здоровы!