- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Соколова А.В.
1
Малишевская Н.П.
2
1 Клиника «Уральская»
2 Государственное бюджетное учреждение Свердловской области «Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии»
В России в течение последних 15 лет отмечается рост заболеваемости меланомой кожи (МК) на 70%. Наиболее неблагоприятны по своим последствиям ошибки в диагностике МК. Проведено клиническое и дерматоскопическое исследование 1030 новообразований кожи у 800 пациентов, последовательно обратившихся на прием к дерматологу. В выборку включены все пациенты с новообразованиями кожи, после удаления которых было произведено гистологическое исследование материала и получено патоморфологическое заключение (n=441). Из 441 гистологического исследования новообразований кожи совпадение с клинически установленным диагнозом было в 355 случаях (80,5%), расхождение — в 86 случаях (19,5%). Из 86 случаев расхождения диагнозов установлено 24 (27,9%) случая гиподиагностики диспластических невусов и меланомы кожи, 34 (39,5%) случая гипердиагностики диспластических невусов и меланомы кожи. Проанализированы причины расхождения клинического и дерматоскопического с патоморфологическим диагнозом в случаях сложной дифференциальной диагностики новообразований кожи, к которым относятся больные с диспластическими невусами и меланомой кожи, особенно на ранних стадиях. Основными причинами гиподиагностики меланоцитарных новообразований кожи являются малый размер новообразования, визуальная однородность цвета, беспигментные или мало пигментированные новообразования, визуально и дерматоскопически определяемые ровные и четкие контуры.
меланома кожи
диспластический невус
ошибки в диагностике меланомы
гиподиагностика меланомы кожи.
1. Демидов Л.В., Харкевич Г.Ю., Маркина И.Т. Меланома и другие злокачественные новообразования кожи // Энциклопедия клинической онкологии: руководство для практических врачей. — М.: РЛС, 2005. — С. 341–364.
2. Малишевская Н.П., Игликов В.А. и др. Эпидемиология злокачественных новообразований кожи на Среднем Урале / Кунгуров Н.В. (ред.) // Злокачественные новообразования кожи: заболеваемость, ошибки диагностики, организация раннего выявления, профилактика. — Курган: Зауралье, 2010. – С. 8-33.
3. Чиссов В.И., Старинский В.В., Петрова Г.В. Качественные новообразования в России в 2011 году (заболеваемость и смертность). — М.: ФП «МНИОИ им. П.А. Герцена» Минздрава России, 2013. — 289 с.
4. Chen S.T., Geller A.C., Tsao H. Update on the epidemiology of melanoma // Curr. Dermatol. Rep. — 2013. — № 2 (1). — Р. 24–34.
5. Малишевская Н.П., Кохан М.М., Соколова А.В и др. Дерматоонкология (злокачественные новообразования кожи, первичные лимфомы кожи): атлас / под общ. ред. проф. Н.В. Кунгурова. – Екатеринбург: Изд-во Урал. ун-та, 2016. – 68 с.
6. Состояние онкологической помощи населению России в 2016 году / под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. — М.: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИРЦ» Минздрава России, 2017. — 236 с.
В России в течение последних 15 лет отмечается рост заболеваемости меланомой кожи (МК) на 70% [1-4]. Наиболее неблагоприятны по своим последствиям ошибки в диагностике МК. О значительном количестве диагностических ошибок на разных уровнях оказания медицинской помощи пациентам свидетельствует сохраняющийся высокий удельный вес больных с МК, выявленной на поздних стадиях опухолевого процесса [5]. За период с 2006 по 2016 год в РФ показатели запущенности по меланоме кожи значительно снизились (-40,6%), однако они по-прежнему остаются на недопустимо высоком уровне (18,9%) для опухолей визуальных локализаций [6]. Следует отметить, что гипердиагностика МК не влечет столь трагических последствий, как гиподиагностика, которая всегда связана с ухудшением прогноза течения заболевания и риском для жизни больного.
Цель исследования — установить причины расхождения результатов клинического и стандартного дерматоскопического обследования с патоморфологическим диагнозом в случаях сложной дифференциальной диагностики НОК. Проведено клиническое и дерматоскопическое исследование 1030 новообразований кожи (НОК) у 800 пациентов, последовательно обратившихся на прием к дерматологу. Из них в 441 (42,8%) случае выполнено удаление НОК радиоволновым или хирургическим методом с последующим гистологическим исследованием. Показаниями для удаления новообразований кожи явились подозрение на МК и диспластические невусы, все случаи сложной дифференциальной диагностики, а также все меланоцитарные новообразования, находящиеся в местах постоянного травмирования или имеющие большие размеры (>6 мм). В случаях подозрения на МК пациенты направлялись в Государственное бюджетное учреждение Свердловской области «Свердловский областной онкологический диспансер» для хирургического иссечения НОК и последующего лечения. В выборку включены все пациенты с верифицированными диагнозами НОК, в том числе пациенты с меланомой кожи на ранних (I-II) стадиях и диспластическими невусами, когда правильная и своевременная диагностика наиболее важна для дальнейшего прогноза течения заболевания (табл. 1).
Таблица 1
Структура новообразований кожи (n=441)
|
Меланоцитарные новообразования кожи |
Число больных с правильно установленным диагнозом, абс. (%) |
|
|
визуальный осмотр с использованием дерматоскопии |
гистологическое заключение |
|
|
Доброкачественные НОК |
349 (79,1%) |
361 (81,9%) |
|
Диспластические невусы кожи |
82 (18,6%) |
67 (15,2%) |
|
Меланома кожи на ранних стадиях |
10 (2,3%) |
13 (2,9%) |
Группу доброкачественных новообразований кожи составили меланоцитарные невусы без признаков дисплазии (n=263), себорейный кератоз (n=74) и гемангиомы кожи (n=12) в случаях их травмирования, с наличием геморрагических корочек на поверхности новообразований, затрудняющих визуальную и дерматоскопическую диагностику.
Таким образом, в данной выборке достоверных различий в правильности постановки диагноза при клиническом осмотре дерматолога с применением рутинной дерматоскопии и результатом гистологии не выявлено (табл. 1).
Из 441 гистологического исследования НОК совпадение с клинически установленным диагнозом было в 355 случаях (80,5%), расхождение — в 86 случаях (19,5%). Совпадение клинического дерматоскопического и гистологического диагнозов (n=355) выявлено в случаях доброкачественных новообразований кожи (n=305), диспластических невусов (n=45) и меланомы кожи (n=6). Из 86 случаев расхождения диагнозов установлено 24 (27,9%) случая гиподиагностики диспластических невусов и меланомы кожи, 34 (39,5%) случая их гипердиагностики.
Проанализированы причины расхождения клинического и стандартного дерматоскопического обследования с патоморфологическим диагнозом в случаях сложной дифференциальной диагностики НОК, к которым относятся больные с диспластическими невусами и меланомой кожи, особенно на ранних (I-II) стадиях (табл. 2).
Таблица 2
Визуальные признаки НОК, влияющие на гиподиагностику диспластических невусов и МК с использованием дерматоскопии (n=24)
|
Признак |
Частота встречаемости |
|
|
абс. |
% |
|
|
1. Малый размер новообразования (<6 мм) |
17 |
70,8 |
|
2. Визуально и дерматоскопически определяемые ровные четкие контуры |
3 |
12,5 |
|
3. Клинически и дерматоскопически определяемая однородность цвета |
6 |
25,0 |
|
4. Беспигментные или мало пигментированные новообразования |
5 |
20,8 |
Примечание: у одного больного могло быть несколько причин гиподиагностики, в связи с чем общая частота встречаемости признака превышает 100%.
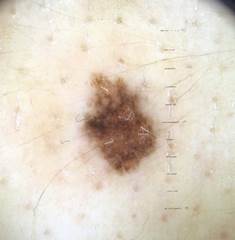
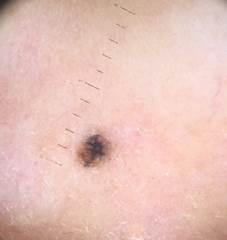
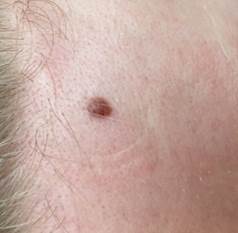
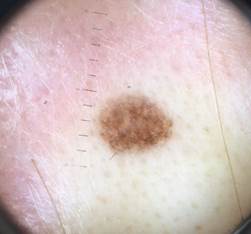
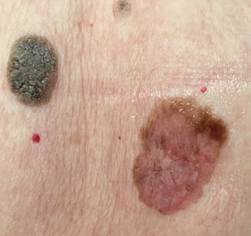
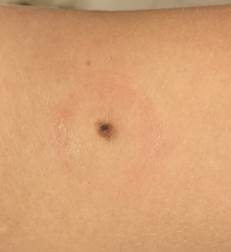
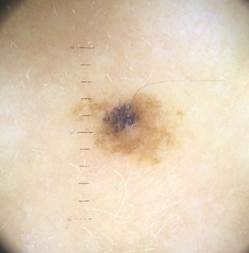
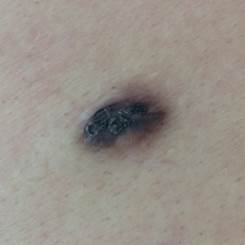
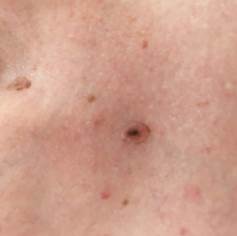
B соответствии с приведенными данными основными причинами гиподиагностики пигментированных новообразований кожи являются малый размер новообразования (70,8%, рис. 1), визуальная однородность цвета (25,0%, рис. 2), беспигментные или мало пигментированные новообразования (20,8%, рис. 3), визуально и дерматоскопически определяемые ровные и четкие контуры (12,5%, рис. 4).
Рис. 1. Линейный размер меланомы кожи меньше 6 мм (дерматоскопическое изображение)
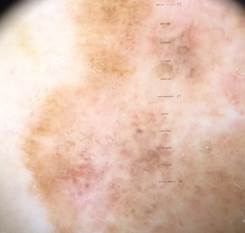
Рис. 2. Клиническое и дерматоскопическое изображение диспластического невуса кожи лба: клинически определяется визуальная однородность цвета
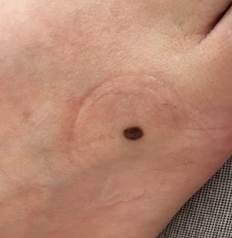
Рис. 3. Клиническое и дерматоскопическое изображение мало пигментированной меланомы кожи живота с участками регресса, выше – себорейный кератоз
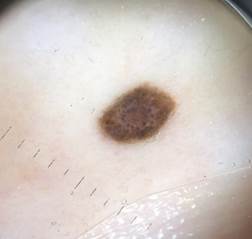
Рис. 4. Клиническое и дерматоскопическое изображение меланомы кожи тыльной поверхности стопы
Проанализированы причины гипердиагностики меланоцитарных новообразований кожи в случаях, когда возникают трудности в дифференциальной диагностике диспластических невусов и меланомы кожи (табл. 3).
Таблица 3
Визуальные признаки НОК, влияющие на гипердиагностику диспластических невусов и МК с дерматоскопией (n=34)
|
Признак |
Частота встречаемости |
|
|
абс. |
% |
|
|
1. Большой (свыше 10 мм) размер новообразования |
13 |
54,2 |
|
2. Клинически и дерматоскопически определяемые неровные контуры и асимметричность новообразования |
9 |
37,5 |
|
3. клинически и дерматоскопически определяемая неоднородность цвета |
15 |
62,5 |
|
4. Наличие в новообразовании фрагментов темно-коричневого и черного цвета при дерматоскопии новообразований |
8 |
33,3 |
Примечание: у одного больного могли быть несколько причин гипердиагностики, в связи с чем общая частота встречаемости признака превышает 100%.
B соответствии с данными таблицы 3 основными причинами, которые приводят к гипердиагностике диспластических невусов и меланомы кожи, являются неоднородность цвета (62,5%, рис. 5, 7), размер новообразований более 10 мм (54,2%, рис. 6), неровные контуры и асимметричность новообразования (37,5%, рис. 5), а также наличие в новообразовании фрагментов темно-коричневого и черного цвета (33,3%, рис. 5-7).
Рис. 5. Клиническое и дерматоскопическое изображение диспластического невуса кожи плеча: неоднородность цвета, неровные контуры и асимметричность новообразования, наличие в новообразовании эксцентрично расположенных фрагментов темно-коричневого и черного цвета
Рис. 6. Пигментированная дерматофиброма кожи бедра
Рис. 7. Клиническое и дерматоскопическое изображение диспластического невуса кожи живота
Результаты расчета показателей диагностической точности, чувствительности и специфичности клинического осмотра с применением дерматоскопии для диагностики НОК продемонстрировали, что чувствительность клинического осмотра с применением дерматоскопии для доброкачественных новообразований кожи (91,2%) на 45,0% выше, чем чувствительность диагностики меланомы кожи (46,2%). Но при этом определяется высокая (99,1%) специфичность клинической и дерматоскопической диагностики меланомы кожи, что свидетельствует о большой вероятности совпадения диагноза с данными патоморфологического исследования. Точность диагностики меланомы кожи составляет 97,5%, что на 9,1% выше, чем точность диагностики доброкачественных новообразований кожи (88,4%) с применением метода дерматоскопии.
На следующем этапе исследования был разработан «показатель гиподиагностики», т.е. число больных, которым необходимо провести клиническое и дерматоскопическое исследование новообразований кожи для того, чтобы у одного из них установленный клинический диагноз не подтвердился результатом гистологического исследования. Показатель гиподиагностики рассчитывали как отношение неверно диагностированных случаев ко всем случаям НОК в данной группе. Этот показатель составил 18,4 в случае диспластических невусов и меланомы кожи, и 63,0 в случае только меланомы кожи. Таким образом, при осмотре 63 больных с НОК в ситуациях сложной дифференциальной диагностики дерматолог допускает один случай гиподиагностики меланомы кожи.
Диагностические ошибки за счет гиподиагностики процесса имеют наиболее неблагоприятные для течения заболевания и прогноза жизни последствия, что диктует необходимость внедрения в клиническую практику новых современных неинвазивных методов обследования меланоцитарных новообразований кожи (спектрофотометрического интрадермального анализа, конфокальной лазерной сканирующей микроскопии).
Библиографическая ссылка
Соколова А.В., Малишевская Н.П. ОШИБКИ В ДИАГНОСТИКЕ МЕЛАНОЦИТАРНЫХ НОВООБРАЗОВАНИЙ КОЖИ // Современные проблемы науки и образования. – 2018. – № 2.
;
URL: https://science-education.ru/ru/article/view?id=27502 (дата обращения: 11.02.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Современная эпидемиологическая ситуация по злокачественным новообразованиям кожи в Российской Федерации характеризуется прогредиентным ростом заболеваемости населения раком кожи и меланомой; увеличением доли злокачественных новообразований (ЗНО) кожи в структуре общей онкологической заболеваемости и сохранением в ней лидирующих позиций, особенно среди женского населения и лиц старше 60 лет; высокими показателями среднегодовых темпов прироста и общего прироста за период 2003–2013 гг., в 2 раза превышающими аналогичные показатели по всей онкологической заболеваемости.
В 2013 г. в РФ было выявлено 75 112 новых случаев ЗНО кожи (С43, С44, С46.0), из них 8974 меланомы (С43) и 66 138 других новообразований кожи. Среди всех ЗНО кожи удельный вес меланомы составил 11,95%, рака кожи — 88,05% [1, 2].
Результаты анализа состояния диагностики ЗНО кожи в РФ свидетельствуют о сохраняющейся проблеме несвоевременной диагностики меланомы. На I стадии опухолевого процесса в 2013 г. было выявлено лишь 29,9% больных. Только каждый пятый больной (19,1%) выявляется активно, каждый четвертый (23,8%) — в запущенных (III, IV) стадиях опухолевого процесса, что сохраняет показатель первогодичной летальности на высоком для опухолей визуальной локализации уровне (12,3% больных меланомой погибают в течение одного года с момента установления диагноза).
Среди задач, предусмотренных национальной онкологической программой [3], — увеличение показателей выявляемости больных на ранних стадиях злокачественного процесса и, как следствие, снижение смертности и инвалидности населения от злокачественных новообразований. Одной из приоритетных задач является обеспечение диагностики опухолевых заболеваний визуальных локализаций, в том числе меланомы кожи (МК), на ранних стадиях.
Данные официальной статистики, некоторых публикаций и собственные клинические наблюдения свидетельствуют о том, что нередко больной со злокачественным новообразованием кожи несвоевременно обращается к врачу, когда опухоль имеет уже распространенный характер (глубокий уровень инвазии, иногда метастазы), либо длительное время наблюдается у врачей общей лечебной сети, дерматологов, косметологов, хирургов с ошибочным диагнозом и, как следствие, получает неадекватную терапию, в ряде случаев стимулирующую дальнейший злокачественный рост [4–9]. Качество диагностики злокачественных новообразований кожи, особенно ранних форм, нельзя признать удовлетворительным [10–12].
Наибольшее значение в диагностике МК имеют квалификация и опыт врача первичного контакта [13]. Однако частота клинической диагностики опухолей кожи врачами общей лечебной сети невысока и находится на уровне 29,9% [6, 14]. Было установлено, что каждый десятый больной с меланомой на своем диагностическом маршруте проходил через 3–5 инстанций, 17,4% пациентов на догоспитальном этапе получали неадекватное лечение, а 7,9% больных были признаны здоровыми.
Проведенный нами анализ запущенных случаев меланомы показал, что они в равной степени обусловлены как поздним обращением пациентов к врачу (49,5%), так и врачебными ошибками в клинической диагностике на «доонкологическом» амбулаторно-поликлиническом этапе диагностического маршрута больных (50,5%) [6].
Ошибки в диагностике МК по своим последствиям наиболее трагичны. О значительном количестве диагностических ошибок на различных уровнях оказания медицинской помощи пациентам (от первичного обращения пациента к врачу до дальнейшего его наблюдения в поликлиниках и районных больницах как общего, так и дерматовенерологического профиля) свидетельствует высокий удельный вес больных с меланомой, выявляемых на поздних (III–IV) стадиях опухолевого процесса.
Частота ошибок клиницистов в распознавании меланомы варьирует от 18% до 81%, при этом даже первичное гистологическое исследование дает до 20–30% ошибочных результатов [8, 15]. Это влечет за собой неадекватную тактику лечения, приводит к появлению запущенных случаев и неблагоприятному исходу, что недопустимо для опухолей визуальной локализации. Так, по наблюдениям О. М. Конопацковой [4] неправильная тактика врачей при амбулаторном обследовании и лечении больных с пигментными новообразованиями на коже (хирургическое вмешательство при отсутствии пред- и послеоперационной цитологической и гистологической верификации) привела в тому, что у 63,6% пациентов была констатирована диссеминация опухолевого процесса в течение первого года после радикального удаления меланомы.
При раннем выявлении МК, когда толщина новообразования не превышает 0,76 мм (по Breslow), пятилетняя выживаемость наблюдается практически у 95% больных [6, 14, 16–18]. В связи с этим основные задачи современной клинической медицины в отношении МК заключаются в ее ранней диагностике и первичной профилактике, что требует информационного обеспечения разрабатываемых профилактических программ. Последнее обусловлено, во-первых, недостаточным уровнем дерматоонкологических знаний и онкологической настороженности врачей «неонкологических» специальностей, в том числе врачей общей практики, во-вторых, рядом объективных причин, связанных с трудностью клинической диагностики беспигментных и акральных меланом.
В повседневной практике не только дерматологу, но и врачам других специальностей часто приходится встречаться с разнообразными пигментированными новообразованиями кожи, требующими особого внимания и адекватной диагностической тактики. Некоторые авторы [19] считают, что на этапе дифференциальной диагностики каждое пигментное новообразование на коже следует рассматривать как потенциальную меланому.
Экспертный анализ клинических диагнозов, установленных больным с МК на догоспитальных этапах их диагностического маршрута, позволил определить наиболее типичные варианты диагностических ошибок. Нередко при МК ставится ошибочный диагноз «фиброма», «себорейный кератоз», «ангиокератома» и другие, что влечет за собой последующую неадекватную лечебную тактику. Проводится либо хирургическое иссечение новообразования в неадекватных границах под местной инфильтрационной анестезией, часто без последующего гистологического исследования, либо удаление новообразования деструктивными методами (диатермокоагуляция, криодеструкция, лазерная аблация) у хирургов, дерматологов или косметологов. Причиной подобных ошибочных действий врача является, по-видимому, абсолютная уверенность в доброкачественности новообразования, основанная на отсутствии или слабо выраженной пигментации опухоли, а также ошибочный, но часто встречающийся среди врачей клинический стереотип, ассоциирующий степень выраженности пигментации новообразования кожи с его злокачественностью, при этом не учитывается возможность развития беспигментных форм меланомы (рис. 1).
Действительно, в большинстве случаев (в 75–80%) визуальная окраска первичной меланомы интенсивно коричневая или черная [6, 14], но в 15,8–16,4% случаев наблюдается розовый цвет (рис. 2), в 7,3% — светло-коричневый (рис. 1), что дезориентирует врача и приводит к диагностическим ошибкам. Последнее убедительно иллюстрируют два клинических наблюдения.
Больной Р., 23 лет. An. morbi: на коже правой надлопаточной области с детства было опухолевидное образование кожи телесного цвета. В течение последних 3–4 месяцев заметил быстрое его увеличение. Наблюдался у дерматолога по месту жительства с диагнозом: «Папиллома кожи спины? Ангиофиброма».
В связи с увеличением размеров другого пигментного новообразования на коже в поясничной области был направлен на консультацию в онкологическое учреждение. Status localis: при клиническом осмотре онкологом: на коже правой надлопаточной области имеется экзофитный папилломатозный очаг розового (!) цвета, неправильной формы с четкими контурами, размером 1,5 × 2 см, безболезненный, эластичный с эрозированной поверхностью, без признаков воспаления. На коже в области поясницы — гиперпигментированная куполообразная папула неправильных очертаний, размером 5 × 8 мм в диаметре, коричневого цвета. Регионарные лимфоузлы не увеличены.
С диагностической целью проведено широкое хирургическое иссечение указанных новообразований под общей анестезией.
Результаты послеоперационного гистологического исследования: в надлопаточной области — эпителиоидный вариант меланомы с изъязвлением, развившейся на фоне меланоцитарного невуса, III стадия инвазии по Breslow. В поясничной области — внутридермальный меланоцитарный невус.
Больной Г., 70 лет. An. morbi: cчитает себя больным с момента, когда заметил появление и быстрое увеличение «пятна» красновато-коричневого цвета на коже нижней трети левого плеча, которое было с детства. Скоро, со слов больного, вокруг пятна появилось воспаление и новые темные мелкие «родинки». Обратился к дерматологу, который с диагнозом «фурункул плеча» направил пациента на лечение к хирургу по месту жительства. С диагнозом «фурункул плеча» в течение месяца лечился у хирурга амбулаторно (перевязки с мазью Вишневского). Процесс прогрессировал, в области очага появилась кровоточивость, постоянно образовывались геморрагические корочки. Направлен на консультацию в онкологический диспансер.
Status localis: при осмотре в поликлинике: на коже нижней трети левого плеча имеется новообразование диаметром до 1,5 см ярко-розового (!) цвета, в центре — наслоение геморрагических корочек, перифокально — воспаление (гиперемия, отечность) и мелкие пигментированные узелковые высыпания. Подмышечные лимфоузлы слева увеличены до 1,5 см, эластичные, подвижные.
С подозрением на меланому госпитализирован в хирургическое отделение, где проведено широкое хирургическое иссечение опухоли. Результат послеоперационного патоморфологического исследования: беспигментная меланома веретеноклеточного типа; инвазия всех слоев дермы до подкожной клетчатки. Окончательный диагноз: меланома нижней трети левого плеча — pT4N0M0 (III ст.).

Проведенный нами анализ визуальной окраски первичных МК у 105 пациентов также показал, что в 82,9% случаев наблюдалась типичная окраска опухоли (коричневая, черная). Но у 17,1% больных МК была нетипичного цвета (телесного, всех оттенков розового, вишневого) (рис. 2). Среди жителей г. Екатеринбурга беспигментные меланомы составили 15,9% случаев [20]. При этом у больных с МК, возникшей на клинически неизмененной коже (de novo), беспигментная форма опухоли регистрировалась в 2,2 раза чаще, чем в случаях развития меланом на фоне меланоцитарных невусов.
Данные других отечественных авторов также свидетельствуют о том, что клинически беспигментные меланомы регистрируются нередко, в 7–10% случаев [6, 14]. Это имеет большое клиническое значение, так как наибольшие объективные трудности в клинической диагностике возникают именно при беспигментной меланоме. Кроме того, существует мнение, что отсутствие пигмента в опухоли имеет и определенное прогностическое значение. Установлено, что клетки меланомы, в которых образование пигмента резко снижено, являются менее дифференцированными, а значит, более злокачественными. Возможно, именно этим обусловлено наличие прямой линейной корреляции между степенью пигментации первичной меланомы и сроками выживаемости больных [14].
Проведенный нами детальный анализ диагностического маршрута 18 больных с беспигментной МК показал, что лишь в 1 случае диагноз был поставлен своевременно — при локализации опухолевого очага на лице, который был клинически расценен как базалиома, и в связи с этим пациент был своевременно направлен к онкологу. В остальных случаях на предыдущих этапах клинической диагностики у хирургов и дерматологов, к которым первично обратились пациенты, беспигментная МК расценивалась как фиброма, гемангиома, пиогенная гранулема, ангиокератома, фурункул, гигрома, трофическая язва, организованный тромбофлебит. В соответствии с этими диагнозами больные получали разнообразную терапию, в том числе с использованием деструктивных методов лечения (криодеструкция, электрокоагуляция) или хирургического иссечения в неадекватных границах с применением местной инфильтрационной анестезии. В результате на момент установления правильного диагноза лишь у 2 (11,1%) больных глубина инвазии меланомы соответствовала II уровню по Breslow. В остальных случаях (88,9%) при послеоперационном патоморфологическом исследовании выявлен III–V уровень инвазии (III — 11,1%, IV — 55,6%, V — 22,2%). Ранние клинические стадии заболевания (I–II) были лишь у 3 (16,7%) больных, у остальных (15 человек, 83,3%) выявлены III–IV стадия с регионарными метастазами в лимфоузлы и мягкие ткани (13 пациентов) и генерализацией опухолевого процесса (2 больных). Среди больных беспигментной меланомой преобладали женщины (72,2%) и акральная локализация опухоли регистрировалась в 2 раза чаще (22,2%), чем в целом среди всех больных с МК (10,5%).
Подногтевые варианты меланомы кожи в начальной стадии опухолевого процесса клинически выглядят как меланонихия. Во всех наблюдаемых некоторыми авторами случаях подногтевых меланом имел место частичный или полный лизис ногтевого матрикса, в 76% — имелись экзофитные, бугристые разрастания, в каждом втором случае поражения носили амеланотический характер [8, 13].
По нашим данным при акральных лентигинозных меланомах в два раза чаще, чем при других локализациях, встречаются беспигментные формы, что объективно затрудняет процесс клинической диагностики. Поэтому визуально беспигментные меланомы подошв нередко проходили под клиническими «масками» очагового гиперкератоза, «сухой» мозоли, подошвенной бородавки. Приводим клиническое наблюдение.
Больной Б., 52 года. An. morbi: cчитает себя больным в течение двух лет, когда появилась «сухая мозоль» на подошвенной поверхности правой стопы в проекции II–III плюсневых костей. Периодически лечился у дерматолога, применял кератолитические пластыри, мази, горячие ванны для ног с последующим срезанием распаренной «мозоли». В дальнейшем в этой области, со слов больного, появилось «темное пятно, которое стало кровоточить». Через 7–8 месяцев развился отек стопы и нижней трети голени, сопровождающийся общим повышением температуры. Обратился к хирургу. Диагностировано «рожистое воспаление», назначено лечение антибиотиками, локально — УФ-облучение. Через 3 месяца заметил увеличение паховых лимфоузлов справа. Только после этого с подозрением на онкопатологию был направлен в онкологический диспансер.
Status localis: на подошвенной поверхности правой стопы в проекции II и III плюсневых костей экзофитное новообразование с багрово-сероватой кровоточащей язвой размером до 2 см. Стопа отечна, кожа гиперемирована. В правой паховой области пальпируется несколько увеличенных лимфоузлов размером от 0,5 до 2,5 см, болезненных, смещаемых.
Проведено хирургическое иссечение опухоли и операция Дюкена.
Результат послеоперационного патоморфологического исследования: в коже — изъязвившаяся эпителиоидноклеточная меланома, III стадия инвазии по Breslow. Метастазы в трех паховых лимфоузлах, в кожном лоскуте бедра и брюшной стенки с их полным замещением опухолевой тканью. Больному назначена полихимиотерапия.
Довольно часто (до 25,0% случаев) на амбулаторных этапах диагностики акральная меланома ошибочно принимается за пиогенную гранулему. Это доброкачественное сосудистое новообразование кожи, возникая чаще именно на акральных участках, как правило, после механической травматизации на клинически неизмененной коже в процессе эволюции может изменить свой типичный красновато-вишневый цвет на фиолетово-синий и даже интенсивный темно-коричневый оттенок. При этом кровоточивость новообразования, появление вследствие этого на его поверхности геморрагических корок, присоединение вторичной инфекции и обусловленное этим наличие признаков воспаления действительно создает значительные объективные трудности для визуальной дифференциальной диагностики. Поэтому в случаях отсутствия надежных дифференциально-диагностических критериев единственно правильным тактическим решением врача, не владеющего методом дерматоскопии, является направление больного к более опытному дерматологу для проведения дополнительного обследования с использованием неинвазивных методов (дерматоскопии, спектрофотометрического интрадермального анализа, конфокальной микроскопии), либо в онкологическое учреждение, где в зависимости от конкретной клинической картины будут проведены дополнительные, адекватные клинической ситуации диагностические исследования с целью уточнения диагноза.
Приводим клиническое наблюдение:
Больная Ш., 30 лет. An. morbi: считает себя больной с момента, когда на тыльной поверхности V пальца левой стопы после механической травмы появился узелок розоватого цвета, который в течение последующих 6 месяцев стал увеличиваться в размерах. Обратилась к дерматологу. С диагнозом: «Пиогенная гранулема?» направлена к хирургу по месту жительства, где под местной анестезией проведено хирургическое иссечение новообразования без последующего гистологического исследования. Через 2 месяца вновь заметила рост «узелка». Хирургом проведена лазерная деструкция, после чего начался быстрый рост новообразования, в связи с чем больная направлена в онкологический центр.
Status localis: на коже тыльной поверхности основной фаланги V пальца левой стопы опухолевидное образование ярко-розового (!) цвета размером 1,0 × 0,5 × 1,5 см, плотно-эластической консистенции, кожа вокруг не изменена. Регионарные лимфоузлы не пальпируются. Предварительный диагноз: «Пиогенная гранулема? Беспигментная меланома?». С диагностической целью проведена ампутация V пальца левой стопы.
Результат патоморфологического исследования послеоперационного материала: беспигментная меланома, IV уровень инвазии по Breslow (pT3N0M0).
Рассматривая проблему ошибок в диагностике МК, следует отметить, что гипердиагностика также встречается довольно часто, но она не влечет столь трагических последствий, как гиподиагностика, которая всегда связана с ухудшением прогноза течения заболевания и риском для жизни больного.
В заключение следует подчеркнуть, что систематический анализ причин позднего выявления злокачественных новообразований кожи, особенно меланомы, клинических и тактических ошибок врачей неонкологического профиля, их обсуждение на совместных с онкологами врачебных конференциях или заседаниях научно-практических обществ будут способствовать формированию онкологической настороженности и более ранней диагностике злокачественных опухолей кожи.
Литература
- Состояние онкологической помощи населению России в 2013 году / Под ред. Каприна А. Д., Старинского В. В., Петровой Г. В. ФГБУ «МНИОИ» им. П. А. Герцена МЗ России, Росс. центр информац. технол. и эпидемиол. исслед. в области онкологии. М., 2014, 235 с.
- World Healthcare Organization. Ultraviolet radiation and the INTERSUN Programme. http://www.who.int/uv/faq/skincancer/en/index1.html (visited on 09-Aug-2013).
- Чиссов В. И., Старинский В. В., Петрова Г. В. Злокачественные новообразования в России в 2009 г. (заболеваемость и смертность). М.: ФГУ «МНИОИ им. П. А. Герцена Минздравсоцразвития России», 2011.
- Конопацкова О. М. Лечение меланом кожи в амбулаторных условиях // Росс. онколог. журн. 2006. № 3. С. 38–41.
- Конопацкова О. М., Оркин В. Ф., Завьялов А. И. Акральная лентигинозная меланома кожи, сочетающаяся с микотической инфекцией стоп и ногтей // Журн. дермато-венерол. и косметол. 1996. № 1. С. 35–36.
- Малишевская Н. П. Ошибки в клинической диагностике злокачественных новообразований кожи. В кн.: Кунгуров Н. В., Малишевская Н. П., Кохан М. М., Игликов В. А. Злокачественные новообразования кожи: заболеваемость, ошибки диагностики, организация раннего выявления, профилактика. Курган: Изд-во «Зауралье», 2010. С. 125–149.
- Молочков В. А. Меланоцитарные невусы и их связь с меланомой // Росс. журн. кож. вен. болезней. 1998. № 2. С. 68–76.
- Селюжицкий И. В., Анфилов С. В., Мурзо А. В. Ошибки в диагностике и лечении подногтевой меланомы // Росс. онкол. журн. 2004. С. 33–34.
- Хлебникова А. Н., Кладова А. Ю., Кириченко Н. А., Сарханн В. С. К проблеме гигантских базалиом // Клин. дерматол. и венерол. 2007. № 1. С. 9–12.
- Гельфонд М. Л. Дифференциальная диагностика опухолей кожи в практике дерматологов и косметологов // Практическая онкология. 2012, т. 13, 2.
- Кубанова А. А., Мартынов А. А. Место злокачественных новообразований кожи в структуре онкологической заболеваемости населения Российской Федерации // Вестник дерматологии и венерологии. 2007, № 6.
- Rigel D. S. Epidemiology of melanoma // Seminars in cutaneous medicine and surgery. 2010, № 12.
- Фрадкин С. З., Залуцкий И. В. Меланома кожи. Минск: Беларусь, 2000. 221 с.
- Анисимов В. В., Вагнер Р. И., Барчук А. С. Меланома кожи. Ч. 1. Эпидемиология, этиология, патогенез, профилактика. СПб: Наука, 1995. 151 с.
- Ильин И. И. Необычный случай гигантской меланомы // Вестн. дерматол. и венерол. 1992. № 5. С. 31–36.
- Паршикова С. М. Опухолеподобные процессы (невусы) и опухоли из пигментообразующей ткани (меланомы). В кн.: Патологоанатомическая диагностика опухолей человека. Рук-во для врачей в двух томах / Под ред. Н. А. Краевского, А. В. Смольянинова, Д. С. Саркисова. М.: Медицина, 1993. Т. 2. С. 558–587.
- Piteiro A. B., Perez-Espana L., Hervella M. et al. Giant basal cell carcinoma // J. Dermatol. 2003; 30: 7: 573–575.
- Takemoto S., Fukamizu H., Yamanaka K. et al. Giant basal cell carcinoma: improvement in the quality of life after extensive resection // Scand J Plast Reconstr Surg Hand Surg. 2003; 37: 3: 181–185.
- Имянитов Е. Н. Эпидемиология и биология опухолей кожи // Практическая онкология. 2012; 13 (2): 61–68.
- Соколова А. В. Клиническая дифференциальная диагностика меланоцитарных невусов кожи с применением метода поверхностной дерматоскопии: Автореф. дисс. … к.м.н. Екатеринбург, 2003. 25 с.
Н. П. Малишевская*, 1, доктор медицинских наук, профессор
А. В. Соколова**, кандидат медицинских наук
* ГБУ СО УрНИИДВиИ, Екатеринбург
** Kлиника «Уральская», Екатеринбург
1 Контактная информация: orgotdel_2008@mail.ru
Grażyna Kamińska-Winciorek1, Waldemar Placek2
1The Center for Diagnostics and Treatment of Skin Diseases, Katowice, Poland
Head of Center: Grażyna Kamińska-Winciorek MD, PhD
2Dermatology, Sexually Transmitted Diseases and Clinical Immunology Clinic,
Head of Department: Prof. Waldemar Placek MD, PhD
Postep Derm Alergol 2015; XXXII, 1: 33–39
DOI: 10.5114/pdia.2014.44029
Краткое содержание
Дерматоскопия — это метод оценки структуры эпидермиса и дермы in vivo. В настоящее время он, вероятно, является наиболее точным нехирургическим методом диагностики меланоцитарных ново- образований. Ошибки диагностики могут приводить к неоправданному удалению доброкачественных новообразований и, что хуже, могут пропустить раннюю меланому. Ошибки дерматоскопического анализа можно разделить на связанные с невозможностью провести надлежащие тесты (процедурные и технические ошибки), и те, которые вытекают из недостатка знаний и опыта в дерматоскопии. В настоящей статье обсуждаются наиболее распространенные ошибки начинающих или неопытных врачей.
КЛЮЧЕВЫЕ СЛОВА: дерматоскопия, дермоскопия, распространенные ошибки, базовые ошибки, неверный диагноз, принципы, правила.
Cancer Foundation. Mr March поддерживается наградой от the Office of Medical Research, University of Nevada School of Medicine. Ms Truong and Ms Strazzulla внесли равный вклад с Drs Kim and Grossman.
Адрес для корреспонденции
Prof. Waldemar Placek MD, PhD, Dermatology, Sexually Transmitted Diseases and Clinical Immunology Clinic, University of Varmia and Masuria, 30 Wojska Polskiego St, 10-229 Olsztyn, Poland, phone/fax: + 48 601 915 419, e-mail: w.placek@wp.pl
Знание основано не только на правде, но и на ошибке.
Карл Густав Юнг
Введение
Дерматоскопия (дерматоскопия, эпилюминесцентная микроскопия, микроскопия поверхности кожи) — это метод in vivo исследования структур эпидермиса и дермы. Это простой проверенный способ диагностики, подразумевающий обследование новообразований кожи, главным образом меланоцитарных, с 10-кратным увеличением в традиционных дерматоскопах и с 70–100-кратным — в видеодерматоскопах (1,2).
Дерматоскопы/дермоскопы используют неполяризованный свет, требующий иммерсии (ультразвуковой гель, масло или вода) или поляризованный свет, который не требует применения каких-либо иммерсионных жидкостей. Использование дерматоскопии на приеме дерматолога увеличивает время консультации, но лишь на 72 секунды (3), поэтому стоит использовать ее для оценки любых новообразований на теле обследуемого пациента во время стандартного осмотра.
Так это описывается в литературе, на практике же дерматоскопия меланоцитарных новообразований кожного покрова всего тела с подготовкой документации и описание занимает от 30 до 40 минут. Дерматоскопия должна быть основным диагностическим инструментом, используемым не только опытными дерматологами, но также для скрининга меланоцитарных новообразований различными специалистами, в том числе онкологами, хирургами и врачами общей практики (2, 4).
Дерматоскопия характеризуется 83 % чувствительностью и 69 % специфичностью при выявлении меланомы (5). В клинической практике чрезвычайно важно правильно оценивать новообразования на теле пациента, основываясь на технических аспектах и базовых знаниях дерматоскопии.
Цель
Настоящая статья представляет авторскую классификацию наиболее распространенных и вероятных ошибок дерматоскопии на основе литературы, доступной на ресурсе PubMed, и личного опыта.
Ошибки
Ошибки дерматоскопического анализа можно разделить на связанные с невозможностью провести надлежащие тесты (процедурные и технические ошибки), и те, которые вытекают из-за недостатка знаний и опыта в дерматоскопии. В Таблице 1 представлена авторская классификация возможных ошибок дерматоскопии.
Процедурные (технические) ошибки
Выбор новообразований для дерматоскопии
Наиболее распространенной ошибкой, которую допускают врачи, является дерматоскопическая оценка только отдельных новообразований — тех, на которые указал пациент, или которые врач выбрал на основе клинической оценки по принципу ABCDE, или морфологической — черные новообразования, наиболее крупные в диаметре, возвышающиеся, или те, которые расположены в местах, где они могут подвергаться травматизации (в зоне нижнего белья, в акральных областях).
Решение об иссечении подозрительных новообразований должно приниматься на основе сравнения их с другими новообразованиями. В исследовании Argenziano и соавторов (6) решение об удалении подозрительного новообразования после морфологической оценки единственного новообразования в дерматоскопии принималось в 55 % случаев, но сокращалось до 14 % после сравнительного анализа с другими новообразования.
Чтобы выбрать несколько новообразований для иссечения, рекомендуется подготовить карту тела пациента, чтобы дать хирургу подсказки. Отметить такие участки можно при помощи фотографий, снятых камерой телефона самого пациента (7). Следует также помнить об обследовании всех новообразований на теле, не только меланоцитарных, но также розовых папул, чтобы не пропустить меланому, соответствующую правилу EFG («возвышающаяся», «плотная при пальпации», «постоянно растущая») (8).
Другой ошибкой является игнорирование небольших меланоцитарных новообразований при дерматоскопической оценке. Многие врачи, основываясь на классификации по правилу ABCD, считают, что меланомой могут быть только новообразования более 5 мм в диаметре.
Согласно литературе, 11,4–38,2 % всех меланом имеют диаметр менее 6 мм (9–12). В исследовании Giorgi и соавторов (13) 34 меланомы были выявлены среди 103 меланоцитарных новообразований диаметром менее 6 мм (33 %). В исследовании Bono и соавторов (14) из 924 меланом 22 (2,4 %) были микромеланомами с диаметром менее 3 мм. Клиническое правило АBCD в диагностике меланомы диаметром менее 6 мм не срабатывает (13).
Дерматоскопия меланомы с диаметром менее 5 мм, как правило, выявляет атипичные сосуды, нерегулярную окраску, присутствие атипичных глобул или точек, нерегулярных радиальных линий и зоны регресса (15) (Рис. 1). Другой ошибкой является использование дерматоскопии с такой периодичностью, при которой не удается установить профиль меланоцитарного невуса. Кроме того, следует проводить тотальное обследование кожных покровов всего тела (TBSE) (16).
Бессмысленно обследование пациента, который не желает раздеваться из чувства стыда, избегая обследование области гениталий, ягодиц; когда пациент не соглашается обследовать конечности, например, не хочет снимать обувь или не дает осмотреть кожу под волосами, а такое поведение встречается часто.
Таблица 1. Наиболее распространенные ошибки при дерматоскопии
| Некорректная оценка отдельных новообразований в дерматоскопии: |
| Недостаток знаний, связанных с определением базовых или главных дерматоскопических паттернов или дерматоскопических структур, в том числе неспособность отличить псевдоподии от периферических глобул; поиск таких структур, как кристаллические, с использованием неполяризованного света. |
Процедурные (технические) ошибки: |
| 1. Выбор новообразований для дерматоскопии. Необходимо обследовать все новообразования на теле в зависимости от количества и расположения: |
| Обследование только отдельных меланоцитарных новообразований, указанных пациентом. Обследование отдельных меланоцитарных новообразований, отобранных врачом на основе клинической оценки по правилу ABCDE или при наличии черных очагов, крупных новообразований, выступающих или расположенных в местах, подвергающих их риску злокачественности за счет травмирования (в зоне нижнего белья, в акральных зонах). Неприменение дерматоскопии к розовым немеланоцитарным невусам. Использование дерматоскопии с периодичностью, не позволяющей установить профиль меланоцитарного невуса. Бессмысленное обследование пациентов без осмотра генитальных зон, ягодиц, межъягодичной зоны, ступней или скальпа (из чувства стыда или из-за несогласия пациентов на обследование данных зон). Недостаток знаний относительно факторов, которые могут влиять на дерматоскопический паттерн или доброкачественное меланоцитарное образование, и нецелесообразное хирургическое удаление (дерматоскопическое исследование загорелых пациентов или использующих автозагар, что может менять цвет дерматоскопического паттерна). Невозможность обследования без планирования контрольных осмотров (каждые три месяца, каждые 6 месяцев, каждые 12 месяцев, менее часто, никогда). |
| 2. Выбор метода дерматоскопии: |
| Неправильное нанесение иммерсионной жидкости во время дерматоскопического обследования с использованием неполяризованного света. Вероятность ошибочного диагноза меланомы, узловой или бессимптомной меланомы вследствие использования не поляризованного дерматоскопа; кристаллические структуры, блестящие белые полосы определяются в поляризованном свете. Невозможность дерматоскопического обследования при длинносрочном контроле отдельных новообразований — невозможность выявления новых очагов, неспособность оценить развитие наблюдаемых меланоцитарных новообразований, особенно медленно растущих меланом in situ с небольшим диаметром. |
Все это может привести к неверной диагностике меланомы. Полнота дерматоскопического обследования должна стать частью медицинской практики. Риск пропустить злокачественное новообразование из-за невозможности проведения тотального обследования кожных покровов всего тела составляет 2,7 % (16).
В настоящее время дерматоскопия является точным методом выявления меланомы и минимизации неоправданных иссечений (так называемое количество, требующее иссечения — NNE, определяемое как отношение общего количества удаленных новообразований к количеству удаленных меланом (17, 18).
Недостаток знаний, относящихся к факторам, которые могут повлиять на дерматоскопический паттерн новообразования, согласно правилу «4 х 4 х 6» (19), может привести к неоправданному хирургическому удалению новообразования. Кроме того, дерматоскопическое обследование загорелых пациентов или тех, кто пользуется автозагаром, что может изменить цвет дерматоскопического рисунка, часто приводит к постановке ошибочного диагноза меланомы (20–22).
Чрезвычайно важно разработать стратегию дерматоскопического контроля для пациентов в зависимости от индивидуальных особенностей. Argenziano и соавторы (23) предлагают производить дерматоскопический контроль для предварительной оценки и последующее наблюдение отдельных новообразований при необходимости каждые 3 месяца вплоть до 54 месяцев (23).
Дерматоскопию следует проводить при краткосрочном мониторинге через 3 месяца (изменение характеристик меланомы наблюдается через 2–4 месяца), среднесрочном контроле с осмотром через 6 месяцев или долгосрочным — с ежегодным осмотром (особенно для медленно растущих меланом) (23).
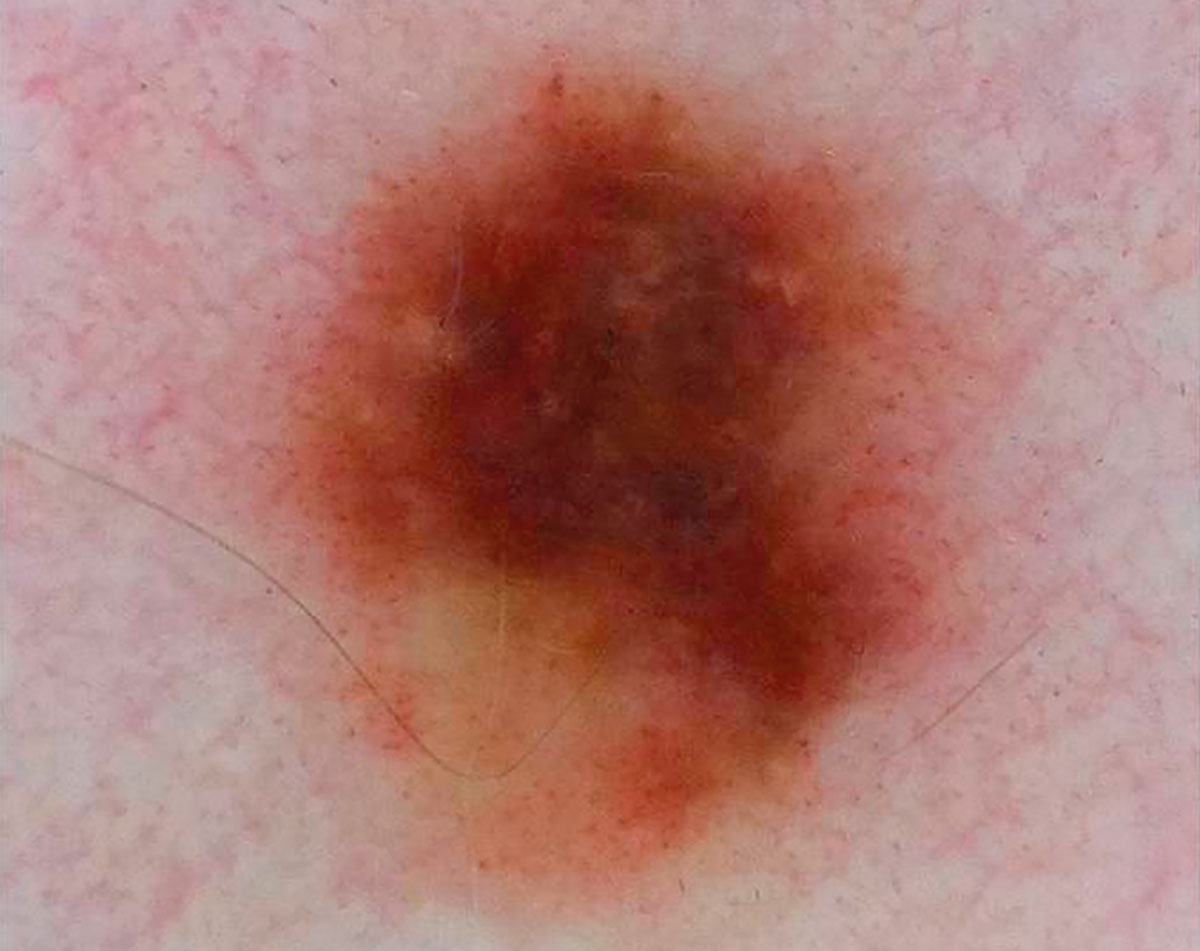
Рисунок 1. Дерматоскопический снимок меланомы in situ диаметром менее 5 мм.
Дерматоскопия показывает присутствие атипичных сосудов, атипичных глобул нерегулярного цвета, нерегулярных радиальных линий и нерегулярных многоцветных, коричневых и сине-серых участков
Степень соответствия составляет 84 % для протокола краткосрочного контроля, 64 % — для среднесрочного и 30 % — для долгосрочного (23). Периодичность контрольных осмотров зависит также от возраста пациента. Средний интервал в дерматоскопическом контроле составляет 20 месяцев (24) из-за вероятности развития медленно растущей меланомы (SGM).
Критерия для наблюдения отдельного новообразования являются асимметрия цвета, сетчатый рисунок и зоны регрессии (24). Ранние меланомы, выявленные цифровым методом, могут быть меньше в диаметре. Дерматоскопическим признаком при диагностике меланомы только лишь в контексте сравнительного исследования было небольшое увеличение диаметра очагов диаметром менее 2 мм (24).
В большом дерматоскопическом исследовании медленно растущей меланомы (25) дерматоскопическими признаками, предполагающими ее развитие, были недостаточные изменения диаметра и рост (75 % случаев) при наиболее медленном росте диаметра до 2 мм, разрушение более крупных структур, замена меланоцитарной сетки бесструктурными участками, появление новых цветовых оттенков (светло-коричневый исчезает, темно-коричневый появляется; такие цвета как красный, серый, черный и синий становятся более заметными) и новые дерматоскопические признаки меланомы, в том числе негативная сеть и сине-белая структура (25).
Выбор оптимального метода дерматоскопии
Иногда ошибка диагноза может произойти из-за небрежного использования дерматоскопии. Кроме упомянутых выше стандартных методов, для проведения дерматоскопического обследования с использованием ручного дерматоскопа важно правильно наносить иммерсионную жидкость во время дерматоскопического исследования в неполяризованном свете (2).
Вероятность ошибочного диагноза при выявлении узловой или бессимптомной меланомы может произойти из-за использования дерматоскопа с неполяризованным светом, тогда как блестящие белые полосы (кристаллы или кристаллические структуры) определяются дерматоскопами, использующими поляризованный свет (27).

Дерматоскоп Handyscope – устройство для мобильной цифровой дерматоскопии (FotoFinder)
Первое в мире устройство для цифровой теледерматоскопии, работающее на iOS и Android. В отличие от множества обычных дерматоскопов, handyscope соединяется с камерой мобильного устройства и использует специализированное программное обеспечение, включающее в себя оценку новообразований искусственным интеллектом, сервисы второго мнения и анализа клинических данных, а также сервисы защищенного облачного хранения дерматоскопических снимков.
Блестящие белые полосы указывают на злокачественность (отношение шансов: 10,534), особенно в случаях меланомы с инвазией, меланомы с высокой оценкой тотальной дерматоскопии (TDS) и тонких бессимптомных меланом (27). Кроме того, недостаточность архивных записей о предыдущих дерматоскопических обследованиях при контроле отдельных новообразований, а также невозможность определить новые очаги, неспособность оценить развитие наблюдаемых меланоцитарных новообразований, особенно медленно растущих меланом (24,25) или меланом in situ маленького диаметра, могут привести к тому, что меланома останется незамеченной.
Согласно Puig и Malvehi (28) дерматоскопическое обследование, тотальное фотографирование всего тела (TBD), цифровая дерматоскопия (DD) имеют важное значение для выявления меланомы. Цифровой контроль (DFU) у пациентов с диспластическими невусами позволяет выявить новые новообразования и изменения в существующих очагах (28).
Сочетание тотального фотографирования всего тела и цифровой дерматоскопии называется двухступенчатым методом цифрового контроля и способствует раннему выявлению меланомы на основе наблюдения макроскопических и дермоскопических изменений (29).
Ошибки, связанные с дефицитом знаний
В широком смысле ошибки, связанные с дефицитом знаний, включают диагностику и терапевтические решения, принятые в результате недостаточных знаний в области дерматоскопии. Неверный выбор новообразований для дерматоскопического обследования может быть связан с недостаточным пониманием дерматоскопического паттерна или структур, неспособностью отличить псевдоподии от периферических глобул, а также недостаток знаний различных алгоритмов дерматоскопического анализа (1, 2, 19, 30-32).
Каждый врач, выполняющий дерматоскопию, должен знать основные правила (контрольные списки): 3-точечное правило Argenziano (4, 33), 7-точечное итальянское правило (34), алгоритм, основанный на анализе паттерна («хаос и признаки») (35), австралийский метод Мензиса, 7 признаков меланомы или метод дерматоскопии Штольца и ABC-правило Блума (36), широко описанные в медицинской литературе в связи с их чувствительностью и специфичностью.
При применении правила ABCD для диагностики меланомы кожи чувствительность составляет 90,5 %, специфичность 72,4 % и диагностическая достоверность 78,1 % (36).
Результаты применения правила ABC показывают соответственно 90,5 %, 87 % и 88,1 %; метода Мензиса — 95,2 %, 77,8 %, 83,3 %; 7-признаков — 94 %, 74,6 % и 80,7 %, 7-точечного метода — 90,5 %, 87 % и 88,1 % (36). Чувствительность при использовании 3-точечного метода дерматоскопии достигает 89,6 % при 94,2 % специфичности (33).
В соответствии с 3-точечным методом следует уделить внимание асимметрии дерматоскопических правил и оценкой только лишь на основании одного из них, например, используя только правило ABCD Штольца. Поиск, например, кристаллических структур в неполяризованном свете — это не только техническая ошибка, но и ошибка, обусловленная дефицитом знаний.
Дерматоскопическая оценка отдельных немеланоцитарных новообразований должна основываться на общей структуре всего рисунка (зависит от выбранных паттернов) и локальных структурах (на основе выбранных дерматоскопических структур и признаков) и базироваться на расположении дерматоскопических структур, а не симметрии новообразования (4, 33). Также следует использовать другой нестандартный критерий — симптом «гадкого утенка» («ugly duckling» [37, 38] или симптом «fancy looking, так называемый признак «black sheep» [39]), а не только алгоритмы дерматоcкопического анализа.
Правило 4 х 4 х 6, предложенное Zalaudek и соавторами (19), позволяет клиницистам фиксировать общий паттерн и фак- торы, которые влияют на терапевтическое решение при установлении дерматоскопического диагноза отдельного меланоцитарного новообразования. Четыре дерматоскопических критерия связаны с цветом, паттерном, распределением пигмента и локализацией новообразования (19).
Шесть факторов, которые влияют на дерматоскопические действия, включают возраст, фототип кожи по Фицпатрику, историю болезни, воздействие ультрафиолета, беременность и динамику роста (19).
4 дерматоскопических критерия
| Черный | Глобульный | Многоочаговый | Акральные участки |
| Серый | Звездчатый | Необычный | Ногти |
| Коричневый | Сетчатый | Центральный | Лицо |
| Синий | Однородный синий |
Равномерный | Слизистая |
6 факторов
| Возраст | Воздействие ультрафиолета |
| Фототип кожи по Фицпатрику | Беременность |
| История болезни | Динамика роста |
Рисунок 2. Правило 4 х 4 х 6, предложенное Zalaudek и соавторами (19).
4 дерматоскопических критерия, распределенных по 4 подгруппам с 6 факторами, влияющими на терапевтическое решение, на основе дерматоскопии.
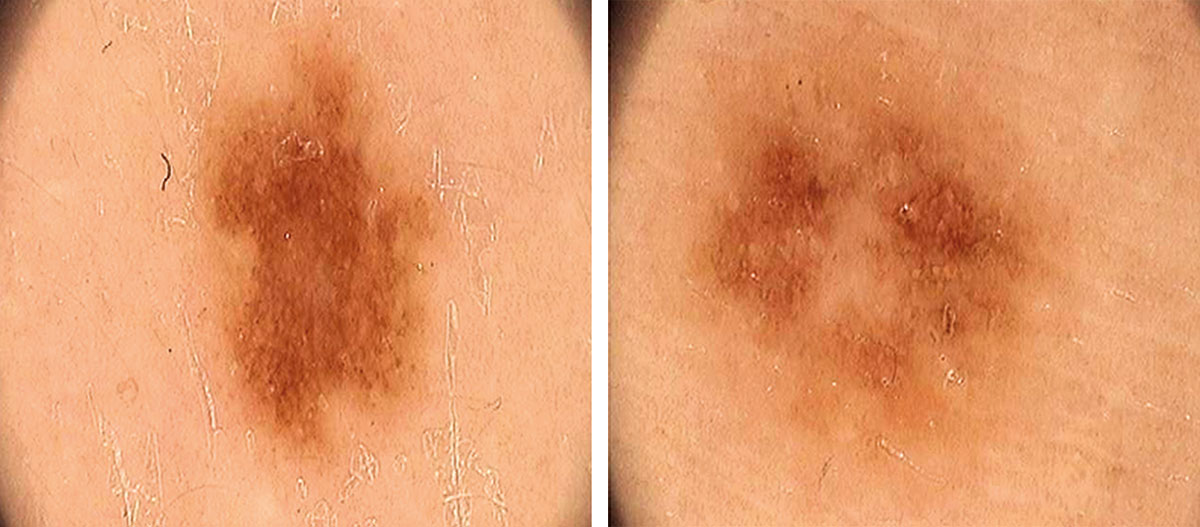
Рисунок 3. Два разных меланоцитарных новообразования у одного и того же пациента
в профиле, типичном для данного пациента
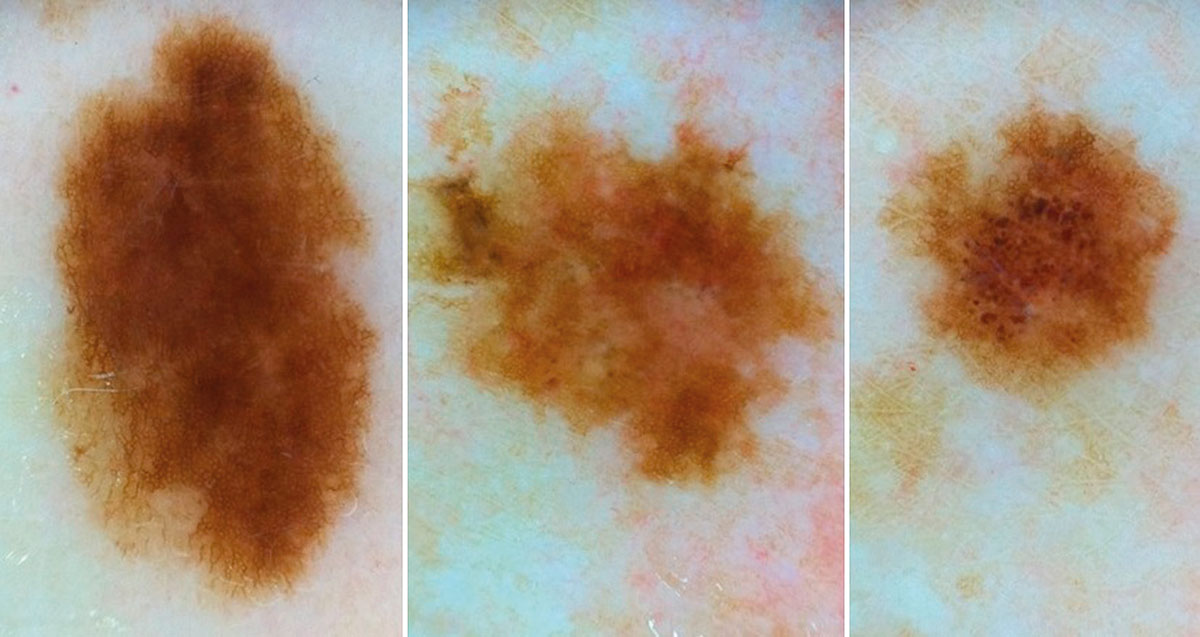
Рисунок 4. Три разных меланоцитарных новообразования у одного пациента
с дерматоскопическим профилем «подозрительное новообразование –
подлежит удалению». На деле «signature nevus», не подлежащие удалению
Правило 4 х 4 х 6, описанное ранее Zalaudek и соавторами (19), показано на Рисунке 2. В дифференциальном диагнозе меланоцитарных новообразований полезно определить так называемый профиль невуса, распространенный и характерный для большинства новообразований (6) (Рисунок 3).
Недостаточное знание критериев определения меланоцитарных новообразований и так называемых «signature nevus», характерных и индивидуальных для конкретного пациента (4) (Рисунок 4), может привести к ненужному хирургическому иссечению новообразований, которые кажутся подозрительными (например, выбор сразу 5–10 меланоцитарных новообразования для удаления во время одного обследования).
В настоящее время дерматоскопия позволяет выявлять меланому in situ диаметром менее 5 мм. В таких случаях стандартные дерматоскопические правила не работают и, следовательно, чрезвычайно важно понимать дерматоскопические признаки меланомы in situ (MIS).
Дерматоскопические признаки in situ меланом — это сетчатый рисунок, сине-серая сеть, многокомпонентная, очаговая, спитцоидная негативная сеть, сеть из глобул синего цвета и глобулярная сетчатая структура (41). Новым признаком меланомы in situ является также «mistletoe sign» (знак омелы) (42).
Меланома in situ, как правило, больше в диаметре, чем диспластический невус; атипичная сеть покрывает более половины площади, обычно присутствуют несколько типов пигментной сети, в центральной и периферийных зонах имеются бело-голубые участки регрессии (43).
В недавнем исследовании Seidenari и соавторов (44) из 22 микромеланом (диаметром менее 4 мм) 12 были определены как меланомы in situ с наиболее частым проявлением атипичной пигментной сети и нерегулярного цвета (44). В диагностике черных узелков должно применяться правило сине-черных точек.
Стандартный дерматоскопический критерий в комбинации с поиском синих и черных цветов в новообразовании дает 90,6 % точность и 92 % специфичность при выявлении узелковой меланомы (45). Предельно важным в дифференциальном дерматоскопическом анализе меланомы является понимание дерматоскопического изображения симулянтов меланомы (черного себорейного кератоза, синего невуса и многих других) (46-48).
Важно подчеркнуть, что терапевтические решения должны приниматься на основе правила 4 х 4 х 6 (19) и никогда на основе единственного дерматоскопического критерия. Что касается исследования Argenziano и соавторов (19), дерматоскопия повышает выявление ранней меланомы за счет трех главных аспектов: дерматоскопические признаки меланомы гораздо раньше выявляются при дерматоскопии, чем при клиническом обследовании; клиницисты чаще проверяют не просто подозрительные, а даже банально выглядящие новообразования и более тщательно наблюдают пациентов (49).
Полное обследование кожных покровов, наблюдение пациентов со множественными родинками, адекватная диагностика новообразований, требующих лечения; использование сравнительного подхода к пациентам с множественными невусами — это ключ к надлежащему выявлению меланомы и предотвращению базовых ошибок (49).
Таким образом, во избежание ошибочной диагностики меланомы Lallas и соавторы (5) рекомендовали обследовать все новообразования на коже, осматривать все участки тела, принимать 10-секундное решение (когда время обследования новообразования дольше, оно требует удаления), наблюдать пациентов со множественными меланоцитарными новообразованиями, всегда иссекать подозрительные узелковые новообразования и сочетать клинический критерий с дерматоскопическими, а также коррелировать клинические критерии с гистопатологическими (50).
В настоящее время дерматоскоп является незаменимым диагностическим инструментом для каждого врача, сравнимым со стетоскопом, который необходим для обследования физического состояния каждого пациента (51).
Конфликт интересов
Авторы не сообщают о конфликте интересов.
Список литературы
1. Kaminska-Winciorek G. Digital dermatology. Cornetis, Wrocław 2008.
2. Kaminska-Winciorek G, Spiewak R. Basic dermoscopy of melanocytic lesions for beginners. Postepy Hig Med Dosw (Online) 2011; 65: 501-8.
3. Zalaudek I, Kittler H, Marghoob AA, et al. Time required for a complete skin examination with and without dermoscopy: a prospective, randomized multicenter study. Arch Dermatol 2008; 144: 509-13.
4. Zalaudek I, Argenziano G, Soyer HP, et al. Dermoscopy Working Group. Three-point checklist of dermoscopy: an open internet study. Br J Dermatol 2006; 154: 431-7.
5. Blum A, Hofmann-Wellenhof R, Luedtke H, et al. Value of the clinical history for different users of dermoscopy compared with results of digital image analysis. J Eur Acad Dermatol Venereol 2004; 18: 665-9.
6. Argenziano G, Cacitrala C, Argido M. Dermoscopy of patients with multiple nevi: improvement management recommendations using a comparative diagnostic approach. Arch Dermatol 2011; 147: 46-9.
7. Kaminska-Winciorek G, Spiewak R. Tips and tricks in the dermoscopy of pigmented lesions. BMC Dermatol 2012; 12: 14.
8. Giacomel J, Zalaudek I, Mordente I, et al. Never perform laser treatment of skin tumors with clinical “EFG” criteria. J Dtsch Dermatol Ges 2008; 6: 386-8.
9. Fernandez EM, Helm KF. The diameter of melanomas. Dermatol Surg 2004; 30: 1219-22.
10. Abbasi NR, Yankowitz M, Gutkowicz-Krusin D, et al. Utility of lesion diameter in the clinical diagnosis of cutaneous melanoma. Arch Dermatol 2008; 144: 469-74.
11. Goldsmith SM. A series of melanomas smaller than 4 mm and implications for the ABCDE rule. J Eur Acad Dermatol Venereol 2007; 21: 929-34.
12. Helsing P, Loeb M. Small diameter melanoma: a follow-up of the Norwegian Melanoma Project. Br J Dermatol 2004; 151: 1081-3.
13. De Giorgi V, Savarese I, Rossari S, et al. Features of small melanocytic lesions: does small mean benign? A clinical-dermoscopic study. Melanoma Res 2012; 22: 252-6.
14. Bono A, Bartoli C, Baldi M, et al. Micro-melanoma detection. A clinical study on 22 cases of melanoma with a diameter equal to or less than 3 mm. Tumori 2004; 90: 128-31.
15. Pupelli G, Longo C, Veneziano L, et al. Small-diameter melanocytic lesions: morphological analysis by means of in vivo confocal microscopy. Br J Dermatol 2013; 168: 1027-33.
16. Argenziano G, Zalaudek I, Hofmann-Wellenhof R, et al. Total body skin examination for skin cancer screening in patients with focused symptoms. J Am Acad Dermatol 2012; 66: 212-9.
17. Argenziano G, Cerroni L, Zalaudek I, et al. Accuracy in melanoma detection: a 10-year multicenter survey. J Am Acad Dermatol 2012; 67: 54-9.
18. Chen L, Dusza S, Grazzini M, et al. Redefining the number needed to excise. Australas J Dermatol 2013; 54: 310-2.
19. Zalaudek I, Docimo G, Argenziano G. Using dermoscopic criteria and patient-related factors for the management of pigmented melanocytic nevi. Arch Dermatol 2009; 145: 816-26.
20. Orpin SD, Preston PW, Salim A. The ‘St Tropez’ sign: a new dermoscopic feature of seborrheic keratoses? Clin Exp Dermatol 2006; 31: 707-9.
21. Hofmann-Wellenhof R, Wolf P, Smolle J, et al. Influence of UVB therapy on dermoscopic features of acquired melanocytic nevi. J Am Acad Dermatol 1997; 37: 559-63.
22. Kaminska-Winciorek G. Dermatoscopy of melanocytic lesions: an influence of ultraviolet radiation. Przegl Dermatol 2008; 95: 463-7.
23. Argenziano G, Mordente, I Ferrara G. Dermoscopic monitoring of melanocytic lesions: clinical outcome and patients compliance vary according to follow-up protocols. Br J Dermatol 2008; 159: 331-6.
24. Argenziano G, Kittler H, Ferrara G, et al. Slow-growing melanoma: a dermoscopy follow-up study. Br J Dermatol 2010; 162: 267-73.
25. Terushkin V, Dusza SW, Scope A, et al. Changes observed in slow-growing melanomas during long- term dermoscopic monitoring. Br J Dermatol 2012; 166: 1213-20.
26. Jaimes N, Marghoob AA. The morphologic universe of melanoma. Dermatol Clin 2013; 31: 599-613.
27. Shitara D, Ishioka P, Alonso-Pinedo Y. Shiny white streaks: a sign of malignancy at dermoscopy of pigmented skin lesions. Acta Derm Venereol 2014; 94: 132-7.
28. Puig S, Malvehy J. Monitoring patients with multiple nevi. Dermatol Clin 2013; 31: 565-77.
29. Salerni G, Carrera C, Lovatto L, et al. Characterization of 1152 lesions excised over 10 years using total body photography and digital dermatoscopy in the surveillance of patients at high risk for melanoma. J Am Acad Dermatol 2012; 67: 836-45.
30. Soyer HP, Argenziano G, Ruocco V, et al. Dermoscopy of pigmented skin lesions. Eur J Dermatol 2001; 11: 270-6.
31. Zalaudek I, Kreusch J, Giacomel J, et al. How to diagnose nonpigmented skin tumors: a review of vascular structures seen with dermoscopy: part II. Nonmelanocytic skin tumors. J Am Acad Dermatol 2010; 63: 377-86.
32. Zalaudek I, Manzo M, Savarese I, et al. The morphologic universe of melanocytic nevi. Semin Cutan Med Surg 2009; 28:149-56.
33. Soyer HP, Argenziano G, Zalaudek I, et al. Three-point checklist of dermoscopy. A new screening method for early detection of melanoma. Dermatology 2004; 208: 27-31.
34. Argenziano G, Catricalà C, Ardigo M, et al. Seven-point checklist of dermoscopy revisited. Br J Dermatol 2011; 164: 785-90.
35. Kittler H. Dermatoscopy: introduction of a new algorithmic method based on pattern analysis for diagnosis of pigmented skin lesions. Dermatooncology: Dermatol Pract Concept 2007; 13: 1.
36. Blum A, Rassner G, Garbe C. Modified ABC-point list of dermoscopy: a simplified and highly accurate dermoscopic algorithm for the diagnosis of cutaneous melanocytic lesions. J Am Acad Dermatol 2003; 48: 672-8.
37. Carli P, Chiarugi A, de Giorgi V. Examination of lesions (including dermoscopy) without contact with the patient is associated with improper management in about 30% of equivocal melanomas. Dermatol Surg 2005; 31: 169-72.
38. Scope A, Dusza SW, Halpern AC, et al. The “ugly duckling” sign: agreement between observers. Arch Dermatol 2008; 144: 58-64.
39. Thomas L. Braun R. Atlas of dermatoscopy. Urban & Partner, Wrocław 2008.
40. Argenziano G, Albertini G, Castagnetti F, et al. Early diagnosis of melanoma: what is the impact of dermoscopy? Dermatol Ther 2012; 25: 403-9.
41. Seidenari S, Bassoli S, Borsari S, et al. Variegated dermoscopy of in situ melanoma. Dermatology 2012; 224: 262-70.
42. Kaminska-Winciorek G, Właszczuk P, Wydmański J. “Mistletoe sign” probably a new dermoscopic descriptor fro melanoma in situ and melanocytic junctional nevus in the inflammatory stage. Postep Derm Alergol 2013; 30: 316-9.
43. Seidenari S, Ferrari C, Borsari S, et al. The dermoscopic variability of pigment network in melanoma in situ. Melanoma Res 2012; 22: 151-7.
44. Seidenari S, Ferrari C, Borsari S, et al. Dermoscopy of small melanomas: just miniaturized dermoscopy? Br J Dermatol 2014; 171: 1006-13.
45. Argenziano G, Longo C, Cameron A, et al. Blue-black rule: a simple dermoscopic clue to recognize pigmented nodular melanoma. Br J Dermatol 2011; 165: 1251-5.
46. Kaminska-Winciorek G, Wydmanski J. Benign simulator of melanoma on dermoscopy-black colour does not indicate always melanoma. J Preclin Clin Res 2013; 1: 6-12.
47. Kaminska-Winciorek G. Letter: “Blue pseudo-veil sign” – a new dermoscopic term? Dermatol Surg 2012; 38: 1574-5.
48. Kamińska-Winciorek G, Spiewak R. Dermoscopy on nevus comedonicus: a case report and review of the literature. Postepy Dermatol Alergol 2013; 30: 252-4.
49. Argenziano G, Albertini G, Castagnetti F, et al. Early diagnosis of melanoma: what is the impact of dermoscopy? Dermatol Ther 2012; 25: 403-9.
50. Lallas A, Zalaudek I, Apalla Z, et al. Management rules to detect melanoma. Dermatology 2013; 226: 52-60.
51. Zalaudek I, Lallas A, Moscarella E, et al. The dermatologist’s stethoscope-traditional and new applications of dermoscopy. Dermatol Pract Concept 2013; 3: 67-71.
Подозрение на меланому
Дискуссия
— Меланома
Здравствуйте, в феврале 2016г. мужу удалили родинку скальпелем под местной анастезией. Результат гистологии- диспластический пигментный невус, эпидермальный компонент которого представлен лентигинозной меланоцинтарной дисплазией. Отмечается эрозирование и хроническое воспаление в дерме, некоторые фокусы скопления меланоцитов имеют повышенную пронеферативную(неразборчиво) активность. Врач сказал что все нормально, мазать марганцовкой. Рана плохо заживала, 6 июня мы обратились опять. Врач за 10 минут обрезал еще вокруг, гистология — смешанный меланоцитарныйневус с выраженными дистрофическими изменениями и участками пограничной активности. Доктор сказал что все нормально и отпустил Рана зажила хорошо но на месте шва через некоторое время появился под кожей бугорок. 28 марта 2017 г мы пошли в онкодиспансер, там у мужа тонкой иглой взяли анализ, который показал метастаз меланомы в рубец. Назначили ПЭТ/КТ и сказали пересмотреть стекла от прошлых операций в другой лаборатори. Мы поехали в 3ю больницу где есть лаборатория. Там врач при нас посмотрел стекла и подтвердил что это был диспластический невус, а стекло с результатом от 28.03.2017 отправил пересмотреть к другому специалисту, который подтвердил меланому и сказал немедленно резать позвонил врачу, нас тут- же приняли сказали сделать ПЭТ/КТ и после срочно на операцию. Результат ПЭТ/КТ- Состояние после удаления образования кожи спины 06.16, повторного иссечения образования п/о рубца по поводу меланомы. Жидкостное образование спины справа без метаболической активности ФДГ (серома?) Убедительных данных о наличии активной специфической ткани на момент исследования не получено. Метастаз тоже нигде не обнаружено. 14 04.2017 под общим наркозом выполнили операцию. Выполнены диагностические исследования: Пересмотр гистологических препаратов от 25.02.16г., 08.06.16г.: меланома кожи, узловая форма, по Кларку3 (3дня назад намподтвердили, что это был диспластический невус) гистология от19.04.17рецидив беспигментной меланомы кожи, толщина0.5мм. Подскажите пожалуйста, может ли ПЭТ/КТ так ошибаться и может ли пигментный невус переродиться в беспигментную меланому? Какой прогноз при полном диагнозе: С43.5 — С43.5- злокачественная меланома туловищаТхN0M0. С уважением Ольга.
Екатерина Сергеевна
Дежурный врач
Здравствуйте. Я могу помочь вам с вашей ситуацией. Напишите ваш вопрос.Только что
Ваш вопрос
— опишите вашу ситуацию;
Ответы врачей
Здравствуйте, Ольга
Сомнений в диагнозе «меланома» у Вас не должно быть, т. к. стеклопрепараты пересматривались неоднократно. Меланома отличается быстрым прорастанием вглубь кожного покрова и развитием метастазов под влиянием распространения раковых клеток гематогенным и лимфогенным путем. За счет этих особенностей меланома является агрессивным злокачественным кожным новообразованием. Для определения распространенности заболевания и исключения метастазов лучше чем ПЭТ/КТ еще не придумали. В дополнение могу еще посоветовать сдать генетическое тестирование меланомной опухоли на предмет наличия мутаций V600E либо V600K в гене BRAF. Для прогноза заболевания необходимо знать: стадию, толщину опухоли по Бреслоу, уровень инвазии по Кларку, количество митозов, наличие или отсутствие изъязвления, общий размер образования и расстояние до ближайшего края резекции (отступ).
Здоровья Вам!

Спасибо за ответ. Но я не понимаю, почему ПЭТ не выявил самого очага меланомы(делали от стоп до макушки), Затем насторожило , что гистолог при пересмотре стекол двух первых резекций подтвердил диспластический невус, а когда мы решили делать операцию у них вдруг нашел меланому, и почему врач делавший нам операцию дал такое скудное описание операции? На все мои вопросы один ответ- так бывает. С уважением ольга
Ольга — 2017-04-29 11:10:51
Ольга
Невус является причиной и относится к факторам риска развития меланомы. А так- же могу сказать что немоловажным при гистологическом исследование является уровень оснащенности лаборатории и наличие высококвалифицированных специалистов. Иногда при сомнениях в гистологической верификации диагноза стеклопрепараты пересматриваются в крупных онкологических центра — лабораториях. Но именно здесь можно сделать акцент на агрессивность самого заболевания. В Вашем случае — диагноз все таки был подтвержден. ПЭТ/КТ делали для уточнения распространенности и исключения метастазов, тем самым планируя возможность проведения и объем оперативного вмешательства. Метастазов не было…, сам очаг был видимо локальным и небольших размеров, поэтому Вас в срочном порядке отправили на операцию. Про скудное описание операции ничего не могу сказать…., не видела. По гистологии не все описано…. При Вашей ситуации: Рецидив в послеоперационный рубец, по Кларку 3, толщина 0,5 — прогноз относительно благоприятный. В настоящее время Ваша задача — четко следовать рекомендация онколога — дальнейшая тактика введения Вашего супруга и правильно подобранное лечение.
Здоровья Вам и Вашим близким.

Жидкостное образование спины справа без метаболической активности ФДГ (серома?) Убедительных данных о наличии активной специфической ткани на момент исследования не получено. Это заключение ПЭТ о месте иссечения невуса . Разве это говорит о наличии меланомы в этом месте? Стекла с диагнозом невус мы отнесли на пересмотр, врач при нас посмотрел стекла и подтвердил что это был диспластический невус, но когда мы решили делать операцию в этой больнице , буквально через 3 дня теже стекла превратились В гистологию по Кларку 3, толщина 0,5
Ольга — 2017-04-29 13:04:36
Ольга
ПЭТ/КТ — довольно таки точный метод обследования, но не 100%. Решающим в онкологи является гистология. Возможно Ваш доктор, который пересматривал стекла…, все же в чем- то засомневался и отправил их на пересмотр…., и тут решающим в определении диагноза была именно гистология, что и подтверждает гистология уже после операции от 19.04.17г.

Эти пятна указывают на рак кожи?
Эти пятна появились месяца 2 назад, не шелушатся, не беспокоят, это пятна рака кожи начальной стадии?
Анна — 2019-01-17 14:31:47
Анна
Никакой это не рак) Успокойтесь. Предположительно это розовый лишай. ( питириаз Жибера) Сразу скажу, заболевание не заразно! Провоцирующими факторами являются недавно перенесённые ОРВИ, стресс. При контакте с водой, раздражении мылом, грубой одеждой, потливости распространяется.
Тактика такая: не мочить 5-7 дней. Исключить спорт. Можно наносить депантенол( бепантен крем)+ гидрокортизоновый крем, смешав 2: 1- 2 раза в сут. При усиление сыпи- отменить наружные средства и ничем не лечить, обратиться к дерматологу! Есть еще один способ лечения — это чемеричная вода, она продается в аптеках без рецепта. Нужно смазывать пораженные участки кожи ватным диском два раза в день не менее 14 дней. Внимательно прочитайте инструкцию к препарату и пользуйтесь осторожно — данный препарат ядовит.
Но самое правильное — обратиться на консультацию к дерматологу, где Вам сделают соскоб с кожи и определят вид возбудителя и его чувствительность к антимикотическим препаратам. Перед визитом к врачу не нужно ничем обрабатывать не менее пяти дней, иначе точный диагноз будет невозможно поставить.

Меланома
Меланома или нет? Эта родинка в таком виде уже лет 15. не беспокоит.
Юлия — 2019-03-17 13:25:31
Юлия
Если новообразование изменило цвет, форму, размер — это повод для скорейшего обращения к дерматологу или онкодерматологу. Если родинка ассиметрична и есть участки разного цвета — как в Вашем случае — тоже нужен очный осмотр, по фотографии в данном случае точно нельзя сказать о природе данного образования. Только после очного осмотра с помощью дерматоскопа можно дать точный ответ. Но я бы рекомендовала Вам удалить данное новообразование хирургическим иссечением на границе со здоровой тканью с последующей гистологией( исследованием на клеточном уровне — чтобы исключить онкологию).

По данному вопросу консультацию проводят практикующие врачи. Медицинское образование проверено администрацией сайта. Сервис несёт полную моральную и юридическую ответственность за качество консультаций. Подозрение на меланому консультация врача на тему дается в справочных целях. По итогам полученной консультации, пожалуйста, обратитесь к врачу, в том числе для выявления возможных противопоказаний. По возможности, будьте готовы ответить на дополнительные вопросы. В противном случае консультация будет дана на основе указанной в вопросе информации и иметь предположительный характер. Не занимайтесь самолечением, консультация врача онлайн не заменяет очный осмотр.
Оставьте отзыв о нашем сервисе
Нам важно знать ваше мнение. Оставьте отзыв о нашем сервисе
Диагностика меланомы и методы ее лечения
Из этой статьи вы узнаете:
-
Особенности и симптомы меланомы
-
Причины возникновения меланомы
-
Основные виды меланомы
-
Диагностика меланомы
-
Стадии меланомы
-
Лечение меланомы
Диагностика меланомы на ранних стадиях позволяет предотвратить развитие заболевания и после определения клинической картины правильно подобрать лечение. По своей сути это агрессивное злокачественное образование, прогрессирующее в результате необратимого генетического перерождения меланобластов и меланоцитов. Именно эти клетки вырабатывают меланин, который отвечает за цвет кожи, ее восприимчивость к загару и образование родинок.
К сожалению, за последние десять лет количество больных меланомой резко увеличилось. Это связано с возросшим воздействием ультрафиолетовых лучей и модой на загар. Как не попасть в зону риска и предотвратить развитие рака кожи, читайте в нашей статье.
Особенности и симптомы меланомы
Пигменты, окрашивающие кожные покровы, глазную радужку и волосы, синтезируются меланоцитами. Пигментированные участки, содержащие избыточное количество меланина, родинки (невусы), появляются на протяжении всей нашей жизни. Невусы склонны становиться злокачественными образованиями под воздействием определенных экзогенных (внешних) и эндогенных (внутренних) факторов. В связи с этим участки на теле с наличием врожденных или приобретенных родинок подвержены риску возникновения меланомы. Чаще всего это эпидермис, реже – слизистые оболочки и глазная сетчатка.
Мутированные клетки начинают беспорядочно делиться, расти, провоцируя формирование опухоли и метастазы. Часто из нескольких доброкачественных невусов формируется одно злокачественное новообразование.
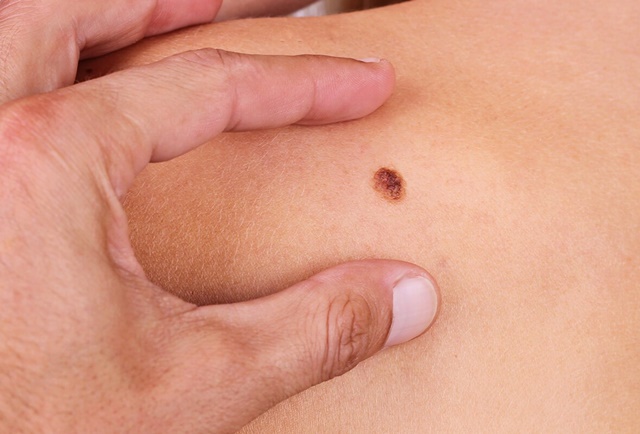
Заболевание имеет разнообразную клиническую картину. Параметры опухоли – структура поверхности, размеры, границы, пигментация, плотность – могут сильно отличаться.
Меланома, которая образовалась из невуса, как правило, развивается в течение продолжительного срока (на протяжении нескольких лет). Затем опухоль начинает стремительно разрастаться и трансформироваться (за 1–2 месяца).
Существенную помощь в раннем выявлении симптомов меланомы оказывают самодиагностика и своевременная консультация онколога. Признаки злокачественного новообразования:
-
кожа зеркально ровная и гладкая, с отсутствием кожных борозд;
-
опухоль увеличивается в размерах и растет по поверхности кожи;
-
ощущается дискомфорт в зоне расположения невуса (зуд, жжение, покалывание);
-
кожа в проблемной области сухая и шелушится;
-
в пораженном опухолью месте наблюдается изъязвление и кровотечение;
-
в зоне роста родинки и вокруг нее развивается воспалительный процесс;
-
появляются дочерние новообразования.
О развитии заболевания могут свидетельствовать внезапно появившиеся уплотнения и узелки под кожей.
Причины возникновения меланомы
Причины появления рака кожи полностью не изучены. Специалисты считают, что очень часто меланома возникает из-за повреждения ДНК-структуры кожных клеток, вызванного действием ультрафиолетовых лучей. Главным источником УФ-излучения является солнце.
В солнечных лучах содержится три разновидности ультрафиолета:
-
ультрафиолет А (УФА);
-
ультрафиолет В (УФВ);
-
ультрафиолет С (УФС).
Ультрафиолет С задерживает атмосфера Земли. Другие два типа ультрафиолета способны пройти сквозь атмосферный слой и повредить кожные покровы, значительно повышая риск развития рака. Лучи УФВ считают одной из главных причин меланомы. Кроме того, рак кожи могут спровоцировать искусственные источники света, такие, как ультрафиолетовые лампы и солярий. Риск меланомы значительно возрастает из-за регулярных солнечных ожогов на коже (от солнца или искусственных источников). Причем вероятность появления заболевания от данных факторов увеличивается независимо от возраста.
Согласно статистическим данным, повышенный риск развития меланомы имеют люди с множеством родинок и большими пигментными пятнами необычной формы. Вероятность развития рака кожи увеличивается на 60 % даже при наличии на теле единственной родинки, имеющей нетипичную форму и слишком большие размеры. В связи с этим необходимо постоянно следить за внешним видом невусов, а также стараться не подвергать кожу длительному воздействию солнечных лучей.
Проведенные исследования показали, что вероятность образования меланомы у человека повышается, если у двух и более ближайших родственников был ранее диагностирован рак кожи.
Все виды рака кожи могут развиваться в результате влияния определенных факторов:
-
светлые бледные кожные покровы, плохо поддающиеся загару;
-
светлый и рыжий оттенок волос;
-
голубой цвет глаз;
-
пожилой возраст;
-
сильная пигментация в виде множества веснушек;
-
шрамы и рубцы, оставшиеся от ожога, или следы от лучевой терапии;
-
болезни, негативно сказывающиеся на иммунной системе (например, ВИЧ);
-
лекарственные средства, действие которых направлено на подавление иммунной системы (иммунодепрессанты), как правило, такие средства применяют после операций по пересадке органов;
-
воздействие на кожу некоторых химических веществ (креозота, мышьяка);
-
ранее диагностированный рак кожи.
Основные виды меланомы
Существуют 3 основных типа меланомы:
-
Поверхностно-распространенная. Опухоль, имеющая меланоцитарное происхождение. Эта разновидность встречается чаще остальных (в 70–75 % случаев) у представителей европеоидной расы среднего возраста. Опухоль имеет небольшие размеры, сложную форму, неровные границы, неравномерную окраску рыже-бурого или бурого оттенка с мелкими синюшными вкраплениями.
При наличии данного новообразования кожа повреждается. В местах поражения появляются выделения (как правило, водянистые). Меланома может разрастаться по поверхности и проникать вглубь. Стадия вертикального роста может наступать спустя месяцы и даже годы.
-
Узловая. Данный тип образования встречается в 14–30 % случаев. Его называют нодулярным (от лат. nodus — узел). Опухоль обладает наиболее агрессивным характером. Вертикальный рост меланомы происходит очень стремительно и занимает от 4–5 месяцев до 2 лет. Развитие раковой опухоли происходит без явных изменений на поверхности кожи. Какие-то повреждения или пигментный невус отсутствуют, оттенок равномерный темно-синего или черного цвета. Иногда опухоль, похожая на узелок или папулу, бывает пигментирована.
-
Злокачественное лентиго. Часто это заболевание диагностируется у пожилых людей старше 60 лет. Его выявляют в 5–10 % случаев. Кожа на открытых участках тела (лице, шее, руках) покрывается узелками (не более 3 мм) темно-синего или коричневого цвета. Опухоль, при которой могут захватываться волосяные фолликулы, характеризуется медленным радиальным ростом в поверхностном слое кожи (20 лет и более) до вертикальной фазы.
Диагностика меланомы
Необходимо тщательно следить за состоянием своих родинок. Если их внешний вид как-то изменился, нужно обязательно обратиться за консультацией к специалисту.
Эффективный метод самоконтроля – ведение дневника родинок, в котором размещаются фотографии, указываются места их расположения, количество. Благодаря такой своеобразной «карте родинок» диагностика меланомы будет более эффективной.
Определить признаки меланомы может не только любой врач при осмотре, но и вы сами. Однако это заболевание редкое, и доктора непрофильных специализаций встречаются с ним только раз за несколько лет. В связи с этим врач, заподозривший меланому, должен вас направить на консультацию к онкологу.
Для подтверждения или опровержения диагноза используются два простых исследования – дерматоскопия или эпилюминесценция. Данные методы диагностики подразумевают изучение вызвавшего подозрение пигментного новообразования с использованием увеличительного прибора. Для осмотра применяют обыкновенную лупу, но чаще пользуются специальным эпилюминисцентным микроскопом (дерматоскопом). Под действием данного аппарата эпидермис становится прозрачным, что существенно облегчает подробное исследование опухоли.
Кроме дерматоскопии, исследование опухоли может проводиться при помощи других безоперационных методов: ультразвука, радиоизотопной диагностики и т.д. При наличии изъязвлений или трещин на поверхности новообразования делают мазок-отпечаток и осматривают под микроскопом на предмет опухолевых клеток. Данный метод называют цитологическим. Если после проведенных манипуляций не удалось точно выяснить, меланома ли это, проводят биопсию (для гистологии). Гистологическое исследование предполагает взятие кусочка ткани из опухоли с целью его изучения под микроскопом.
Российские и зарубежные специалисты неоднозначно относятся к биопсии меланомы, так как даже нанесение минимальной травмы может спровоцировать стремительный рост опухоли и ее распространение по всему организму. Но иногда допустимо применение эксцизионной биопсии, при которой подозрительное новообразование и область вокруг (2–10 мм) полностью иссекается. Затем на разрез накладывают швы. В это же время гистолог проводит анализ срезанной ткани под микроскопом. Вся процедура выполняется в операционной. Ее продолжительность не превышает 10–15 минут. Если проведенная гистология подтверждает диагноз, хирург сразу проводит повторную операцию. Ее объем зависит от выявленной стадии заболевания.
Как правило, эксцизионную биопсию выполняют под общим наркозом. При проведении местного обезболивания имеется риск распространения злокачественных клеток вместе с раствором анестетика, вводимым в ткани, расположенные вокруг опухоли. При общем наркозе есть возможность выполнения более обширной операции, если гистология подтвердит онкологический диагноз.
После хирургического вмешательства проводят дополнительное обследование (компьютерная, позитронно-эмиссионная томография и магнитно-резонансная томография, анализы крови и т. д.), чтобы выяснить, не распространился ли раковый процесс в другие органы.
Меланома характеризуется быстрым метастазированием, образованием дочерних опухолей, которые доставляются с помощью тока крови, лимфы, контактным путем к другим тканям и органам. Считается, что лимфоузел, расположенный рядом с опухолью, задерживает самые первые метастазы. По-другому он называется сторожевой или сигнальный. Таких лимфатических узлов может быть несколько. Их количество зависит от анатомического расположения опухоли. Чтобы определить самые первые метастазы при отсутствии явных изменений в структуре сторожевого лимфоузла, проводят биопсию.
В зоне удаленной меланомы под кожу вводится пигментный раствор синего цвета и слабое радиоактивное химическое вещество. Эту контрастную жидкость пускают по лимфатическим протокам, по которым могли бы двигаться злокачественные клетки.
Первый лимфатический узел, куда попадает контрастная жидкость, является сторожевым. Хирург находит его и удаляет, не задевая другие. Удаленный лимфоузел исследуют под микроскопом.
Наличие в лимфоузле раковых клеток свидетельствует о том, что и в других лимфатических узлах могут быть метастазы. Если злокачественные клетки отсутствуют, риск метастазирования минимален.
С помощью биопсии сигнального лимфоузла диагноз уточняется, и врач принимает решение, нужно ли удалять другие близлежащие лимфатические узлы. Эта операция называется лимфодиссекция.
Стадии меланомы
Для описания степени глубины проникновения меланомы в кожу (толщины опухоли), а также площади ее распространения различают несколько стадий. Курс лечения строится в зависимости от определенной стадии заболевания.
-
Стадия 0 — меланома только на поверхности кожи.
-
Стадия 1А — толщина меланомы менее 1 мм.
-
Стадия 1В — толщина меланомы 1–2 мм, либо менее 1 мм, но поверхность кожи повреждена (образовались язвы), или ее клетки делятся быстрее обычного (митотическая активность).
-
Стадия 2А — толщина меланомы 2–4 мм либо 1–2 мм, но на поверхности кожи образовались язвы.
-
Стадия 2В — толщина меланомы больше 4 мм либо 2–4 мм, и на поверхности кожи образовались язвы.
-
Стадия 2С — толщина меланомы более 4 мм, и на поверхности кожи образовались язвы.
-
Стадия 3А — меланома проникла в 1–3 ближайших лимфоузла, но они не увеличены, на меланоме нет язв, и она не распространилась дальше.
-
Стадия 3В — на меланоме образовались язвы, она проникла в 1–3 ближайших лимфоузла, но они не увеличены; или на меланоме нет язв, она проникла в 1–3 ближайших лимфоузла, и они не увеличены; или меланома распространилась на небольшой участок кожи или лимфатические протоки, но не на ближайшие лимфоузлы.
-
Стадия 3С — на меланоме образовались язвы, она проникла в 1–3 ближайших лимфоузла, они не увеличены; или меланома распространилась на 4 и более ближайших лимфоузла.
-
Стадия 4 — клетки меланомы распространились на другие органы, например, легкие, мозг или прочие участки кожи.
Лечение меланомы
Если заболевание диагностировано на начальных стадиях (0 и 1), опухоль и небольшой участок вокруг нее просто удаляются хирургическим путем. На величину отступа влияет толщина меланомы и часть тела, на которой она расположена (обычно не более 1 см).
Если площадь удаленных тканей обширная, и края раны сшить невозможно, разрез закрывают кусочком кожи, взятой с другого участка тела (например, со спины). Вероятность повторного возникновения рака после удаления опухоли на 0 и 1 стадии очень мала. Поэтому после операции не назначается какое-либо дополнительное лечение. Нужно будет до выписки несколько раз посетить врача для проведения плановых осмотров.
Если меланома диагностирована на 2 или 3 стадии, ее лечение заключается в хирургическом удалении опухоли. По окончании операции разрез ушивается или закрывается кожей, взятой с другого участка тела.
Надо сказать, что на данных стадиях меланома в большинстве случаев образует метастазы. В связи с этим прямо во время операции хирург может произвести биопсию одного или нескольких сигнальных лимфоузлов.
Если в ходе исследования обнаружились метастазы в близлежащих лимфатических узлах, хирург удаляет их все, что позволяет уменьшить риск попадания злокачественных клеток в другие органы. Такой вид операции называют полной лимфодиссекцией.
Иногда после этого хирургического вмешательства нарушается отток лимфатической жидкости от органов, расположенных в нижней части тела, что приводит к образованию лимфатических отеков (лимфодемы).
После операции по удалению опухоли необходимо регулярно посещать онколога для повторных осмотров. Врач наблюдает за процессом реабилитации. Кроме того, доктору важно не допустить появления опухоли вновь. В некоторых случаях онкологи назначают после проведенной операции адьювантную терапию, заключающуюся в приеме разнообразных лекарственных средств, уменьшающих риск возникновения рецидива рака и прогресса метастазирования.
В современной медицине не разработаны единые стандарты адьювантной терапии для лечения меланомы 2 и 3 стадии. Процесс находится на этапе клинических испытаний. Иногда достичь положительной динамики удается с помощью препаратов высокодозного интерферона. В некоторых случаях лечащие врачи предлагают своим пациентам участвовать в такого рода исследованиях.
Если у пациента выявлена меланома 4 стадии, побороть заболевание бывает затруднительно. Сложно полностью избавиться от рака в следующих случаях:
-
диагностирована последняя стадия болезни;
-
начался процесс метастазирования, опухоль распространилась в другие органы;
-
произошел рецидив рака, то есть опухоль появилась вновь.
Но даже в такой ситуации стоит надеяться на лучший исход. Ведь есть возможность замедлить процесс развития раковой опухоли, облегчить течение болезни, продлить жизнь на максимально возможный срок. Онкологи выполняют операцию по удалению вновь появившейся меланомы, проводят лучевую терапию, назначают курс медикаментозного лечения.
В последнее время медицина в сфере лечения меланомы достигла значительных успехов. Лекарственные препараты регулярно обновляются, в стационарах вводят в схему терапии новейшие формулы. Одним из передовых направлений является применение вемурафениба – препарата, действующего на генном уровне. Но он подойдет не всем, поэтому вопрос о его назначении решает лечащий врач. Нередко пациентам предлагают участвовать в клинических испытаниях.
На сегодняшний момент в сфере онкологии проводится активное изучение сигнальных ингибиторов, способных блокировать белки BRAF и МЕК. Уже разработаны лекарственные препараты, прерывающие такие сигналы. Однако большинство из этих средств используются только в клинических опытах.
Почему клиенты выбирают Клинику эстетической медицины и Салон красоты Veronika Herba:
-
Это Клиника эстетической медицины и Салон красоты, где вы сможете ухаживать за собой по умеренной стоимости, при этом вашим лицом и/или телом будет заниматься не рядовой косметолог, а один из лучших дерматологов в Москве. Это совершенно другой, более высокий уровень сервиса!
-
Получить квалифицированную помощь вы можете в любое удобное для себя время. Клиника эстетической медицины и Салон красоты работает с 9:00 до 21:00 без выходных. Главное — заранее согласовать с врачом дату и час приема.
Запишитесь на консультацию специалиста по телефону +7 (495) 085-15-13, и вы сами в этом убедитесь!
Сайт издательства «Медиа Сфера»
содержит материалы, предназначенные исключительно для работников здравоохранения. Закрывая это сообщение, Вы подтверждаете, что являетесь дипломированным медицинским работником или студентом медицинского образовательного учреждения.
Первый МГМУ им. И.М. Сеченова, Москва, 119991, Российская Федерация
Мордовцева В.В.
Государственный институт усовершенствования врачей Министерства обороны РФ
Опыт диагностики меланомы кожи диаметром менее 6 мм
Авторы:
Сергеев Ю.Ю., Мордовцева В.В.
Журнал:
Клиническая дерматология и венерология. 2018;17(4): 97‑105
Как цитировать:
Сергеев Ю.Ю., Мордовцева В.В.
Опыт диагностики меланомы кожи диаметром менее 6 мм. Клиническая дерматология и венерология.
2018;17(4):97‑105.
Sergeev IuIu, Mordovtseva VV. Experience in the diagnosis of skin melanoma smaller than 6 mm in diameter. Klinicheskaya Dermatologiya i Venerologiya. 2018;17(4):97‑105. (In Russ.).
https://doi.org/10.17116/klinderma20181704197

?>
Читать метаданные
Несмотря на новые возможности адъювантной терапии меланомы кожи, своевременная диагностика этой опухоли остается ключевым прогностическим фактором, влияющим на общую выживаемость. В статье приводится описание серии случаев меланомы кожи диаметром менее 6 мм. Клинические, дерматоскопические и гистологические проявления ранних меланом отличаются от привычных при этой злокачественной опухоли. Так, все образования лишены полихромии и окрашены только в два цвета. Такие типичные для меланомы признаки, как неправильная форма и неравномерна окраска, встречаются всего в 67 и 58% случаев соответственно. Среднее значение дерматоскопического алгоритма диагностики меланомы ABCD составило 4,2 балла, 7-балльного алгоритма Argenziano — 2,2 балла. Чувствительность указанных алгоритмов составила 16 и 50% соответственно. Отличительными особенностями гистологической картины стали слабовыраженный полиморфизм ядер, отсутствие особенностей роста, характерных для наиболее часто встречающихся форм меланомы, незначительный педжетоидный рост и отсутствие/низкий митотический индекс. Ранняя диагностика рака кожи в настоящее время невозможна без комплексной оценки новообразования кожи, учитывающей клиническую картину, данные дерматоскопического осмотра и результаты гистологического исследования, а потому требует междисциплинарного подхода.
Авторы:
Сергеев Ю.Ю.
Первый МГМУ им. И.М. Сеченова, Москва, 119991, Российская Федерация
Мордовцева В.В.
Государственный институт усовершенствования врачей Министерства обороны РФ
Размер меланоцитарного образования является одним из традиционных дифференциально-диагностических критериев, используемых в диагностике меланомы кожи. Согласно клиническому правилу ABCD и мнемоническому правилу ФИГАРО диаметр образования более 6 мм является основанием для подозрения меланомы. Анализ пигментных образований при помощи указанных алгоритмов может привести к осмотру только крупных образований в процессе скрининга и сформировать у врача ложное представление о начальных проявлениях этой злокачественной опухоли. В то же время изменение порогового значения в 6 мм может обусловить ухудшение клинической диагностики меланомы. Так, при уменьшении порогового значения даже на 1 мм снизится специфичность клинического правила ABCD на 16%, а при увеличении на 1 мм — чувствительность метода уменьшится на 12% [1].
Под нашим наблюдением за период 2015—2017 гг. находились 12 пациентов, которым по результатам клинико-дерматоскопического осмотра был предварительно поставлен диагноз меланомы кожи, несмотря на маленький размер образований — не более 6 мм. Клинические и дерматоскопические характеристики опухолей приведены в табл. 1 и 2.
Гистологическая картина образований не была однотипной (рис. 8).
В литературе встречаются единичные публикации, посвященные ранним проявлениям меланомы. A. Bono и соавт. [2] описали опыт диагностики 206 меланоцитарных образований диаметром не более 3 мм, 23 из которых оказались меланомой. По результатам гистологического исследования 21 опухоль была представлена поверхностно-распространяющейся формой меланомы, 2 — узловой. Только 4 образования были меланомой in situ. Авторы подчеркивают роль дерматоскопического осмотра в диагностике мелких пигментных образований — показатель чувствительности повышается на 40% по сравнению с клинической диагностикой. Также A. Bono и соавт. [3] описали 11 случаев узловой меланомы кожи диаметром менее 6 мм. Клинически пять опухолей имели симметричные очертания, три были однотонно окрашены. Из 8 образований, осмотренных также при помощи дерматоскопа, меланома была заподозрена в 6 случаях.
V. de Giorgi и соавт. [4] описали клинико-дерматоскопические характеристики 103 меланоцитарных образований диаметром менее 6 мм, из которых 34 оказались меланомой. 17 образований соответствовали хотя бы двум диагностическим критериям клинического правила ABCD и только пять — трем. Типичные дерматоскопические признаки меланомы, за исключением атипичных точек, встречались в мелких меланомах достоверно чаще по сравнению с меланоцитарными невусами. Наиболее часто определяемыми признаками мелких меланом по результатам исследования оказались атипичная пигментная сеть, атипичные глобулы, атипичные полосы и зоны регрессии. Перечисленные структуры, по мнению авторов, позволяют клиницисту заподозрить меланому, несмотря на размер образования. По результатам гистологического исследования все опухоли были представлены поверхностно-распространяющейся формой меланомы, из которых 18 были in situ.
S. Seidenari и соавт. [5] описали клинико-дерматоскопические проявления 482 меланом, из которых выделили группу 22 «микромеланом» — образований, диаметром не более 4 мм. Эта группа опухолей достоверно чаще встречалась на коже нижних конечностей и у более молодых пациентов по сравнению с выборкой меланом, включенной в исследование. Клинически 12 образований привлекли внимание врача за счет неоднородной или темной окраски, остальные 9 «микромеланом» выглядели банально. Наиболее частыми дерматоскопическими признаками «микромеланом» оказались атипичная пигментная сеть, атипичные точки и глобулы и эксцентричные зоны гиперпигментации. Однако авторы обратили внимание на более редкое наличие асимметрии и полихромии. Также значения дерматоскопического правила ABCD и 7-балльного алгоритма Argenziano были несколько ниже по сравнению со всей выборкой меланом, включенной в исследование. По результатам гистологического исследования, 12 образований были меланомой in situ.
N. Emiroglu и соавт. [6] описали дерматоскопическую картину 71 меланомы, из которых 29 имели диаметр менее 6 мм. Такие типичные признаки меланомы как бело-голубая вуаль, зоны регрессии, розовая вуаль и мультикомпонентная модель встречались в мелких образованиях достоверно реже. По результатам гистологического исследования, 24 опухоли были представлены поверхностно-распространяющейся формой меланомы, по две — лентиго-меланомой и узловой формой и одна — десмопластической. Восемь образований из 29 были меланомой in situ.
G. Salerni и соавт. [7] описали 8 случаев меланомы кожи диаметром от 2,5 до 4,5 мм. Клинически только две опухоли имели неровные края, а три были асимметричны и имели полихромную окраску. Дерматоскопическая картина семи образований была представлена атипичной пигментной сетью и только в пяти случаях структуры и окраска были асимметричны. В четырех случаях показанием для удаления послужили задокументированные изменения наблюдаемых образований. По результатам гистологического исследования, все опухоли были представлены поверхностно-распространяющейся формой меланомы, а шесть образований были in situ [7]. В зарубежной литературе [8—10] встречаются описания единичных случаев меланомы кожи диаметром не более 2 мм.
Отечественные авторы описывали случаи меланомы кожи диаметром менее 6 мм. А.М. Ахматова и соавт. [11] наблюдали пациентку 20 лет с инвазивной поверхностно-распространяющейся формой меланомы кожи плеча диаметром 4 мм. Значения дерматоскопических алгоритмов диагностики меланомы были высокими — результат правила ABCD составил 6,1 балла, 7-балльного алгоритма Argenziano — 5 баллов. Нами описан случай инвазивной поверхностно-распространяющейся формы меланомы кожи спины диаметром 5 мм у пациента 29 лет. Опухоль характеризовалась типичной для меланомы мультикомпонентной моделью строения и была представлена зонами регрессии и эксцентричной зоной гиперпигментации [12].
Анализ данных литературы свидетельствует о том, что любая форма меланомы начинается с небольшого образования, причем маленький размер опухоли не гарантирует отсутствия метастатического процесса. Внешние проявления мелких меланом могут быть неспецифичны и имитировать обычные меланоцитарные невусы. Совершенствование диагностики меланомы кожи, в особенности ранних форм, является таким же важным направлением развития помощи больным меланомой, как и разработка новых лекарственных препаратов.
Учитывая возможные неспецифические клинические и иногда дерматоскопические признаки, а также не ярко выраженную гистологическую картину начинающихся меланом необходимо тщательнее подходить к вопросам скрининга рака кожи. К сожалению, определенных клинических критериев для выбора образований, требующих дерматоскопического осмотра, не существует. Ориентируясь только на внешние проявления пигментированных новообразований кожи, собственный опыт в дерматоонкологии или анамнестические данные (недавнее появление, изменение «родинки») врач выявляет только 62% подозрительных меланоцитарных образований [13]. Анализ «подозрительного» для врача пигментного образования в отрыве от всех остальных образований пациента является грубой ошибкой. Так, использование сравнительного подхода в оценке множественных меланоцитарных невусов позволяет сократить количество удалений доброкачественных образований на 41% [14]. Врач, проводящий дерматоскопический осмотр, должен четко знать типичные модели строения меланоцитарных невусов (ретикулярная, глобулярная, гомогенная и т. д.), структурные особенности образований в зависимости от расположения на коже, возраста пациента, типа его кожи, и учитывать возможные физиологические состояния (беременность) или внешние воздействия (недавняя инсоляция) [15]. При множественных клинически и дерматоскопически атипичных меланоцитарных образований показано тщательное динамическое наблюдение за пациентом с фотодокументированием дерматоскопических проявлений всех атипичных образований. Наиболее значимыми изменениями со стороны меланоцитарных образований, выявляемыми при дерматоскопии, являются очаговые изменения окраски или структур образования (рис. 7, 
Гистологическая диагностика начальной стадии меланомы, в первую очередь меланомы in situ, очень сложна. Особенно это верно в отношении опухолей небольшого диаметра. Длительное время размер опухоли, превышающий 6 мм (позже 4—5 мм), считали также и гистологическим критерием диагностики меланомы. M. Tan и A. Ackerman [19] были первыми и, возможно, единственными среди дерматопатоморфологов своего времени, кто выступил с критикой этого подхода, говоря о том, что размер образования не имеет значения, ведь «все меланомы были когда-то меньше». Они же провели тщательный анализ того, как менялись критерии диагностики меланомы в опубликованных англоязычных статьях и руководствах за период с 1947 по 2000 г. Рекомендуемые в разные годы критерии отражали представления авторов, нередко ошибочные в соответствии со временем публикации, о природе меланомы и характере ее роста. В основном рекомендации носили описательный характер, иногда довольно расплывчатый, редко — противоречивый. Сам A. Ackerman [20] более 20 лет разрабатывал и совершенствовал гистологические критерии меланомы, подчеркивая важность точных формулировок, не оставляющих места для разночтений и двусмысленности. Вместе с соавторами он предложил 15 диагностических критериев меланомы, описывающих структурную организацию опухоли и три цитологических критерия. При этом 10 из 15 критериев «архитектуры» опухоли относятся только к эпидермальным структурам и эпителию придатков кожи. Другими словами, эти 10 критериев являются диагностическими критериями меланомы in situ. Следует отметить, что A. Ackerman не признавал образных сравнений и «домысливания» событий, происходящих в опухоли, которые невозможно увидеть и оценить в фиксированном срезе при микроскопическом исследовании. К сожалению, даже такие ценнейшие публикации не всегда доходят до того читателя, которому они крайне необходимы. В патоморфологии постоянное самообразование так же необходимо, как опыт и базовая квалификация. Неудивительно, что ранняя гистологическая диагностика меланомы сегодня, как и раньше, считается областью экспертной оценки в патоморфологии меланоцитарных новообразований кожи.
В свете экспертной оценки представляют интерес результаты исследования, проведенного недавно в США [21]. 1187 патоморфологам из 10 американских штатов было предложено поставить диагноз по 8976 гистологическим препаратам различных меланоцитарных новообразований кожи. Как видно из табл. 3, диагнозы
Необходимо также отметить важность предоставления патоморфологу исчерпывающей клинической информации с акцентом на данные дерматоскопии. Наш опыт свидетельствует, что подозрение на меланому при дерматоскопическом исследовании не следует игнорировать.
Таким образом, диагностический процесс в медицине и в XXI веке остается достаточно субъективным и строго зависящим от опыта врача. В руках специалистов в настоящее время появился дополнительный метод исследования кожи, позволивший иначе взглянуть на клиническую диагностику пигментных новообразований кожи. На наш взгляд, диагноз меланомы кожи, особенно ранних форм, должен базироваться не столько на гистологическом исследовании, сколько на сопоставлении данных клинического осмотра, дерматоскопической картины и гистологического исследования. Такой подход позволит улучшить современные представления о развитии меланомы.
Сведения об авторах
Ю.Ю. Сергеев — http://doi.org/0000-0002-4193-1579
В.В. Мордовцева — https://di.org/0000-0002-6396-2720
Yu.Yu. Sergeev — https://di.org/0000-0002-4193-1579
V.V. Mordovtseva — https://di.org/0000-0002-6396-2720
Меланома или меланобластома – злокачественное новообразование (рак кожи), развивающееся из меланоцитов. Что это, и какие функции выполняет?
Меланоциты – специализированные клетки, которые вырабатывают меланин, определяющий цвет кожи человека, и его способность к загару. Так же меланоциты выполняют защитную функцию, препятствуя пагубному влиянию ультрафиолетового излучения.
Меланома кожи считается самым агрессивным видом рака. Опухолевый процесс развивается очень стремительно. Ошибочно считать, что меланома появляется только из родинок.

Процента развития данного вида рака из родинок составляет всего 30%, остальное приходиться на чистые участки кожи. Меланома может образоваться даже под ногтями.
Несмотря на то, что по большей части меланома развивается именно на кожных покровах, она может возникать в прямой кишке, влагалище, различных структурах глаза, ротовой полости.
Причины возникновения меланомы
Существует множество теорий возникновения раковых состояний. Наука до сих пор не определилась с причинами развития опухолевого процесса, однако в отношении каждого вида опухолей существует предпосылки и факторы риска. Для меланомы это:
- систематическое длительное попадание ультрафиолетового излучения на кожные покровы (солнечный свет, искусственный свет в соляриях);
- хронические ожоги;
- регулярная повторяющаяся механическая травма родинок, пигментных пятен, невусов;
- ионизирующая радиация;
- хроническое электромагнитное излучение;
- предрасположенность кожных покровов – низкая пигментация (белая кожа, обильное количество веснушек);
- наследственность (риск заболевания увеличивается, если в семье кто-то перенёс данный вид рака кожи);
- иммунодефицитные состояния;
- расстройства гормонального фона (повышенный уровень половых и меланоцитстимулирующих гормонов);
- поздняя беременность (после 30);
- использование оральных контрацептивов.
Симптомы меланомы

Рак кожи чаще всего возникает на нижних конечностях или спине, однако локализация может быть самой разнообразной. Как было сказано, возникнуть может на месте родинки, в местах травмы кожного покрова или на обычной не травмированной чистой коже (см. фото выше).
Злокачественное новообразование меняет меланоцит, однако он продолжает продуцировать пигмент меланин, поэтому новообразование приобретает чёрный, коричневый цвет.
Встречаются так же бесцветные меланомы.
Одним из симптомов меланомы является чёрный ободок по краю опухоли на коже.
Характерным признаком меланомы считается асимметричность образования и его большой размер. Поначалу изменение кожи часто не воспринимается человеком за рак.
На первых порах меланома похожа на родинку, однако необычного внешнего вида.
Симптомы при меланобластоме делят на раннюю и позднюю:
- Ранние (первые) признаки заболевания:
- возвышение ранее плоских родинок;
- зуд, жжение, кровоточивость, изъязвление;
- изменение плотности (ранее твёрдая родинка становится мягкой);
- гиперемия и отёк прилегающих тканей;
- рост первичного очага новообразования;
- новые участки пигментации вокруг первичного очага новообразования;
- формирование корочки;
- изменение цвета ногтевой пластинки на руках и ногах;
- потемнение кожи, не связанное с длительным нахождением на солнце;
- Меланому от невуса (доброкачественная опухоль кожных покровов) можно отличить по следующим признакам:
- невус является плоским образованием на кожных покровах;
- невус имеет симметричную форму и плавные ровные очертания;
- невус не имеет свойства увеличиваться в размере.
- Поздними симптомами меланомы являются:
- кровотечение из образования и других пигментированных участках кожных покровов;
- болевой синдром, возникающий на пораженной коже;
- нарушение целостности кожи.
Стадии развития меланомы

Стадию развития меланомы врач определяет согласно толщине новообразования:
- Нулевая стадия – «рак на месте» – при данной стадии меланома не проросла ещё в толщину эпидермиса;
- Начальная стадия – размер опухоли менее одного миллиметра с повреждением кожи или до двух миллиметров без повреждения (см. как выглядит на фото ниже);
- Вторая стадия – толщина образования до двух миллиметров с повреждённой поверхностью кожи или больше двух миллиметров без повреждения;
- Третья стадия – наличие метастаза в один из регионарных лимфоузел (лимфатические сосуды);
- Четвёртая стадия – рост опухоли и прорастание подлежащие ткани, наличие метастазов по всему организму.
Поражение метастазами меланомы происходить наиболее часто на коже, в подкожных тканях, печени, головном мозге и костях (позвоночник, рёбра, черепные и тазовые кости).
Классификация
- Поверхностно-распространяющаяся меланома. Обычно данный тип меланомы развивается на родинке или неповреждённом участке кожи.

- Узловая меланома является более злокачественным типом заболевания.

- Лентигинозная меланома (веснушка Хатчинсона) развивается чаще на лице, ушах, шеи, кистях. Считается наиболее благоприятной формой данной патологии (медленный рост в сочетании с низким риском метастазирования);

- Акрально-лентигинозная меланома характеризуется быстрым развитием и ростом, часто дает метастазы. Преимущественно диагностируется у людей с тёмной кожей;

- Беспигментный рак кожи встречается достаточно редко.

Как осуществляется диагностика

В первую очередь врач-специалист осматривает пораженный участок кожи.
Тщательный визуальный осмотр осуществляется с помощью специального устройства – дерматоскопа.
Что это?
Это аппарат инструментального исследования, позволяющий осуществить обследование кожного новообразования без хирургического вмешательства.

Дерматоскоп позволяет увидеть признаки злокачественного течения образования, которые не видны невооружённым взглядом. Научный прогресс поспособствовал созданию цифрового дерматоскопа, благодаря которому можно увидеть трёхмерное изображение патологии на экране.
В обязательном порядке больной с подозрением на рак кожи сдает кровь для обнаружения онкомаркеров. Онкомаркерами называют специфические вещества, которые выделяет злокачественное образование.
Биопсия является обязательным диагностическим методом при подозрении на раковую принадлежность патологии.
Материал проходит гистологическое и морфологическое исследование, которое позволяет определить степень злокачественности опухоли, стадию и клиническую форму меланомы.
Дополнительными методами исследования являются:
- компьютерная томография;
- сцинтиграфия;
- УЗИ регионарного лимфоузла и внутренних органов.
Данные методы используются для обнаружения метастазов опухоли.
Лечение меланомы
На ранних стадиях заболевания осуществляется хирургическое лечение, которое является наиболее эффективным. Возможно применение медикаментозной терапии. На поздних этапах развития меланобластомы используют лучевые методы лечения.
Медикаментозная терапия меланомы

При меланоме кожи применяется три схемы медикаментозного лечения:
- перед оперативным иссечением опухоли для уменьшения размера меланомы и дефекта, что останется после (не адъювантная терапия);
- основная терапия, когда хирургическое вмешательство не представляется возможным;
- после оперативного удаления новообразования с целью профилактики рецидивов (адъювантная терапия).
Медикаментозное лечение меланомы представляет собой иммунотерапию, радиотерапию и химиотерапию.
Иммунотерапия меланомы проводиться с помощью биологических препаратов, созданных в лабораторных условиях, однако схожих с белками иммунитета человеческого организма.
Применяемые лекарственные средства:
- Интерферон-альфа используется при адъювантной терапии, предупреждая рецидивы иссеченной опухоли;
- Интерлейкин-2 применяется для профилактики метастазирования;
- Пегинтерферон-альфа-2b оказывает эффективную противорецидивную профилактику;
- Ипилимумаб – препарат, созданный на основе моноклональных антител; специфически воздействует на организм, повышая иммунный ответ на злокачественные процессы;
Химиотерапия и радиотерапия
При химиотерапии меланомы препараты разносятся по кровеносным сосудам, проникают во все органы, ткани и оказывают системное действие.
Данный вид терапии при меланоме не достаточно эффективный, более того происходит разрушение здоровых клеток организма, что делает химиотерапевтические препараты нежелательными к применению.
Химиотерапия проводиться в комплексе с иммунотерапией, дабы снизить возможность развития побочных явлений.
Препараты использующиеся при данном виде терапии: Дакарбазин, Паклитаксел, Карбоплатин.
Химиотерапия вызывает ряд побочный эффектов:
- облысение;
- анемия;
- слабость, потеря аппетита;
- повышенная кровоточивость;
- тошнота, рвота, понос.
Радиотерапия представляет собой метод лечения с помощью сильного излучения, которое летально воздействует повреждённые опухолью клетки. Метод не применяется при первичной меланоме.
Радиотерапия назначается после лимфодиссекции, как способ профилактика рецидива.
Сопровождается данный вид терапии побочными явлениями (выпадение волос, тошнота, рвота, кожные проявления), однако все нежелательные эффекты от радиотерапии проходят по окончанию лечения.
Хирургическое лечение
Оперативное вмешательство с последующим удалением опухоли является основным методом лечения меланомы, особенно на начальной стадии заболевания.
Существуют следующие хирургические способы удаления опухоли:
- Простое иссечение – подходит данный метод для плоских меланом и предполагает малоинвазивное вмешательство. Вместе с повреждёнными участками удаляются и здоровые ткани вокруг для профилактики рецидива;
- Широкое иссечение тканей – производиться после биопсии, результаты которой показали наличие опухолевого процесса;
- Ампутация – применяется, если меланома локализовалась на пальце;
- Лимфодиссекция – удаления лимфоузлов, расположенные в непосредственной близости от опухоли.
- Операция при метастазирующей меланоме – не позволяет излечить пациента от опухоли, однако улучшает качество его жизни, посредство удаление симптоматики, которую дает метастаз в каком-либо органе.
Вспомогательные методы лечения
При меланоме обязательно показана диета, которая предполагает правильное питание для снижения эффектов от химиотерапии.
При меланоме необходимо следовать таким правилам:
- Уменьшить количество потребления жиров и сделать упор на белки и углеводы;
- Готовить пищу необходимо исключительно на пару или в духовке;
- Категорически запрещено больному с меланомой садиться на различные диеты для похудения;
- Необходимо есть через каждые два-три часа небольшими порциями;
- Исключить из употребления алкогольные напитки;
- Увеличить количество продуктов в рационе, в состав которых входят витамины Е и А и фолиевая кислота;
- Увеличить употребление продуктов с антиоксидантами (брокколи, морковь, тыква).
Запрещено употреблять в пищу:
- Свинину и говядину;
- Сливочное масло;
- Фаст-фуд;
- Выпечку;
- Мороженное;
- Шоколад;
- Семечки;
- Кедровые орешки.
Благотворно на состояние пациента с меланомой повлияют такие продукты:
- Зелёный чай;
- Рыба;
- Овощи как сырые, так и варенные (особенно тыква, редька, помидоры);
- Фрукты или свежевыжатые соки;
- Мясо птицы;
- Морепродукты.
Профилактика
Людям, которые предрасположены к развитию меланомы, необходимо соблюдать некоторые правила, которые уменьшат риск заболевания:
- Снижение продолжительности пребывания на солнце является основной профилактикой от меланомы;
- Необходимо защищать открытые участки кожи от попадания прямых лучей солнца (надевать кофты с рукавом, шляпы или кепки и штаны);
- Рекомендуется использование солнцезащитного крема;
- Знания об первых признаках и симптомах меланомы необходимы, чтобы в случае выявления одного из них немедленно обратиться к врачу и начать лечение;
- Необходимо осматривать кожные покровы на наличие новых образований или изменения старых, чтобы не пропустить трансформацию родинки в меланому;
Сколько проживет больной после установления диагноза?
Прогноз при данном раковом заболевании зависит от нескольких факторов, одним из которых есть метастазирование опухоли.
Если меланома дала метастазы, то срок жизни больного зависит от количества пораженных органов:
- один – семь месяцев;
- два – до четырёх месяцев;
- более двух органов – менее двух месяцев.
Одним из факторов, влияющих на продолжительность жизни пациента, является локализация опухолевого процесса. Прогноз более благоприятный при расположении меланомы на предплечье и голени, менее – волосяной части головы, кисти, стопы и слизистых оболочек.
Меланома очень часто рецидивирует. Учёные установили, что злокачественный процесс способен запуститься вновь даже спустя десять лет после полного излечения.
Однако при обнаружении меланомы первой стадии, при своевременном удалении данного образования прогноз более чем благоприятный (97% процентов пациентов выживают).
Какие рекомендации после лечения меланомы?
Для больных, которые смогли пережить рак кожи, существует перечень обязательных правил, которые необходимо выполнять, чтобы избежать или своевременно выявить рецидивирование заболевания.
В первую очередь каждый месяц больной должен самостоятельно или с помощью родственников осматривать свои кожные покровы на наличие подозрительный образований и первых тревожных симптомах рецидива.
Пациент должен соблюдать график посещения специалиста для консультации и обследований (по показаниям).
Больным с вылеченной первой стадией заболевания рекомендуется посещать врача один раз в три месяца последующие несколько лет. Со второй, третьей и четвёртой стадией – раз в месяцах на протяжении четырёх лет.
Так же очень важно избегать солнечного света, прекратить посещение соляриев, если пациент пользовался данными услугами до болезни.
Такие больные должны качественно изменить свой образ жизни. Приветствуются занятия спортом, должная продолжительность сна, правильное и сбалансированное питание. Отказ от вредных привычек (употребление алкоголя, никотина) является важным мероприятием в профилактике рецидива.
Занятия спортом не подразумевают сильные физические нагрузки. Это могут быть пешие прогулки, аэробика, фитнес.
Данное заболевание является сильнейшим стрессом для психики. И даже если болезнь удалось победить неприятные воспоминания всё равно могут будоражить разум такого человека. Поэтому важно применять методы профилактики стресса (медитация, релаксация). Рекомендуются походы к психотерапевту, если пациент не может самостоятельно справится с негативным эмоциональным фоном от заболевания.
Так же важно участие семьи и близких людей в реабилитации после лечения меланомы. Регулярное общение, поддержка, совместное времяпрепровождение только благотворно скажутся на психологическом состоянии больного.