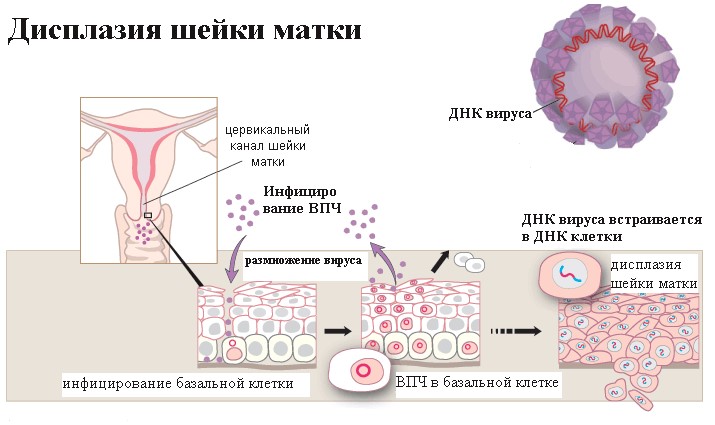
ЛЕКЦИИ ф
Новости клинической цитологии Russian News of Clinical Cytology
2020, т.24, №1, с. 17-22 2020, vol.24, no 1, pp.17-22
https://doi.org/10.24411/1562-4943-2020-10103
ОШИБКИ ЦИТОЛОГИЧЕСКОМ ДИАГНОСТИКИ ЗАБОЛЕВАНИИ ШЕЙКИ МАТКИ
Н.Н. Волченко, О.В. Борисова
МНИОИ им. ПА. Герцена — филиал ФГБУ «НМИЦ радиологии» Минздрава России, Москва, Россия.
Резюме: в данной статье авторы анализируют наиболее распространенные ошибки интерпретации цитологической картины мазков с шейки матки, приводящие к гипо- и гипердиагностике. Отражены диагностические проблемы, приводящие к ошибочным цитологическим заключениям и возможные пути их решения. Особое внимание уделено доброкачественным поражениям, которые имитируют предрак и рак шейки матки: незрелая плоскоклеточная метаплазия, герпес, микрогландулярная гиперплазия, и на-ооборот, поражения, которые наиболее часто недооцениваются цитологом: дисплазия на фоне атрофии, эндоцервикальная аденокарцинома, рак на фоне постлучевых изменений.
Ключевые слова: шейка матки, ошибки, цитологическое исследование.
Информация об авторе:
Волченко Н.Н. — док-р.мед.наук, проф., заведующая отделом онкоморфологии МНИОИ имени П.А. Герцена филиала ФГБУ «Национальный медицинский центр радиологии» МЗ РФ,
https://orcid.org/0000-0003-0421-4172 Борисова О. В. — канд.мед.наук., с.н.с. отделения онкоци-тологии МНИОИ имени П.А. Герцена филиала ФГБУ «Национальный медицинский центр радиологии» МЗ РФ, https://orcid.org/0000-0001 -5160-3168
Автор, ответственный за переписку: Борисова Олеся Владимировна — канд.мед.наук., с.н.с. отделения онкоцитологии МНИОИ им. П.А. Герцена e-mail: borisova07@bk.ru
Как цитировать:
Волченко Н.Н., Борисова О. В. Ошибки цитологической диагностики заболеваний шейки матки. Новости клинической цитологии России. 2020;24(1 ):17-22. https:// doi.org/10.24411 /1562-4943-2020-10103
К ошибкам цитологической диагностики относят расхождения цитологических и гистологических данных об опухолевой или неопухолевой природе поражения, злокачественности или до-
брокачественности процесса, ошибки в определении гистологической формы опухоли. Критерием достоверности цитологических заключений служат данные гистологического исследования операционного или биопсийного материала, а также ближайшие и отдаленные результаты лечения больных.
Анализ цитологических ошибок в зависимости от причин их вызывающих показал, что ошибки могут быть систематизированы по трем основным группам: объективные, субъективные и технические. Объективные ошибки обусловены особенностями строения опухоли, отсутствием четких признаков злокачественности и гистогенетической принадлежности опухоли, степени дифференци-ровки, четких дифференциально-диагностических критериев. Субъективные ошибки вызваны недостаточной профессиональной подготовкой, отсутствием клинических данных, неправильной трактовкой врачом-клиницистом морфологических заключений, неиспользование или неправильное использование современных методов уточняющей диагностики, а также проведение исследования на неадекватном материале. Ошибки по техническим причинам обуславливаются нарушением процессов получения и обработки материала. Все эти факторы могут привести к гипо- и гипердиагностике опухолевого процесса [1].
Неадекватное взятие материала с шейки матки для цитологического исследования является причиной 2/3 ложнонегативных результатов (аномальный эпителий не попадает в препарат). Наша статья посвящена ошибкам интерпретации цитологической картины, которые обусловлены неправильной оценкой цитологом имеющихся морфологических изменений, и хотя составляют они 1/3 от всех ошибок, их анализ наиболее важен для цитолога.
Большое значение на морфологическую трактовку влияет правильно оформленное направление с указанием возраста, фазы менструального цикла, анамнеза, клинических данных, данных визуального осмотра шейки матки, позволяющее цитологу сопоставить клинические данные с морфологическими.
Залогом адекватной оценки является получение информативного материала. Необходимо внимательно и не торопясь просматривать весь препарат, так как единичные патологические комплексы могут быть пропущены цитологом.
Цель данного исследования — улучшить цитологическую диагностику заболеваний шейки матки путем анализа, наиболее часто встречающихся цитологических ошибок.
Реактивные изменения плоского эпителия
Реактивные изменения плоского эпителия представляют наибольшие трудности при дифференциальной диагностики с дисплазией и раком и развиваются как реакция на какой-то патологический процесс — воспаление, наличие инфекции, гормональные процессы, после различных инструментальных манипуляций на шейки матки.
Наиболее частые диагностические ошибки между CIN и неопухолевыми морфологическими изменениями шейки матки:
незрелая плоскоклеточная метаплазия (реактивная атипия, репаративные изменения); атрофия плоского эпителия; герпетическая инфекция.
Незрелая плоскоклеточная метаплазия
Незрелая плоскоклеточная метаплазия, реактивная атипия и репаративные процессы — это морфологически сходные изменения клеток, связанные с регенеративными изменениями при эктопии, когда происходит пролиферация и диффе-ренцировка резервных клеток в плоский эпителий, заменяющий эктопированный эндоцервикальный железистый эпителий. Этот процесс незрелой плоскоклеточной метаплазии может сопровождаться выраженными реактивными изменениями вплоть до атипии в виде укрупнения и гиперхромии ядер, появления крупных нуклеол, нарушения полярности клеточного пласта, что можно ошибочно принять за CIN3 [2] (таблица 1) (вклейка 8, рис.1,2).
Все морфологические цитологические критерии дифференциальной диагностики между незрелой плоскоклеточной метаплазией и CIN3 достаточно относительны, и цитологически однозначно решить вопрос о характере процесса крайне сложно. Достаточно часто имеет место дисплазия мета-
плазированного эпителия, так как ВПЧ для внедрения и репликации использует чаще всего процессы метаплазии (зону трансформации), которую сложно дифференцировать также с незрелой плоскоклеточной метаплазией (вклейка 8, рис. 3). Кроме того, выделяют папиллярную незрелую метаплазию, чаще связанную с ВПЧ низкого риска (типы 6, 11 или 42), реже с ВПЧ высокого риска (16, 16/18 и 33 типы) и, возможна, смешанная ВПЧ инфекция (6/16 и 11/58 типов). Гистологически папиллярная незрелая метаплазия образует либо папиллярные структуры, либо слегка приподнятую плоскую бляшку. Койлоцитоз выявляется в более половине случаев. Папиллярная незрелая метаплазия представляет собой отдельную подгруппу LSIL, демонстрирующую продуктивную ВПЧ-инфекцию. Во всех этих случаях в настоящее время рекомендовано применять ИЦХ исследование с белком р16(ШК4а) (возможно, совместно с белком Ki67 (набор CINtek plus)), который является суррогатным биомаркером HSIL (CIN 2-3). Иммуноморфо-логическое исследование с белком p16(INK4a) является вспомогательным методом позволяющим дифференцировать атипическую реактивную незрелую плоскоклеточную метаплазию от CIN и папиллярной незрелой плоскоклеточной метаплазии, связанной с ВПЧ высокого канцерогенного риска [3,4] (вклейка 8, рис. 4).
Атрофия плоского эпителия
Около 30% случаев рака шейки матки (РШМ) встречаются у женщин старше 60 лет, а уровень смертности составляет около 70% в этой возрастной группе из-за поздней диагностики. Тестирование на ВПЧ показывает более высокую чувствительность и специфичность при выявлении CIN у пожилых женщин, тогда как при цитологическом исследовании чрезвычайно низкая чувствительность (около13-30%). Это, в первую очередь, связано с тем, что у женщин в постменопаузе из-за гормональных изменений зона трансформации, где развиваются предраковые поражения, находится высоко в цервикальном канале и поэтому недоступна для надлежащего обследования и получения адекватного материала для цитологического исследования [5]. Но так же, по нашим данным, имеет место гиподиагностика CIN3 плоского эпителия на фоне атрофии.
Таблица 1
Дифференциальная диагностика незрелой плоскоклеточной метаплазии и CIN3
Незрелая плоскоклеточная метаплазия ^N3 плоского эпителия
Клетки парабазального типа с повышенным ядерно-ци-топлазматическим соотношением Клетки парабазального типа с резко нарушенным ядерно-цитоплазматическим соотношением
Гиперхромия ядер выражена слабо или умеренно Резко выражена гиперхромия ядер
Полиморфизм ядер отсутствует или умеренно выражен Выражен полиморфизм и атипия ядер
Митозы редкие в базальных слоях эпителия, отсутствуют патологические митозы Митозы на разных уровнях эпителиального пласта, патологические митозы
Сохраняется полярность клеток Потеря полярности клеток
Таблица 2
Дифференциальная диагностика атрофии плоского эпителия и ^N3 на фоне атрофии
Атрофия плоского эпителия ОК3 плоского эпителия на фоне атрофии
Более или менее однородная цитологическая картина из клеток глубоких слоев плоского эпителия, расположенных в скоплениях и разрозненно Появление на фоне однородной цитологической картины атрофии плотных скоплений из гиперхромных клеток
Возможно наличие «голых ядер» клеток, иногда гигантских с признаками атипии, но без гиперхромии Наличие отдельно лежащих не гиперхромных «голых ядер» не характерно
Скопления из клеток недостаточно плотные Плотные скопления, ядра наползают друг на друга
Сохраняется относительная полярность ядер в скоплениях Ядра в скоплениях неорганизованы, расположенны в различных направлениях
Клетки среднего размера, гиперхромия в клетках не-выражена, контур ядер ровный Клетки могут быть различного размера от мелких до крупных, гиперхромные, контур ядер может быть неровный
Хроматин однородный, ядрышки могут быть при реактивных изменениях Хроматин тяжистый, неоднородный, грубый; полиморфизм ядер от слабого до выраженного; могут быть ядрышки
Клетки чаще округлой формы Клетки могут быть округлой формы, на отдельных участках вытянутой формы
Атрофия плоского эпителия — это чаще физиологический процесс, сопровождающийся нарушением созревания клеток в эпителиальном пласте и преобладанием клеток глубоких слоев плоского эпителия. Дисплазия плоского эпителия — это патологический процесс, при котором нарушается стратификация клеточного пласта (созревание клеток) вследствие потери способности клеток к дифференцировки с одновременной атипией ядер. Часто при атрофии плоского эпителия может быть реактивная атипия, которую сложно дифференцировать с дисплазией (вклейка 9, рис. 5). С другой стороны, цитолог может пропустить дисплазию плоского эпителия на фоне атрофии. Для CIN3 на фоне атрофии характерно появление плотных комплексов из крупных или мелких клеток с ги-перхромией ядер, ядра в комплексах наползают друг на друга, характерен полиморфизм клеток и ядер, хроматин неоднородный тяжистый, нарушение структурированности клеток в скоплениях (таблица 2) (вклейка 9, рис. 6,7,8).
Диффренциальная диагностика атрофии с реактивной атипией эпителия от CIN3 на основании только морфологического исследования в некоторых случаях достаточно сложная задача, поэтому рекомендуется также иммуноморфологическое исследование с белком рЩШЕ^) или набором CINtek plus.
Герпетическая инфекция шейки матки
Генитальный герпес является относительно распространенной инфекцией, вызываемой вирусом простого герпеса 1 и 2 типов. В последнее время наблюдается рост числа инфекций, вызванных вирусом простого герпеса 1 типа. Большинство новых случаев генитального герпеса не диагностируются, так как клинические симптомы кра-тковременны или во многих случаях заболевание протекает бессимптомно. В острый период герпе-
тической инфекции (2-3 недели) на шейки матки, влагалище или вульве может быть язва, клинически имитирующая рак [6]. Если в этот период взять мазки, то цитологическую картину при незнании морфологических критериев герпетической инфекции также можно принять за рак. Наблюдается резкое увеличение размеров клеток и ядер в отдельных клетках плоского, эндоцервикально-го и метапластического эпителия, характерной чертой является наличие многоядерных клеток с большим количеством «плотно упакованных» крупных, иногда гигантских ядер с выраженными признаками гиперхромиии и полиморфизма, просматриваются крупные нуклеолы. Цитологические признаки атипии могут быть выражены резче, чем при раке (вклейка 10, рис. 9).
Предраковые поражения шейки матки
Главной целью цитологического исследования мазков шейки матки является выявление диспла-зии и рака шейки матки (РШМ). Дисплазия I и II степени диагностируются, как правило, всегда без особых проблем. Имеет место небольшая гипердиагностика ВПЧ-инфекции и легкой дисплазии вследствие реактивных или гормональных изменений клеток плоского эпителия в виде укрупнения ядер. Для избежания гипердиагностики ВПЧ-инфекции необходимо внимательно просматривать цитологические препараты с целью выявления истинных койлоцитов.
В настоящее время гинекологическая практика сталкивается с проблемами, связанными с двусмысленной интерпретацией ASC-US. С момента своего появления в 1988 году, ASC-US является проблематичным и спорным диагнозом. Заключение ASC-US может быть вызвано качеством мазка и его интерпретацией. Тестирование на ВПЧ, коль-поскопия и биопсия рекомендуется для лечения
пациентов с цитологическим заключением ASC-US (вклейка 10, рис.10). Доказано, что при цитологическом заключении ASC-US HSIL при гистологическом исследовании выявляется от 10% до 20% наблюдений, инвазивный рак — 0,1% [7,8]. Поэтому в классификацию Bethesda введена категория ASC-H (атипичные клетки плоского эпителия, не исключающие тяжелое плоскоклеточное внутри-эпителиальное поражение). При цитологическом заключении ASC-H, ASC-US или AGC(NOS) рекомендовано иммуноцитохимическое исследование с белком р16(ШК4а).
Наиболее часты ошибки определения степени дисплазии шейки матки. Более чем у 2/3 больных с CIN и микроинвазивным раком одновременно присутствуют эпителиальные повреждения разной степени в разном сочетании от CIN 1-2 до микроинвазивного рака, что отражает процесс канцерогенеза, свидетельствуя о прогрессии неопластического процесса в результате появления все новых очагов неоплазии от эпителиальных клонов с нарастающими генетическими повреждениями. В связи с этим разделение предрака шейки матки на 3 степени CIN условно и необходимо для воспроизведения диагноза, который должен устанавливаться по максимальной степени повреждений [8]. Поэтому CIN3 при цитологическом исследовании зависит от появления в цитологических препаратах даже единичных комплексов глубоких слоев плоского эпителия с признаками атипии, а не от количества и степени полиморфизма клеточных элементов.
РШМ
Плоскоклеточный РШМ хорошо диагностируется цитологически. Наибольшие проблемы возникают при высокодифферецированном плоскоклеточном раке, особенно веррукозном, когда ядра мелкие, фактически пикнотичные, без выраженных признаков полиморфизма, но необходимо обращать внимание на ороговение цитоплазмы, наличие ороговения сразу должно настораживать в отношении плоскоклеточного рака (вклейка 10, рис. 11). Цитологически можно пропустить малодифференцированный плоскоклеточный рак из мелких клеток, которые можно принять за глубокие слои плоского эпителия, особенно на фоне атрофии. Появление «грязного» фона, некроза, разрушенных клеток, относительно более выраженный полиморфизм и гиперхромия клеточных элементов, свидетельствуют в пользу инвазивного рака (вклейка 10-11, рис.12,13).
Аденокарцинома шейки матки
В развитых странах заболеваемость плоскоклеточным раком шейки матки снижается, тогда как доля аденокарцином растет, особенно среди молодых женщин, и составляет 7-17%. Диагностика аденокарциномы шейки матки, особенно ранняя, представляет серьезную проблему. Цитологическое исследование имеет ограниченные
возможности в диагностике аденокрацином шейки матки: поражения желез, часто расположены в цервикальном канале, более трудны для получения адекватного материала для цитологического исследования, предраковые поражения желез и аденокарциному эндоцервикального типа сложно обнаружить цитологически, потому что атипия может быть слабо выражена или отсутствовать (вклейка 11, рис. 14,15), также отсутствуют четкие критерии для обоснования кольпоскопическо-го подозрения на предраковое поражение желез [9]. Часто процесс расположен глубоко в криптах, а слизистая практически не изменена. Чувствительность цитологического метода в диагностики цер-викальных аденокарцином составляет около 60%, необходимо отметить, что чувствительность ВПЧ-тестирования при аденокарциномах также составляет 60-85%, так как высока доля ВПЧ-негативных аденокарцином шейки матки [10]. Цервикаль-ные аденокарциномы охватывают разнообразную группу опухолей с несколькими различными гистологическими типами, которые включают эн-доцервикальную, эндометриоидную, кишечную, аденоплоскоклеточную, виллогландулярную, пер-стневидноклеточную, серозную, мезонефральную, муцинозную и желудочного типа. Эндоцервикаль-ная аденокарцинома характеризуется наличием в глубоких слоях эндоцервикса многочисленных желез, которые существенно различаются по форме и размерам, могут быть выстланы клетками в один слой, иногда без признаков атипии. Часто опухоль прорастает глубоко в шейку матки и распространяется по криптам вверх по стенке цервикального канала, затрудняя постановку диагноза.
Дифференциальная диагностика аденокарци-ном шейки матки включает:
1. реактивные изменения при эндоцервиците;
2. трубная метаплазия;
3. эндометриоз эндоцервикса;
4. микрогландулярная гиперплазия;
5. атипия желез, обусловленная действием инфекционных агентов, радиации, лекарств и гормонов.
Наиболее часто аденокарциному шейки матки необходимо дифференцировать с микроглан-дулярной гиперплазией. Микрогландулярная гиперплазия — это поражение слизистой оболочки шейки матки характеризующееся пролиферацией цилиндрического эпителия, иногда с образованием сосочковоподобных структур, часто связанно с употреблением противозачаточных средств или беременностью (таблица 3) (вклейка 11, рис. 16).
При любом цитологическом подозрении на патологию железистого эпителия рекомендуется использовать термин AGS(NOC) по классификации Бетесда для более углубленного обследования цер-викального канала.
При низкодифференцированных раках возможна ошибка в определении гистологической формы между плоскоклеточным и железистым раком, так как теряются специфические признаки принадлежности к той ткани, из которой возникла
Таблица 4
Дифференциальная диагностика между лучевым патоморфозом и постлучевыми изменениями
Таблица 3
Дифференциальная диагностика микрогландулярной гипреплазии и эндоцервикальной аденокарциномы
Микрогландулярная гиперплазия Эндоцервикальная аденокарцинома
Многочисленные мелкие плотно упакованные железы, иногда без просвета. В просвете желез часто обнаруживаются нейтрофилы Округлые или овальные железы со слабой продукцией муцина
Железы выстланы уплощенным кубическим эпителием Эпителий напоминает цервикальный с псевдостратификацией
Цитоплазма зернистая, содержит перинуклеарные вакуоли Цитоплазма эозинофильная
Ядра однообразные нежные пузырьковидные с единичными ядрышками Ядра укрупненные, вытянутые, гиперхромные, с заметными ядрышками и апоптотическими тельцами
Митозы редкие или отсутствуют Характерны поверхностные «всплывающие» митозы
Рецидив рака на фоне постлучевых изменений Постлучевые изменения в неопухолевых клетках
Гигантские клетки с уродливыми гиперхромными ядрами Могут быть гигантские клетки с уродливыми гиперхромными ядрами
Увеличение размеров клеток и ядер Клетки и ядра могут быть крупнее, чем в раке
Гиперхромия ядер более выражена Гиперхромия ядер менее выражена
В некоторых клетках сохраняется плотный гиперх-ромный грубый хроматин, присутствуют крупные нуклеолы Характерна разряженная деконденсированная структура хроматина, фрагментация ядер, крупные нуклеолы
Цитоплазма более плотная, сохраняются признаки ороговения Цитоплазма клеток похожа на метаплазированный эпителий, как правило, обильная с дегенеративно-дистрофическими изменениями
опухоль (вклейка 12, рис. 17). Определение гистологической формы является важным, так как аденокарцинома обладает более неблагоприятным прогнозом и тактика хирургического лечения даже при небольшом очаге поражения более агрессивна (как правило, экстирпация матки с придатками, лимфаденэктомия и резекция большого сальника), при плоскоклеточном раке при небольших очагах поражения иногда возможно органосохраняющее лечение.
Цитологически в некоторых наблюдениях крайне сложно дифференцировать лечебный па-томорфоз опухолевых клеток от постлучевых изменений в неопухолевых клетках и решить вопрос о наличии или отсутствии рецидива заболевания. К основным цитоморфологическим признакам лучевых повреждений опухолевых и неопухолевых клеток относятся: гигантсткие клетки с уродливыми гиперхромными ядрами, увеличение размеров клеток и ядер, гиперхромия, могут быть выражены ядрышки, встречается фрагментация ядер, многоядерность, дистрофические изменения в виде вакуолизации, лизис и пикноз ядер, некроз, разрастание соединительной ткани, снижение митотической активности, увеличение числа патологических митозов, отложение в зоне опухоли рогового вещества, солей извести, кристаллов холестерина, скопление макрофагальных и лим-
фоидно-гистиоцитарных клеток. При постлучевых изменениях цитологическая картина может быть более «страшная», чем при рецидиве заболевания (вклейка 12, рис. 18). О резистентности опухоли к проводимой терапии или рецидиве заболевания свидетельствует появление на фоне вышеописанных изменений опухолевых клеток или скоплений из клеток с плотным гиперхромным грубым хроматином как до начала лечения (таблица 4) (вклейка 12, рис. 19,20).
Заключение
Морфологическая диагностика доброкачественных, предопухолевых и злокачественных процессов шейки матки многогранна и трудна. С целью снижения диагностических цитологических ошибок необходимо разрабатывать наиболее информативные дифференциально-диагностические морфологические критерии определенных нозологических форм с использованием современных морфологических классификаций, применением высокотехнологичных методов уточняющей диагностики, а также повышение квалификации врачей-морфологов.
Авторы заявляют об отсутствии конфликта интересов.
Литература/References
1. Чиссов В.И., Трахтенберг А.Х. Ошибки в клинической онкологии. М.: Медицина; 2001. [Chissov V.I., Trakhtenberg A.Kh. Errors in clinical oncology. M.: Medicine; 2001 (In Russ.).]
2. Sazonova Vlu., Fedorova V.E., Danilova N.V. Algorithm for the differential diagnosis of precancerous and regenerative changes in the cervix uteri. Arkh. Patol. 2013 Jan-Feb;75(1):46-51.
3. Skapa P., Robova H., Rob L., Zamecnik J. p16(INK4a) immunoprofiles of squamous lesions of the uterine cervix-implications for the reclassification of atypical immature squamous metaplasia. Pathol. Oncol. Res. 2013 0ct;19(4):707-14. https://doi.org/10.1007/s12253-013-9633-1.
4. Hong S.A., Yoo S.H., Choi J., Robboy S.J., Kim K.R. A Review and Update on Papillary Immature Metaplasia of the Uterine Cervix: A Distinct Subset of Low-Grade Squamous Intraepithelial Lesion, Proposing a Possible Cell of Origin. Arch. Pathol. Lab., Med. 2018 Aug;142(8):973-981. https://doi.org/ 10.5858/ arpa.2017-0267-OA.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
5. Hermansson R.S., Olovsson M., Hoxell E., Lindstrom A.K. HPV prevalence and HPV-related dysplasia in elderly women. PLoS One. 2018. Jan 10;13(1):e0189300. https://doi.org/10.1371/journal.pone.0189300.
6. Garland S.M., Steben M. Genital herpes. Best Pract. Res. Clin. Obstet Gynaecol. 2014 Oct;28(7):1098-110. https://doi.org/10.1016/j.bpobgyn.2014.07.015.
7. Saslow D., Solomon D., Lawson H.W., Killackey M., Kulasingam S.L., Cain J. et al. American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology screening guidelines for the prevention and
early detection of cervical cancer. CA Cancer J.Clin. 2012 May-Jun;62(3):147-72. https://doi.org/10.3322/ caac.21139.
8. Короленкова Л. И. Цервикальные интраэпители-альные неоплазии и ранние формы рака шейки матки: клинико-морфологическая концепция церви-кального канцерогенеза. Москва; 2017. [Korolenkova L. I. Cervical intraepithelial neoplasia and early forms of cervical cancer: a clinical and morphological concept of cervical carcinogenesis. Moscow; 2017. (In Russ.).]
9. Mancini S., Ravaioli A., Giuliani O., Vattiato R., Falcini F., Ferretti S., Costa S., Bucchi L. Incidence and survival trends of cervical adenocarcinoma in Italy: Cytology screening has become more effective in downstaging the disease but not in detecting its precursors. Int. J. Cancer. 2017 Jan 1;140(1):247-248. https://doi/org/10.1002/ ijc.30435.
10. Xie F., Zhang L., Zhao D., Wu X., Wei M., Zhang X., Wu X., Fang H., Xu X., Yang M., Qi D. Prior cervical cytology and high-risk HPV testing results for 311 patients with invasive cervical adenocarcinoma: a multicenter retrospective study from China’s largest independent operator of pathology laboratories. BMC Infect. Dis. 2019 Nov. 11;19(1):962. https://doi. org/10.1186/s12879-019-4614-y.
Участие авторов:
Концепция и дизайн исследования: Н.Н.В., О.В.Б. Сбор и обработка материала: Н.Н.В., О.В.Б. Написание текста: О.В.Б. Редактирование: Н.Н.В.
ERRORS IN CERVICAL CYTOLOGICAL DIAGNOSTICS
N.N. Volchenko, O.V. Borisova
PA Herzen Moscow Oncology Research Institute, Branch, National Medical Radiology Research Center, Ministry of Health of Russia, Moscow, Russia
Summary: in this article, the authors analyze the most common mistakes in the interpretation of cytological pictures of smears with the cervix, leading to hypo- and overdiagnosis. Diagnostic problems are reflected, lead to erroneous cytological conclusions and possible solutions. Particular attention is paid to benign lesions that mimic cervical precancer and cancer: immature squamous metaplasia, herpes, microglandular hyperplasia, and vice versa, a lesion that are often underestimated by a cytologist: dysplasia amid atrophy changes, endocervical adenocarcinoma, cancer amid post-radiation changes.
Key words: cervix, errors, cytological examination.
Corresponding author:
Borisova O.V. https://orcid.org/0000-0001-5160-3168- email: borisova07@bk.ru
To Cite This Article: Volchenko N.N., Borisova O.V. Errors in cervical cytological diagnostics. Russian News of Clinical Cytology 2020;24(1):17-22. https://doi.org/10.24411/1562-4943-2020-10103
The authors declare no conflict of interest.
Information about the authors:
Volchenko N.N. — https://orcid.org/0000-0003-0421-4172 Borisova O.V. — https://orcid.org/0000-0001-5160-3168
Illustrations for the article «ERRORS IN CERVICAL CYTOLOGICAL DIAGNOSTICS» Volchenko N.N., Borisova O.V., рage 17
Рис. 1. Незрелая плоскоклеточная метаплазия с реактивны- Рис. 2. Незрелая плоскоклеточная метаплазия (репаративные
ми изменениями. Окр. по Паппенгейму, х500.
Fig. 1. Immature squamous metaplasia with reactive changes.
Pappenheim stain, х500.
изменения). Окр. по Паппенгейму, х500. Fig. 2. Immature squamous metaplasia (reparative changes). Pappenheim stain, х500.
Рис. 3. CIN3 метаплазированного эпителия. Окр. по Паппенгейму, х500.
Рис. 4. Иммуноцитохимическое исследование с белком p16(INK4a). Отмечается ядерная и цитоплазматическая экс-
Fig. 3. CIN3 in metaplasized epithelium. Pappenheim stain, х500. пРессия белка р^ШЮк) при ОШ ш-та^азиротанното
эпителия. Окр. по Паппенгейму, х200.
Fig. 4. Immunocytochemistry with protein p16 (INK4a). Nuclear and cytoplasmic expression of p16 protein (INK4a) is noted in CIN3 metaplasized epithelium. Pappenheim stain, х200.
Illustrations for the article «ERRORS IN CERVICAL CYTOLOGICAL DIAGNOSTICS» Volchenko N.N., Borisova O.V., рage 17
Рис. 5. Реактивная атипия плоского эпителия на фоне атро- Рис. 6. CIN3 плоского эпителия на фоне атрофии.
фии. Окр. по Паппенгейму, х200. Окр. по Паппенгейму, х500.
Fig. 5. Reactive atypia of squamous epithelium with atrophy. Fig. 6. CIN3 of squamous epithelium with atrophy.
Pappenheim stain, х200. Pappenheim stain, х200.
Рис. 7. CIN3 плоского эпителия на фоне атрофии. Окр. по Паппенгейму, х500.
Fig. 7. CIN3 of squamous epithelium with atrophy. Pappenheim stain, х500.
Рис. 8. CIN2 плоского эпителия на фоне атрофии. Окр. по Паппенгейму, х500. Fig. 8. CIN2 of squamous epithelium with atrophy. Pappenheim stain, х500.
Illustrations for the article «ERRORS IN CERVICAL CYTOLOGICAL DIAGNOSTICS» Volchenko N.N., Borisova O.V., рage 17
Рис. 9. Многоядерные клетки с гиперхромными полиморф- Рис. 10. Атипия плоского эпителия неясного значения — ASC-
ными ядрами при герпетической инфекции. US. Окр. по Паппенгейму, х500.
Окр. по Паппенгейму, х500. Fig. 10. ASC-US of squamous epithelium. Pappenheim stain,
Fig. 9. Polynuclear cells with hyperchromic polymorphic nucleus х500. with herpetic infection. Pappenheim stain, х500.
Рис. 11. Плоскоклеточный веррукозный рак. Окр. по Паппен- Рис. 12. Малодифференцированный плоскоклеточный рак
гейму, х500. из мелких клеток. Окр. по Паппенгейм, х500. Fig. 11. Verrucous squamous cell carcinoma Pappenheim stain, Fig. 12. Low-grade squamous cell carcinoma from small cells.
х500. Pappenheim stain, х500.
Illustrations for the article «ERRORS IN CERVICAL CYTOLOGICAL DIAGNOSTICS» Volchenko N.N., Borisova O.V., рage 17
Рис. 13. Малодифференцированный плоскоклеточный рак на Рис. 14. Аденокарцинома эндоцервикального типа.
фоне атрофии. Окр. по Паппенгейму, х500.
Окр. по Паппенгейму, х500.
Fig. 13. Low-grade squamous cell carcinoma in the presence of Fig. 14- Endocervical type adenocarcinoma.
atrophy. Pappenheim stain, х500.
Pappenheim stain, х500.
Рис. 15. Аденокарцинома эндоцервикального типа. Окр. по Паппенгейму, х500.
Рис. 16. Микрогландулярная гиперплазия цилиндрического эпителия. Окр. по Паппенгейм, х500.
Fig. 15- Endocervical type adenocarcinoma. Pappenheim stain, Fig. 16. Microglandular hyperplasia of the cylindrical epithelium.
х500.
Pappenheim stain, х500.
Illustrations for the article «ERRORS IN CERVICAL CYTOLOGICAL DIAGNOSTICS» Volchenko N.N., Borisova O.V., рage 17
Рис. 17. Низкодифференцированный рак, цитологически сложно дифференцировать между плоскоклеточным и железистым. Окр. по Паппенгейму, х500.
Fig. 17. Low-grade cancer, it is cytologically difficult to differentiate between squamous and glandular type. Pappenheim stain, х500.
Рис. 19. Малодифференцированный плоскоклеточный рак на фоне постлучевых изменений. Окр. по Паппенгейму, х500. Fig. 19. Low-grade squamous cell carcinoma with postradiation changes. Pappenheim stain, х500.
Рис. 18. Постлучевые изменения клеток плоского эпителия. Окр. по Паппенгейму, х500. Fig. 18. Postradiation changes of squamous cells. Pappenheim stain, х500.
Рис. 20. Плоскоклеточный ороговевающий рак на фоне постлучевых изменений. Окр. по Паппенгейму, х500. Fig. 20. Squamous keratinizing cancer with postradiation changes. Pappenheim stain, х500.
Эрозия, ВПЧ и рак шейки матки: от мифов и слухов до правдивой информации
Часть 1. О цитологических мазках
Среди женского населения постсоветских стран за последние несколько лет распространяется истерия по поводу очередной новой, доселе неизвестной нашим женщинам инфекции, связанной с половыми органами человека. Слухи и мифы о вирусе папилломы человека (ВПЧ) достигли колоссальных масштабов. Информация об этой инфекции, которая предоставляется на многих веб-сайтах и форумах, настолько неточная, настолько ложная, что не удивительно, что наши женщины, особенно молодые, чуть с ума не сходят, когда у них находят вирус папилломы человека и пугают развитием рака. И тогда что только не используют для избавления несчастной «больной» от этой страшной инфекции! А о вакцине, которая начала применяться во многих странах для профилактики ВПЧ-инфекции и рака шейки матки, вообще столько нелепой и просто тупой информации, столько глупых, бессмысленных дебатов, что доходит до позора даже «продвинутых ученых» на фоне мировой общественности. Поэтому пора расставить многие точки над «і» в отношении этой инфекции. Итак, чем чаще всего пугают современных женщин постсоветских государств врачи? Эрозиями, которые чуть ли не рак уже, поэтому нужно срочно лечить хирургически – прижигать, замораживать, вообще играться модными и дорогостоящими процедурами. Жаль, что наши врачи, а тем более женщины, не знают, что понятие «эрозия шейки матки» не является диагнозом, то есть такое понятие в современной гинекологии не используется уже 30-35 лет минимум.
Для многих читателей эта большая статья может показаться сложной, так как она содержит большое количество научной и медицинской терминологии. Однако, если вы решили пропустить эти статьи и почитать их в другое время (или вообще не читать), мы снова пройдемся по важным фактам об «эрозии» и всем, что с ней связано.
Истинная эрозия – это редкое явление и не требует лечения в 99% случаев. У большинства молодых женщин имеется нормальное физиологическое состояние шейки матки (ШМ) – эктопия, которая не требует никакого лечения. Также, причиной покраснения шейки матки, что врач называет весьма туманным, расплывчатым понятием «эрозии», может быть воспалительный процесс, который тоже необходимо диагностировать правильно – знать конкретно возбудителя. Чаще всего «находят» тех возбудителей, которые не имеют никакого отношения к воспалению ШМ. Так как ни знаний по гинекологии, ни логики на фоне возникшего страха (ужаса!) нет у большинства женщин, начинаются длительные хождения по врачам с длительными бессмысленными схемами диагностики и лечения, не имеющими никакого отношения к истинному состоянию дел.
Поэтому важно, чтобы вы запомнили правдивое утверждение: понятие эрозии в современной гинекологии не используется, поэтому если ставят диагноз «эрозии» нужно не в панику впадать и поспешно прижигать или морозить, а спрашивать у врача: что конкретно он подразумевает под понятием «эрозии». Конкретно! Увы, многие врачи объяснить толком не смогут, потому что учились по старым учебникам советской эпохи, где процесс возникновения эрозии описан неправильно (с точки зрения современной медицины), а жирным шрифтом выделено, что это якобы предраковое состояние и ведет к раку. Это ложь! Конечно, на фоне тотального, массового психоза продолжительностью в 30 лет по вопросам эрозии шейки матки принять новую, свежую информацию, а самое главное, противоположную тому, чем переполнены все имеющиеся источники информации на тему женского здоровья, не просто. Потому что, все так говорят. Даже «заслуженные» профессора и академики. Женщины, просыпайтесь! Хватит быть спящими красавицами. Мир ведь ушел в сторону прогресса уже довольно далеко, поэтому просыпайтесь.
Итак, «эрозии» не являются предраковым состоянием и в рак не переходят. А что переходит? Логически — предраковое состояние шейки матки. Что же в современной гинекологии подразумевают под предраковыми состояниями? Об этом мы поговорим дальше. Начнем с важной статистики по всему миру. Каждый год в мире диагностируется около 500 000 новых случаев рака шейки матки, и 240 000 женщин умирает из-за этой болезни. Данные эти приблизительные, потому что ВОЗ имеет весьма старые отчеты, за 2007 год. За последние 30 лет в развитых странах количество новых случаев рака шейки матки понизилось почти наполовину, в некоторых – на 70-90%, как и уровень смерти от рака шейки матки. Это значит, что понизилась частота возникновения рака шейки матки благодаря какой-то чудной профилактике? Нет, просто в странах Европы и Северной Америке вот уже 50 лет пользуются мазком на цитологию, который называют чаще тестом Папаниколау или PapSmear. Этот скрининговый тест позволяет определить состояние покровного эпителия шейки матки,.. если он взят правильно.
Таким образом, введение мазка на цитологию в гинекологическую практику многих стран мира позволило выявить большое количество случаев рака шейки матки, особенно на начальных его стадиях. Чем больше врачи пользовались этим тестом, тем больше случаев рака выявляли, поэтому закономерно, что в статистических отчетах появилась волна «подъема роста случаев рака шейки матки», что вызвало панику как среди женщин, так и среди врачей. Сейчас эта волна пришла к весьма низкому уровню – более-менее стабильному, но только в тех странах, где этот тест используется уже несколько десятилетий и количество женщин, не прошедших тестирование, незначительное. В развивающихся странах, наоборот, мазок на цитологию только начали вводить, а поэтому наблюдается рост заболеваемости раком шейки матки.
Если я упомянула мазки на цитологию, возникает вопрос: как должны браться эти мазки, чтобы результаты были достоверными? Во-первых, никто в медицинских институтах не учит будущих врачей, как правильно брать любые мазки, а не только на цитологическое исследование. Во-вторых, мало кто из врачей знает, как правильно интерпретировать полученные результаты. Такое негативное явление в современном образовании наблюдается во многих странах. Мазки на цитологию должны отражать клеточное состояние слизистой шейки матки и канала шейки матки – ничего более, хотя могут быть вспомогательным фактором в постановке других диагнозов (трихомониаз, например), если их «чтение» проводится толковым, опытным врачом-лаборантом. Другими словами, вы должны понять, что все результаты соприкасаются с субъективизмом медперсонала, то есть человеческим фактором: насколько правильно взяты мазки, насколько правильно обработаны, насколько правильно просмотрены. И здесь важно также понимать, что люди нередко невнимательны, устают, бывают равнодушными к работе, просто халтурят, подтасовывают результаты под вознаграждающую сторону и т.д. Человеческий фактор медицинских кадров – до сих пор враг номер один в медицине. И его не улучшить никакими приказами и директивами – восприятие обязанностей по выполнению работы полностью зависит от ответственности каждого человека – его совести. В современной гинекологии для взятия мазков на цитологию существуют специальные инструменты, обычно одноразовые. Они имеют свои плюсы и минусы, хотя значительно упрощают работу врача или медсестры. Когда-то забор материала проводился шпателями или пинцетами (ветви пинцета разделяли пополам), сейчас большой популярностью пользуется цитобраш (цитощеточка) и шпатель с удлиненным концом. Во многих постсоветских медицинских учреждениях забор материала на цитологическое исследование проводят старым методами. Практически, во многих странах требуется специальная дополнительная подготовка (обучение) медицинского персонала для проведения цитологического исследования (забора мазков). Для начала необходимо ватным тампоном осторожно удалить выделения с поверхности шейки матки, если таковы есть. После этого осторожно, не грубо делают забор материала со всей поверхности шейки матки одним движением руки, то есть не касаются шейки матки несколько раз, не дергают, словно чистят зубы зубной щеткой. Если необходимо перенести материал на стекло, делают это тоже очень осторожно, но быстро, одним движением по кругу, понимая, что грубое нанесение мазка приведет к повреждению клеток и тогда «читать» такие мазки будет трудно. Для забора клеток с канала шейки матки инструмент (но уже другой, если не пользуются специальными современными инструментами для проведения этого теста) осторожно – повторю еще раз — очень осторожно вводят в канал шейки матки, но не глубоко. Грубое введение приведет к повреждению сосудов и кровотечению (а кровь в материале уже исказит любые мазки), боли, повреждению слизистой. Крови после взятия таких мазков быть не должно, если забор материала был произведен правильно. Когда женщины жалуются, что они кровили почти сутки или больше, или у них были выраженные болевые ощущения после взятия мазка, это означает, что исследование проводили не по правилам, грубо, поэтому результаты могут быть далеко не достоверными. Использование цитощеточки позволяет проводить забор материала без боли. Только у женщин, у которых есть сужение канала шейки матки (стеноз) по каким-то причинам (после хирургического лечения, у старших женщин) забор материала для исследования может быть затруднено и сопровождаться болью. Если материал с канала шейки матки необходимо перевести на стекло, опять же, важно не размазывать его туда-сюда, а провести инструментом (шпателем или пинцетом) сверху вниз один раз, поворачивая его по часовой стрелке. Получится широкая полоска материала. Таким образом, на одном стекле в виде круга будет материал с поверхности шейки матки, а рядом в виде прямоугольника или полоски – с канала шейки матки. Когда материал высохнет, на стекле он едва заметен – ведь важно посылать на исследование не выделения, а тканевой материал. Когда в цитологический мазок попадают влагалищные выделения, просмотреть клеточный состав материала будет очень трудно и даже невозможно. Такое размещение материала для врача-лаборанта необходимо для того, чтобы ему было легче определить, где шеечная часть, а где клетки из канала шейки матки, потому что от этого будет зависеть насколько точные будут результаты.
И каковы же должны быть результаты? Чаще всего результаты неинформативны и их можно выбрасывать в мусорное ведро. Почему? Потому что описаны очень скудно и не по правилам современной гинекологии/цитологии. Поверхность влагалищной части шейки матки выстлана многослойным плоским эпителием, значит в результатах должны быть клетки плоского эпителия, что обычно видят и описывают. А вот канал шейки матки выстлан однослойным цилиндрическим эпителием. Задумайтесь внимательно – всего один слой клеток. Именно поэтому мазки нужно брать очень осторожно, почти нежно, потому что повредить этот слой можно легко. А это прямая дорога к инфицированию. Это становится открытой раной. В канал шейки матки желательно «внедряться» как можно реже – только по строгим показаниям. Поэтому шокируют чистки канала шейки матки, так называемые соскобы, которые проводят всем направо-налево, особенно молодым женщинам, потому что у них якобы полип шейки матки или еще что-то непонятное врачу… Такое грубое вмешательство может привести к сужению канала шейки матки (стенозу) за счет спаек, которые могут возникнуть после грубого вмешательства или соскоба, нарушению выработки шеечной слизи (что может стать причиной бесплодия) и другим негативным последствиям. Задумайтесь над этим!
Зная, что в канале шейки матки совершенно другой вид эпителия, вы, конечно, понимаете, что и во второй части результатов мазка должно быть указано, что имеются клетки цилиндрического (кубического, железистого, гранулярного – менее распространенные названия) эпителия. А что чаще всего мы имеем в результатах? Все те же клетки плоского эпителия. Логически возникает вопрос: а что они там делают, если их там в норме нет (единичные клетки плоского эпителия – я еще соглашусь, попали при взятии анализа)? Значит ли это, что у женщины есть какая-то патология? Ничего подобного. Это значит, что мазок не качественный: его взяли неправильно, или же в лаборатории его никто не смотрел или лаборант, смотревший его, не компетентен в вопросах цитологии. Чаще всего проблема не во врачах-лаборантах (хотя как часто врачи лабораторий звонят врачам-гинекологам и просят их не присылать «халтурные» мазки, а научиться делать забор материала правильно?), а в некачественности взятого материала.
Довольно часто современные врачи не берут клеточный материал с канала шейки матки, так как чаще всего такие мазки рассчитаны на скрининг плоскоклеточного рака. Если берут, то только со входа в канал шейки матки, где размещена зона трансформации. Но об этом мы поговорим чуть позже.
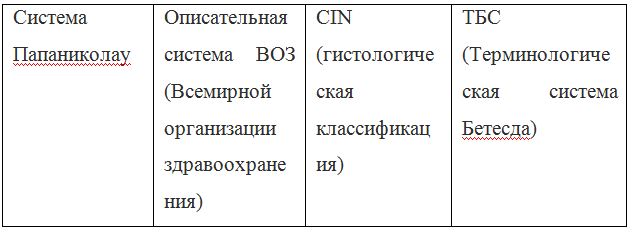
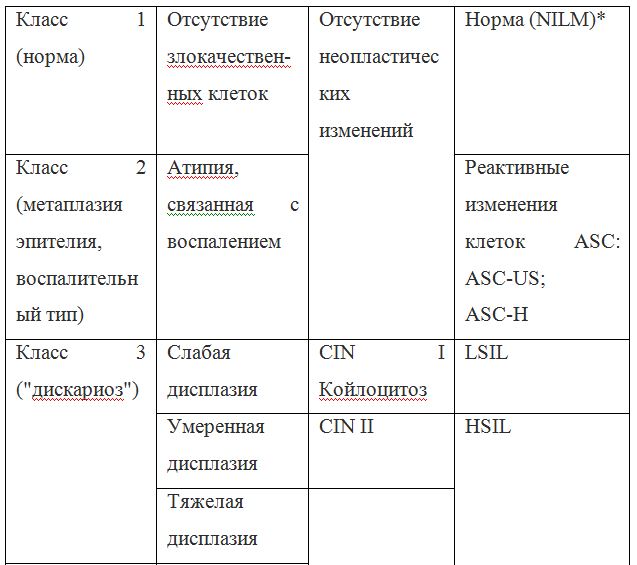
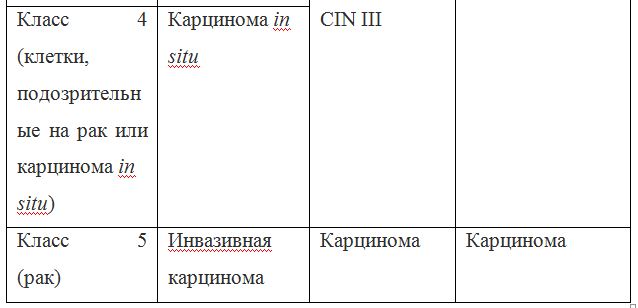
Современная цитологическая классификация результатов мазков требует конкретной интерпретации. Специфическую медицинскую терминологию для цитологических мазков разработали ученые Папаниколау и Траут в 1954 году. Классификация цитологического исследования шеечных мазков по Папаниколау включает пять классов и она почти не изменилась:
• Норма
• Атипичные клетки плоского эпителия неясного значения (ASC-US)
• Низкая степень плоскоклеточного интраэпителиального поражения (LSIL)
• Высокая степень плоскоклеточного интраэпителиального поражения (HSIL)
• Рак
В советских республиках, как и постсоветских странах, такая классификация не использовалась правильно или полноценно, поэтому в описаниях результатов могло быть написано или норма, или весьма скупо «клетки плоского эпителия», реже «атипичные клетки», еще реже «дисплазия» или «подозрение на рак».
Мне повезло в том отношении, что на заре моей практики заведующей онкологической цитологической лабораторией была женщина-врач высокого профессионального уровня, которая требовала от своих подчиненных добросовестного выполнения обязанностей. Она также звонила многим гинекологам, приходила к ним на прием и объясняла детально, что важно для получения качественного цитологического мазка, как проводить забор материала правильно и т.п. Таких прекрасных специалистов, мастеров своего дела, было не так много в те времена (90-е годы), а еще меньше их теперь. Но правила забора цитологических мазков почти не изменилась, хотя появились новые инструменты и модернизировались технологии.
В 1978 году была принята новая терминология в классификации патологии эпителия шейки матки и влагалища. Термин «дисплазия» был заменен термином «неоплазия»,цервикальную интраэпителиальную неоплазию 1, 2 и 3-й степени (CIN 1, 2, 3) не считали злокачественными процессами шейки матки. Таким образом, от понятия «дисплазии» отказались еще 30 лет тому, однако я буду использовать этот термин по ходу статьи, потому что наши женщины и наши врачи все еще пользуются словом «дисплазия» повсеместно.
В 1988 г. была создана американская системная классификация — Bethesdasystem, которой с 1991 года пользуются врачи большинства стран мира. Эта система имеет 6 основных классов (и несколько подклассов), в также включает классификацию Папаниколау, и используется для интерпретации результатов цитологии и биопсии, когда проводится забор кусочков тканей:
• Норма
• Цервикальная интраэпителиальная неоплазия 1 степени (раньше ее называли легкой или слабой дисплазией) – CIN1
• Цервикальная интраэпителиальная неоплазия 2 степени (раньше называли умеренной или средней дисплазией) – CIN2
• Цервикальная интраэпителиальная неоплазия 3 степени (раньше называли тяжелой или выраженной дисплазией) – CIN3
• Карцинома на месте (Carcinomainsitu)
• Инвазивный рак шейки матки
В 2001 году классификация была пересмотрена и дополнена, и сейчас ею руководствуются медицинские учреждения и лаборатории многих стран мира.
Термины «дисплазия» и «неоплазия» используются среди врачей все реже и реже. Современное определение состояния дисплазии называется «интраэпителиальным поражением», «интраэпителиальным образованием», «интраэпителиальной опухолью».Это лабораторный диагноз, основанный на результате цитологического мазка и/или гистологического исследования.
Из двух приведенных классификаций цитологических мазков и биопсии, к предраковым состояниям относят — Высокую степень плоскоклеточного интраэпителиального поражения (HSIL), что есть Цервикальная интраэпителиальная неоплазия 3 степени (раньше называли тяжелой дисплазией) – CIN3. Все другие заболевания и состояния шейки матки не относятся к предраковым состояниям.
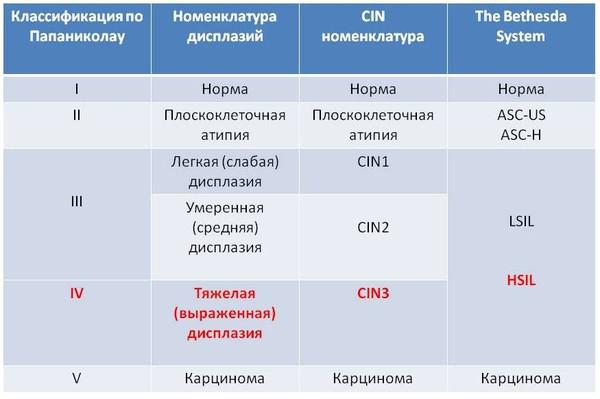
Приведенная ниже таблица отображает взаимосвязь между старой и современной классификацией цитологических исследований.
Красным шрифтом выделено предраковое состояние шейки матки. По старой классификации легкая и умеренная дисплазии относят к третьему классу и не относят к предраку. В новой классификации к предраку относят только итраэпителиальное поражение высокой степени, что некоторыми врачами может интерпретироваться как умеренная дисплазия, а другими как тяжелая. Различие можно определить только на тканево-клеточном уровне по степени (глубине) поражения эпителия. Если у вас обнаружена легкая дисплазия и врач запугивает вас, что это предрак и необходимо срочно лечить, это проявление отсталости от современной гинекологии и онкологии. Насколько чувствительны цитологические мазки в отношении выявления предраковых и раковых состояний шейки матки? Во многих публикациях вы найдете цифру, характеризующую чувствительность теста, – 98%, особенно в выявлении тяжелой дисплазии и рака. Однако, такой процент является идеальным или желаемым, и может быть достигнут только при проведении высококачественного тестирования с соблюдением всех правил забора цитологических мазков. Как показывают исследования, уровень ложно-отрицательных результатов чрезвычайно высокий и может доходить до 50% (даже в тех странах, где цитологическое исследование используют уже несколько декад).
Почему результаты могут быть ложными в таком большом количестве? Когда получают ложно-положительные результаты, то есть ставят худший диагноз, это чревато лишним вмешательством, как диагностическим, так и лечебным. Но когда уровень ложно-отрицательных результатов высокий, это может привести к тому, то рак ШМ будет выявлен не вовремя. А кто хочет оказаться в роли жертвы ошибочных результатов? Никто.
На качество мазков влияют очень многие факторы. Наличие выделений, крови, слизи, любрикантов кардинально меняет состояние взятого материала и может привести к неточным результатам. Также, существует фактор высушивания: на воздухе взятый материал, если его не перенести на стекло или в специальную среду быстро, тоже может менять свои качества, что приведет к ошибкам в интерпретации мазков. Поэтому очень важно строго соблюдать правила забора мазков на цитологическое исследование.
Как показывают данные ряда исследований, у 30% новых случаев рака шейки матки последние цитологические мазки были в норме. К сожаленью, у 55% женщин рак шейки матки выявляется уже в стадиях выраженного развития (инвазии) и распространения (3 и 4 стадии). Практическая чувствительность цитологического исследования составляет всего лишь 50% (хотя во многих источниках даже с учетом ложных результатов говорят о чувствительности в 65-90%).
Не так давно в гинекологии начали использовать жидкостное цитологическое исследование, или жидкостную цитологию (ThinPrep), и этот метод начал пользоваться большой популярностью. Клеточный материал переносится в специальный раствор, который механически разделяет клетки эпителия от загрязнения кровью и выделениями, слизи, мертвых клеток. Такие мазки просматривать намного легче, так как нет скопления клеток, а кроме того, оставшийся материал можно использовать для тестирования на инфекцию ВПЧ. Для жидкостной цитологии уровень ложно-отрицательных результатов составляет от 15 до 35%.
Как часто необходимо проводить забор мазков на цитологию? Очень часто нашим женщинам приходится слышать, что они должны посещать для этой цели гинеколога каждые полгода. Современные рекомендации кардинально отличаются от старых. Скрининг на наличие рака шейки матки по новым рекомендациям должен начинаться не с началом половой жизни, а в 21 год, независимо от того, когда начата половая жизнь. Это рациональный подход основан на многочисленных данных науки, клинических исследований, статистики заболеваемости и практической пользе теста. Во-первых, рак шейки матки у женщин и девушек до 19 лет – чрезвычайно редкое явление, встречается с частотой один-два случая на 1 миллион женщин. Во-вторых, даже при инфицировании ВПЧ очищение организма от этого вируса происходит в течение 1-2 лет почти у всех молодых женщин без всяких негативных последствий для организма, несмотря на то, что 70-80% молодых женщин заражаются этим вирусом с началом половой жизни. Об этой инфекции мы поговорим позже. Но в цитологических мазках молодых женщин могут быть временные изменения, вызванные вирусной инфекцией, в том числе в виде дисплазий, что в свою очередь может привести к лишнему ажиотажу и ложным действиям в виде слишком объемных обследований и поспешного лечения. Представьте себе состояние молоденькой девушки, которая только начала половую жизнь, а ей вдруг врач говорит, что у нее в мазке обнаружены изменения, ВПЧ-инфекция и ей гарантирован рак шейки матки, если она не будет срочно лечиться. Знакомая ситуация?
Женщины моложе 30 лет должны проходить цитологическое исследование один раз в три года, если результат тестирования на ВПЧ инфекцию отрицательный. Такая частота забора мазков тоже имеет рациональное объяснение. Возраст в 21-30 лет является самым спокойным в отношении развития рака шейки матки, поэтому не должен осложняться дополнительными скринингами. Большая частота тестирования не повышает уровень выявления предраковых и раковых состояний шейки матки у этой возрастной категории женщин. Исследования показали, рак шейки матки диагностируется у женщин 30-64 лет при исследовании каждые три года тоже не часто – 3-4 случая на 100 000 женщин. Современные рекомендации гласят, что женщины этой возрастной группы могут проходить цитологическое исследование один раз в три года при наличии отрицательного скрининга на ВПЧ инфекцию, а также если предыдущий цитологический мазок был в норме. Риск развития умеренной и тяжелой дисплазии у женщин с негативными результатами для цитологического исследования и определения ВПЧ-инфекции чрезвычайно низкий и не повышается в течение последующих 4-6 лет. Поэтому скрининг должен проводиться один раз в три года. По достижению 65-70 лет и наличии 3 нормальных цитологических мазков в течение предыдущих 10 лет женщина может прекратить тестирование на рак шейки матки. Однако, если женщина ведет активную половую жизнь в этом возрасте и имеет несколько половых партнеров, она должна продолжать проходить цитологическое обследование. Более подробно рекомендации будут представлены в последней части этой объемной статьи.
Перед тем, как мы обсудим детально вопрос о вирусе папилломе человека, важно вспомнить о кольпоскопии, которая очень популярна в России, на Украине и в ряде других стран мира, в основном бывших советских республиках. В других странах кольпоскопия используется редко, в силу своей дороговизны – всего лишь как дополнительный метод диагностики предракового состояния и рака шейки матки. Проведение кольпоскопии требует специальной подготовки врача, наличие дорогостоящей аппаратуры. Она может помочь в прицельной биопсии (заборе участков ткани для гистологического исследования), при наличии спорных результатов цитологии, для контроля процесса заживления ШМ, в ряде других случаев, но не является информативной, если ею злоупотребляют. Она не должна превращаться в коммерческий метод диагностики и проводиться всем подряд женщинам. Поэтому в большинстве стран мира для постановки диагноза предракового состояния и рака шейки матки используют цитологическое исследование, с или без тестирования на ВПЧ, и гистологическое исследование, которое можно провести с использованием кольпоскопии или без нее.
Врач гинеколог-онколог. Руководитель сети Университетских клиник. Эксперт по патологиям вульвы и шейки матки, ведущий консультирующий врач в Центре патологии шейки матки в Санкт-Петербурге. Стаж 20+ лет. Принимает в Университетской клинике. Стоимость приема 3000 руб.
Не стоит паниковать, поскольку предрак – это ещё не злокачественная опухоль. Однако медлить с лечением не стоит, поскольку такое состояние может перейти в онкологию за короткое время. Причём чем быстрее проходит такой процесс, тем более злокачественная опухоль образуется в итоге.
Обследование по результатам цитологии при предраковых состояниях шейки матки
При тяжёлой степени дисплазии назначаются биопсия с гистологией. У женщины берётся образец ткани с подозрительных участков шейки матки, который отправляют в лабораторию. Во время гистологического исследования учитываются не только строение и форма клеток, но и свойства самой ткани. Это позволяет более точно поставить диагноз и исключить злокачественное перерождение.
Выбор методов диагностики и лечения при выявленном предраке
Лечение предраковых состояний зависит от распространенности, тяжести процесса и сопутствующих патологий:
- При слабо выраженных явлениях предрака показано наблюдение. Женщине нужно периодически посещать врача, проходить кольпоскопию (осмотр шейки матки) и сдавать анализы на цитологию.
- При обнаружении клеток с признаками поражения папилломавирусом (ВПЧ) пациентка сдает ПЦР-анализ, выявляющий возбудителя и позволяющий определить его тип. Ей назначается лечение, подавляющее развитие вируса. Нередко это полностью устраняет проявления предрака, особенно если он обнаружен рано.
- При наличии в результатах цитологии клеток с неясной атипией (ASC-US, ASC-H, AGC, AGC), назначается анализ на флору. Если он показал воспаление или инфекцию, проводят лечение выявленных заболеваний. Это нужно, поскольку такие клеточные изменения могут быть вызваны воспалительным или инфекционным процессом.
Кольпоскопия
Цервикальная щеточка
ПЦР-анализ
Если при повторной цитологии, проведённой после терапии, снова выявляются «сомнительные» клетки, женщине назначают биопсию с гистологией. В этом случае в 20% обнаруживается предрак, а примерно в 1% случаев – онкология.
Варианты хирургического лечения при цитологии с сомнительными клетками
Умеренная и тяжелая степень предрака лечится хирургически. Метод лечения зависит от расположения патологических очагов и их глубины.
Неглубокие очаги удаляют с помощью лазера, радионожа, фотодинамической терапии (ФДТ) – лечения светом. Эти методы убирают очаги предрака без образования рубцов, деформации тканей и других остаточных явлений. Растяжимость шейки при этом почти не страдает, поэтому такие методики отлично подходят для женщин, планирующих в перспективе беременность и роды.
Лазер
Радионож
Фотодинамическая терапия
При тяжелой степени предрака проводится конизация – удаление конусообразного участка шейки с захватом части цервикального канала. Операция может проводиться я с помощью радионожа или хирургического инструмента. Получившийся «конус» отправляют на гистологический анализ, чтобы убедиться в отсутствии на его краях измененных клеток. Их отсутствие указывает на полное удаление патологического очага.
В Университетской клинике применяются современные методы лечения предраковых патологий шейки матки, позволяющие удалить все измененные клетки, минимально травмируя окружающие здоровые ткани
Чем раньше обнаружен предраковый процесс, тем легче он лечится, поэтому регулярная сдача анализа на цитологию позволит обнаружить заболевание на самой ранней стадии. Это позволит избавиться от обнаруженных болезней максимально щадящим способом.
Продолжение статьи
- Интерпретация (расшифровка) результатов цитологии
- Расшифровка цитологии: интерпретация лицевой стороны единого бланка
- Расшифровка цитологии: интерпретация данных по результатам цитологического анализа
- Расшифровка цитологии: интерпретация результатов цитологического анализа согласно их классификации по Папаниколау
- Интерпретация зарубежной терминологии, используемой для расшифровки цитологии
- Расшифровка цитологии: интерпретация протокола цитологического обследования при дисплазии шейки матки
- Расшифровка результатов цитологии при предраковых патологиях
- Расшифровка цитологии: интерпретация протокола цитологического обследования при раке шейки матки
- Расшифровка цитологии: дальнейшие действия при плохой интерпретации анализов
В статье обозначены проблемы в организации профилактики рака шейки матки и обсуждается диагностический алгоритм заболеваний шейки матки: стандартизованный забор клеточного материала с шейки матки; применение жидкостной цитологии; иммуноцитохимическое исследование онкомаркера р16. Предлагается алгоритм действий врача-гинеколога.
1. Актуальность проблемы
Рак шейки матки — злокачественная опухоль, этиологическим фактором которой являются вирусы папилломы человека (HPV) серотипов № 16, 18, 33, 35 и др. Согласно Всемирной базе данных по онкологической заболеваемости — GLOBOCAN (GLOBOCAN 2002 Database Jun. 2006), частота вновь выявляемых случаев рака шейки матки составляет в Российской Федерации 16,2 на 100 тыс. населения в год, в то же время смертность от данной опухоли — 10,1 на 100 тыс. населения в год. Организация цитологического скрининга позволила существенно снизить заболеваемость и смертность от рака шейки матки. Вместе с тем сохранился ряд:
1. Отсутствие стандартизованного забора материала — неадекватно взятый материал с шейки матки приводит к ложно-негативным результатам;
2. Проблема ложноположительных цитологических заключений (когда мазок показывает дисплазию там, где ее нет на самом деле) не дискредитирует идею цитологического скрининга в целом, т.к. в большинстве случаев она разрешается ценой относительно малоинвазивных воздействий (биопсия шейки, повторная цитология после пробного лечения). Тем не менее, в каждом конкретном случае эта проблема создает ряд неудобств врачу и пациентке:
-необходимость выполнения биопсии (стоимость, инвазия, время)
-необходимость повторных визитов к врачу
-негативное психологическое воздействие на пациентку, связанное с информацией о возможности развития у нее рака
3. Даже если диагноз дисплазии верифицирован гистологически, вероятность перехода дисплазии в рак составляет менее 50% (Хансон К.П., Имянитов Е.Н. Практическая онкология 2002). Вместе с тем, как на клиническом, так и на микроскопическом уровне в настоящее время отсутствуют достоверные прогностические критерии дальнейшего биологического поведения дисплазии (Nasser SM, Cibas ES, Crum C, et al. Cancer 2003).
4. Если консенсус в лечебной тактике по отношению к тяжелой дисплазии и Са in situ уже достигнут, то при умеренной и легкой дисплазии многое зависит от мнения лечащего врача. Он должен сопоставить цитологическое заключение, клиническую и кольпоскопическую картину, возраст пациентки и т.п. и принять решение (в диапазоне от наблюдения без лечения до конусовидной эксцизии шейки матки). При этом зачастую врач стоит перед нелегким выбором, т.к. агрессивная тактика не всегда оправдана (особенно у молодых пациенток), а необоснованно выбранная выжидательная тактика грозит развитием рака. Ситуация усугубляется тем, что в этом вопросе нет ни единства во мнении среди врачей, ни определенных общепринятых стандартов (Ашрафян Л.А., Харченко Н.В., Огрызкова В.Л., Антонова И.Б. Практическая онкология 2002).
5. Проблема ложноотрицательных цитологических заключений в налаженной системе цитологического скрининга нивелируется ежегодным повторением цитологического мазка. Однако при разовом цитологическом исследовании (когда пациентка до этого не была охвачена скринингом) в некоторых случаях требуются дополнительные гарантии отсутствия неопластического процесса.
6. Особо остро проблема ложноположительных и ложноотрицательных цитологических заключений стоит в отношении клеток железистого эпителия. В то время как аденокарцинома шейки может вообще не проявляться в цитологическом мазке, причиной выраженных изменений клеток железистого эпителия (даже с цитологической картиной аденокарциномы) могут являться реактивные процессы или эндометриоз (Krane J.F., Granter S.R. Cancer 2001).
7. Среди экспертов нет единого мнения по поводу тактики в отношении пациенток, которые инфицированы штаммами HPV высокого онкогенного риска, но нет дисплазии в цитологическом мазке. Мнение о том, что требуется лечить всех носителей и контактных лиц, сегодня уже дискредитировало себя, потому что большая часть носителей никогда не заболеет раком шейки матки.
Для разрешения данных проблем предлагается следующий диагностический алгоритм заболеваний шейки матки:
1. Стандартизованный забор клеточного материала с шейки матки;
2. Применение жидкостной цитологии;
3. Иммуноцитохимическое исследование онкомаркера р16ink4α.
Каждый из перечисленных пунктов обсуждается на последующих страницах статьи.
2. Забор материала
При отсутствии видимой патологии с шейки матки обязательно берется соскоб, для цитологического исследования.
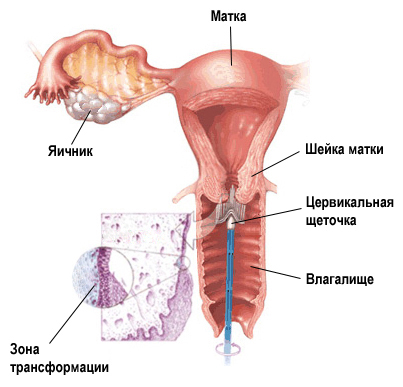
Учитывая отсутствие видимой патологии, материал берется со всей поверхности шейки матки и из шеечного канала. В связи с тем, что рак чаще всего развивается в месте соединения плоского эпителия шейки матки с цилиндрическим эпителием цервикального канала, по периметру маточного зева (так называемая зона превращения), соскоб для забора материала при скрининге должен обязательно включать эту зону и эпителий шеечного канала.
Принципиальное значение при этом имеет использование специального инструмента, гарантирующего взятие материала со всех указанных зон и обеспечивающего информативность препарата. Использование приспособленных инструментов и средств недопустимо, так как это приводит к снижению эффективности скрининга, вплоть до нулевых результатов.
3. Жидкостная цитология
Более пятидесяти лет назад доктор Папаниколау, чьим именем впоследствии был назван метод (Рар-тест), разработал метод цитологического исследования клеток цервикального канала по мазку на стекле. Рар-тест широко используется в скрининговых исследованиях для диагностики рака шейки матки, предраковых и фоновых состояний. В странах северной Европы, где хорошо организованы скрининговые исследования, лечение предопухолевых состояний и ранних форм рака позволило уменьшить смертность от инвазивной цервикальной карциномы на 50 — 70 %. По опубликованным данным, в Финляндии в 1992 г. заболеваемость была снижена до 2,8 случаев на 100000 женщин. В России в 1998 г. было выявлено 11 937 новых случаев заболевания, что составляло 15,3 на 100000 женщин, из которых 6,078 умерло (Syrjänen S., Shabalova I., Petrovichev N. et al. J Lower Genital Tract Disease 2002). В Англии по данным на 1987/88 гг. заболеваемость составляла 9 на 100000 женщин, смертность в 1997 г. — 3,7 на 100000. При этом около 4 млн. женщин в год проходили цитологическое скрининговое исследование цервикальных мазков (Payne N, Chilcott J, McGoogan E. University of Sheffield 2000.). В настоящее время выявление группы риска при цитологическом исследовании цервикальных мазков во время профилактических осмотров и дальнейшего наблюдения позволяют уловить процесс озлокачествления на самых ранних стадиях.
Необходимой предпосылкой для точной оценки морфологии клеток в мазке является правильно сделанный и хорошо окрашенный мазок. Эффективность цитологической диагностики в значительной мере определяется качеством приготовления препаратов. В настоящее время все большее распространение получает новая технология приготовления цитопрепаратов, так называемая жидкостная цитология. Важной технологической особенностью метода жидкостной цитологии (ЖЦ), улучшающей качество исследования, является то, что исследуемый материал берется в специальный стабилизирующий раствор, который обеспечивает его сохранность без разрушения и потери клеток. При этом весь клеточный материал сохраняет без изменения свои морфологические и иммуноцитохимические свойства. Для метода ЖЦ известно несколько систем: Cytospin, AutoCytePrep (CytoRich), LABONORD Easy Prep, Thin Prep.
В последние пять лет в разных странах проводилось много исследований, в которых сравнивалась эффективность традиционной техники и ЖЦ, используя для подтверждения диагнозов гистологическую экспертизу, как «золотой стандарт» и оценку цитопрепаратов согласно классификации TBS (The Bethesda System). В исследовании участвовали как поликлинические, так и стационарные отделения, обследовавшие тысячи пациентов (Grace A et al. Cytopathology 2002.). По обобщенным данным чувствительность традиционного метода колеблется в широком диапазоне значений: 34,5 — 89 %; а для метода ЖЦ имеет более стабильные значения: 71,4 — 95 %. Соответственно специфичность методов составляла: 36 — 76,9 % и 58 — 76,2 %. Авторы исследований резюмировали, что метод ЖЦ является более надежным лабораторным тестом, уменьшает количество ложноотрицательных результатов, уменьшает количество неудовлетворительных для анализа препаратов и время, необходимое цитологу для оценки препарата.
Исследование мазков по Папаниколау, полученных традиционным методом сбора материала, показывает, что не все, а только от 6,5 до 18 % взятых клеток наносятся на мазок. Кроме того, многие из этих клеток в результате плохого нанесения трудно или невозможно анализировать. Не вызывает сомнения, что традиционный метод анализа цитологического мазка имеет высокую диагностическую эффективность. Тем не менее, существует мнение, что метод имеет от 6 до 55 % ложноотрицательных результатов. По данным обзора Fahey чувствительность традиционного метода составляет 55-65 %, а специфичность — 65-70 % (Fahey MT, Irwig L, Macaskill P. American Journal of Epidemiology 1995).

Причиной большинства (около 2/3) ложных результатов, снижающей качество работы лаборатории, является ошибка взятия или переноса материала для приготовления мазков. Материал для цитологического исследования получают с поверхности слизистой оболочки. Слизь, присутствующая во взятом материале, мешает перенести на мазок клетки, также материал невозможно равномерно перемешать. Материал может быть неравномерно распределен на стекле. Слишком толстый мазок является причиной получения неполноценного материала. При переносе материала на стекло традиционным способом клетки целого региона шейки матки могут не попасть в препарат. Подсушивание и потеря прилипших к инструменту клеток значительно уменьшает диагностическую информативность микропрепаратов (рис. 2). Метод ЖЦ позволяет исключить эти негативные факторы (Амелюшкина В.А. Лабораторная медицина 2002).

Однако рутинное окрашивание мазков дает нам информацию о состоянии шейки матки на настоящий момент, но оно не способно оценить онкогенный потенциал изменений в тех случаях, когда не выявляется рак. Таким образом, применение только цитологического метода недостаточно для скрининга рака шейки матки.
Преимущество жидкостной цитологии состоит в том, что она из одного забора материала способна дать до 5-6 «серийных» (то есть одинаковых по клеточному составу) мазков. Это дает возможность применения дополнительных методов исследований. Длительное время таким дополнительным методом исследования применяли определения ДНК вируса папилломы человека высокого онкогенного риска. Однако в настоящее время известно, что скрининг ВПЧ инфекции, осуществленный у женщин соответствующего возраста, может идентифицировать пациенток с низким риском развития рака шейки матки в случае негативного теста, но ПЦР ВПЧ бесполезна для обнаружения пациентов с высоким риском прогрессии. Для достижения данной цели нам необходим тест, позволяющий выявлять проявление онкогенного потенциала вируса — таким образом, наше внимание должно быть перенесено от агента к хозяину. (Miller AB. Lancet 2001).
4. Иммунноцитохимическое исследование онкомаркера р16
Нормальный клеточный цикл состоит из G1, S, G2 и M фаз. Эпителий шейки матки представляет собой динамическую ткань с постоянным клеточным обновлением. Киназа, которая обеспечивает прохождение клетки из G1 в S фазу клеточного цикла — это E2F. В норме она неактивна, находясь в связанном состоянии с белком супрессором Rb (продукт гена ретинобластомы) (рис. 3).

Белок р16(INK4a) осуществляет контроль разобщения комплекса E2F-Rb, не допуская безудержной пролиферации клетки. Однако синтез р16(INK4a) в норме по механизму обратной связи сдерживается, таким образом, концентрация данного белка в нормальной клетке чрезвычайно мала, что проявляется негативной иммуноцитохимической реакцией (рис. 4).

Белок Е7 вируса папилломы человека ВПЧ высокого онкогенного риска при своем взаимодействии с продуктом гена ретинобластомы приводит к разобщению комплекса E2F-Rb.

E2F остается постоянно в активном состоянии, стимулируя безудержную пролиферации клетки. Р16(INK4a) пытается сдержать пролиферацию клетки, что приводит к бесконтрольному его синтезу (рис. 5). Однако р16 лишен своей мишени, что в условиях отсутствия обратной связи значительно повышает его концентрацию в клетке. Иммуноцитохимически это проявляется позитивной реакцией (рис. 6), что является биомаркером инициации канцерогенеза в эпителии шейки матки (Nieh S., Chen S.F., Chu T.Y. et al. Gynecol Oncol. 2003).

Было достоверно показано, что экспрессия р16 связана с низкой, умеренной и тяжелой дисплазией (с внутриэпителиальными плоскоклеточными поражениями шейки матки как высокого, так и низкого Grade, LSIL и HSIL соответственно классификации ВОЗ), причем экспрессия р16 не встречалась в плоском эпителии без признаков дисплазии (Bibbo M. et al. Acta Cytol 2002). В то же время, хотя отмечалась четкая корреляция обнаружения ДНК вируса папилломы человека с дисплазиями, имелось также большое количество ПЦР-позитивных на HPV случаев (с эписомальной локализацией HPV), в которых, при последующем гистологическом исследовании отсутствовал предрак и рак (Nieh S., Chen S.F., Chu T.Y. et al Gynecol Oncol. 2005). Данное явление подтверждалось негативной иммуноцитохимической реакцией на р16ink4α в диспластических клетках (рис. 7).

Таким образом, иммуноцитохимическое определение экспрессии р16 на мазках, приготовленных при помощи жидкостной цитологии, может позволить:
1. Достоверно оценивать потенциал дисплазии в отношении развития рака шейки матки и, соответственно, выбирать более консервативную или более агрессивную тактику лечения;
2. Уточнять заключения цитолога. Дополнительному исследованию на р16, с нашей точки зрения, подлежат все случаи атипической цитологии (кроме инвазивного рака шейки матки), неопределенные цитологические заключения (атипические клетки плоского эпителия неясного значения-ASCUS) и все изменения железистого эпителия (Murphy N. , Heffron B., King B. et al. Virchows Arch 2004);
3. Разрешать спорные вопросы при выявлении гинекологом высокоаномальной кольпоскопической картины, не сопровождающейся изменениями в цитологическом мазке;
4. Во многих случаях обоснованно отказаться от биопсии;
5. У большинства пациенток пожилого возраста с цитологической картиной дисплазии на фоне атрофического цервицита обоснованно избрать выжидательную тактику, отказавшись не только от лечения, но и от биопсий, и увеличить интервалы между диспансерными осмотрами. У небольшого числа р16-позитивных пациенток этой возрастной группы, напротив, обоснованно избрать более активную тактику;
6. Определять индивидуальную тактику в отношении пациенток, инфицированных штаммами вируса папилломы человека высокого онкогенного потенциала, если у них нет цитологических и кольпоскопических изменений. У женщин с позитивной ПЦР на HPV выделить группу пациенток, у которых уже инициирован канцерогенез в эпителии шейке матки, и направить на них необходимое лечебное воздействие. Соответственно в более многочисленной группе р16 негативных женщин необходимо продолжить мониторинг;
7. Усовершенствовать мониторинг пациенток, прошедших органосохраняющее лечение по поводу «тяжелой дисплазии» или «рака in situ», добавив определение р16 к рутинному цитологическому исследованию. Это позволит у пациенток наибольшего риска повысить чувствительность цитологического исследования и тестировать персистирующую папилломавирусную инфекцию до появления морфологических изменений.
5. Алгоритм действий врача-гинеколога
1. Забор материала мы рекомендуем проводить при помощи одноразовой цервикальной щеточки (cervix-brush, рис. 8): она вводится во влагалище под контролем глаза. Конус щеточки осторожно направляется в цервикальный канал. После введения в него конуса, щеточка прижимается к поверхности шейки и производится 5 полных круговых вращений — три по часовой стрелке и два — против часовой стрелки. Перед проведением данных манипуляций необходимо тщательно очистить шейку матки от слизи. Щеточку с материалом необходимо опустить в контейнер с жидкой транспортной средой и тщательно ополоснуть ее там. Жидкая среда и клеточная среда должны храниться в холодильнике при температуре от +2 до +8 оС. Клеточная суспензия стабильна в течение 10 дней.
Рисунок 8. Цервикальная щеточка.
2. Лабораторный этап занимает от 3 до 5 дней и включает в себя центрифугирование среды с получением монослойных мазков, рутинное окрашивание по Романовскому-Гимзе, иммуноцитохимическое исследование на р16ink4a.
3.Интерпретация результатов. Заключение включает в себя два подраздела: жидкостную цитологию и иммуноцитохимическое исследование на р16ink4a. Формулировка заключения жидкостной цитологии не отличается от традиционной, однако, его интерпретация должна проводиться в зависимости от выявление онкомаркера р16ink4a. Особенно это относится к дисплазиям шейки матки.
— Если выявляется позитивная реакция на онкомаркер р16ink4a, больной должно быть предпринято хирургическое лечение в размере конизации шейки матки. Мы рекомендуем проводить данное лечение в специализированных онкологических учреждения.
— Если выявляется негативная реакция на онкомаркер р16ink4a, то проводится консервативное лечение на местах.
Л.И. Мальцева, Г.А.Раскин, Л.Н.Фаррахова, А.В.Ахметзянова, В.С.Петров, Р.Ш.Хасанов
Казанская государственная медицинская академия
Казанский государственный медицинский университет
Клинический онкологический диспансер МЗ РТ
Литература:
1. Ашрафян Л.А., Харченко Н.В., Огрызкова В.Л., Антонова И.Б. Принципы лечения премикроинвазивного рака шейки матки.// Практическая онкология. — 2002. — Том 3. — С. 173-178;172. Хансон К.П., Имянитов Е.Н. Современные представления о канцерогенезе рака шейки матки.// Практическая онкология — 2002. — Том 3. — С. 145-155;18
3. Bibbo M., Klump W.J., DeCecco J., Kovatish A.J. Procedure for immunocytochemical detection of p16INK4A antigen in thin-layer, liquid-based specimens.// Acta Cytol. — 2002. — V.46 — P. 25-29;15
4. Cripe T.P., Haugen T.H., Turk J.P. et al. Transcriptional regulation of the human papillomavirus-16 E6-E7 promoter by a keratinocyte-dependent enhancer, and by viral E2 trans-activator and repressor gene products: implications for cervical carcinogenesis. // EMBO J. — 1987. — V. 6(12) — P.3745-3753;2
5. GLOBOCANDatabase Jun. 2006. http://www.dep.iarc.fr/globocan/globocan.htm; 3
6. Jenison S.A., Yu X.P., Valentine J.M., Galloway D.A. Characterization of human antibody-reactive epitopes encoded by human papillomavirus types 16 and 18. // J Virol. 1991 — V.65(3) — P. 1208-1218;1
7. Klaes R., Froedrich T., Spitkovsky D. et al. Overexpression of p16(INK4A) as a specific marker for dysplastic and neoplastic epithelial cells of the cervix uteri.// Int J Cancer. 2001 — V.92(2) — P.276-84;4
8. Meyer J.L., Hanlon D.W., Andersen B.T. et al. Evaluation of p16INK4a expression in ThinPrep cervical specimens with the CINtec p16INK4a assay: correlation with biopsy follow-up results.// Cancer. — 2007. — V. 111(2). — P. 83-92;20
9. Murphy N. , Heffron B., King B. et al. P16INK4A positivity in benign, premalignant and malignant cervical glandular lesions: a potential diagnostic problem.// Virchows Arch. — 2004. — V. 445 — P.610-615;12
10. Nasser S.M., Cibas E.S., Crum C. et al. The significance of the Papanicolaou smear diagnosis of low-grade squamous intraepithelial lesion cannot exclude high-grade squamous intraepithelial lesion.// Cancer. — 2003. — V.99. — P.272-276;16
11. Negri G., Egarter-Vigl E., Kasal A. et al. p16INK4A is a useful marker for the diagnosis of adenocarcinoma of the cervix uteri and its precursors.// Am J Surg Pathol. — 2003. — V. 27 — P.187-193;13
12. Nieh S., Chen S.F., Chu T.Y. et al. Expression of p16 INK4A in Papanicolaou smears containing atypical squamous cells of undetermined significance from the uterine cervix. // Gynecol Oncol. — 2003. — V.91(1) — P.201-8;5
13. Nieh S., Chen S.F., Chu T.Y. et al. Is p16(INK4A) expression more useful than human papillomavirus test to determine the outcome of atypical squamous cells of undetermined significance-categorized Pap smear? A comparative analysis using abnormal cervical smears with follow-up biopsies.// Gynecol Oncol. 2005 — V.99(3) — P.578-84;6
14. Rocco J.W., Sidransky D. p16(MTS-1/CDKN2/INK4a) in cancer progression.// Exp Cell Res. — 2001. — V.264 — P.42-55; 7
15. Ronco G., Cuzick J., Pierotti P. et al. Accuracy of liquid based versus conventional cytology: overall results of new technologies for cervical cancer screening: randomised controlled trial. BMJ. — 2007. — V. 335(7609). — P. 28 — 38;19
16. Sano T., Oyama T., Kashiwabara K., Fukuda T., Nakajima T. Immunohistochemical overexpression of p16 protein associated with intact retinoblastoma protein expression in cervical cancer and cervical intraepithelial neoplasia.// Pathol Int. — 1998. — V.48 — P.580-5;8
17. Ylitalo N., Josefsson A., Melbye M. et al. A Prospective Study Showing Long-Term Infection with Human Papillomavirus 16 before the Development of Cervical Carcinoma in situ. // Cancer Research. — 2000. — V. 60 — P. 6027-6032;14
При этом заболевании на слизистой нижней части матки и влагалища образуются участки измененных клеток плоского эпителия (покрывающего слоя). Обычно дисплазия поражает вагинальную область и шейку матки одновременно, что осложняет ситуацию. Дисплазию эпителия относят к предраковым патологиям.
Прием гинеколога — 1000 руб. Комплексное УЗИ малого таза — 1000 руб. Расширенная кольпоскопия — 1300 руб. Прием по результатам УЗИ или анализов — 500 руб (по желанию)
Что такое дисплазия
В интернете эту болезнь часто описывают, как аномальный рост клеток. На самом деле, патология гораздо серьезнее, чем это примитивное описание. Дисплазию эпителия ВОЗ характеризует как комплекс нарушений, включающий:
- клеточную атипию — видоизменение или замена клеток на несвойственные данной ткани;
- сбой в дифференцировке клеток — генетический код, отвечающий за функции клеток, их размер, форму и обмен веществ;
- сбой в архитектонике ткани — строение, структура и т.д.
Дисплазия — это не только клеточная атипия, это отклонения во всем тканевом комплексе.
Из-за бессимптомности заболевания на первых стадиях, лечение дисплазии влагалища часто начинается поздно, когда патологический процесс охватывает большую часть площади слизистой шейки матки и влагалища. Диагностируется ранняя дисплазия влагалища обычно на плановом приеме у гинеколога или во время осмотра, связанного с другой патологией.
Причины развития дисплазии влагалища
Основные причины перерождения клеток — генетическая предрасположенность и инфицирование онкогенными вирусами папилломы человека (ВПЧ), HSV-2, HPV и HIV.
Развитие дисплазии ускоряют:
- Гормональные проблемы, связанные с климаксом — недостаток эстрогенов (гипоэстрогения), прием противозачаточных без рецепта и др.;
- Заболевания, изменяющие флору влагалища и ослабляющие иммунитет: вагинит, кольпит;
- Состояния, истощающие ткани, например, натирание влагалища гинекологическим кольцом, использование вибраторов, некачественных презервативов и тампонов.
В группе риска женщины с вредными привычками — курящие, употребляющие фастфуд и алкоголь и проживающие в районах с плохим экологическим профилем.
Причины дисплазии шейки матки
Самая частая причина диспластических изменений шейки – инфицирование папилломавирусом. Типы ВПЧ 16 и 18 обнаруживаются в 98 % случаев дисплазии.
Заболевание провоцируют:
- воспалительные процессы во влагалище;
- травматизация шейки при родах и абортах;
- гормональная дисфункция;
- сниженный иммунитет;
- алкоголь и курение;
- слишком ранняя и беспорядочная сексуальная жизнь;
- пренебрежение гигиеной половых органов.
При дисплазии нарушается структура эпителия, а слизистая не выполняет защитные функции. При выраженных диспластических изменениях женщину направляют на консультацию к онкологу.
Стадии развития дисплазии
Диспластический процесс — продолжение гиперплазии — увеличения количества клеток, вызванного хроническим воспалением и перерождением. Часто к гиперплазии и дисплазии присоединяется атрофия (отмирание) тканей, так как эти процессы имеют общие генетические механизмы.
Если быть точными, термин «дисплазия» для характеристики переходных предраковых процессов в медицине не применяется. При патологии во влагалищном секторе шейки матки состояние обозначается CIN (cervical intraepithelial neoplasia), предраковые изменения во влагалище обозначаются — VaIN, вульвы — VIN.
Различают три степени дисплазии:
- Легкая, слабо выраженная (Д I) – затронуто до 1/3 толщины эпителиального слоя;
- Умеренная, средняя (Д II) – измененные клетки прорастают на 2/3 эпителиальной ткани;
- Тяжелая, выраженная (Д III) — весь слой изменен. Эта степень дисплазии — начальная стадия рака шейки и влагалища.
Определяющий критерий степени дисплазии — выраженность клеточной атипии. Чем тяжелее степень, тем больше размер, гиперхромность и полиморфизм клеточных ядер. Дисплазия эпителия может регрессировать (обратный процесс), быть стабильной или прогрессировать. Как быстро пойдет процесс озлокачествления зависит от степени выраженности и длительности заболевания. Чем значительнее дисплазия, тем меньше вероятность регрессии.
Дисплазия тяжелой степени расценивается гинекологами как облигатный предрак, гарантирующий развитие рака. Поэтому больные облигатным предраком ставятся на учет к онкологу.
Симптомы дисплазии влагалища
В начале болезни пациентки ничего не чувствуют. Очаги дисплазии во влагалище обнаруживаются случайно при гинекологическом осмотре. Единственный симптом, указывающий на заражением вирусом ВПЧ (он вызывает патологию в 90% случаев), который больная может увидеть невооруженным глазом, — мелкие бородавки (остроконечные кондиломы) в области половых органов.
По мере развития патологии появляются:
- краснота и сухость слизистой влагалища;
- кровотечения после полового акта или спринцевания;
- выделения с неприятным запахом;
- зуд, жжение и отек вагинальной области.
При тяжелой дисплазии возникают боли в крестце, отеки ног. Во время ходьбы ощущается дискомфорт в области влагалища.
Гинеколог проводя осмотр с помощью кольпоскопа (оптического прибора) видит изменения слизистой оболочки влагалища в виде выступающих красноватых или светлых пятен с неровными очертаниями. Дисплазийные участки бывают большими и затрагивают шейку матки. Для уточнения диагноза, слизистую смазывают растворами уксуса или Люголя (расширенная кольпоскопия). При запущенной дисплазии видны мозаичность слизистой и сосочковые разрастания.
Окончательный диагноз ставится после проведения биопсии подозрительных участков, при которой гинеколог берет часть клеток на анализ.
Симптомы дисплазии шейки матки
При этом состоянии в эпителии шейки появляются клетки, отличные по строению от нормальных. Процесс затрагивает базальную мембрану и верхний слой тканей. Заболевание часто не дает симптомов, поэтому, чтобы вовремя распознать заболевание, необходимо регулярно делать кольпоскопию и сдавать анализы.
При выраженной диспластической патологии женщины жалуются на зуд, боль и жжение в вагине. Выделения становятся желтоватыми или кровянистыми. Возможны контактные кровотечения.
Для подтверждения диагноза проводится кольпоскопия со взятием мазка из шейки и цервикального канала на гистологическое и цитологическое обследование. При дисплазии на шейке виден измененный участок, а в шеечной слизи обнаруживаются диспластичные клетки.
Как вылечить дисплазию влагалища
Из-за термина «предраковое состояние» пациентки, столкнувшись с дисплазией влагалища или шейки матки, погружаются в депрессию. Но на деле все не так страшно!
Лечение зависит от степени дисплазии:
- Легкая степень дисплазии не требует лечения до момента ухудшения состояния. Если доктор замечает изменения, видоизмененные клетки разрушают лазером, химическими веществами или современным радиоволновым методом. Остроконечные кондиломы удаляют этим же методом, так как они могут переродиться в рак.
- При глубокой дисплазии или начавшемся раковом перерождении показана вагинэктомия — удаление дисплазийных участков. Если процесс зашел слишком далеко, то для сохранения органа, трансплантируют кожу с ягодиц или бедер.
Лечение дисплазии шейки матки
Лечение зависит от тяжести дисплазии. При поражении слизистой первой степени применяют выжидательную тактику, особенно у нерожавших. Каждые полгода проводится плановое обследование, и, если заболевание не прогрессирует, рекомендуется профилактическое посещение гинеколога.
В более тяжелых случаях применяется оперативное лечение. Наиболее эффективные методы:
- Иссечение пораженных тканей — электроэксцизия (конизация);
Радиоволновой — самый современный способ лечения дисплазии, рекомендуемый европейскими гинекологами. - Ампутация шейки применяется в редких, особо тяжелых случаях, когда нет возможности помочь другим способом — это делают онкологи.
Для борьбы с вирусом папилломы (ВПЧ) применяют противовирусные препараты и средства для стимуляции иммунитета. Параллельно проводят лечение сопутствующих патологий.
Что нужно знать о лечении дисплазии: 5 шагов к выздоровлению
- Шаг №1 – Идите к гинекологу без паники! Опасения, что дисплазия слизистой влагалища и шейки матки не лечится, неверно. Нельзя вылечить причину дисплазии — вирус папилломы человека, а вот ее очаги и связанные с ней неприятные симптомы при правильном лечении устраняются.
- Шаг №2 – Пройдите полноценную диагностику! Гинеколог возьмет ткани для проведения гистологического анализа, чтобы определить природу дисплазии и исключить рак. Забор пробы в проводится при кольпоскопии с прицельной биопсией, когда врач выбирает для анализа конкретные участки. Параллельно сдается комплекс анализов, определяющих типа вируса папилломы, если он выступает причиной атипичных изменений клеток влагалища. Если же дисплазия шейки матки или влагалища имеет воспалительно-инфекционную природу, определяют возбудителя и его чувствительности к антибиотикам.
- Шаг №3 – Комплексное лечение. Лучший результат лечения дисплазии влагалища дает удаление патологических очагов. Это делается хирургическим или аппаратным методом, но только комплексный подход к терапии дает устойчивый результат.
- Шаг №4 – Выбирайте малотравматичные методы лечения дисплазии. Сейчас классическое хирургическое иссечение тканей при помощи скальпеля используется крайне редко. Предпочтение специалисты отдают малотравматичным и безопасным методикам, таким как лазерная коррекция и радиоволновая методика. Процедуры проводятся под местной анестезией. Операция не оставляет рубцов, имеет четкую направленность действия, обладает антибактериальным эффектом. Запаивание кровеносных сосудов во время процедуры исключает кровотечение.
- Шаг №5 – Если требуется обширное вмешательство — соглашайтесь! Если поражение дисплазией имеет внушительные размеры, может потребоваться иссечение большого участка тканей влагалища. Восстановить женское здоровье и нормальную половую активность женщины в послеоперационном периоде поможет современная методика пластики влагалища.
Лечение дисплазии женских органов, вопреки распространенным заблуждениям, эффективно и безопасно, при этом женщина получает возможность предотвратить онкологию и сохранить нормальную сексуальную активность
Профилактика онкологических заболеваний влагалища и шейки матки
Профилактика болезни заключается в своевременном лечении ИППП (половых инфекций), воспалений и гормональных нарушений. Девочкам рекомендуется вакцинация против вируса папилломы вакциной Гардасил.
Где лечат дисплазию влагалища и шейки матки в СПБ
Лечение дисплазии требует серьезного подхода, так как болезнь считается опасным предраковым состоянием. Гинекологи медицинского центра Диана в Санкт-Петербурге обладают многолетним опытом лечения дисплазии эпителия, что позволило нам разработать эффективный и безопасный подход к лечению этой патологии.
Мы рады помочь каждой пациентке с диагнозом «дисплазия», и применяем только современные подходы к лечению и инновационное аппаратное оборудование — новейший радиоволновой нож «Фотек».
Тяжелая дисплазия шейки матки (или цервикальная интраэпителиальная неоплазия CIN III) — патологический процесс, при котором в покровном эпителии шейки матки появляются атипичные клетки. Измененные эпителиальные клетки отличаются от нормальных: они становятся крупными, бесформенными, с множественными ядрами, исчезает разделение эпителия на слои. В отличие от умеренной степени, когда патологические изменения захватывают более половины толщи эпителия, при тяжелой форме дисплазии процесс распространяется по всей толще эпителиального пласта.
Тяжелая дисплазия эпителия шейки матки — это предраковое состояние, предшествующее развитию инвазивного рака. Ежегодно в мире диагностируется около 40 млн новых случаев заболевания у женщин разного возрастая, из них больше 10 млн — пациентки с тяжелой степенью дисплазии, не лечившиеся ранее.

Главный редактор, заведующий хирургическим отделением
Задать вопрос
Врач-хирург высшей квалификационной категории, доктор медицинских наук, профессор кафедры общей хирургии АГМУ.
Содержание
- Причины
- Симптомы
- Диагностика
- Лечение
- Мой подход к лечению
- Радиоволновая хирургия
- Почему важно регулярное обследование
- Дисплазия шейки матки — чем опасна и можно ли не лечить?
- Причины дисплазии шейки матки
- Факторы риска, которые вызывают развитие дисплазии шейки матки:
- Симптомы
- Чем опасна дисплазия шейки матки?
- Диагностика и лабораторные исследования
- Лечение дисплазии шейки матки
- Профилактика дисплазии
- Дисплазия шейки матки
- Дисплазия шейки матки, симптомы
- Что такое биопсия шейки матки?
- Лечение дисплазии шейки матки
- Медикаментозное лечение
- Основные условия для проведения радиоволновой терапии
- Основные показания к хирургическому лечению:
- Лечение дисплазии шейки матки
- Консервативное лечение – возможно ли это?
- Оперативное лечение
- Лечение во время беременности
- Осложнения при хирургическом лечении шейки матки
- Дисплазия шейки матки
- Причины развития
- Симптоматика
- Диагностические мероприятия
- Терапевтический курс
- Профилактические меры
- Диагностика и лечение дисплазии шейки матки в Москве
- Вопросы и ответы
Причины
По данным эпидемиологических исследований, причиной заболевания, как правило, являются онкогенные типы вируса папилломы человека. При длительном присутствии вируса в организме женщины происходят изменения в строении клеток, т.е. развивается дисплазия. Кроме повреждения клеток, выстилающих шейку матки (появляются изменения в клеточном ядре, меняется форма клеток и др.), вирус способен повреждать гены клеток, что приводит к аномалии практически всего слоя плоского эпителия, происходит интенсивное размножение клеток.
Существуют также отягчающие факторы, способные увеличить риск развития дисплазии шейки матки тяжелой степени. Основными факторами риска являются:
- длительные воспалительные процессы в половых органах;
- гормональные нарушения, вызванные менопаузой, беременностью;
- многочисленные беременности;
- иммунодефицитные состояния;
- генетическая предрасположенность к злокачественным образованиям;
- бесконтрольный прием в течение длительного времени гормонсодержащих препаратов.
Незащищенные половые контакты, частая смена партнеров, раннее начало половой жизни, курение также увеличивают вероятность заболевания.
Симптомы
При этом заболевании практически отсутствуют характерные признаки, поэтому болезнь нередко становится «случайной находкой» во время профилактического обследования. Но инфицирование папилломавирусом приводит к хроническому воспалительному процессу в шейке матки, который может стать причиной появления определенных симптомов. Также дисплазия может протекать при фоновых заболеваниях: эрозии, лейкоплакии, кольпите, цервиците и др., при которых характерно появление тех или иных признаков. Поэтому симптомы дисплазии шейки матки тяжелой степени могут проявляться в виде:
- болей во время полового акта;
- появлении выделений или кровотечений при сексуальных контактах;
- зуда в зоне гениталий;
- ноющих болей внизу живота.
Поскольку подобные проявления встречаются при других урогенитальных патологиях, необходимо пройти обследование для выявления причины появившихся симптомов. Для диагностики предусмотрено множество эффективных способов.
Диагностика
Классическим скрининговым методом диагностики является цитологическое исследование, позволяющее обнаружить атипичные клетки. Также проводится расширенная кольпоскопия — осмотр шейки матки с помощью оборудования, способного увеличить зону обследования в несколько раз. Для диагностики также предусмотрены различные тесты, в том числе на определение вируса папилломы человека. При обнаружении патологических изменений во время осмотра или по результатам анализов назначается дальнейшее обследование, куда входит гистологическое исследование частиц ткани, взятых из очагов патологии во время биопсии.
При необходимости женщине рекомендованы дополнительные методы обследования: цервикоскопия, иммуногистохимическое исследование соскоба и биоптата, расширенный анализ на наличие урогенитальной инфекции, обследование на иммуно-интерфероновый статус. Весьма информативными методами диагностики являются: МРТ органов таза, гистероскопия с раздельным диагностическим выскабливанием, гистология аспирата, взятого из полости матки и другие обследования, с помощью которых можно получить данные о вовлечении в патологический процесс других органов. Все вышеперечисленные методы диагностики доступны пациенткам нашей клиники.
Лечение
Если при заболевании легкой степени возможно спонтанное излечение, а вероятность озлокачествления не превышает 1%, то тяжелая стадия — наиболее неблагоприятная форма болезни; рак развивается в 12% случаев. Поэтому лечение при тяжелой дисплазии шейки матки только хирургическое, целью которого является удаление изменённых тканей.
Сегодня существуют различные методики лечения: криотерапия, электрокоагуляция, радиохирургия, деструкция с помощью лазерного воздействия, фотодинамическая терапия и др. Однако многие из них не рекомендованы для лечения заболеваний шейки матки, поскольку приводят к излишнему повреждению здоровых тканей, появлению отеков после операции, потере эластичности в этой зоне и др.
Мой подход к лечению
Дисплазия шейки матки чаще всего поражает женщин репродуктивного возраста, причем количество заболевших в последние годы только увеличивается. Поскольку характерные симптомы отсутствуют, женщина нередко обращается к врачу, когда заболевание перешло в тяжелую степень. Между тем, существуют малотравматичные методики, с помощью которых можно радикально избавиться от очагов патологии даже в запущенной стадии, при этом повреждение здоровых тканей практически отсутствует. К тому же нет повреждения глубоких структур, после заживления формирование рубцов исключено. Современные методы лечения могут быть использованы даже у молодых пациенток, планирующих рождение ребенка в дальнейшем.
Радиоволновая хирургия
«Золотым» стандартом при удалении очагов патологии считается радиоволновой метод, при котором выполняется атравматичный разрез и коагуляция тканей с помощью аппарата Surgitron (США). Рассечение при использовании радиоволны происходит за счет выделяемого тепла, которое возникает при сопротивлении тканей во время проникновения в них направленных высокочастотных волн. В этом случае используется свойство патологически измененных клеток, обладающих наибольшим сопротивлением, что ведет к их более быстрому разрушению. При этом методе сам электрод не нагревается, к тому же отсутствует прямой контакт с тканями.
Высокочастотная энергия, сконцентрированная на конце электрода, приводит к всплеску молекулярной энергии внутри клетки, происходит нагрев ткани, при котором патологически измененные клетки фактически испаряются. Методика относится к малотравматичным и имеет ряд преимуществ:
- здоровые клетки не разрушаются (в отличие от электрокоагуляции или диатермокоагуляции с использованием низкочастотного электрохирургического оборудования);
- нет риска кровотечения во время процедуры;
- в послеоперационном периоде отсутствует отек, воспалительный процесс, болевой синдром;
- быстрое заживление;
- риск рубцовой деформации шейки матки минимален, поэтому методика может быть использована у пациенток, планирующих рождение детей в дальнейшем.
Операция проводится под контролем видеокольпоскопа, что обеспечивает максимальную точность и глубину воздействия — это также повышает безопасность радиоволновой хирургии для здоровых тканей. Поскольку не затронутые патологическим процессом ткани практически не повреждаются в ходе процедуры, нарушение анатомии и функциональности цервикального канала также исключены, что важно для нормального течения беременности и родов в дальнейшем.
Почему важно регулярное обследование
Надо учитывать, что дисплазия относится к предраковым заболеваниям. К сожалению, несмотря на имеющиеся эффективные способы диагностики и лечения, нередко у молодых пациенток нелеченая дисплазия на фоне беременности быстро трансформируется в рак 3-4 стадии.
Для предотвращения развития тяжелой дисплазии шейки матки во всем мире активно используются скрининговые программы, позволяющие обнаружить изменения даже при отсутствии каких-либо симптомов. А использование малотравматичных процедур позволяет добиться полного излечения. Для сокращения времени диагностики и быстрейшего перехода к лечению в нашей клинике разработана специальная лечебно-диагностическая схема, благодаря которой постановка окончательного диагноза и выбор оптимального метода лечения занимает минимум времени.
За моими плечами — многолетний опыт лечения пациенток с дисплазией шейки матки разной степени тяжести. Для каждой женщины я подбираю тактику лечения только индивидуально, учитывая степень дисплазии, величину поражения, возраст, сопутствующие заболевания, а также желание пациентки сохранить репродуктивную функцию. Результаты лечения обобщены в различных научных публикациях, которые можно найти в отечественных и зарубежных рецензируемых изданиях. Я также провожу семинары, посвященные лечению заболеваний женской половой сферы, участниками которых являются специалисты научных центров, клиник различного значения, а также курсанты постдипломного обучения.
Дисплазия шейки матки — чем опасна и можно ли не лечить?
Дисплазия шейки матки – или CIN (Cervical Intraepithelial neoplasia) — предраковое состояние, характеризующееся структурными и функциональными изменениями клеток слизистого эпителия шейки матки.
В отличие от эрозии, которая возникает в результате механического повреждения тканей, при дисплазии наблюдаются клеточные атипические изменения, поэтому природа этих болезней совершенно разная.
На начальных стадиях дисплазия шейки матки может никак себя не проявлять, поэтому важно хотя бы раз в год записываться на прием к гинекологу в клинику, проходить профилактические осмотры и обследование для своевременной диагностики и эффективного лечения.
На III степени прогрессирования дисплазия шейки матки может перерасти в тяжелое заболевание – рак (инвазивная карцинома). Определением, диагностикой и лечением патологии занимается врач-гинеколог. Лечение дисплазии III стадии проводится специалистом-онкогинекологом.
Степени дисплазии шейки матки
Причины дисплазии шейки матки
Согласно клинической практике в гинекологии, большинство случаев предраковых заболеваний имеет риск возникновения на фоне инфицирования ВПЧ, который, как правило, передается половым путем при незащищенном половом акте.
Длительное нахождение вируса в женском организме и клетках многослойного плоского эпителия способствует атипичному клеточному перерождению и развитию дисплазии в зоне ШМ. В большинстве случаев иммунитет женщины обезвреживает инфекцию.
Однако если иммунная защита нарушена, вирус неконтролируемо размножается, что приводит к появлению патологических изменений и трансформаций в клетках. У пациенток с вероятностью развития цервикальной неоплазии распространенность онкогенных типов вируса папилломы человека чрезвычайно велика.
Факторы риска, которые вызывают развитие дисплазии шейки матки:
- гормональные нарушения, неконтролируемое употребление гормонсодержащих препаратов;
- половая жизнь в раннем возрасте;
- воздействие хронической инфекции на слизистую ШМ;
- курение;
- постоянные стрессы, несбалансированный рацион, отсутствие режима дня и другие внешние факторы, провоцируют подавление иммунной реактивности.
Симптомы
На ранних этапах дисплазия шейки матки никак себя не проявляет. Отсутствует специфическая клиническая картина. Часто на фоне дисплазии появляется микробная инфекция, которая предрасполагает к развитию цервицита (воспаление шейки матки и цервикального канала), кольпита. Симптомы воспалительного процесса во влагалище:
- покраснение, жжение, зуд слизистой;
- патологические выделения неприятного запаха.
В шейке матки отсутствуют нервные окончания, поэтому жалобы на боль при дисплазии практически всегда отсутствуют. Однако женщину должны насторожить такие симптомы, которые не являются нормой:
- кровянистые выделения после половой близости, не связанные с менструацией;
- тянущие, ноющие боли в нижней части живота;
- дискомфорт во время полового акта.
Дисплазия: симптомы и характерные признаки
Чем опасна дисплазия шейки матки?
Диагностические мероприятия по выявлению дисплазии ШМ на начальных стадиях и адекватная терапия под наблюдением опытного гинеколога позволяет полностью излечить заболевание и предотвратить малигнизацию измененных тканей.
Отсутствие лечения на третьей стадии приводит к развитию тяжелого, смертельно опасного заболевания – раковой опухоли шейки матки.
Цервикальный рак занимает третье место после рака молочной железы и рака эндометрия. Бессимптомное течение злокачественного процесса приводит к тому, что у более 40% пациенток онкологическое заболевание диагностируется на поздних (II-IV) стадиях. Это существенно влияет на благоприятность прогноза и эффективность лечения.
Диагностика и лабораторные исследования
Установить точный диагноз и определиться с планом терапии можно с помощью обязательных методов диагностики:
- гинекологический скрининг в зеркалах;
- расширенная кольпоскопия;
- цитологический ПАП-анализ или мазок Папаниколау для исследования клеточного слоя;
- соскоб с ШМ;
- тест на ВПЧ, определяющий штамм вируса и вирусной нагрузки на организм;
- общий анализ крови.
Лечение дисплазии шейки матки
Если результаты комплексной диагностики подтверждают наличие диспластических изменений в эпителии влагалищной части шейки матки, ситуация требует немедленно начинать лечение.
Отсутствие своевременной терапии и тактики лечения способствует прогрессированию патологии и перерождению атипичных клеток в раковые.
Как лечить дисплазию шейки матки?
Дисплазию I стадии можно вылечить консервативным путем. Какие группы медикаментозных препаратов назначаются:
- Противовирусные. Подавляют активность ВПЧ, блокируют процесс размножения инфекции:
- Протефлазид; ; и др.
- Лаферон; ; и др.
Дисплазия II-III стадии лечится хирургическим путем. Методы хирургического вмешательства:
- удаление или прижигание (абляция) участка с поражениями щадящими способами: криотерапия, радиоволновая и лазерная терапия, электрокоагуляция;
- конизация или полная ампутация шейки матки.
Необходимо сказать, что процедура хирургической операции по удалению патологических тканей на шейке матки способствует увеличению риска преждевременных родов.
Сама по себе цервикальная интраэпителиальная неоплазия первой степени на течении беременности и родов никак не отражается и зачастую опасности не представляет.
Средний возраст женщин, которым предлагают пройти хирургическую коррекцию цервикальной внутриэпителиальной неоплазии — тридцать лет (активный репродуктивный возраст).
Хирургическая операция нередко связана с неблагоприятным течением последующей беременности. Частота и тяжесть осложнений возрастают с увеличением сложности операции и глубины иссекаемых тканей.
Профилактика дисплазии
При своевременном выявлении на консультации и лечении дисплазии шейки матки прогноз обычно благоприятный. Главным фактором развития и прогрессирования дисплазии шейки матки является длительное инфицирование канцерогенными типами вируса папилломы человека.
Для предупреждения заражения этой патологией рекомендуются профилактические вакцины. У пациентки с ЦИН часто бывает обнаружен вирус простого герпеса 2 типа, цитомегаловирусную инфекцию, хламидийную урогенитальную инфекцию, бактериальный вагиноз, ассоциированный с резким снижением или отсутствием вагинальной лактофлоры, повышенным ростом во влагалище Gardnerella vaginalis и Atopobium vaginae, повышение концентрации в бакпосеве грибов рода Candida, Mycoplasma hominis.
Устранение, профилактика и своевременное выявление данных факторов способны снизить вероятность развития предраковой патологии шейки матки.
Все лекарства, доступные к продаже в аптеках Вашего города, а также цены на них, Вы можете увидеть на нашем сайте, введя в поисковой строке название лекарства и запустив поиск.
Дисплазия шейки матки
Поставленный диагноз «дисплазия шейки матки» — это сигнал женского организма, который требует внимания и помощи. Женский организм не в силах в одиночку преодолеть критические пороги заболевания. Женщины часто дисплазию шейку матки сравнивают с эрозией. Действительно, эрозию шейки матки и дисплазию шейки матки могут вызывать похожие этиологические факторы, но тактика ведения и лечения данных заболеваний принципиально разная.
Дисплазию шейки матки относят к предраковым состояниям эпителия шейки матки. Однако это не значит, что дисплазия шейки матки обязательно реализуется в рак. На вопрос можно ли вылечить дисплазию шейки матки, ответ очевиден: можно, если вовремя и правильно начать лечение!
Что же такое дисплазия шейки матки? Как образно и понятно объяснить диагноз простой женщине. Постараемся Вам помочь.
Представьте, что в норме эпителий, покрывающий шейку матки, имеет строгую слоистость. Слои эпителия располагаются строго последовательно. Нижний слой (базальный), затем идет парабазальный, промежуточный, поверхностный слои эпителия. Представьте свою шейку матки в виде салата « под — шубой».
Когда слои неправильно располагаются, возникает хаотический, диспластический процесс. В зависимости от выраженности изменений в эпителии шейки матки различают легкую, умеренную и тяжелую дисплазию шейки матки.
Дисплазию 1 степени ставят при выявлении полиморфных клеток с особыми (гиперхромными) ядрами и высоким ядерно-цитоплазматическим соотношением, а также при нарушении дифференцировки в нижней трети пласта многослойного плоского эпителия. Дифференцировка в верхних двух третьих эпителия происходит нормально.
Дисплазия шейки матки 2 степени характеризуется наличием клеточного атипизма и многочисленных митозов (делений клеток) в нижней половине эпителиального пласта. В верхней половине дифференцировка клеток не изменена.
Дисплазия шейки матки 3 степени характеризуется клеточным атипизмом в двух третях толщины эпителия..
Рак на месте или по латыне «cancer in situ» — состояние, когда все слои эпителия шейки матки поражаются полностью.
Среди причин, способствующих возникновению дисплазии шейки матки, различают экзогенные: (ВПГ, вирус простого герпеса и др. половые инфекции) и эндогенные факторы (хронические воспалительные заболевания органов малого таза и мочеполовых органов, нарушение гормонального гомеостаза, снижение иммунного ответа и др.) и смешанные факторы.
Исследования последних лет доказано, что в 50-80 % образцов умеренной и тяжелой дисплазии эпителия шейки матки обнаружен ВПЧ высокой степени онкогенного риска (преимущественно 16 и 18 типов).
Дисплазия шейки матки, симптомы
При дисплазии шейки матки как самостоятельном заболевании жалобы больных и симптоматика чаще отсутствуют. Боли внизу живота и кровянистые выделения из половых путей появляются только в особо запущенных случаях, когда заболевание развивалось на протяжении нескольких лет.
Дисплазия шейки матки может быть выявлена на обычном профилактическом осмотре. Надо отметить, что дисплазия шейки матки — это полностью предотвратимое заболевание для женщины, которая регулярно следит за своим здоровьем и выполняет обязательное цитологическое исследование на профилактическом визите у врача гинеколога или специально обученной медицинской сестры.
Если у женщины выявлены изменения в цитологии, указывающие на дисплазию 1 , 2 или 3 степени далее проводится углубленное обследование по протоколу лечения, утверждённому Министерством здравоохранения.
При сочетании дисплазии с фоновым заболеванием шейки матки больные могут предъявлять жалобы на бели, зуд наружных половых органов и т.д. В данной ситуации выполняется исключение половых инфекции, в том числе гонореи, ВПЧ, герпеса. Проводится противовоспалительное лечение с учетом диагностических находок.
С помощью специального прибора (кольпоскопа) уточняют характер данной болезни, выявляют наличие, распространенность и степень выраженности кольпоскопических проявлений дисплазии шейки матки с последующим забором материала из очага поражения для прицельного цитологического исследования. Цитология мазков позволяет установить степень выраженности дисплазии.
Для дальнейшего установления диагноза прицельно берут биопсию шейки, делают эндоцервикальный соскоб и их гистологически исследуют. Результаты исследования являются решающими в постановке диагноза дисплазии или рака шейки матки!
Что такое биопсия шейки матки?
Биопсия шейки матки – это инвазивный метод обследования шейки. С подозрительного участка шейки матки берется 1 или несколько участков ( кусочков) ткани шейки матки специальным инструментом. В медицинском центре Гармония биопсия шейки матки выполняется радиоволновым методом с помощью американского аппарата Сургитрон специальной радиоволновой петлей.
Манипуляция выполняется бескровно (используется два режима радиоволнового воздействия аппарата Сургитрон: разрез и коагуляция сосудов шейки матки) и безболезнено. Полученный материал помещается в специальную пробирку с формалином, фиксируется и далее передается для углубленного исследования в гистологическую лабораторию, где помещается в парафиновую среду. Далее парафиновые блоки исследуются врачом патоморфоологом под особым микроскопом. Врач патологоморфолог выносит окончательный диагноз.
Лечение дисплазии шейки матки
Лечение зависит от того, возникла дисплазия на основе предшествующих заболеваний шейки матки: цервицит, эрозия шейки матки, вирусное поражение шейки матки и т.д. или диагностировано впервые как самостоятельное заболевание.
Метод лечения определяют строго индивидуально, исходя из особенностей кольпоскопии, степени дисплазии: легкой, средней или тяжелой. Также лечение зависит от возраста больной и особенностей детородной функции, строения шейки локализации диспластического процесса, сопутствующих болезней. Однако радикальность вмешательства определяют по степени дисплазии.
Медикаментозное лечение
Чаще всего показано больным легкой дисплазией. При ее назначении используют два методологических подхода: выжидательную тактику и немедленную локальную деструкцию. В нашем медицинском центре мы используем радиоволновой метод лечения.
Выжидательная тактика основана на том, что у 30-60 % больных возможна спонтанная регрессия поражения шейки матки. Тогда необходимы постоянные цитологическое исследования в динамике (1-3 мес.), медикаментозное купирование воспалительного процесса, подавление пролиферативных изменений, регуляция менструального цикла. Если нет эффекта (регресса дисплазии) в течение 3 месяцев, следует изменить тактику лечения в сторону более радикальных мер.
Медикаментозное лечение показано также больным с легкой дисплазией назначают средства, подавляющие пролиферативную активность, обладающие противовирусным и иммуномодулирующим эффектом. Ретиноиды (предшественники и аналоги витамина А) подавляют пролиферацию, стимулируют киллеры и активность цитотоксических клеток. Подофиллин, трихлоруксусная кислота малоэффективны и токсичны. Они способны также подавлять патологические митозы с эффективностью 86 %. 5-Фторурацил применяют по методике лечения плоских папиллом или в форме мази (крема), которую наносят на поверхность шейки матки 2 раза в день на протяжении 2 нед. Интерферон стимулирует активность лимфоцитов, повышает уровень иммуноглобулинов, обладает антипролиферативной и антивирусной активностью. Его назначают в инъекциях, местно в виде геля или мази до 4 раз в сутки на протяжении 20 дней.
Второй методологический подход заключается в локальном удалении (деструкции) патологического очага или радикальной терапии.
Хирургическое устранение дисплазии независимо от метода разрушения патологической ткани должно быть достаточной глубины. Обычно крипты в цервикальном канале бывают глубиной до 7,8 мм, в среднем 3,4 мм. Поражение крипт тяжелой дисплазией и внутриэпителиальным раком бывает протяженностью до 5,2 мм (средняя глубина их проникновения по криптам − 3,2 мм). Поэтому при деструкции на глубину 3 мм полностью разрушается весь патологический очаг у 95 % больных, а на глубину 4 мм − у 99 %.
Криогенное воздействие − идеальное и оптимальное лечение легкой и умеренной дисплазии, особенно патологических очагов размером до 2,5−3 см. Криотерапия тяжелой дисплазии допускается, но не является методом выбора. Обычно используют большие температурные режимы при экспозиции 8−10 мин. Процедуру проводят в два этапа. Однако когда нужно промораживать более половины длины шейки матки и невозможен гистологический контроль после операции, от такой деструкции лучше отказаться.
В нашем медицинском центре Гармония мы используем современный метод лечения дисплазии шейки матки- радиоволновую терапию (РВТ).
РВТ показана больным легкой и умеренной дисплазией. Перед РВТ женщину полностью обследуют по регламентирующим протоколам. Исключают половые инфекции, сифилис, ВИЧ, гепатит С и В. Выполняют УЗИ органов малого таза, биопсию шейки матки, кюретаж цервикального канала, аспират из полости матки или РДВ. Шейку матки обрабатывают маркерами (раствором Люголя) для определения границ поражения.
Основные условия для проведения радиоволновой терапии
- нет данных (цитологической-эндоскопического скрининга), свидетельствующих о раке шейки матки;
- лечение должен проводить специалист, знающий основы кольпоскопии.
При дисплазии 3 степени вопрос лечения дисплазии решается совместно с онко-гинекологом. В последнее время достаточно часто проводят хирургическое лечение дисплазии. Ампутация шейки матки по Штурмдорфу показана больным, у которых дисплазия сочетается с элонгацией шейки при опущении матки.
Основные показания к хирургическому лечению:
- возраст больных старше 50 лет,
- отсутствие условий для конизации вследствие анатомических изменений,
- атрофии шейки,
- сглаживание сводов,
- тяжелая дисплазия на всем протяжении эндоцервикса;
- неэффективность предшествовавшего лечения либо невозможность иного лечения.
Согласно методическим рекомендациям белорусских онкогинекологов, целесообразно лечить дисплазии индивидуально в зависимости от клинической картины болезни и возраста женщины.
У женщин моложе 40 лет с умеренной дисплазией допустимо радиоволновое лечение шейки матки. Больным, у которых умеренная дисплазия сочетается с обширным эктропионом, деформацией шейки матки, а также старше 45 лет необходима диатермоэлектроэксцизия шейки матки либо операция типа операции Штурмдорфа, Эммета. Хирургическое вмешательство следует расширять до удаления шейки матки с телом матки у больных с сопутствующими умеренной дисплазии опухолями и опухолевидными образованиями матки и придатков (особенно у женщин в климактерический и менопаузальный периоды).
Дисплазия шейки матки может сочетаться с раком в начальных стадиях. Тогда в основном выполняют конусовидное иссечение или ампутацию шейки матки. Вследствие сглаженности влагалищных сводов, атрофических изменений полового аппарата у женщин старше 45-50 лет невозможно выполнить органосохраняющие вмешательства, поэтому операцию следует расширить до простой гистерэктомии (удаление шейки матки и тела матки).
Наблюдение за оперированными пациентками проводят акушеры-гинекологи общей лечебной сети путем контрольных осмотров с кольпоскопическим и цитологическим исследованиями.
Больную легкой дисплазией достаточно осмотреть 2 раза в году. Женщине с умеренной дисплазией контрольные осмотры необходимы каждые 3 месяца, а с тяжелой дисплазией − не реже 1 раза в месяц. Оперированных снимают с диспансерного учета при получении трех отрицательных результатов кольпоскопического и цитологического исследований, но не ранее чем через 2 года. Если после специального лечения вновь выявляют признаки дисплазии, женщину нужно направить к онкогинекологу для углубленного обследования и лечения в онкологическом учреждении.
Информация, расположенная на сайте носит строго информационный характер и не может быть использована самостоятельно.
Получить квалифицированную помощь можно у наших врачей гинекологов, прошедших специальную подготовку по патологии шейки матки. Запись по контактным телефонам или на сайте.
Лечение дисплазии шейки матки
В Университетской клинике «Я здорова!» можно получить полноценное и квалифицированное лечение различных заболеваний шейки матки, в том числе и дисплазии.
Тактика ведения пациенток с дисплазией шейки матки представляет собой непростую задачу, прежде всего, с позиций диагностики стадии заболевания, поскольку именно этот факт является основным при выборе подходов.
Администрация сайта старается своевременно обновлять прайс-лист, но во избежание возможных недоразумений просим уточнять стоимость услуг на день обращения по телефону: +7 (495) 565-30-44 или в клинике у администраторов. Не является договором публичной оферты.
Первичный прием (осмотр, консультация) акушером-гинекологом (В01.001.001)
Хирургическое лечение заболеваний шейки матки с использованием различных энергий, I категория сложности (А16.20.036)
Хирургическое лечение заболеваний шейки матки с использованием различных энергий, II категория сложности (А16.20.036)
Биопсия шейки матки радиоволновая конусовидная, I категория сложности (А11.20.011.002)
Биопсия шейки матки радиоволновая конусовидная, II категория сложности (А11.20.011.002)
Биопсия шейки матки радиоволновая конусовидная, III категория сложности (А11.20.011.002)
Раздельное диагностическое выскабливание цервикального канала (А11.20.008.002)
Согласно современной классификации дисплазия шейки матки бывает двух видов.
- Легкая форма (LSIL, CINI) – легкое доброкачественное поражение шейки матки, которое может быть вызвано вирусом папилломы человека как высокого, так и низкого онкогенного риска. В большом количестве случаев дисплазия такой степени тяжести в течение нескольких месяцев регрессирует (исчезает) сама.
- Тяжелая (HSIL, CINII, CINIII) — это поражение шейки матки, которое с высокой вероятностью может приводить к раку. Такая форма дисплазии связана с более агрессивными типами вируса папилломы человека и требует крайне серьезного отношения со стороны врача. К сожалению, наблюдения за такими пациентками в течение 30 лет в отсутствии лечения показали 30%-ю вероятность прогрессии в рак шейки матки.
Поскольку дисплазия CIN II является некоторым промежуточным состоянием между легкой формой и тяжелой, в данном случае рекомендуется дополнительное обследование, которое заключается в иммуногистохимическом исследовании экспрессии белка р16. Если он присутствует, то в этом случае такую промежуточную дисплазию относят к тяжелой форме (HSIL), если нет, то к легкой, что и определяет тактику лечения.
Консервативное лечение – возможно ли это?
В случае если у молодой женщины после кольпоскопии регистрируется нормальная картина при наличии дисплазии CIN I и CIN II (по данным цитологического и/или гистологического исследований) и отсутствии белка р-16, достаточно проводить динамическое наблюдение с цитологическим исследованием через 6 и 12 месяцев и обследованием на ВПЧ 1 раз в 6 месяцев.
Оперативное лечение
Если у пациентки любого возраста выявлена дисплазия тяжелой (CIN III) или промежуточной степени CIN II с наличием маркера р16 при иммуногистохимическом исследовании, то показано оперативное лечение дисплазии в виде абляции или эксцизии шейки матки радиоволновым или лазерным методом с последующим гистологическим исследованием.
Медикаментозного лечения таких изменений шейки матки не существует!
Абляция – это метод лечения с помощью различных энергий, когда производится разрушение патологической ткани.
Эксцизия – вариант лечения, при котором пораженный участок удаляется полностью и может быть исследован гистологически (с помощью микроскопа).
Процедуру эксцизии выполняют под местным обезболиванием, обязательно под контролем кольпоскопии, которая позволяет установить границы пораженного участка шейки матки. Специальным электродом с помощью радиоволновой, лазерной или аргоноплазменной энергии проводят удаление дисплазии шейки матки.
В послеоперационном периоде рекомендуют воздержаться от спринцевания, половых контактов, использования тампонов в течение не менее 4 недель. Это необходимо для того, чтобы процесс заживления раневой поверхности на шейке матки полностью завершился. На 2-3 недели исключают физические нагрузки и тепловые процедуры. Эти сроки являются критическими для возможного отторжения сформированной ранки после хирургического лечения. Кровянистые выделения в течение 10-20 дней являются нормой после операции. В случае незначительного болевого синдрома (хотя, как правило, его не бывает) можно использовать любые традиционные анальгетики.
К сожалению, после лечения дисплазии радиоволновым или лазерным методом полностью расслабляться нельзя. Контрольную кольпоскопию, цитологическое исследование и ВПЧ-тест рекомендуют выполнять через 2 месяца после проведенного лечения, но не раньше указанного срока. Согласно европейским рекомендациям, после лечения дисплазии CIN II и CIN III требуется проведение цитологического исследования через 6, 12 и 24 месяца, а затем с ежегодным интервалом еще в течение 5 лет. Американские руководства являются более строгими и требуют проведения комбинированных исследований: ВПЧ-тест и цитология через 12 месяцев и 24 месяца. При двойном негативном результате можно перейти к 3-летнему интервалу скрининга в течение как минимум 20 лет после лечения.
Лечение во время беременности
В случае выявления HSIL (изменений с высоким риском развития атипических изменений) во время беременности рекомендуется проводить динамическое наблюдение (кольпоскопия, цитологическое исследование) каждые 3 месяца. Поскольку эксцизия во время беременности может спровоцировать истмико-цервикальную недостаточность и выкидыш на поздних сроках, только при подозрении на распространение процесса и инвазию атипических клеток проводится оперативное лечение.
Осложнения при хирургическом лечении шейки матки
Одним из самых частых осложнений при лечении является послеоперационное кровотечение. По данным литературы оно может встречаться в 5 % всех случаев. Вероятность этого осложнения зависит от степени поражения, доли удаленной части шейки матки и особенностей структуры тканей конкретной пациентки.
В Университетской клинике «Я здорова!» работают врачи с более чем 20-летним опытом лечения различных заболеваний шейки матки, в том числе дисплазии. Все гистологические исследования проводятся в ведущем учреждении страны экспертами-патоморфологами («Национальный медицинский исследовательский центр онкологии им. Н. Н. Блохина» Минздрава России). Это центр, который дает экспертные заключения и пересматривает препараты из других учреждений, устанавливая окончательный диагноз. При необходимости врачи клиники имеют возможность проведения полноценных консилиумов с ведущими онкогинекологами страны.
Дисплазия шейки матки
Дисплазия — патология, проявляющаяся в виде атипических изменений эпителиальных клеток влагалищной части шейки матки. Гинекологи рассматривают заболевание как предраковый процесс. На ранних стадиях дисплазия обратима: своевременное начало лечения позволяет предотвратить формирование злокачественного новообразования. В группу риска входят женщины в возрасте 25–35 лет. Ежегодно врачи фиксируют 1,5 случая заболевания на каждую тысячу пациенток данного возрастного интервала. Диагностика и лечение дисплазии шейки матки осуществляются гинекологом. При наличии соответствующих показаний врач может направить пациентку к онкологу и хирургу.
Причины развития
В 95% случаев заболевание формируется на фоне инфицирования пациентки онкогенными типами вируса папилломы человека. В течение 12–18 месяцев после попадания на слизистую оболочку влагалища вирусная инфекция провоцирует изменения в строении плоских эпителиальных клеток. Другими причинами дисплазии шейки матки могут стать:
- угнетение функций иммунитета пациентки на фоне приема иммунодепрессантов;
- систематическое курение в активной или пассивной формах;
- хронические инфекционные заболевания мочеполовой системы;
- эндокринные нарушения, вызванные беременностью, преждевременной менопаузой или приемом гормональных препаратов;
- ранняя беременность и роды.
Риск развития патологических изменений в эпителии шейки матки возрастает при травматических повреждениях прилежащих тканей.
Шейка матки представляет собой узкое цилиндрическое тело, внутри которого располагается цервикальный канал. Наружный зев органа расположен во влагалище, внутренний — в полости матки. Внутренняя поверхность цервикального канала выстлана эпителием, состоящим из цилиндрических клеток. На стенках шейки матки расположены железы: продуцируемая ими слизь препятствует попаданию патогенной микрофлоры из влагалища в матку. В нормальном состоянии эпителий цервикального канала окрашен в ярко-красный цвет. Дисплазия приводит к нарушению строения слизистой оболочки: атипичные клетки обладают увеличенным размером и нетипичной формой.
Диспластический процесс может затрагивать различные слои плоского эпителия. Гинекологи выделяют три степени патологии на основании глубины формирования атипичных клеток. Легкая дисплазия шейки матки (CIN I по международной классификации) характеризуется незначительными изменениями в морфологии клеточных структур. Патология затрагивает верхнюю треть многослойного эпителия.
Умеренный диспластический процесс (CIN II) развивается в верхней и средней трети эпителиальных тканей. Тяжелая дисплазия (CIN III) затрагивает всю толщу эпителия и рассматривается гинекологами как неинвазивный рак. Патология не распространяется в прилежащие мышцы, сосуды и нервные окончания (инвазивный рак шейки матки поражает во все перечисленные структуры).
Симптоматика
Симптомы дисплазии шейки матки неспецифичны. Каждый четвертый клинически регистрируемый случай изменений в плоском эпителии выявляется случайно. Часто течение патологии осложняется вторичными инфекциями, симптоматика которых схожа с кольпитами или цервицитами. Пациентки сталкиваются со следующей симптоматикой:
- выраженным зудом;
- острым болевым синдромом;
- систематическими выделениями из влагалища, обладающими нетипичным запахом и цветом.
Диспластическое поражение шейки матки может самостоятельно регрессировать после устранения воспаления-первопричины. В 80% случаев этого не происходит — патология отличается прогрессирующим течением. Осложненное течение дисплазии сопровождается образованием остроконечных кондилом влагалища, вульвы и заднего прохода. Нередко заболевание развивается на фоне хламидиоза или гонореи.
Диагностические мероприятия
Диагностика дисплазии шейки матки состоит из нескольких этапов. На первом пациентке предстоит пройти осмотр наружного зева цервикального канала. Процедура выполняется гинекологом с помощью влагалищного зеркала. Во время осмотра врач сможет обнаружить изменение окраски слизистой оболочки, атипичные разрастания эпителия и другие признаки морфологических изменений клеточных структур.
Следующий этап диагностики — кольпоскопия и проведение диагностических проб. Используя оптический аппарат, врач осматривает поверхность шейки матки и наносит на нее йод или слабый раствор уксусной кислоты. Участки дисплазии не окрасятся в цвет, характерный для здоровых тканей.
Лабораторные анализы проводятся посредством микроскопии соскобов с разных участков наружного зева цервикального канала. Признаки злокачественного перерождения эпителиальных клеток становятся показанием к проведению биопсии. Гинеколог выполняет забор биоптата — небольшого кусочка тканей, затронутых диспластическим процессом. Последующее цитологическое исследование позволит установить степень дисплазии и изучить строение атипичных клеток.
Наличие маркеров, свидетельствующих о присутствии в организме женщины онкогенных типов вируса папилломы, определяется в ходе ПЦР-теста. На основании этих данных и выявленных у пациентки симптомов гинеколог разрабатывает стратегию лечения дисплазии шейки матки.
Терапевтический курс
При назначении лечения врач учитывает степень дисплазии шейки матки, диагностированную у пациентки. Выявление дисплазии первой степени позволяет избрать выжидательную тактику. Успешное лечение причины развития диспластического процесса позволяет рассчитывать на самостоятельный регресс атипических изменений в эпителии. В подобных случаях девушкам рекомендуются ежеквартальное прохождение цитологических исследований, посредством которых осуществляется контроль за состоянием шейки матки.
Медикаментозный курс основан на иммуномодулирующих препаратах. Эти средства могут назначаться женщинам, столкнувшимся с рецидивами патологии после ранее проводившегося лечения.
Хирургические вмешательства выполняются при риске малигнизации очага дисплазии. Предотвратить злокачественное перерождение атипичных клеток позволяют малотравматичные методы: криодеструкция, электрокоагуляция, радиоволновая или лазерная терапия. Дисплазия третьей степени становится показанием к ампутации шейки матки или иссечению пораженного патологическим процессом участка тканей.
Профилактические меры
Профилактика дисплазии шейки матки предполагает соблюдение пациентками комплекса рекомендаций. Девушкам необходимо:
Профилактические меры адресованы пациенткам с семейным анамнезом, отягощенным онкологическими патологиями репродуктивной системы.
Диагностика и лечение дисплазии шейки матки в Москве
АО «Медицина» (клиника академика Ройтберга) обладает всем необходимым оборудованием для диагностики и лечения диспластических процессов, развивающихся в наружном зеве цервикального канала. Прием пациенток осуществляется в современном диагностическом комплексе, построенном с учетом последних достижений медицины.
Вопросы и ответы
Какой врач лечит дисплазию шейки матки?
Лечение патологии осуществляется гинекологом. При осложненном течении заболевания пациентке могут потребоваться консультации с хирургом, онкологом и иммунологом.
Может ли диспластический процесс стать причиной рака шейки матки?
Да, может. Вероятность злокачественного перерождения очага дисплазии определяется в ходе лабораторных анализов. При высоком риске малигнизации диспластического процесса пациентке показано хирургическое вмешательство.
Влияет ли патология на репродуктивное здоровье пациенток?
Лечение умеренной дисплазии не оказывает влияния на репродуктивные способности женщин. Препятствием для зачатия и рождения ребенка может стать иссечение шейки матки при выявлении у пациентки неинвазивного рака.
Медицинский эксперт статьи
Новые публикации
Цитология шейки матки
, медицинский редактор
Последняя редакция: 19.10.2021
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Цитология шейки матки — лабораторное исследование, которое определяет клеточную структуру cervix uteri (шейки матки), а также клеток цервикального канала. Один из вариантов цитологии шейки матки впервые был применен в начале XX века ученым из Греции Папаниколау (Papanikolaou) с целью раннего выявления и профилактики онкозаболеваний в гинекологии.
С тех пор тест PAP используется повсеместно наряду с новым методом – ThinPrep (жидкостная цитология), что позволяет своевременно определять и эффективно лечить скрытые хронические и предраковые заболевания шейки матки.

Показания к проведению
Основная задача, которую решает цитология шейки матки, это – предотвращение онкологического процесса. Раннее обнаружение атипичных клеток позволяет вовремя остановить РШМ (рак шейки матки), который по статистике стоит на третьем месте в ряду самых распространенных онкопатологий у женщин. Опасность бессимптомного течения болезни велика, поэтому главная цель процедуры – это своевременное выявление предраковых изменений в клетках. Это дает возможность не только увеличения процента и срока выживаемости, но и уверенную надежду на благополучное излечение. Метод ПАП в практике гинекологии считается одним из самых быстрых и точных для получения данных о наличии или отсутствии начальных стадий онкопроцессов, раковых заболеваний или фоновых патологий неопухолевой этиологии, которые могут спровоцировать угрожающий жизни рак. Многие врачи называют цитологию шейки матки «золотым стандартом» диагностики и скринингового наблюдения таких внутриэпителиальных изменений и состояний:
- Разнообразные клеточные аномалии высокой или низкой степени.
- Наличие или отсутствие патогенной микрофлоры для диагностики состояния слизистой оболочки шейки матки.
- Нарушения нормального ритма менструального цикла (частота цикла, его задержка или отсутствие).
- Все виды заболеваний вирусного происхождения – ВПЧ (вирус папилломы человека) – кондиломы, Herpes simplex генитальный (герпес).
- Инфертильность (бесплодие).
- Дефекты слизистого покрова шейки матки (все виды эрозии).
- Длительный цикл терапии с помощью гормональных лекарственных средств.
- Аномальные выделения из влагалища, в том числе с кровью, особенно после сексуальных контактов.
Цитология шейки матки необходима в качестве скринингового обследования, если:
- Планируется беременность
- Роды происходят несколько раз подряд (например, 3-4 раза в течение 4 лет).
- Первые роды произошли в раннем возрасте (до 18 лет).
- Женщина часто меняет сексуальных партнеров.
- Период постменопаузы (климактерический период).
- Запланирована контрацепция в формате внутриматочной спирали.
- Ранее цитология никогда не проводилась, либо женщина не обследовалась последние 3 года.
- Последний забор тканевого материала не соответствует нормам или определил изменения в клетках.
- Осмотр шейки матки с помощью зеркала показывает видимые патологические изменения (цвет, структура).
- У женщины выявлены заболевания, связанные с иммунодефицитом (ВИЧ).
- Семейный анамнез отягощен онкозаболеваниями (кто-то из прямых родственников болел или болен в настоящее время онкозаболеванием).
В целом, ежегодное скрининговое цитологическое обследование должно быть обязательным для каждой женщины, достигшей совершеннолетия. Если же цитология шейки матки показывает явно выраженные клинические отклонения клеточного материала, обследование нужно проводить чаще — минимум 2 раза в год или в режиме комплексного терапевтического плана.
Подготовка
Подготовка, которую предполагает цитология шейки матки, не относится к разряду сложных. Сама процедура происходит очень быстро, практически без дискомфорта и неприятных ощущений, а подготовка заключается в следующих действиях:
- Исключить санацию (гигиенические процедуры) в виде спринцеваний
- Несколько дней до процедуры (2-3 дня) следует придерживаться режима воздержания в интимной жизни
- Не пользоваться гигиеническими тампонами, таблетками, жидкостями, кремами, свечами и гелями для влагалища
- За 2 часа до теста женщине нужно воздержаться от мочеиспускания
Чтобы цитология шейки матки показала достоверный результат, важно знать такую информацию:
- ПАП-тест и менструальный цикл не совместимы. Процедуру проводят за 3-5 дней до начала месячных или после них, лучше всего это делать в 10-12 день цикла.
- Цитология не будет точной при любом инфекционном заболевании, особенно в острой фазе, как правило, анализ проводят после базового лечения. Исключение – необходимость получения результата cito, в таком случае, цитология шейки матки проводится дважды – во время болезни и спустя 2 месяца для цитологического контроля.
- Мазок во время проведения интравагинальной терапии будет не информативным, его следует производить спустя 5-7 дней после окончания лечения.
- Не рекомендуется делать забор тканевого материала при воспалительных процессах во влагалище, показателями которых могут быть выделения, зуд, жжение.
Уточнения условий подготовки к процедуре можно получить у лечащего гинеколога.
К кому обратиться?
Техника проведения
Цитология шейки матки считается обязательной процедурой комплексного гинекологического осмотра. Это стандарт, который позволяет своевременно выявить риски многих заболеваний, включая онкологические.
Гинеколог производит соскоб с внешнего участка шейки матки (экзоцервикса), а также с поверхности слизистой влагалища специальным шпателем (шпатель Эйра). Клетки канала шейки (цервикального канала) забирают с помощью эндобраша — цервикального зонда, что позволяет получить достаточное количество информативного материала.
Также врач может использовать такие инструменты для забора клеточного материала:
- Для мазка заднего свода шейки — шпатель Эйра.
- Аспирационный инструмент — спиретте, для забора эндоцервикального материала.
- Скринет также предназначен для забора биологического материала из цервикального канала.
- Cervex-Brush — стерильная медицинская щеточка для забора мазка с T-зоны (поверхности шейки и цервикального канала).
- Стандартный пинцет.
- Гинекологическое зеркало.
- Цервикальная двухсторонняя ложка (ложечка Фолькмана) для мазка на микрофлору слизистой цервикального канала и определения инфекционных заболеваний.
Все современные инструменты являются стерильными, большинство из них используются индивидуально для каждой женщины.
Техника проведения цитологии:
- Осмотр на гинекологическом кресле с помощью зеркал, в это же время производится забор материала на цитологию. Стенки влагалища расширяют, процедура мазка (соскоб) может доставить кратковременный легкий дискомфорт, но чаще всего цитология проходит безболезненно.
- Одновременно с проведением соскоба забирается и материал для бактериологического исследования (микрофлора). Совместно с цитологией может проводиться кольпоскопия, но это бывает только по показаниям, обычно эту процедуру назначают отдельно.
- Образцы материала наносятся на специальное стекло, закрепляются, фиксируются и передаются лаборанту для проведения точного микроскопического исследования с помощью окрашивания. Существует и новый метод цитологии шейки матки — жидкостный (ThinPrep), в этом случае материал помещается в колбу и также передается в лабораторию.
Очень важна маркировка анализа. В лабораторию должно поступать стекло с материалом и специальным бланком, где указываются такая информация:
- Номер стекла в соответствии с номером направления бланка.
- Название медицинского учреждения, где проводилась процедура.
- Дата анализа.
- ФИО пациента.
- Возраст пациента.
- Числа, даты последнего менструального цикла.
- Предварительный (клинический) диагноз.
Цитология шейки матки не занимает много времени, вся процедура длится не более 10-15 минут.
Что показывает цитология шейки матки?
Главные показатели цитологии шейки матки заключаются в двух словах – отрицательный или положительный результат, иными словами тест показывает, есть ли в мазке признаки онкологического заболевания, инфекционной, бактериальной, вирусной патологии.
Рассмотрим более подробно, что показывает анализ:
- Отрицательный результат означает, что клетки эпителия не подвергаются воздействию патологических процессов, патогенная флора не обнаружена, структура клеток не разрушена вирусами
- Положительные показатели говорят о том, что в слизистом покрове шейки матки выявлены аномальные клетки, их структура и количество выходят за рамки стандартных норм. Атипичные клеточные элементы могут быть разнообразными по форме, типу и размерам, соответственно трактовка анализа напрямую связана с этими критериями.
В современной гинекологической практике традиционной для пользования считается классификация результатов от автора теста, методика Папаниколау. Метод PAP-smear test предполагает детальное описание состава, структуры клеток, разделяя их на 5 категорий:
- Стадия I – клеточных изменений не обнаружено, атипии нет, что говорит о практически здоровом состоянии шейки матки. Цитологическая картина в пределах нормы
- Стадия II – тест обнаружил некоторое количество аномальных по структуре клеток с признаками воспаления, что может считаться относительной нормой, учитывая распространенность воспалительных процессов в половой сфере. Как правило, женщине назначаются дополнительные диагностические процедуры для уточнения причины, характера, стадии и возбудителя воспаления.
- Стадия III –анализ показывает наличие небольшого количества локально сгруппированных атипичных клеток, имеющих аномалии в строении ядра или цитоплазмы. Это также не является прямым указанием на угрожающую патологию, однако может быть сигналом о риске развития онкопроцесса. Дополнительной процедурой, уточняющей ПАП-тест, может быть морфологический анализ тканевого материала шейки матки (гистология). Биопсия помогает исключить риски или же подтвердить начало патологического процесса, который можно остановить своевременным лечением.
- Стадия IV -анализ показывает четкую картину злокачественных трансформаций небольшого количества клеток. Как правило, аномальные клетки имеют слишком большую ядерную массу, клеточное содержимое (цитоплазма), хромосомы также имеют признаки патологических изменений. Эта стадия указывает на возможное начало онкозаболевания (дисплазию). Уточнить диагноз помогают дополнительные обследования — кольпоскопию, забор материала на гистологию, возможна и повторная цитология.
- Стадия V -тест определяет довольно большое количество измененных клеток, что говорит о наличии онкопроцесса. В таких случаях результаты цитологии являются началом комплексного диагностического процесса, направленного на определение типа онкологии, ее стадии и вектора лечебных мероприятий.
Расшифровка результатов
Интерпретировать результаты теста может и должен только лечащий врач. Любая информация, добытая в недрах сети Internet, может быть только ознакомительной и первичной. Ниже приведенные данные являются общедоступными и помогут снизить тревогу женщин, опасающихся непонятных цифр и знаков в анализе.
Цитология шейки матки по статистке выявляет следующее:
- Каждый девятый тест из десяти определяет норму, то есть следующую цитологию можно смело проводить через 1-2 года для профилактики и скрининга состояния шейки матки. Анализ следует повторять регулярно, несмотря на хороший результат, так как он не может быть на 100% точным и не исключает риск заболеваний полностью.
- Каждый второй из ста мазков не является информативным в полной мере из-за нехватки биологического или клеточного материала. В таких случаях цитологию шейки матки повторяют
- Каждый двадцатый тест показывает наличие атипичные изменения, однако это вовсе не говорит о развившемся онкопроцессе. Скорее это сигнал и повод для более тщательного обследования и последующего лечения.
- Результат теста может показывать плохие показатели, но это не может считаться однозначным и окончательным диагнозом. Для уточнения характера патологического процесса и его прогнозов требуются дополнительные обследования, которые назначает врач.
Расшифровка результатов цитограммы может проводиться разными методами. Классическим является классификатор Папаниколау, однако в современной гинекологии также принято учитывать и другие варианты интерпретации теста, например, американскую систему Bethesda System.
Информацию о состоянии эпителиальной ткани шейки матки можно отразить в следующей таблице:
|
Наличие доброкачественных изменений |
Патологические изменения эпителиальной ткани: дисплазия, атипия |
Инвазивный рак |
|
|
Плоскоклеточный инвазивный рак |
|
Пациент нуждается в дополнительном обследовании, наблюдении и комплексном лечении. Также необходим скрининговый цитологический контроль |
Необходимы дополнительные диагностические процедуры |
Необходимо гистологическое исследование материала, возможно, уточнение диагноза после оперативного вмешательства |
Также вас могут ввести в тревожное состояние латинская аббревиатура в бланке анализа, хотя на самом деле все расшифровывается просто, по «территории» забора материала:
- Уретра — это буква U.
- Эндоцервикс, цервикальный канал — С.
- Влагалище – буква V.
Остальную информацию вам предоставит лечащий врач.

Нормы цитологии шейки матки
Нормой в цитологии шейки матки считается полное отсутствие атипичных изменений в клеточном материале, а также здоровое состояние микрофлоры. «Хорошие» клетки должны соответствовать нормам по морфологическим стандартам, то есть по размеру, содержимому (структуре) и форме. В цитограмме подробно описывается материал, взятый с поверхностного слоя шейки матки и из эндоцервикса.
Нормы цитологического обследования выглядят таким образом:
- Цитология шейки матки содержит клетки однослойного цилиндрического эпителия. Как вариант, тест может показать наличие эпителия многослойного (метаплазированного), это тоже считается нормой, если мазок был взят в переходном участке во влагалище.
- Многослойные эпителиальные клетки в мазке из участка влагалищной части шейки также считаются нормой, если в них не обнаружено никаких изменений.
- Любые отклонения от нормы, изменения в морфологии клеток описываются в заключении и могут быть показателями первичных воспалительных процессов, укладывающихся в рамки нормы.
- Отклонения от норм в ПАП-тесте не означает наличие онкологического процесса, за исключением показателя HSIL. Это говорит о высокой степени риска развития рака.
Также следует учитывать, что существуют показатели, указывающие на доброкачественные аномалии клеток. Это, конечно, не является нормой, однако и не может быть причиной для усиленной тревоги по поводу онкологии.
Перечень изменений в рамках относительной нормы, которые может показать цитология:
- Атипия воспалительной этиологии.
- Атипичные изменения, спровоцированные вирусом папилломы.
- Смешанные атипичные изменения.
- Атипичные отклонения неясной природы, требующие уточнения.
К процессам, при которых могут быть отклонения от нормальных границ, относятся следующие заболевания:
- ВПЧ — вирус папилломы человека.
- Герпес.
- Кандидоз.
- Трихомониаз.
- Беременность.
- Длительный прием лекарственных препаратов, особенно антибиотиков.
- Вагинит.
- Применение контрацептических средств (свечи, таблетки).
- Контрацепция с помощью спирали.
По классификации Траута и Папаниколау нормой цитологии шейки матки могут считаться первые 2 класса из пяти, а именно:
- I – нормальная цитологическая картина
- II — ASC-US или наличие атипичных клеток неуточненного значения
Относительной нормой может считаться класс III, где степень риска развития патологии обозначена как низкая.
Плохая цитология шейки матки
Что означают плохие результаты ПАП-теста?
Плохая цитология шейки матки не обязательно указывает на последнюю стадию рака. Точную расшифровку исследования может дать только специалист, то есть, гинеколог. Согласно общепринятой классификации плохая цитология — это патологические изменения в эпителиальном слое шейки и цервикального канала.
По общепринятой методике изменения обозначаются таким образом:
- 0 – материал для теста неудовлетворительный (некачественный, в малом количестве, неинформативный в силу недостаточной подготовки пациента).
- 1 класс – норма.
- 2 класс — наличие атипичных отклонений.
- 3 класс — различные степени дисплазии.
- 4 класс — предраковое состояние, начальная стадия.
- 5 класс — инвазивный рак.
Наиболее тревожным из вышеперечисленных изменений считается 5 класс, однако любая форма дисплазии также является опасным сигналом. Рассмотрим виды дисплазии более подробно:
- Легкая степень дисплазии — это признак начавшегося воспалительного процесса. Его нельзя пропускать, так как воспаление может протекать практически бессимптомно и в дальнейшем перейти в более тяжелую форму.
- Умеренная дисплазия — это уже угрожающий сигнал, свидетельствующий, что риск развития онкопроцесса очень велик.
- Тяжелая степень дисплазии — это практически предраковые состояния.
Недиагностированная дисплазия наряду с прочими провоцирующими факторами может привести к действительно опасному состоянию — онкопроцессу.
Любая женщина, узнав, что цитология шейки матки показывает плохой результат, испытывает страх. Попробуем немного снизить его уровень с помощью информирования.
Что делать, если тест показал наличие явных атипичных клеток?
Прежде всего не впадать в панику, а слушать и выполнять все назначения врача. Гинеколог обычно проводит подробное консультирование, как по поводу дополнительных диагностических процедур, так и по перспективе лечения и прогнозу заболевания.
Обычно назначаются и проводятся такие мероприятия:
- Повторная цитология шейки матки.
- Биопсия (гистологический анализ ткани пораженного участка шейки матки).
- Кольпоскопия.
- Выскабливание эпителия цервикса.
- Развернутый анализ крови.
- ВПЧ-тест.
- При выявлении дисплазии проводят ее лечение (чаще с помощью прижигания).
- Если определяется сопутствующая вирусная инфекция, лечат не только женщину, но и ее полового партнера.
Своевременная диагностика и адекватное лечение дают надежду на исцеление при условии соблюдения всех назначений врача и регулярном мониторинге состояния шейки матки.
Сколько дней делается цитология шейки матки?
Цитология шейки матки считается стандартной процедурой, технология которой отработана до мелочей. Период забора материала не превышает 15-20 минут, включая общий гинекологический осмотр. Далее анализ передается в лабораторию, где уже требуется более длительный отрезок времени для точного и тщательного микроскопического исследования. Если ПАП-тест проводился по всем правилам, процесс обработки материала займет около 8 дней. Результат можно будет узнать у лечащего врача спустя 2 недели после самой процедуры, иногда это происходит быстрее, если анализ проводится в режиме cito. Также случается, что информация о показателях теста может поступить и позже. Это чаще всего связано с дополнительными заборами, например, биохимический анализ секрета на микрофлору или биопсия по показаниям.
Гистологические исследования и кольпоскопия могут быть назначены в один и тот же день с цитологией, а их обработка займет немного больше времени, чем работа над одним ПАП-тестом. Такие комплексные диагностические мероприятия позволяют получить полную, развернутую картину и дают возможность точнее определиться с курсом лечения.
В заключение отметим, что цитология шейки матки должна быть обязательной процедурой для каждой женщины. Снижение количества случаев развития рака все еще остается неразрешенной задачей, как для врачей, так и для самих женщин. Своевременные, регулярные осмотры, анализы и тесты позволят быть уверенной в собственном здоровье. Сохранить все функции половой сферы в состоянии гармонии – эта задача решаема, в том числе и с помощью профилактических мер, среди которых важное место занимает цитология шейки матки.
Что такое цитология шейки матки? Как осуществляется взятие мазка на цитологическое исследование? Как правильно расшифровать результаты анализа? Что такое nilm,ASC-US, LSIL, HSIL, CIS, AGC, AIS в результатах цитологии? На эти и другие вопросы отвечает кандидат медицинских наук акушер-гинеколог Хоперская Ольга Викторовна.
Цитологическое исследование (цитология) является основным методом скрининговой оценки состояния эпителия шейки матки. Основная задача цитологического скрининга заключается в поиске измененных эпителиальных клеток (атипичных, имеющих отличное от нормальных эпителиальных клеток строение).
Термин «атипичные клетки» подразумевает как клетки с признаками дисплазии – легкой, умеренной или тяжелой (предраковые клетки), так и собственно раковые клетки. Разница между ними – в степени выраженности изменений в строении клеток.
Цитологический скрининг необходимо выполнять всем женщинам (исключая девственниц и пациенток, перенесших экстирпацию (удаление) матки), начиная с 21 года, заканчивая в 69 лет (при отсутствии в исследованиях изменений), регулярность сдачи анализа – 1 раз в год, согласно приказу 572н (1 ноября 2012), однако допустимо сдавать анализ 1 раз в три года (приказ МЗРФ №36 ан, от 3 февраля 2015).
В настоящее время существует две альтернативных методики фиксации и исследования биологического материала, ключевым отличием которых для пациентов является их эффективность.
ПАП-тест и жидкостная цитология
Забор материала осуществляется однотипно (стандартизированный забор): комбинированной щеткой или двумя цитологическими щеточками (рисунок 1), так как эпителий должен быть взят как с наружной вагинальной поверхности шейки матки (эктоцервикса), так и с внутренней – из цервикального канала (эндоцервикса). Необходимость забора клеточного материала из цервикального канала обусловлена тем, что зона стыка эпителиев (цилиндрического и многослойного плоского неороговевающего –места, где чаще всего начинаются «нехорошие» процессы (90-96%случаев)) с возрастом смещается ближе к центру и внутрь цервикального канала.
Рисунок 1 – Цитологические щетки (слева – комбинированная, справа – 2 цитологические щетки)
Рекомендуют осуществлять забор цитологического материала до бимануального (двуручного) вагинального обследования, кольпоскопии и ультразвукового исследования. Не следует сдавать мазки при наличии вагинита (воспалительного процесса во влагалище), в период его лечения, во время менструации. Также за двое суток необходимо половое воздержание.
Техника забора биоматериала:
- пациентка лежит на гинекологическом кресле;
- во влагалище вводят зеркало, визуализируя шейку матки;
- область наружного зева аккуратно промакивают ватным тампоном с целью удаления слизи;
- при использовании двух цитощеток: первую щетку располагают на влагалищной поверхности шейки матки и в экзоцервиксе и поворачивают на 360⁰ по часовой стрелке 5 раз, а вторую – в цервикальном канале на глубине около 2 см и поворачивают не менее 3 раз против часовой стрелки;
- при использовании комбинированной цитощетки: в цервикальный канал вводится центральная часть щетки, имеющая короткие щетинки, расположенные горизонтально, при этом длинные щетинки располагаются на влагалищной части шейки матки, щетку поворачивают по часовой стрелке 3 – 5 раз.
Отличия ПАП-теста и жидкостной цитологии
- В случае выполнения традиционного цитологического исследования (ПАП-теста) полученный материал распределяют на предварительно обезжиренном предметном стекле равномерным тонким слоем, что не всегда возможно, ввиду присутствия человеческого фактора (микропрепарат изготавливает непосредственно специалист), а также при наличии воспалительного процесса или кровянистых выделений (эпителиальные клетки часто могут быть заслонены нагромождениями лейкоцитов и эритроцитов и не видны под микроскопом). Ввиду вышесказанного, 10% мазков окажутся неинформативными, что потребует проведения повторного анализа. Кроме того, большая часть собранных клеток остается на цитощетках, для проведения дополнительных исследований (в случае получения сомнительного результата) будет необходим повторный забор.
- Чувствительность ПАП-теста (вероятность достоверного обнаружения «нездоровых» клеток) составляет 55-74%, а специфичность (гарантия того, что «нездоровые» клетки будут установлены при их присутствии в мазке) – 63,2 – 99,4%. Метод жидкостной цитологии имеет ряд преимуществ перед традиционным исследованием.
- При проведении жидкостной онкоцитологии забор материала всегда выполняется комбинированной цитологической щеточкой, собранный материал вместе со съемной щеточкой помещается в специальную емкость (виалу), заполненную стабилизирующим раствором, что предотвращает потерю биоматериала и обеспечивает его длительное хранение и выполнение дополнительных исследований в случае необходимости.
- Информативность жидкостной цитологии выше, что обеспечивается автоматической системой приготовления и окрашивания микропрепаратов, позволяющей расположить эпителиальные клетки в один слой, отделив их от других клеточных элементов. Оценка препаратов также производится автоматически при помощи системы CytoScreen.
- Количество неадекватных мазков при использовании жидкостной методики в 10 раз ниже, чем при использовании традиционной и не превышает 1%.
- Оставшийся в результате проведения жидкостной онкоцитологии биологический материал может впоследствии быть использован для дополнительных исследований, к примеру — иммуноцитохимического определения белка p16(INK4α) или определения высокоонкогенных типов вирусов папилломы человека.
В 99% случаев результат, полученный при использовании жидкостной цитологии, совпадает с результатами гистологического исследования.
Единственный недостаток метода – он не включен в систему обязательного медицинского страхования, т. е. анализ платный.
Результаты цитологии шейки матки
Согласно действующим клиническим рекомендациям от 2017 года, расшифровка результатов анализа должна проводиться по системе Бетесда, хотя можно встретить цитологическое заключение по системам Папаниколау, ВОЗ и CIN (гистологическая классификация). Сравнение систем приведено в таблице 1.
Таблица 1 — Соотношение классификаций предраковых поражений шейки матки
Клиническое значение будут иметь состояния определенные по терминологической системе Бетесда, поэтому, к примеру, умеренная дисплазия, тяжелая дисплазия и карцинома in situ = CIN II и CIN III = HSIL, и тактика ведения всех перечисленных состояний многослойного плоского эпителия будет одинакова (категория HSIL).
Расшифровка результатов
Итак, Вы держите в руках онкоцитологическое заключение. Расшифровка результата, а также выбор тактики ведения на его основании (с учетом возраста и особенностей образа жизни), должны проводиться не Вами, а Вашим лечащим врачом! Именно он направляет Вас на необходимые дополнительные исследования и выбирает тактику лечения, в случае необходимости. Но, кто из нас не заглянет в интернет, чтобы посмотреть, что же все-таки обозначают вынесенные в цитологическом заключении аббревиатуры и к чему готовиться? Думаю, любой переживающий о своем здоровье человек.
Ниже рассмотрим расшифровку аббревиатур терминологической системы Бетесда с ориентировочной (согласно действующим клиническим рекомендациям (2017) тактикой ведения.
Если изменены клетки плоского эпителия:
NILM
NILM (negative for intraepithelial lesion or malignancy) — негативный в отношении дисплазии или рака результат — это норма, совершенно исключающая возможность наличия атипических (измененных, с признаками возможного озлокачествления) клеток. Если Вы видите в своем заключении аббревиатуру NILM – поздравляю! Встречается подразделение негативного в отношении дисплазии или рака мазка на NILM 1 и NILM 2, имея в виду под первым абсолютную норму, а под вторым – сопутствующие реактивные (воспалительные) изменения в мазке, которые могут быть обусловлены, например, бактериальным вагинозом. Уточнить причину аббревиатуры NILM 2 в цитологическом заключении поможет мазок на флору или ПЦР – диагностика. В отношении же цитологического исследования беспокоиться не о чем. Показан рутинный (обычный) скрининг в соответствии с возрастом: не реже 1 раза в три года до 29 лет; не реже 1 раза в 5 лет в сочетании с ВПЧ-тестированием в возрасте старше 29 лет; и не реже 1 раза в 5 лет в сочетании с ВПЧ-тестированием в возрасте старше 29 лет.
ASC-US
ASC-US (atypical squamous cells of undetermined significance, клетки плоского эпителия с атипией неясного значения) – это наиболее частый из вариантов отклонений, встречающихся в цитологических заключениях. Суть заключается в том, что обнаружены клетки, отличающиеся по своему строению от нормальных, но утверждать, что отличия обусловлены именно дисплазией, а не другими причинами – реактивными состояниями (воспалительный процесс, гипоэстрогения), невозможно. Согласно данным статистики, гистологическая картина СIN III (дисплазия тяжелой степени) при данном цитологическом заключении встречается не чаще, чем в 2% случаев. Поэтому, волноваться не стоит. Зато стоит провести ВПЧ – тест (нужно отметить, что ASC-US не сопровождается ВПЧ – инфицированием лишь в одной трети случаев), и если он отрицательный — спокойно жить дальше, сдав через 1 – 3 года оба анализа (онкоцитологию и ВПЧ – тестирование).Если же ВПЧ будет обнаружен, врач назначит Вам кольпоскопию, по результатам которой возможно и взятие биопсии (участка ткани шейки матки). При отсутствии кольпоскопических изменений через год будет необходимо повторить цитологическое исследование и ВПЧ – тестирование.Возможна и иная тактика: повторное цитологическое исследование через год. Если снова получено заключение «ASC-US» – кольпоскопия и ВПЧ – тестирование, а если «NILM» — дополнительных исследований не требуется и можно жить спокойно до очередного скрининга.
ASC-Н
ASC-Н (atypical squamous cells, cannot exclude HSIL, клетки плоского эпителия с атипией неясного значения не исключающие HSIL) – здесь также обнаружены измененные клетки, но вероятная причина их появления – дисплазия. Врач назначит Вам и кольпоскопию с биопсией и ВПЧ – тестирование, дальнейшая тактика будет определена в зависимости от полученных результатов.
LSIL
LSIL (low grade squamous intraepithelial lesion, плоскоклеточное интраэпителиальное поражение низкой степени) – в исследуемом материале обнаружены атипичные клетки, соответствующие диспластическим изменениям легкой степени. Врач направит Вас на ВПЧ – тестирование и, при положительном тесте – на кольпоскопическое исследование, где, возможно, будет выполнена и биопсия. При отрицательном ВПЧ — тесте цитологическое исследование и ВПЧ тестирование нужно будет пройти через год. Подробнее о ВПЧ читайте в статье Обнаружен ВПЧ (вирус папилломы человека)!
HSIL
HSIL (high grade squamous intraepitelial lesion, плоскоклеточное интраэпителиальное поражение высокой степени) – в мазке обнаружены атипичные клетки, соответствующие диспластическим изменениям тяжелой степени. Врач направит Вас на кольпоскопическое исследование и эксцизию (иссечение участка измененной ткани петлей) / конизацию (удаление конусовидного участка шейки матки включая влагалищную поверхность и нижнюю часть цервикального канала) с последующим гистологическим исследованием полученного биоматериала. К категории HSIL по классификации Бетесда относится и карцинома in situ (см. таблицу 1, описательная система ВОЗ).
CIS
CIS (carcinoma in situ, карцинома «in situ» — внутриэпителиальный рак) – в препарате определяются злокачественно измененные клетки плоского эпителия. Данная аббревиатура предполагает, что патологический процесс не выходит за пределы эпителия, базальная мембрана не повреждена, подлежащая строма не вовлечена, что и отличает карциному «in situ» от инвазивного (проникающего в подлежащие ткани) рака. (Подробнее читайте в статье Рак шейки матки)
Однако цитологическое исследование не дает представления о пространственном расположении клеток с признаками атипии, установить глубину проникновения патологического процесса в ткани позволяет только гистологическое исследование.
Если изменены клетки цилиндрического эпителия:
AGC
AGC (atypical glandular cells, атипичные клетки железистого эпителия) — наличие в собранном материале измененных клеток цилиндрического эпителия, что в большинстве случаев означает расположение патологического процесса внутри цервикального канала.
AIS
AIS (adenocarcinoma in situ, эндоцервикальная аденокарцинома «in situ» (с латинского — «на месте»)) —наличие злокачественно измененных клеток цилиндрического эпителия. Как и в случае СIS, предполагается, что патологический процесс не выходит за пределы эпителия и базальная мембрана не повреждена. Но мы помним, что онкоцитологическое исследование не может определить глубину поражения тканей. Она лишь оценивает уровень злокачественных изменений в клетках, по которым и устанавливает степень дисплазии или определяет атипичные клетки, как злокачественные. Помимо ВПЧ – тестирования и кольпоскопии лечащий врач назначит Вам выскабливание цервикального канала, а если Вы старше 35 лет, то и аспирационную биопсию эндометрия, для получения гистологического заключения о глубине поражения и исключения патологического процесса в полости матки.
Вышеприведенные тактики ведения в зависимости от результатов цитологических исследований ориентировочны. Тактику ведения в каждом конкретном случае определяет лечащий врач, учитывая индивидуальные характеристики пациента (возраст, наличие или отсутствие детей, сопутствующие заболевания, факт инфицирования ВПЧ, личные качества).
Дорогие девушки, женщины, призываю Вас регулярно проводить цитологическое исследование и желаю получать исключительно «NILM» в заключении.
Ещё больше интересного и полезного про здоровье, лекарства и болезни в нашем телеграм-канале
Подписывайтесь, чтобы ничего не пропустить!
Афанасьев Максим Станиславович.
Д.м.н., профессор Сеченовского университета, онколог, хирург, онкогинеколог, гинеколог-иммунолог, эксперт по лечению дисплазии, предраковых и опухолевых заболеваний шейки матки.
«В июне мне поставили диагноз «дисплазия шейки матки 1 стадии». Мой гинеколог сказала, что лечение легкой дисплазии шейки матки не требуется, она пройдет самостоятельно.
В июле того же года уточненный диагноз выглядел уже так: «дисплазия шейки матки 3 степени». В августе – «рак ин ситу»… Тогда, в одном шаге от рака, мне очень повезло – я нашла в интернете публикации Максима Станиславовича и прошла у него лечение.
Пусть мой случай послужит примером того, каким стремительным может быть развитие дисплазии, и у вас может не быть в запасе нескольких лет, о которых так любят говорить гинекологи на приеме».
Ольга, 37 лет.
Многие мои пациентки приходят ко мне с похожей историей. Я написал эту статью, чтобы развеять некоторые укоренившиеся заблуждения по поводу дисплазии 1 и ответить на непростой вопрос, нужно ли ее лечить.
Дисплазия дисплазии рознь.
Это заболевание вызывается разными причинами. И если в одних случаях наблюдательная тактика действительно может закончиться самоизлечением, то в других случаях дисплазия переходит в тяжелые формы, которые считаются предвестниками рака.
Я расскажу, как понять, опасная у вас дисплазия, или нет. И при наличии показаний настоятельно призываю активно ее лечить.
Современный безоперационный метод фотодинамической терапии (ФДТ), который я применяю в своей практике, позволяет надежно избавиться от атипичных клеток и от вируса папилломы человека, остановить прогрессирование дисплазии и переход ее в рак.
Что такое дисплазия шейки матки
Дисплазия – это изменение клеток плоского эпителия шейки матки и появление так называемых атипичных клеток. Такие клетки имеют увеличенное бесформенное ядро или множество ядер, активно делятся, нарушается их правильное расположение в эпителии и способность выполнять заложенную природой функцию. Именно гигантские ядра и активное деление ищет цитолог, когда рассматривает ваш мазок на атипические клетки (PAP-тест).
|
|
| Нормальная клетка плоского эпителия и атипические клетки с увеличенными ядрами. |
Причины атипии клеток можно условно разделить на бактериальные и вирусные.
Бактериальная дисплазия первой степени по своей сути – это хроническое воспаление шейки матки (цервицит, кольпит). Клеточные изменения в этом случае вызываются агрессивной средой. Такая форма дисплазии не требует онкологической настороженности. После правильного противовоспалительного лечения размер ядер и форма клеток возвращаются в норму.
И совсем другое дело, если клетка заражается вирусом папилломы человека (ВПЧ) высокого онкогенного риска.
Вирус в эпителии может существовать в двух формах – в «спящем» и активном состоянии. В момент ослабления иммунитета ВПЧ переходит в агрессивную стадию, генетический материал вируса встраивается в ДНК клетки и запускает развитие болезни.
Обычно такие дефектные клетки с измененной ДНК организм ремонтирует или уничтожает. Но вирус папилломы «выключает» сигнализацию, и поломанная клетка теряет возможность сообщить «ремонтным бригадам» о своей болезни. Наша иммунная система продолжает воспринимать ее как здоровую, поэтому не препятствует делению и трансформации.
|
|
Встроенный в ДНК вирус активно воспроизводит сам себя, стимулирует клетку активно делиться, с каждым делением повреждения накапливаются.
Так заболевание прогрессирует до дисплазии умеренной и тяжелой степени, которые уже относятся к предраковым заболеваниям шейки матки и требуют лечения у онкогинеколога. Этот же механизм лежит в основе развития рака шейки матки.
Признаки слабой дисплазии шейки матки: какие симптомы должны вас насторожить
Дисплазия не имеет симптомов. Это основная причина, по которой вы минимум один раз в год должны посещать своего гинеколога, даже если у вас нет никаких жалоб.
Иногда на фоне дисплазии наблюдаются выделения необычного цвета и запаха, зуд и жжение, но эти симптомы не являются проявлением дисплазии и лишь показывают наличие сопутствующего воспаления.
Что такое LSIL шейки матки и CIN 1
Исторически сложилось так, что у дисплазии 1 степени много названий. Одна из причин – богатство эпитетов русского языка. Это все одно и то же заболевание:
- слабо выраженная дисплазия шейки матки,
- дисплазия 0 степени,
- дисплазия эпителия низкой степени,
- слабая дисплазия плоского эпителия,
- начальная стадия дисплазии,
- дисплазия легкой степени,
- дисплазия 1 типа,
- небольшая дисплазия и т.д.
Вторая причина состоит в том, что диагноз «дисплазия 1» много раз меняла свое официальное название. До 1988 года международным названием дисплазии была Cervical Intraepithelial Neoplasia – цервикальная интраэпителиальная неоплазия шейки матки 1 степени. Сокращенно CIN I, или ЦИН 1 шейки матки.
Но так как термин «неоплазия» означает «новообразование», то есть опухоль, название скорректировали. Современное международное название этого заболевания LSIL – low grade squamous intraepithelial lesion – низкая степень интраэпителиального поражения. Термин «поражение» более точно отражает характер изменения клеток.
В отличие от LSIL, дисплазия тяжелой степени с обширным поражением эпителия называется HSIL – high grade squamous intraepithelial lesion – высокая степень плоскоклеточного интраэпителиального поражения. В группу HSIL включают умеренную дисплазию и рак «на месте» (рак «in situ»).
Нужно запомнить, что сейчас заболевание называется LSIL. И только так.
Но так как гинекологи до сих пор используют самые разнообразные формулировки, то же самое позволим себе и мы.
Правильная диагностика дисплазии 1 степени: как держать заболевание под контролем
Чтобы обнаружить дисплазию вовремя, вам нужно посещать гинеколога хотя бы один раз в год, а с 21 лет в обязательном порядке проводить дополнительные исследования.
Вот инструкция, что нужно делать и для чего.
ШАГ 1. Осмотр гинеколога. Он называется осмотром в зеркалах.
Часто ограничиваются только этим этапом, и тогда в медицинской карте вместо вызывающего настороженность подозрения на LSIL может появиться диагноз «эрозия шейки матки». Действительно, в этом случае даже подготовленный специалист не всегда может «на глаз» отличить одно от другого.
Главное в этом случае – не начинать активное лечение эрозии, так как оно может ускорить процесс перехода слабовыраженной дисплазия шейки матки в тяжелую форму. Нужно пройти дополнительные исследования, чтобы исключить присутствие атипических клеток и ВПЧ.
ШАГ 2. Мазок из шейки матки на цитологическое исследование.
Второе название этого анализа – ПАП тест (PAP тест).
Анализ на выявление/исключение атипических клеток проходит несколько этапов, и крайне важно соблюсти технологию проведения анализа на каждом из них.
Цитологическое исследование начинается не в лаборатории, а в кабинете вашего гинеколога, и первый его этап – правильный забор материала.
Мазок из шейки матки берется специальной щеткой – такой, как на иллюстрации. Это очень важно! Только такая щетка позволяет взять клетки для анализа со всей окружности шейки матки и из цервикального канала. Это существенно снижает вероятность, что какой-либо измененный участок будет пропущен.
Раньше для этой цели использовались шпатели. Сегодня они уже не актуальны.
|
|
| Так выглядит самая лучшая щетка для забора мазка с шейки матки на атипичные клетки. |
|
|
| Такая щетка позволяет взять клетки для анализа со всей окружности шейки матки и из цервикального канала. |
Вторым этапом мазок наносится на стекло и отправляется в лабораторию цитологу, который окрасит его и определит наличие или отсутствие атипичных клеток. При дисплазии 1 цитолог в заключении напишет «цитограмма соответствует LSIL», или «плоский эпителий с явлениями LSIL».
Будет лучше, если вы сдадите не классический ПАП-тест, а мазок из цервикального канала методом жидкостной цитологии. Он считается самым достоверным. В этом случае содержимое щетки не наносится на стекло. Головка щетки целиком погружается в контейнер со специальным раствором и отправляется в лабораторию.
Для большей достоверности рекомендую проводить цитологической исследование методом ЖИДКОСТНОЙ ЦИТОЛОГИИ.
|
|
| При выполнении жидкостной цитологии в лабораторию в специальном растворе отправляется наконечник щеточки целиком. |
Согласно письму МЗ РФ от 2 ноября 2017 г. N 15-4/10/2-7676 О направлении клинических рекомендаций (протокола лечения) «Доброкачественные и предраковые заболевания шейки матки с позиции профилактики рака», при отсутствии в мазке атипических клеток его рекомендуется сдавать 1 раз в 3 года.
Через призму своего опыта не могу с этим согласиться и рекомендую делать цитологический мазок 1 раз в год.
По разным причинам достоверность цитологического анализа для дисплазии легкой формы составляет от 60 до 90%. В моей практике много девушек 20-30 лет с раком ин ситу, и женщин до 40 лет с инвазивным раком шейки матки, которые регулярно проходили цитологическое обследование один раз в три года. Если бы цитология сдавалась 1 раз в год, такого развития событий можно было бы избежать – «перехватить» и пролечить заболевание на безопасной стадии дисплазии.
Многие мои коллеги также отмечают тот факт, что между впервые выявленной лёгкой дисплазией (LSIL) и CIN III (HSIL) проходит всего лишь несколько месяцев.
ШАГ 3. Расширенная кольпоскопия.
Это осмотр шейки матки под микроскопом, в ходе которого шейка окрашивается специальными растворами.
Важно понимать, что диагноз «дисплазия I степени» не ставится ни на основании осмотра, ни на основании кольпоскопии. Но кольпоскопия дает гинекологу много сопутствующей информации и позволяет установить диагноз более точно. Например, показывает плоские кондиломы и подозрительные участки на шейке матки, которые еще до появления визуальных проявлений дисплазии могут говорить об опасной вирусной природе заболевания.
Чтобы увидеть проблемные участки, шейка матки окрашивается последовательно уксусом и раствором Люголя. После обработки раствором уксусной кислоты на эпителии влагалищной части шейки матки появляются белесые участки (так называемый уксусно-белый эпителий). Обработанные уксусной кислотой участки окрашиваются Люголем. Проблемные зоны также прокрашиваются неравномерно – видны так называемые «йод негативные зоны». Это первые признаки дисплазии, вызванной ВПЧ.
|
|
| Белесые участки на шейке матки после обработки уксусным раствором (слева) и неравномерное окрашивание шейки матки после обработки раствором Люголя (справа). Здоровая шейка матки окрашивается равномерно. |
Не связанные с ВПЧ заболевания проявляются по-другому: шейка матки приобретает избыточно яркий оттенок или покрывается большим количеством «пузырьков» (кист).
Обработка эпителия шейки матки уксусной кислотой и раствором Люголя – абсолютно безвредная для здоровья процедура.
Обычно кольпоскопию рекомендуют делать только после выявления атипических клеток в цитологическом мазке (смотрите ШАГ 2) или после выявления ВПЧ высокого онкогенного риска (ШАГ 4). Но практика показывает, что зачастую цитологический мазок показывает отсутствие атипии даже при ее наличии. И только кольпоскопия позволяет заподозрить неладное.
Поэтому я настоятельно рекомендую делать расширенную кольпоскопию ежегодно.
ШАГ 4. Определение вирусной нагрузки.
Если в цитологическом мазке выявляются атипические клетки, необходимо продолжить обследование и подтвердить вирусную причину изменения клеток – сдать жидкостной Digene-тест на количественное определение вирусных частиц ВПЧ-инфекции.
Если вам исполнилось 30 лет, этот анализ нужно сдавать один раз в год вне зависимости от результата цитологического исследования.
Дело в том, что ВПЧ в каком-то количестве присутствует практически у каждого из нас. И только превышение нормы позволяет говорить об активности вируса и оценить ее.
Поэтому я не могу согласиться с рекомендацией все того же Письма МЗ РФ от 02.11.2017 года № 15-4/10/2-7676 о необходимости качественных тестов на ВПЧ.
Качественный тест на определение ВПЧ высокого онкогенного риска не является информативным. Он показывает только присутствие или отсутствие вируса в эпителии. Но факт его наличия не несет никакой значимой информации – ВПЧ присутствует у 80-90% людей, и у подавляющего большинства не вызывает заболевания. Поэтому я не вижу очевидной необходимости сдавать мазок на ПЦР.
Digene-тест относится к количественным методам исследования и является значительно более информативным. Он определяет так называемую вирусную нагрузку. Только если результат Digene-теста отрицательный (когда вирусная нагрузка менее 0,8 единиц), можно говорить, что начальная дисплазия вызвана инфекцией без участия вируса папилломы и она не требует особого противоопухолевого лечения. Достаточно будет вылечить воспаление. Только в случае сочетания с эктопией или псевдоэрозией шейки матки, возможно, потребуется «прижигание» лазером или радиоволной (Сургитроном, Фотеком).
Если наряду с выявленными ранее атипическими клетками количественный анализ показывает превышение нормального порога по ВПЧ высокого онкогенного риска, можно обоснованно говорить, что состояние дисплазии имеет вирусную природу. Обычно при ЦИН1 количественный анализ показывает более высокие значения ВПЧ, чем при любом другом виде дисплазии. Вопреки литературным данным, такое состояние не подлежит самоизлечению и рано или поздно прогрессирует в HSIL и инвазивный рак.
Иммунитет организма достаточно силен, чтобы долго сдерживать активность вируса и «перерождение» дисплазии в опухоль. Но мои наблюдения последних 10 лет показывают, что из легкой стадии в тяжелую и даже в инвазивный рак дисплазия в ряде случаев переходит менее чем за 12 месяцев.
Поэтому при наличии в клетках атипии и высоких значений вируса папилломы я настоятельно советую своим пациенткам выполнить лечение дисплазии 1 степени безоперационным методом фотодинамической терапии.
Не стоит успокаиваться «нестрашным» диагнозом «дисплазия шейки матки низкой степени» и упускать время в ожидании, когда само пройдет.
Есть и еще одно показание. Изредка бывает так, что при наличии атипичных клеток Digene-тест не выявляет папилломавирус. Дело в том, что вирусы трансформируются, постоянно появляются новые серотипы вируса папилломы, не известные существующим тест-системам.
При этом кольпоскопия выявляет плоскую кондилому на наружных или внутренних половых органах или лейкоплакию на сводах влагалища. Оба эти заболевания однозначно имеют вирусную природу. Они говорят о присутствии вируса в организме и его высокой активности. Соответственно, наличие атипических клеток на их фоне должно вызывать онкологическую настороженность. В этом случае отсутствие в анализе папилломавируса не является основанием для отказа от фотодинамического лечения дисплазии шейки матки легкой степени.
ШАГ 5. Иммуногистохимическое определение экспрессии белка p16
Это анализ, материал для которого берется из того же контейнера, что и для Digene-теста.
p16 – белок, который появляется в стареющих клетках и говорит иммунной системе о необходимости отправить клетку на утилизацию. Обычно опухолевые клетки пытаются подавить экспрессию p16, чтобы начать бесконтрольно делиться. Но вопреки логике, в клетках, подвергшихся трансформирующему действию ВПЧ, отмечается увеличение экспрессии данного белка, что служит признаком перехода вируса в активную фазу и интеграции ДНК вируса высокого онкогенного риска в геном клетки. Так как этот процесс необратим, анализ на p16 является маркером запуска канцерогенеза.
При наличии атипических клеток или подозрительной картине расширенной кольпоскопии я считаю этот анализ обязательным. Он является определяющим тестом в выборе тактики и метода лечения дисплазии.
Определение белка p16 НЕ ПРОВОДИТСЯ при нормальном заключении цитограммы при отсутствии атипических клеток.
Положительный анализ на p16 на фоне CIN I — II говорит о том, что клетки уже подверглись трансформации вирусом. Такое изменение клеток необратимо – активный вирус делает клетку невидимой для радаров иммунной системы.
Именно поэтому положительный результат этого анализа говорит о настойчивой необходимости незамедлительного лечения даже дисплазии легкой степени. Дальше заболевание будет только прогрессировать. Наблюдательная тактика на фоне экспрессии p16 губительна, и рекомендация «подождать-понаблюдать» может привести к раку ин ситу. Лечиться необходимо.
Наличие атипических клеток и выявленная экспрессия белка p16 – ОБЪЕКТИВНОЕ ПОКАЗАНИЕ к проведению лечения методом фотодинамической терапии.
ШАГ 6. Биопсия.
Биопсия – это забор небольшого кусочка ткани шейки матки для гистологического исследования. Этот анализ более информативен, чем цитологическое исследование. Но так как процедура забора материала считается травматичной, то необходимость биопсии определяется лечащим врачом индивидуально. Обычно она требуется при подозрении на тяжелую степень дисплазии.
Легкая дисплазия шейки матки 1 степени может очень быстро перейти в тяжелую дисплазию
Зачем нужно лечить ВПЧ-ассоциированную дисплазию 1 степени, если не понятно, перейдет она в тяжелую дисплазию, или нет? Из литературы нам известно, что самоизлечение от ВПЧ возможно даже для серотипов высокого онкогенного риска. Но по нашему наблюдению не все так оптимистично.
Если диагностика не включает те пять обязательных этапов, о которых я написал выше, то на основании только осмотра и отрицательного цитологического заключения часто ставится неверный диагноз.
Я постарался выделить основные причины, почему врач может пропустить серьезное заболевание или недооценить риски.
|
|
| Трансформация клеток начинается в глубоком базальном слое, и атипические клетки на начальных стадиях дисплазии могут не попадать в цитологический мазок. |
Причина 1. Мой опыт показывает, что часто «дисплазия 1» – не всегда верно поставленный диагноз. Вирусом поражаются самые глубокие слои эпителия шейки матки – базальные клетки. Так как атипические клетки начинают свое развитие на глубине и постепенно «поднимаются», зачастую оценить стадию процесса глазом невозможно даже при использовании кольпоскопа. А цитологическая щеточка «собирает» материал только из верхних слоев эпителия.
Поэтому на фоне хорошей кольпоскопии и цитологии часто бывает так, что после взятия биопсии – кусочка ткани, который позволяет оценить проблему на всей ее глубине, от эпителиального до базального слоя, – диагноз ухудшается до предракового HSIL.
Причина 2. Раньше дисплазия легкой степени считалась фоновым процессом. К истинному предраку относили только 2 и 3 степени. Считалось, что переход с одной стадию на другую занимает около 3-5 лет.
На самом деле, невозможно дать прогноз о скорости прогрессирования дисплазии. Мои наблюдения и наблюдения коллег показывают, что вирусные поражения сегодня гораздо быстрее проходят все стадии, и процесс опухолевого роста может начаться в пределах 12 месяцев после постановки диагноза «дисплазия 1».
Чтобы не быть голословным, предлагаю ознакомиться с сообщением из форума woman.ru:
«Летом в июле поставили диагноз «дисплазия 1-2 степени», пропили курсы противовирусных препаратов и свечей, в декабре сделали ДЭК (диатермоэлектрокоагуляцию) и отправили материал на биопсию. Пришло «дисплазия тяжелой степени с переходом в плоскоклеточный рак шейки матки». Я в ужасе, в шоке… Не сплю (вообще!) уже дня 4. Как за 5 месяцев с 1 степени в тяжелую?…
…
Что делать?! Лечится ли это? Собираем всё для онкодиспансера, делаем вот уже 4 дня все платные анализы, УЗИ, ФГДС и др.
У меня двое детей, очень боюсь не увидеть, как они закончат школу… Сижу, реву».
Думаю, что все-таки не стоит проверять на себе скорость прогрессирования вирусной дисплазии.
Причина 3. Я уже говорил, что дисплазия зарождается в глубоком базальном слое клеток. При лечении популярным сегодня методом щадящей эксцизии у нерожавших женщин хирург старается удалить минимальный объем тканей. И если после операции в этом слое остаются зараженные вирусом клетки, они с высокой вероятностью могут дать рецидив дисплазии с переходом ее в более тяжелую стадию.
Причина 4. Любая инфекция – не важно, вирусная или бактериальная, – имеет длительный период скрытого течения. Этот период называется персистенцией, когда вирус присутствует в клетке в «спящем» состоянии. Невозможно предсказать момент ослабления иммунитета, который послужит толчком к пробуждению вируса и развитию болезни. Это может быть и обычная простуда, и пережитый стресс. Иммунитет снижают даже сильные положительные эмоции. Тогда персистирующий ВПЧ высокого онкогенного риска встраивается в ДНК клетки и начинает ее трансформацию.
Возможно, что на момент осмотра у врача вирус уже перешел в активную форму, но повреждения еще не накопили критическую массу, они почти не заметны глазу или не вызывают подозрений.
Причина 5. Разные штаммы папилломавируса имеют разную степень агрессии, которую также невозможно предсказать по результатам осмотра или цитологического анализа. И там, где один штамм будет годами персистировать, второй за несколько месяцев трансформирует клетку сначала – в атипическую, а потом – в раковую.
Без уточняющих исследований невозможно дать никакой гарантии, что ваша дисплазия будет вести себя спокойно, и что через год в своем заключении цитолог не напишет ничего хуже «LSIL».
Причина 6. Если дисплазия 1 вызывается вирусом папилломы человека высокого онкогенного риска, и вирус встроился в ДНК клетки, в своей практике я не наблюдал ни одного случая самоизлечения – дисплазия всегда прогрессирует.
К вирусам высокого онкогенного риска относятся серотипы 16, 18, 31, 33, 35, 39, 45, 51, 52 и 56. Самые опасные – 16 и 18 серотипы вируса, они являются причиной тяжелой дисплазии и рака шейки матки в 80% случаев.
Я смотрю на вирусную дисплазию системно, вне зависимости от ее степени.
Учитывая тот момент, что самостоятельный регресс легкой дисплазии исключить нельзя, при отсутствии кольпоскопических признаков ВПЧ инфекции я склоняюсь к наблюдению.
Если же CIN I сопутствуют очевидные вирусные признаки папилломавирусной инфекции (плоская кондилома, уксусно-белый эпителий, экспрессия белка p16) – то обязательно рекомендую проводить лечение безоперационным методом ФДТ.
Потому что при таком сочетании отягчающих факторов времени на раздумья у нас может просто не быть.
Отзыв о лечении от Елизаветы, г. Ярославль
Уважаемый Максим Станиславович, оставляя этот отзыв, сначала хочу рассказать с чего началась моя история. Итак, я пришла на профилактический прием к гинекологу, врач заметила изменения на матке, узнав результаты анализов, стало понятно, что у меня ВПЧ и дисплазия первой степени… Врач дала рекомендацию, чтобы я снова прошла обследование спустя полгода, НО я, не понимая серьезности данной ситуации, пришла через год уже к платному врачу-гинекологу. Сдала анализы, диагноз был таков, cr in situ. Врач предложила два варианта либо коанизацию, либо инновационный мпетод ФДТ, но, чтобы не травмировать молодой организм (мне 23 года) настаивала на ФДТ. После этого я начала шерстить интернет в поисках лучшего врача, и тут нашла именно Вас, с огромным опытом, а самое главное с большим количеством положительных отзывов от вылеченных пациенток. Без сомнений выбрала Вас, после этого связалась с администратором Оксаной, и буквально в течение двух дней мне назначили дату ФДТ, что очень удобно, ведь я живу в г. Ярославль. Приехав в Москву в клинику, я ощутила высочайший уровень сервиса.
Эту историю я написала ради того. Чтобы высказать слова благодарности и для того, чтобы девушки с такой же проблемой, не сомневаясь, шли именно к Вам, потому что Вы квалифицированный и грамотный врач, который нацелен на результат.
Какие причины увеличивают риск развития дисплазии
Возникает закономерный вопрос, почему после заражения вирусом папилломы – а его носителями по разным данным являются до 95% населения планеты – лишь единицы из них столкнутся с заболеванием? Какие факторы дают возможность вирусу выйти из «спящего» состояния и начать активное деление?
Иммунитет может долго сдерживать развитие вируса в клетке. Но на фоне ослабления иммунитета вирус переходит в активное состояние. Вот основные факторы риска:
1. Стресс. Эмоциональные переживания снижают иммунитет, и даже сильные положительные эмоции являются стрессом для организма.
2. Псевдоэрозия (эктопия) шейки матки – это физиологическая особенность организма, которая тем не менее создает благоприятные условия для инфицирования большим количеством вируса. Этому риску наиболее подвержены молодые женщины с неустановленными стабильными отношениями с противоположным полом.
3. Воспалительные заболевания (кольпит, цервицит). Эндометрий влагалища и шейки матки выполняет функцию кожи – защищает от инфекций. Воспалительные заболевания не только снижают его барьерную способность, но я являются благоприятным условием для прогрессирования вируса. Поэтому женщины с часто возникающими воспалениями относятся к группе риска по развитию дисплазии.
4. Курение. Никотин сам по себе является одним из самых сильных канцерогенов, а его концентрация в слизи цервикального канала зачастую значительно выше, чем в крови. Второй фактор канцерогенного действия сигареты – смолы. Они радикально меняют свойства слизи влагалища и цервикальной пробки, ослабляют местный иммунитет и делают эпителий крайне уязвимым пред ВПЧ и другой инфекцией.
5. Наследственность. Генетическая предрасположенность к развитию атипических процессов, которая зачастую может реализовываться даже без участия ВПЧ. Вам нужно быть особенно внимательной к себе, если ваши прямые родственницы имеют диагноз «дисплазия шейки матки» или «рак шейки матки».
6. ВПЧ высокого онкогенного риска. Эти серотипы увеличивают риск развития дисплазии, так как лучше других вирусов приспособлены к защите от подавления иммунной системой.
Почему лечение дисплазии шейки матки 1 степени классическими методами зачастую заканчивается рецидивом
Согласно рекомендациям Минздрава, лечение CIN 1 не проводится. Если биопсия подтверждает дисплазию слабой степени, женщину отпускают под наблюдение – считается, что в 90% случаев выздоровление наступает самопроизвольно и лечение ЦИН 1 не требуется.
Сама биопсия (кусочек ткани шейки матки) в случае CIN I уже может оказаться не только диагностической, но и лечебной процедурой, когда пораженный участок удаляется вместе с забранным материалом.
При отсутствии кольпоскопических признаков ВПЧ инфекции и нормальной вирусной нагрузке я также склоняюсь к наблюдению LSIL.
В некоторых случаях на фоне легкой дисплазии назначается лазерная абляция (прижигание) эпителия или радиоволновая эксцизия – удаление участка пораженной ткани.
Но иногда, вопреки всем рекомендациям, при LSIL выполняется конизация и даже удаление всех гениталий (когда дисплазия сочетается, например, с миомой матки). Я расцениваю такой подход как неоправданный лечебный риск – это когда риск проводимого лечения превышает риск самого заболевания.
Дело в том, что и биопсия, и эксцизия, и конизация, и удаление гениталий позволяют устранить диспластический эпителий. Но причина вирусной дисплазии – ВПЧ – остаётся. А так как любое лечебное воздействие само по себе является для вируса провоцирующим фактором, это приводит к высокому проценту рецидивов.
Противовирусные препараты сегодня не показывают эффекта в подавлении вируса, поэтому целесообразность их назначение остается под большим сомнением.
Минздрав рекомендуют начинать лечение только в том случае, если дисплазия LSIL переходит в стадию HSIL.
С такой тактикой я тоже не могу согласиться.
Запомните!
- если в цитологическом анализе обнаружены атипические клетки,
- если CIN I по данным кольпоскопии сопутствуют очевидные вирусные признаки папилломавирусной инфекции,
- если иммуногистохимическое исследование показывает экспрессию белка р16,
ТО ПРИМЕНЕНИЕ НАБЛЮДАТЕЛЬНОЙ ТАКТИКИ ВАМ ПРОТИВОПОКАЗАНО!
Эти факторы говорят об активном процессе и требуют незамедлительного лечения.
Международное медицинское сообщество особенно акцентирует внимание на том, что любой случай инвазивного рака шейки матки – всегда есть упущенная возможность своевременной диагностики и лечения дисплазии.
И свою первоочередную задачу я вижу в том, чтобы не дать всем думающим женщинам пополнить статистику упущенных возможностей.
Как лечить дисплазию шейки матки 1 степени, чтобы избежать рецидива
Можно ли вылечить дисплазию 1 степени? Можно, и сделать это можно без операции.
В отличие от конизации, фотодинамическая терапия – это нетравматичный терапевтический метод. Он прицельно воздействует на дисплазию сразу в нескольких направлениях:
1. разрушает атипичные клетки,
2. уничтожает пораженные ВПЧ клетки в слизистой шейки и цервикального канала,
3. уничтожает сопутствующую инфекцию (цервицит).
ФДТ полностью уничтожает клетки, пораженные вирусом папилломы человека, что служит надежной профилактикой предрака шейки матки. Ведущий онкологический институт Росси, МНИОИ им. Герцена рекомендует лечение ВПЧ-инфекции методом ФДТ в качестве профилактики рецидива дисплазии.
Используя для лечения ФДТ, мы сохраняем целостность шейки и матки – то есть, полноценный орган для самостоятельного зачатия, вынашивания и здоровых родов. Сохраняя целостность органа, мы сохраняем и его врожденную систему собственного иммунитета – здоровая шейка надежно защищает себя и матку от инфекций.
Поэтому не торопитесь принимать решение в пользу хирургического метода конизации – сделать операцию вы всегда успеете.
Как проходит лечение LSIL методом ФДТ предлагаю прочитать здесь.
Можно ли выздороветь без лечения CIN I: мифы и реальность
В гинекологии принят постулат, что дисплазия шейки матки 1 степени самопроизвольно регрессирует в течение года у 95% пациенток. И с одной стороны я готов подписаться под этой цифрой.
Но с другой стороны, когда говорят о самоэлиминации (самоустранении) вируса, очень важно понимать, что под этим имеют в виду. Давайте посмотрим на заболевании пристально и вспомним все, что о нем знаем.
Зачастую атипия клеток (то есть, дисплазия), появляется как реакция клеток на воспаление, вызванное грибами и бактериями. Лечение основного диагноза (цервицита или кольпита) приводит к закономерному выздоровлению.
Но дисплазия CIN I плоского эпителия шейки матки может быть вызвана вирусом папилломы человека, латинское название этой группы вирусов Human papilloma virus, или HPV. Их больше 140 серотипов. И далеко не все из них онкогенные.
К ВПЧ низкого онкологического риска относятся серотипы 3,6,11,13,32,42, 43,44,72 и 73. Эти вирусы тоже вызывают диспластические изменения, но перед этим долго персистируют в клетке и не встраиваются в структуру ДНК, поэтому могут подавляться иммунной системой.
Но если дисплазия 1 степени вызывается вирусами высокого онкогенного риска, говорить о спонтанном выздоровлении не приходится. Эти вирусы встраиваются в ДНК клетки, делают ее невидимой для иммунитета и беспрепятственно вызывают ее опухолевую трансформацию. Поэтому дисплазия 1 вирусной природы чаще всего требует лечения.
Преимущества лечения CIN 1 шейки матки методом ФДТ
- ФДТ – это нехирургический метод лечения, который сохраняет целостность органа – важную составляющую врожденного иммунитета.
- Избирательное уничтожение патологических клеток без воздействия на здоровые.
- Эффективность избавления от вируса папилломы и других инфекций в зоне воздействия составляет более 93%.
- Гарантированная профилактика рака шейки матки.
- Восстановление целостности шейки матки и ее иммунного статуса, профилактика повторного заражения ВПЧ.
Отзыв о лечении
В 2013 году мне поставили диагноз CIN1, дисплазия шейки матки 1ст с переходом во влагалище.
Не зная о существующих новых методах лечения, я согласилась на экстирпацию матки без придатков. После операции, решив, что избавилась от своего недуга, я успокоилась, и больше не думала о недавно существовавшей проблеме вплоть до марта 2017 года, когда я обратилась к гинекологу на плановый осмотр.
В который раз позволю себе акцентировать внимание на очень серьезной проблеме российской онкогинекологии.
По многим причинам врачи назначают необоснованно агрессивное лечение LSIL – от конизации до удаления матки.
Я считаю, что такие назначения связаны с неоправданным лечебным риском, когда риски от проводимого лечения превышают риски самого заболевания.
Врачом при осмотре были выявлены изменения купола культи влагалища, при кольпоскопии обнаружена йоднегативная зона влагалища, умеренная дисплазия. Гинеколог сказал мне, что существует такой новый метод, как фотодинамическая терапия.
Я начала искать информацию и прочитала в отзывах пациентов о М. С. Афанасьеве, что он успешно практикует такой метод лечения. Обратившись к нему за консультацией, он мне всё подробно объяснил и назначил день проведения первой терапии. ФДТ прошла хорошо, остались положительные впечатления, сразу возникло полное доверие к Максиму Станиславовичу. В клинике я провела 5 часов (два часа капельница, потом сама процедура).
После всего я отправилась домой, небольшой дискомфорт в обработанной зоне присутствовал, но на следующий день уже ничего не чувствовала. Через три месяца второй сеанс, который длился около двух часов.
05.09.2018 я приехала в клинику на контрольный осмотр, итог: йодположительная проба влагалища, уксусно-белого эпителия нет, сделали биопсию — дисплазии нет, я здорова!
М. С. Афанасьев — врач с большой буквы, очень грамотный специалист своего дела, к тому же прекрасный человек. По велению судьбы, я попала именно к нему, отчего я безмерно счастлива!
Чтобы получить консультацию, показана ли вам фотодинамическая терапия, и рассчитать цену процедуры, высылайте вашу историю болезни и анализы на e-mail doctor@drafanasev.com. Или звоните по телефону
8 (800) 555-77-26
в Москве.
Прием ведет Афанасьев Максим Станиславович, акушер-гинеколог, онкогинеколог, онколог, иммунолог, доктор медицинских наук, профессор и член ученого совета Первого МГМУ им. И.М. Сеченова МЗ РФ, эксперт по лечению атипической гиперплазии матки.
Прием проводится в двух клиниках в Москве, а также в Санкт-Петербурге, Махачкале, Курске, Ставрополе, Барнауле, Самаре, Набережных Челнах, Салавате, Челябинске, Сургуте и других регионах России. Уточнить дату, место приема в вашем городе и записаться на консультацию вы можете у администратора по телефону +7 (495) 204-18-93.
После лечения я поддерживаю обратную связь со всеми пациентками и решаю все возникающие вопросы. Гепатит и положительный ВИЧ статус не является противопоказаниями для лечения методом ФДТ.
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
- при профилактических осмотрах цитологические мазки следует брать у женщин независимо от жалоб, наличия или отсутствия изменений слизистой оболочки. Цитологическое исследование следует повторять не реже, чем раз в три года;
- желательно получать мазки не ранее, чем на 5-е сутки менструального цикла и не позднее, чем за 5 суток до предполагаемого начала менструации;
- нельзя брать материал в течение 48 ч после полового контакта, использования любрикантов, раствора уксуса или Люголя, тампонов или спермицидов, спринцевания, введения во влагалище медикаментов, свечей, кремов, в т. ч. кремов для выполнения ультразвукового исследования;
- беременность – не лучшее время для скрининга, так как возможны неправильные результаты, но, если нет уверенности, что женщина придет на обследование после родов, лучше мазки взять;
- при симптомах острой инфекции желательно получать мазки с целью обследования и выявления патологических изменений эпителия, этиологического агента; также необходим цитологический контроль после лечения, но не ранее, чем через 2 мес. после окончания курса.
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.
Цитологические изменения в железистом эпителии
| Bethesda Терминология, разработанная в г. Bethesda (США, 2001 г.) | Терминология, принятая в России |
|---|---|
| ОЦЕНКА КАЧЕСТВА МАЗКА | |
| Материал полноценный | Материал адекватный (дается описание клеточного состава мазка) |
| Материал недостаточно полноценный | Материал недостаточно адекватный (дается описание клеточного состава мазка) |
| Неудовлетворительный для оценки | Клеточного состава недостаточно для уверенного суждения о характере процесса |
| Удовлетворительный для оценки, но ограниченный чем-то (определить причину) | |
| В пределах нормы Метаплазия (норма) | Цитограмма без особенностей (в пределах нормы) – для репродуктивного возраста Цитограмма с возрастными изменениями слизистой оболочки: — атрофический тип мазка — атрофический тип мазка c лейкоцитарной реакцией Эстрогенный тип мазка у женщины в постменопаузе Атрофический тип мазка у женщины репродуктивного возраста |
| ДОБРОКАЧЕСТВЕННЫЕ ИЗМЕНЕНИЯ КЛЕТОК | |
| Инфекции | |
| Trichomonas vaginalis | Трихомонадный кольпит |
| Грибы, морфологически сходные с родом Candida | Обнаружены элементы гриба типа Candida |
| Кокки, гонококки | Обнаружены диплококки, расположенные внутриклеточно |
| Преобладание коккобациллярной флоры | Флора коккобациллярная, возможно, бактериальный вагиноз |
| Бактерии, морфологически сходные с Actinomyces | Флора типа Актиномицетов |
| Прочее | Флора типа Leptotrichia |
| Флора – мелкие палочки | |
| Флора – смешанная | |
| Клеточные изменения, связанные с вирусом Herpes simplex | Эпителий с изменениями, связанными с Herpes simplex |
| Возможно, хламидийная инфекция | |
| Реактивные изменения | |
| Воспалительные (включая репаративные) | Найденные изменения соответствуют воспалению с реактивными изменениями эпителия:дегенеративные, репаративные изменения, воспалительная атипия, плоскоклеточная метаплазия, гиперкератоз, паракератоз, и/или др. |
| Атрофия с воспалением (атрофический |
Атрофический кольпит
Атрофический тип мазка, лейкоцитарная реакция Эпителий слизистой оболочки с гиперкератозом Эпителий слизистой оболочки с паракератозом Эпителий слизистой оболочки с дискератозом Резервноклеточная гиперплазия Плоскоклеточная метаплазия Плоскоклеточная метаплазия с атипией |
| Лучевые изменения | Эпителий слизистой оболочки с лучевыми изменениями |
| Изменения, связанные с использованием внутриматочных контрацептивов | |
| ПАТОЛОГИЧЕСКИЕ ИЗМЕНЕНИЯ ПЛОСКОГО ЭПИТЕЛИЯ | |
|
Клетки плоского эпителия с атипией неясного значения (ASC-US*) Клетки плоского эпителия с атипией неясного значения не исключающие HSIL (ASC-Н) |
Найденные изменения трудно дифференцировать между реактивными изменениями эпителия и дисплазией Обнаружены клетки, трактовка которых затруднена (с дискариозом, укрупненными ядрами, гиперхромными ядрами и т.д.) |
| Изменения плоского эпителия (не опухолевые, но достойные динамического наблюдения) | |
| Плоское интраэпителиальное поражение низкой степени (LSIL): папилломавирусная инфекция, слабая дисплазия (CIN I) |
Эпителий слизистой оболочки с признаками папилломавирусной инфекции
Найденные изменения, возможно, соответствуют слабой дисплазии. |
| Плоское интраэпителиальное поражение высокой степени (НSIL): умеренная, тяжелая дисплазия и внутриэпителиальный рак (CINII, CIN III) |
Найденные изменения соответствуют умеренной дисплазии.
Найденные изменения соответствуют тяжелой дисплазии. Найденные изменения подозрительны по наличию внутриэпителиального рака. |
| Инвазивный рак | |
| Плоскоклеточный рак |
Плоскоклеточный рак Плоскоклеточный рак с ороговением Плоскоклеточный рак из мелких клеток |
|
Железистая гиперплазия Найденные изменения соответствуют эндоцервикозу |
|
|
Атипичные клетки железистого эпителия (возможные предположения): – Неясного значения (AGUS); – подозрительные на неоплазию; – эндоцервикальная аденокарцинома in situ (AIS); – аденокарцинома |
Железистая гиперплазия с атипией по типу дисплазии (I, II, III) Аденокарцинома |
| Клетки эндометрия цитологически доброкачественные (у женщины в менопаузе и т. д.) | |
|
Аденокарцинома эндометрия Аденокарцинома другой локализации Аденокарцинома без дополнительной характеристики |
Аденокарцинома, возможно аденокарцинома эндометрия Аденокарцинома БДУ (без дополнительного уточнения) |
| Другие злокачественные опухоли (по возможности определить нозологическую форму) | |
| Оценка гормонального статуса |
* при возможности ASCUS должны быть определены как сходные с реактивными, репаративными или предраковыми процессами;
** изменения, связанные с воздействием вируса папилломы человека, ранее обозначаемые как койлоцитоз, койлоцитарная атипия, кондиломатозная атипия, включены в категорию слабо выраженных изменений клеток плоского эпителия;
*** по возможности следует отметить, относятся ли изменения к CIN II, CIN III, есть ли признаки cr in situ;
**** гормональная оценка (проводится только по вагинальным мазкам):
– гормональный тип мазка соответствует возрасту и клиническим данным;
– гормональный тип мазка не соответствует возрасту и клиническим данным: (расшифровать);
– гормональная оценка невозможна в связи с: (указать причину).
Трактовка цитологического заключения
Цитологическое заключение “Цитограмма в пределах нормы” в случае получения полноценного материала может рассматриваться как указание на отсутствие патологических изменений шейки матки. Заключение о воспалительных поражениях требует уточнения этиологического фактора. Если этого нельзя сделать по цитологическим мазкам, необходимо микробиологическое или молекулярное исследование. Цитологическое заключение о реактивных изменениях неясного генеза требует дополнительной (уточняющей) диагностики.
Заключение ASC-US или ASC-H также диктует необходимость обследования и/или динамического наблюдения больной. Практически во всех современных руководствах по ведению больных с поражениями шейки матки эти диагностические категории имеются. Разработан также алгоритм обследования женщин в зависимости от выявленных патологических изменений.
Интеграция различных лабораторных методов
В диагностике заболеваний шейки матки важное значение имеют клинические данные, результаты исследования на микрофлору (классические микробиологические (культуральные), методы АНК (ПЦР, RT-PCR, Hybrid Capture, NASBA, и др.).
При необходимости уточнения патологического процесса (ASC-US, ASC-H) цитологическое исследование по возможности дополняют молекулярно биологическими (p16, онкогены, метилированная ДНК и др.).
Исследования для обнаружения ВПЧ имеют низкую прогностическую значимость, особенно у молодых женщин (до 30 лет), в связи с тем, что у большинства пациенток этой возрастной группы ВПЧ-инфекция имеет транзиторный характер. Однако несмотря на низкую специфичность теста в отношении интраэпителиальных опухолей и рака, именно у женщин моложе 30 лет он может использоваться в качестве скринингового с последующим цитологическим исследованием. Чувствительность и специфичность значительно увеличиваются при комплексном использовании цитологического метода и исследования для обнаружения ВПЧ, особенно у больных с сомнительными цитологическими данными. Этот тест важен при ведении пациенток с ASC-US, при динамическом наблюдении для определения риска рецидива или прогрессирования заболевания (CIN II, СIN III, carcinoma in situ, инвазивный рак).