Диагностика заболеваний редко обходится без инструментальных и лабораторных исследований. Оценки симптомов недостаточно — нужно узнать, что происходит внутри органов и тканей. Одним из наиболее точных методов обследования является биопсия. Врач производит забор тканевого материала в области предполагаемого патологического процесса с целью его дальнейшего изучения. Микроскопический анализ полученного образца помогает выявить характерные для определенного заболевания изменения. В онкологической практике биопсия считается информативным методом уточнения типа опухоли, ее стадирования.
- Что это за анализ?
- Показания к проведению
- Виды и способы проведения биопсии
- Подготовка
- Может ли биопсия быть ошибочной?
Что это за анализ?
Биопсия — высокоинформативный способ обследования, применяемый в случае необходимости анализа клеток в определенной анатомической области. Забор тканей с их последующим обследованием с помощью микроскопии дает возможность точно оценить клеточный состав. Без такой процедуры сложно обойтись, если врач подозревает наличие доброкачественного или злокачественного новообразования в определенном органе. Это уточняющее исследование, дополняющее результаты других диагностических процедур. Онколог анализирует результаты биопсии, рентгенографии, эндоскопии и иммунологических тестов совместно.
Онкологические заболевания развиваются быстро и угрожают жизни пациента. Нужно как можно раньше выбрать наиболее эффективную схему лечения. Именно с этой целью проводится биопсия. По результатам процедуры врач приходит к выводу, какие травматичные или даже опасные с точки зрения осложнений способы лечения уместны в данном случае. Подбирается тактика оперативного вмешательства, радиотерапии, химиотерапевтического лечения. Все это было бы невозможно без точного определения типа опухоли, ее стадии и распространенности в организме. Нужны цитологические и гистологические тесты.
В качестве примера можно привести злокачественное новообразование прямой кишки, растущее в нижней части органа. В качестве основного метода лечения выполняется иссечение этой анатомической структуры с последующим формированием колостомы для выделения каловых масс. Если диагноз не был полностью подтвержден, подобное вмешательство не проводят. Оно может по ошибке сделать пациента инвалидом.
Показания к проведению
Подобная диагностическая процедура требуется, если врач предполагает о наличии патологического процесса, подтверждение которого невозможно с помощью других способов исследования. В большинстве случаев это онкологические болезни, однако область применения биопсии ими не ограничивается. Например, такое исследование часто назначают гастроэнтерологи для оценки состояния слизистой оболочки органов пищеварительного тракта. Определяется вид воспалительного процесса, подбирается способ его лечения. В гинекологии и эндокринологии этот метод дает возможность определить причину нарушения фертильности, обнаружить ранние признаки воспаления и дисплазии.
Также биопсия необходима для определения особенностей течения и степени тяжести патологического процесса при болезнях печеночной ткани, почек, головного мозга, мышц и других анатомических структур. Это важно для подбора и изменения схемы медикаментозной терапии. По результатам анализа врач определяет прогностические данные.
Виды и способы проведения биопсии
В современной клинической практике чаще всего используют следующие методики выполнения биопсии:
- Мазки, соскобы и бритвенный метод. Зачастую специалисту требуется небольшое количество материала для постановки диагноза. Можно выполнить мазок и получить все необходимые данные при его последующей микроскопии. Например, такой способ часто применяют в гинекологии. Бритвенная биопсия предполагает иссечение тонкого участка кожного покрова с помощью скальпеля или другого инструмента.
- Тонкоигольная пункция. Такая процедура тоже подходит для случаев, когда достаточно получить немного клеток. В область предполагаемого патологического процесса вводится тонкая игла, захватывающая тканевой образец.
- Толстоигольная пункция. Позволяет произвести забор большого образца тканей без иссечения. Ее назначают при злокачественном новообразовании молочной железы, печеночной ткани, предстательной железы. Трепан-биопсия подходит для исследования кожного покрова, костномозговых структур. Используется специальный инструмент в форме цилиндра.
- Аспирационный метод. Это современная техника забора материала, при котором используется вакуумный прибор в форме цилиндра. В качестве механизма применяется отрицательное давление. Прибор присоединяют к игле. Аспирация дает возможность взять несколько образцов в разных участках анатомической структуры.
- Операционная биопсия. Проводится непосредственно во время операции, когда врач иссекает опухолевую ткань. Это высокоинформативное исследование, позволяющее оценить состояние большого количества тканей. Минус такого вида процедуры — определить тип болезни можно только после операции. Плюсом можно считать совмещение лечебной практики с достоверной диагностикой.
- Эндоскопическая биопсия. Проводится во время диагностики внутренних полостных структур, вроде пищеварительного или респираторного тракта. С помощью эндоскопа врач осматривает подозрительные участки тканей и выбирает место забора материала. Плюсом такой техники можно считать повышенную точность результатов исследования.
Способ проведения диагностики выбирают в зависимости от анамнеза пациента.
Подготовка
В большинстве случаев специально готовиться не следует. Достаточно прийти к врачу в день проведения процедуры и подписать необходимые документы. Специалист объяснит, как будет проходить обследование. Расскажет о рисках и возможных неприятных ощущениях. Определенные виды биопсии выполняют под местным обезболиванием. Реже требуется наркоз. Пациент может сам выбирать комфортный для него способ выполнения диагностики. В случае наркоза нужны специальные подготовительные процедуры.
Для биопсии характерны стандартные осложнения, возникающие при других видах вмешательств. Возможно кровоизлияние, инфицирование тканей. Реже возникает травматизация внутренних органов. Такие негативные последствия редки, но врач обязательно уведомляет пациента о рисках.
Может ли биопсия быть ошибочной?
Достоверность исследования зависит от способа его проведения, анамнеза пациента, опыта врача и других факторов. Например, при пункции специалист может получить образец тканей без злокачественных клеток, если игла попала в соседнюю с опухолью область. В этом случае возможен ложноположительный результат. Онкологи учитывают такую вероятность, и всегда назначают уточняющие исследования. Диагноз не ставится только на основе результатов одной процедуры. Всегда проводится комплексная оценка состояния организма.
Пересмотр стекол
Москва,
Духовской переулок, 22Б
350015,
Краснодар,
Северная ул, 315
198035,
Санкт-Петербург,
Межевой канал, д.4, лит.А
603155,
Нижний Новгород,
Большая Печёрская ул., д.26
Обновлено: 06 июля 2022
52599
При онкологических заболеваниях материал опухоли берут для гистологического или цитологического исследования. Это необходимо для подтверждения диагноза и определения тактики дальнейшего ведения пациента.
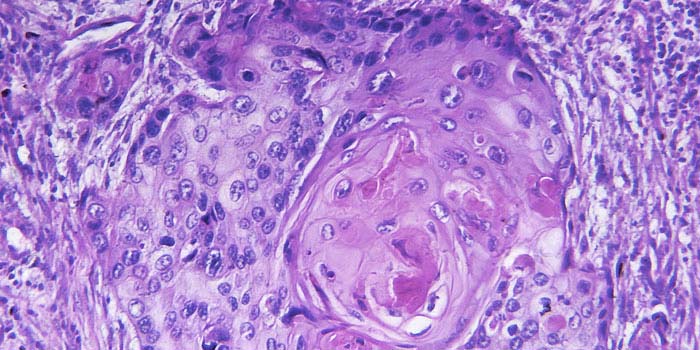
Пересмотр гистологических стекол: опухолевая ткань
Полученный во время операции или на биопсии образец ткани (или клеточный материал) специальным образом фиксируют и окрашивают, чтобы изучить под микроскопом и иммуногистохимическими методами. Последние позволяют даже определить органопринадлежность опухоли. [1]
Что такое блоки и стекла?
Эти термины обозначают ткань, полученную во время биопсии и подготовленную особым образом. В первую очередь образцы заливают раствором формалина и проводят специальную обработку. Это нужно для того, чтобы зафиксировать материал, чтобы клетки не разрушились. Затем ткани необходимо придать нужную степень плотности. Для этого ее помещают в парафин – так получаются гистологические блоки.
Гистологические блоки, образец ткани помещен в парафин
Но и такие образцы пока еще не готовы к исследованию. Ткань в блоке нельзя рассмотреть под микроскопом, потому что она не пропускает свет, а слои клеток накладываются друг на друга. Чтобы ткань стала прозрачной и доступной для изучения, блок нужно нарезать на очень тонкие слои с помощью специального инструмента – микротома. Эти тоненькие слои помещают на стекла и фиксируют – получаются гистологические стёкла. [2,3]
Гистологические стекла
Если у пациента обнаружен рак, то лаборатория обязана хранить гистологические блоки пожизненно, а если патологии не выявлено – в течение пяти лет. Гистологические стекла при диагностированном онкологическом заболевании тоже хранятся пожизненно. Если нужно выполнить пересмотр, то можно обратиться в лабораторию, где проводилось исследование, и получить оба этих вида материала. [4]
Когда и почему необходим пересмотр стекол?
Если морфологическое заключение не соответствует клинической картине опухоли, а также снимкам МРТ или КТ, то стекла отправляют на пересмотр в другое лечебное учреждение. Обычно пересмотром стекол занимаются специалисты с многолетним стажем работы и уникальным опытом диагностики редких опухолей. Дополнительный ручной пересмотр исключает возможность ошибки, связанной с использованием автоматических анализаторов.
Почему могут возникать ошибки при первичном просматривании стекол?
- неправильный забор материала, например, захвачен не весь слой эпителия, и невозможно судить о глубине поражения;
- проведена биопсия участка здоровой ткани;
- некачественная обработка материала в лаборатории;
- малое количество изученных срезов;
- недостаточная квалификация патоморфолога. [5]
Качественное микроскопическое и иммуногистохимическое исследование позволяет начать оправданное и своевременное лечение опухоли, а значит, увеличивает шансы на излечение и выживаемость пациента при онкологических заболеваниях. Оптимально, если морфологический диагноз будет подтвержден двумя специалистами.
Список литературы:
- Tatyana S. Gurina; Lary Simms. Histology, Staining. Treasure Island (FL): StatPearls Publishing; 2021 Jan-.
- В. А. Корьяк, Л. А. Николаева. Основы гистологической техники. Учебное пособие.
- Гистологическое изучение микропрепаратов тканей и органов. Гистология, эмбриология, цитология. Под ред. д.м.н., доц. Н. Ю. Матвеевой. Владивосток, Медицина ДВ, 2015.
- Приказ МЗ РФ № 179н от 24.03.2016 г. «О правилах проведения патолого-анатомических исследований».
- P. Morelli, E. Porazzi, M. Ruspini, U. Restelli, and G. Banfi. Analysis of errors in histology by root cause analysis: a pilot study. J Prev Med Hyg. 2013 Jun; 54(2): 90–96.
Как часто женщине нужно проверяться на рак груди?
Здесь нет однозначного ответа. Никто точно не скажет, как часто молодой здоровой женщине до 40 лет нужно ходить к врачу. Когда врач сидит на 10-минутном приеме, ему легче сказать: «Приходите раз в год. Все, до свидания, следующий, заходите». У меня прием длится полчаса, и я специально оставляю хотя бы пять минут в конце, чтобы объяснить, что нет универсальных рекомендаций. Нужно уделять внимание своей груди, осматривать ее, но как часто это делать — тоже никто не знает. Самообследование не приводит к снижению смертности от болезни, но при этом каждую четвертую опухоль женщины находят сами. На сегодня мы еще не изобрели таких диагностических методов, которые нам до биопсии скажут: с грудью все ок или не ок.
После 40 лет все более-менее понятно: с этого возраста риск заболеть раком молочной железы достоверно увеличивается. Одни медицинские организации говорят, что скрининг (Обследование здоровых людей с целью выявить у них заболевание, которое пока никак себя не проявляет. — Прим. ред.) пора делать с 40 лет, другие — с 45 лет. Частота обследований тоже отличается. Рекомендации немного расходятся в зависимости от системы здравоохранения. В Америке есть как минимум две организации, которые занимаются разработкой программы скрининга: Рабочая группа по профилактике заболеваний (USPSTF) и Американское онкологическое общество. У них разные рекомендации, потому что в некоторых штатах преобладает афроамериканское население, которое болеет тяжелее. В Великобритании проверяют с 50 лет раз в три года.
Сам скрининг проводят до 75 лет, это связано с продолжительностью жизни. Нет смысла проводить скрининговое обследование, если ожидаемая продолжительность жизни менее 10 лет. Потому что, скорее всего, то, что мы обнаружим, не сократит жизнь этого человека, а медицинской системе обойдется дорого.
В России насчет скринингов все говорят разное. Например, некоторые гинекологи считают, что после 40 лет маммографию нужно делать ежегодно или хотя бы раз в два года, а после 50 лет — ежегодно. Но на самом деле мы не знаем, как часто нужно проходить маммографию. Поэтому пропагандировать, что это надо делать раз в год, без объяснения того, что это за исследование и что делать с его результатами, — неправильно.
И каждый раз думаю: боже, сколько неправильных действий могут повлечь за собой какие-либо рекомендации. Из-за этого я завела свой блог. Мне кажется, что основная проблема не в том, делаем мы маммографию или не делаем, а в том, что мы не общаемся с пациентами. У меня много пациенток, которые приходят с болью или находят у себя уплотнение, и тогда мы с ними прицельно разбираемся, что боль в молочной железе — это не спутник онкологического заболевания, что уплотнение — это просто локальный фиброаденоматоз, так ведет себя железистая ткань. Мы можем сходить с пациенткой на УЗИ и уточнить это или понаблюдать динамику.
Рекомендации — это такая штука, которая нас может поддержать. Но принимаем решение мы сами: врач и пациент. У меня была молодая пациентка, которая прошла химиотерапию, операцию и была вынуждена принимать препарат, вызывающий искусственную менопаузу. В какой-то момент она сказала, что больше не может, мы обсудили все риски и приняли решение отказаться от лекарства, тем самым повысив вероятность рецидива. Но это было общее решение. Без желания пациента его лечить никто не будет.
Кому-то дают странную рекомендацию ходить каждые полгода на УЗИ. Вот пациентка ходит, делает очередное УЗИ, ей говорят, что все нормально, проходит два месяца, и она приходит ко мне с шишкой. А там рак. И она сидит в слезах на приеме: «Я ходила каждые полгода, потому что мне так сказали». Скрининг направлен на то, чтобы поймать рак, когда еще нет симптомов. Но не всех можно поймать.
Есть такая фраза, что мы скринингом пытаемся поймать «орлов» и «зайцев» — это быстрые, стремительные, очень внезапные раки, а ловим «черепашек», потому что они ползут-ползут и вот в какой-то момент мы находим их на маммографии.
«Черепашек» нужно лечить или можно их не трогать?
«Черепашки» — это не камни, которые не двигаются. Они все равно прогрессируют. Мы никогда не узнаем, как они себя поведут, потому что неэтично не лечить рак. Нет критериев, которые бы сказали, можно злокачественную опухоль наблюдать или ее нужно сразу же лечить. Вот есть карцинома in situ, это неинвазивный рак. После того, как его обнаружили, у женщины в восемь раз увеличивается риск инвазивного рака.
Инвазивный рак — один из основных раков молочной железы, это порядка 70% случаев. Пока опухоль внутри молочного протока — это нулевая стадия рака, он не может метастазировать. Инвазивный рак — это уже опухоль, которая вышла за пределы протока и у нее появляется шанс дать метастазы. И вот, казалось бы, что карциномы in situ можно наблюдать без вмешательства, но нет, потому что они могут развиваться в инвазивную опухоль.
А вот дольковая карцинома in situ не является злокачественной опухолью. Это стало понятно совсем недавно — в 2017 году, до этого к ней относились так же, как к внутрипротоковой карциноме. А теперь стало понятно, что она доброкачественная и ее не нужно оперировать. На сегодня нет таких форм рака молочной железы, которые этично наблюдать, в отличие например от некоторых видов рака предстательной железы.
Как врач определяет, рак перед ним или не рак?
В тот момент, когда мы ловим что-то в груди, мы не знаем, что это. Это кот в мешке. Биопсия все решает, и без нее лечение от рака никто не начнет. Даже пункция (Подвид биопсии, когда берут взвесь клеток, а не кусочек ткани. — Прим. ред.) не является основанием для лечения.
Решение о том, проводить биопсию или нет, принимают согласно критериям BI-RADS — Breast Imaging Reporting and Data System. Это шкала от нуля до шести, по которой рентгенолог ставит балл на основании маммографии, УЗИ или МРТ. BI-RADS 0 означает, что нужен дополнительный анализ, BI-RADS 2 — что опухоль доброкачественная, BI-RADS 4 — что есть подозрение на рак. С этим результатом пациентка приходит к онкологу или клиническому рентгенологу, и он принимает решение, делать биопсию или нет.
Рентгенолог может поставить BI-RADS 3. Это меньше 2% вероятности того, что есть рак молочной железы. Если BI-RADS больше, то нужно будет принять решение о биопсии, но образование совершенно не обязательно окажется раком. На биопсии рак уже нельзя перепутать с чем-то. Если это опухоль, это опухоль.
Если посмотреть на графики заболеваемости раком груди и смертности от него в России, видно, что заболеваемость растет, а смертность нет. Как это можно объяснить, по-вашему?
Это реально так. Проблема в том, что мы не можем понять достоверно: это потому, что мы делаем скрининг и лечим лучше, чем раньше, или только потому, что просто лечим лучше? Прерывать то или другое для того, чтобы выяснить причину, — неэтично, потому что от рака умирают.
Основной плюс маммографии не только в том, чтобы держать смертность под контролем. Маммография сильно влияет на объем лечения. Когда мы обнаруживаем опухоль на первой стадии, без симптомов, у нас есть возможность пролечить минимально: прооперировать и назначить профилактические таблетки. Когда этот же рак доходит до стадии клинических симптомов, мы уже не можем только этим обойтись. Тогда мы должны прооперировать еще подмышку, что увеличивает риски лимфатического отека, провести химиотерапию, которая снижает качество жизни, и так далее.
Может ли врач пропустить рак?
Конечно, это огромная проблема. В трети случаев рак может быть не найден при маммографии. Есть, во-первых, рентгенонегативные раки, которые на рентгене не видны. Именно поэтому очень важно сначала осмотреть пациента, а потом назначать исследования. А то может прийти 45-летняя женщина на маммографию, и ей напишут по результатам снимка: все ок. И она думает: ага, значит, эта шишечка — ничего страшного.
Да, бывает, что доктор ошибается, считает, что в анализах нет ничего страшного и не надо делать биопсию, или получает неинформативную биопсию и назначает какую-нибудь травку, просто чтобы пациента не оставлять без наблюдения. Хорошо, если пациент придет на следующее обследование пораньше.
А может врач, наоборот, перестраховаться там, где не надо?
У меня сейчас наблюдается пациентка. Что-то ее забеспокоило, закололо, и она пришла. Ей сделали маммографию, рентгенолог написал, что все нормально, а я вижу на снимке скопление кальцинатов (солей кальция) и тень в этом месте. То есть то ли он не видел, то ли он просто копипаст сделал, не понятно. И вот здесь начинаются минусы гипердиагностики.
Я говорю: «Вы знаете, тут что-то подозрительное, надо идти и делать не скрининговую маммографию, а прицельную, на которой сомнительное место фотографируют при увеличении». Естественно, пациентка волнуется. Она записывается на процедуру, ждет. По результатам снимка ей пишут BI-RADS 4, то есть нужно делать биопсию. Я тоже нервничаю, потому что недавно в том же самом месте писали, что все нормально, BI-RADS 2, а теперь когда я отправила эту пациентку досмотреть, пишут 4.
Потом мы идем на УЗИ, там ничего нет. Она записывается на МРТ — опять ожидание, ведь МРТ делают в определенный день цикла, а он у нее скачет. Она получает результат МРТ, там все нормально, но я прошу коллегу пересмотреть.
Мультимодальных диагностов молочной железы, которые владеют всеми методами диагностики, у нас в стране немного. Мне говорят: «Тут ничего нет, это нормальные кальцинаты, не подозрительные. Понятно, почему они тебя заинтересовали, но на прицельном снимке все ок». Я отвечаю: «Но рентгенологи BI-RADS 4 ставят, что они там видят-то?» Пациентка все это время была как на пороховой бочке.
Вот что происходит из-за гипердиагностики. Биопсию ей мы делать не стали. Но через полгода все нужно повторять, потому что я не могу отпустить ее на два года до следующего осмотра.
Это проблема интерпретации снимков?
Да, это проблема чтения снимков. Не знаю, может, я запустила эту волну и коллеги напугались, может, смотрел кто-то не совсем опытный. Проблема в том, что у нас нет метода диагностики до биопсии, который отвечает на вопрос: да-да, нет-нет.
В скандинавских странах одна из образцовых систем скрининга: там сидят два опытных рентгенолога и отсматривают снимки. Если их мнение совпадает, пациентке выдают диагноз. А если у них мнение не совпадает, то с ними проводят работу над ошибками. А у нас на скрининге, наоборот, сидят люди, которые вчера выпустились, потому что опытным интереснее где-нибудь еще.
Маммограмму еще нужно качественно отснять. Даже с прицельной маммограммой можно ошибиться. Но, каким бы ни было качество снимка, если человек не умеет интерпретировать, у него недостаточно опыта или он перестраховывается — от ошибок не уйти.
Еще надо понимать, что у одного доктора может быть этих маммограмм тридцать штук за день. Это же нереально. Человек может принять до семи, максимум девяти взвешенных решений, если он себя круто прокачал. А у нас люди продолжают сидеть, принимать по тридцать человек и отсматривать по тридцать снимков.
Какие еще есть минусы у гипердиагностики помимо лишних обследований и волнений?
Человек может проходить ненужную биопсию, ведь кто-то сделал бы биопсию в случае с моей пациенткой, о котором я рассказывала выше. Рентгенолог же поставил BI-RADS 4. Каждый рентгенолог может ошибиться, не только неграмотный или тот, который перестраховался.
Бывают более неоднозначные случаи. У меня была пациентка из государственной поликлиники, которая пришла с заключением BI-RADS 4 с обеих сторон груди. Я смотрю ее на УЗИ — там ничего. Смотрю маммограмму — ну да, есть скопление кальцинатов, но даже я вижу, что ничего страшного, хотя я не рентгенолог.
Ей вполне могли сделать биопсию, лечить бы не лечили, но понервничать заставили. Гипердиагностика неприятна именно из-за ненужных процедур, ненужных биопсий и больших переживаний по этому поводу.
Еще есть проблема в том, что в некоторых клиниках просто так назначают обследования. До «Чайки» я работала в клинике, где после каждого пациента меня вызывали на ковер и спрашивали: «Почему вы не назначили пациентке анализ крови, мочи, кала, где УЗИ?» Я говорю: «Без симптомов УЗИ делать не надо». А они ссылаются на рекомендации акушеров-гинекологов, на внутренние протоколы, которых никто никогда не видел. Онкомаркеры — это вообще любимейшая тема. «Почему вы ей не назначили онкомаркеры?» — говорят. Потому что их никому не надо назначать.
Так что я представляю себе этот кошмар, с которым пациентки могут встретиться. Поэтому лучше идти в клинику и к врачу, которому доверяешь
Получение в раках проводимой биопсии биологического образца для его последующего изучения, как и сами результаты диагностического исследования, могут быть ошибочными. Помимо человеческого фактора и неточности в самой аппаратуре, медики выделяют и иные предрасполагающие факторы, влияющие на точность итогового результата.
Ошибка в биопсии
Образец забранной ткани для последующего гистологического анализа может быть получен самыми разными методами, которые существуют в рамках малоинвазивной хирургии. Так в ходе проведения пункционного вида биопсии – материал забирают посредством трубки и иглы с режущим краем. При этом стоит помнить – необходимый объем биопата не всегда может в шприц, и соответственно полученный результат может быть отрицательным. Потому возникает потребность в повторении забора биопата.
При отсутствии возможности полностью удаления опухоли – врачи проводят иссечение ее части. Но и в этом случае может быть ошибка в результатах диагностики, поскольку забранный образец может отличаться от основной массы и объема новообразования. Так тотальное удаление новообразования – точный метод диагностики в данном случае.
Ошибки в биопсии и основные причины
В случае проведения гистологии забранного биопата – возможны ошибки и основными причинами, которые приводят к ним, врачи называют следующие:
- Неправильно выбрано место для проведения прокола иглой. В этом случае биопсийный инструмент не проникает достаточно глубоко внутрь, проводится только поверхностный забор биопата с пораженного участка. Этот образец не может в полной мере покажет клиническую картину течения патологического процесса.
- Из очага новообразования невозможно взять достаточное количество биологического материала для анализа – чаще всего это происходит по причине особенностей роста новообразования.
- При нарушении правил забора и последующего хранения биологического материала.
- Также ошибка может быть следствием неправильной технологии, несоблюдение правил и этапов приготовления для последующего исследования забранного биопата.
- Причина ошибки может крыться и в низком уровне квалификации врача, проводящего само исследование биопата и недостаточная квалификация медика, проводящего интерпретацию полученных лабораторных анализов.
На итоги результатов биопсии могут влиять и медикаменты, которые пациент принимал накануне проведенного забора биологического материала. Но в большинстве своем ошибок при исследовании биопата и трактовке результатов диагностики не возникает, либо его процент минимален и не может влиять на итог всего процесса диагностики.
21.09.2018
Врач онколог, маммолог, хирург Алексей Галкин. Стаж 18+ лет. Принимает в Университетской клинике. Стоимость приема от 2000 руб.
Все зависит от конкретных обнаруженных патологических процессов. Некоторые патологии не опасны переходом в онкологию. Поэтому при их обнаружении нужно обратиться к маммологу, который назначит лечение.
Риск перерождения в рак различных патологий молочной железы
| Степень риска | Заболевания |
| Низкая | Фиброзно-кистозная мастопатия при отсутствии атипии ( предрака) |
| Незначительное разрастание (гиперплазия) различных тканей железы без наличия атипии | |
| Доброкачественные опухоли – гамартомы, липомы, фиброаденомы, аденомы размером менее 3 мм, мелкие кисты | |
| Воспалительные процессы | |
| Посттравматические состояния | |
| Диабетическая мастопатия – изменения в молочных железах, вызванные диабетом | |
| Средняя | Значительное разрастание тканей железы, особенно протоков (протоковая гиперплазия) |
| Крупные кисты, фиброаденомы размером более 3 мм, протоковые папилломы | |
| Твердые включения- кальцинаты и фиброзный аденоз | |
| Высокая | Мастопатия и гиперплазия (разрастание тканей), сопровождающиеся появлением атипии-предрака |
Что делать, если при трепан биопсии обнаружена доброкачественная опухоль
Тактика при обнаружении доброкачественных опухолей молочной желез может быть различной. При небольших новообразованиях возможна выжидательная тактика – женщине нужно будет периодически посещать врача и проходить УЗИ. Образования которые растут, болят или мешают подлежат удалению.
Что делать, если трепан биопсия показала мастопатию
При обнаружении мастопатии требуется комплексное обследование, поскольку заболевание очень часто становится следствием гормональных сбоев. Женщине нужно сдать кровь на гормоны яичников, гипофиза и щитовидной железы, пройти УЗИ малого таза и щитовидной железы. Назначается лечение, позволяющее уменьшить симптомы заболевания. Требуется врачебное наблюдение.
Что делать, если трепан биопсия обнаружила рак
Лечебная тактика при обнаружении злокачественных опухолей зависит от типа, распространённости, стадии новообразования, наличия метастаз и других факторов. Применяется хирургическое лечение, которое может сочетаться с химио- и лучевой терапией, применением гормональных препаратов.
Где сделать трепан биопсию и пройти лечение при плохих результатах
В Университетской клинике можно сделать трепан-биопсию молочной железы, получить в короткие сроки результаты, пройти дополнительные исследования и пролечить выявленные заболевания. Поэтому при любых патологических изменениях и уплотнениях в груди лучше не ждать, а обратиться к врачу
В клинике принимает достаточно опытный врач маммолог, владеющий самыми современными методиками диагностики и лечения патологий молочных желез. Врач онколог-маммолог закончила ординатуру и аспирантуру по специальности «онкология», неоднократно проходила профессиональную переподготовку в области хирургии онкологии и маммологии. Высокая квалификация этого доктора позволяет разобраться даже в нетипичных, нестандартных и других тяжелых случаях заболеваний молочных желез.
Продолжение статьи
- Текст 1. Трепан-биопсия. Что это? Как проводят исследование.
- Текст 2. Что показывает трепан биопсия. Расшифровка результатов
- Текст 3. Злокачественные опухоли молочной железы, выявляемые во время трепан биопсии
- Текст 4. Иммуногистохимические исследования тканей, полученных в ходе трепан-биопсии молочной железы
- Текст 5. Что делать если трепан биопсия показала плохой результат
С. Х. Аль-Шукри, С. Ю. Боровец, М. А. Рыбалов
Кафедра урологии Санкт-Петербургского государственного медицинского университета
имени акад. И. П. Павлова
В данном обзоре оцениваются преимущества и недостатки основных методов диагностики и
стадирования рака предстательной железы, приводятся сведения о современных высокотехнологичных методах стадирования и номограммах. Рассматриваются причины ошибок, возникающих
при диагностике и стадировании рака предстательной железы.
Ключевые слова: рак предстательной железы; диагностика; стадирование.
Введение
Повышение эффективности лечения рака предстательной железы (РПЖ) является одной из наиболее актуальных проблем современной урологии.
В мире РПЖ занимает 3–4 место в структуре заболеваемости злокачественными новообразованиями.
В России заболеваемость РПЖ в 2004 году составляла 6,9 %, а в 2009 году — уже 10,7 % [1]. При этом
за последние три десятилетия возросло число мужчин, умерших от этого заболевания [2].
I. МЕТОДЫ ДИАГНОСТИКИ РПЖ
Методы диагностики рпж — включают оценку
результатов пальцевого ректального исследования
(ПРИ), определении уровня ПСА в плазме крови.
Окончательный диагноз РПЖ может быть установлен только по результатам биопсии предстательной
железы, которую целесообразно выполнять под
ТРУЗ-контролем. При клиническом стадировании
для уточнения границ местного распространения
новообразования предстательной железы и для выявления местных и отдаленных метастазов в дополнение используют различные методы, позволяющие
получить изображение: компьютерную томографию
(КТ), магнитно-резонансную томографию (МРТ),
сцинтиграфию костей скелета и др. Однако результаты этих методов могут быть интерпретированы ошибочно как в пользу гипо, так и гипердиагностики.
Работы многих исследователей посвящены оптимизации скрининга и ранней диагностики РПЖ [3–5].
1.1. ПРИ. До внедрения в широкую клиническую практику ПСА, ПРИ было единственным
методом диагностики РПЖ. Большинство злокачественных новообразований РПЖ располагаются
в периферической зоне простаты и могут быть выявлены с помощью ПРИ, если их объем превышает
0,2 см 3. Положительная прогностическая ценность ПРИ варьирует от 4 % до 11 % у мужчин с уровнем ПСА от 0 до 2,9 нг/мл, и от 33 % до 83 % —
от 3 до 9,9 нг/мл и выше [6]. В связи с тем, что оба
этих метода имеют независимую друг от друга диагностическую ценность, рекомендовано применять
их комбинацию.
1.2. ПСА и его производные. Несмотря на то, что
уровень ПСА в плазме крови повышается при различных заболеваниях предстательной железы —
РПЖ, доброкачественной гиперплазии предстательной железы (ДГПЖ) и простатите, ПСА остается
практически единственным маркером, применяемым в целях ранней диагностики РПЖ. Однако
единых общепринятых международных стандартов
в отношении пороговых значений ПСА, которые
могли бы использоваться для диагностики РПЖ,
не существует [7]. Результаты недавнего исследования по профилактике РПЖ, проведенного в США,
подтвердили, что у многих мужчин РПЖ может
присутствовать, несмотря на низкий уровень ПСА
крови [8] (см. табл. 1).
При использовании более высоких условных
границ уровня ПСА (>4 нг/мл) для принятия решения о целесообразности проведении биопсии простаты повышается и риск пропустить клинически
значимый РПЖ; в тоже время при снижении этого
показателя (< 4 нг/мл) возрастает доля неоправданно выполненных биопсий простаты, когда новообразование отсутствует. До настоящего времени нет
данных литературы, которые позволили бы определить оптимальное пороговое значение ПСА, при
котором необходима биопсия простаты для выявления непальпируемого, но клинически значимого
РПЖ [9].
Таблица 1. Риск РПЖ при низком уровне ПСА в плазме крови
| Уровень ПСА, нг/мл | Риск РПЖ, % |
| 0-0,5 | 6,6 |
| 0,6–1 | 10,1 |
| 1,1–2 | 17,0 |
| 2,1–3 | 23,9 |
| 3,1–4 | 26,9 |
Производные ПСА — скорость нарастания и время удвоения ПСА — были предложены различными
исследователями [10, 11], однако при углубленном
изучении оказалось, что они не представляют большей ценности по сравнению с ПСА, и в настоящее
время не включены в клинические рекомендации
по диагностике РПЖ [9].
В отличие от них, расчет % свободного ПСА
оказался более значимым показателем, используемым преимущественно для выявления РПЖ у больных при значениях ПСА от 4 до 10 нг/мл и отрицательном результате ПРИ. РПЖ выявляют более
чем у половины мужчин с % свободного ПСА < 10,
в то время как при % свободного ПСА > 10 частота
выявляемости РПЖ на превышает 8 % [12].
1.3. PCA3. Относительно новый и интенсивно
исследуемый в настоящее время маркер — PCA3
(простатоспецифический некодирующий мРНК),
который определяют в осадке мочи после массажа простаты. Этот маркер имеет более высокую
чувствительность и специфичность по сравнению с ПСА, не зависит от объема простаты и наличия простатита у больного [13]. Сравнительно
небольшое число опубликованных работ по анализу диагностической ценности этого маркера
не позволяет рекомендовать его для широкого
использования в клинической практике. В связи
с этим в настоящее время этот маркер можно рассматривать как экспериментальный метод диагностики РПЖ.
1.4. ТРУЗИ. Классическая картина гипоэхогенного образования, расположенного в периферической зоне простаты, встречается не всегда, поэтому
ТРУЗИне относят к методам, позволяющим достоверно определять наличие РПЖ. ТРУЗ-контроль
получил широкое распространение при выполнении биопсии простаты.
1.5. Биопсия простаты. Биопсия предстательной железы является достоверным методом верификации диагноза РПЖ. Многими авторами были
предложены различные методики выполнения
этого исследования, отличающиеся по количеству
и участкам расположения биопсийных вколов.
При объёме ПЖ 30–40 см3 необходимо проводить
биопсию не менее чем из 8 точек. С увеличением
количества точек более 12, точность анализа существенно не изменяется [14]. На основании результатов Британского исследования по диагностике и лечению РПЖ была рекомендована биопсия
из 10 точек [15].
II. МЕТОДЫ СТАДИРОВАНИЯ РПЖ
2.1. ПРИ. Принято выделять клиническое стадирование, основанное на данных ПРИ, определении
уровня ПСА, рентгенологических, радиоизотопных
и других клинических методах исследования, а также патологоанатомическое стадирование, которое
становится возможным после морфологического
анализа удаленной предстательной железы, семенных пузырьков и лимфатических узлов. Патологоанатомическое стадирование более точно позволяет
оценить распространение болезни и судить о ее прогнозе. Наиболее важными патологоанатомическими прогностическим факторами после радикальной
простатэктомии являются степень дифференцировки новообразования, позитивный хирургический
край, экстракапсулярное распространение опухоли, ее инвазия в семенные пузырьки и метастазирование в тазовые лимфатические узлы. Сведения
об ошибках патологоанатомического стадирования
не включены в настоящий обзор литературы.
ПРИ позволяет определить не только наличие
РПЖ, но и степень его местного распространения.
Пальпируемая опухоль в простате — это признак,
характерный для низкодифференцированного РПЖ
(степень злокачественности по Gleason — 8–10 баллов). Чувствительность и воспроизводимость
ПРИ весьма низкие, что приводит как к недооценке, так и к переоценке степени распространения
РПЖ. Чувствительность метода при определении
клинической стадии РПЖ не превышает 30 % [16].
Стадия рака простаты правильно диагностируется
с помощью данного исследования менее чем в 50 %
случаев [17].
2.2. ПСА. Более высокий уровень ПСА в плазме крови косвенно указывает на большую степень
распространения РПЖ, но не позволяет достоверно
предсказать ни клиническую, ни патоморфологическую его стадию [18, 19].
2.3. ТРУЗИ позволяет выявить только 60 % опухолей простаты, остальные не распознаются из-за
эхогенности, сходной с таковой у окружающих
здоровых тканях. При этом остаются недиагностированными более 60 % РПЖ на стадии рТ3 [20].
ТРУЗИ в комбинации с цветной допплерографией
позволяет визуализировать проходящие через капсулу кровеносные сосуды, что типично при экстракапсулярном распространении новообразования
[21, 22]. Однако эта методика имеет низкую воспроизводимость, в связи с чем ее относят к категории
вспомогательных.
2.4. Биопсия простаты. По результатам биопсии простаты можно оценить степень местного распространения РПЖ, а также степень злокачественности новообразования в баллах по шкале Gleason.
Процент пораженной ткани — наиболее надежный
прогностический фактор риска инвазии опухоли
в семенные пузырьки и экстракапсулярного распространения новообразования.
2.5. КТ и МРТ недостаточно надежно позволяют
судить о степени распространения РПЖ, чтобы рекомендовать их как обязательные методы обследования. МРТ с эндоректальной катушкой позволяет
более точно определить стадию РПЖ и прорастание
опухоли в семенные пузырьки. Однако на фоне геморроидальных и воспалительных изменений ПЖ
или после ее биопсии интерпретация данных может
быть затруднена [9]. Сочетание контрастной МРТ
и МРТ в Т2‑режиме усиления и применение МРТспектроскопии позволяет лучше верифицировать
опухолевую ткань и диагностировать экстракапсулярное распространение опухоли [23].
Недостатки методов визуализации при РПЖ:
- Ложноотрицательные результаты из-за постбиопсийной крови.
- Артефакты от газа в прямой кишке, перистальтики.
- Ложноположительные очаги.
- Ложноотрицательные результаты ЭМРТ при
РПЖ с инвазией в прямую кишку. - Выявление РПЖ в центральной зоне.
- Невыявляемые очаги рака.
- Высокая зависимость от опыта рентгенолога.
Пути решения: - МРТ до биопсии или через 4 недели после нее.
- Подготовка пациента (микроклизма).
- Динамическое контрастирование.
- МРТ с поверхностной катушкой.
- МР-спектроскопия.
- Субспециализация.
2.6. Высокотехнологичные методы стадирования РПЖ. К новым перспективным методам, позволяющим получить изображение, можно отнести
ПЭТ, при помощи которого диагностируют около
70 % РПЖ на стадии рТ2 и pT3a‑4 [9]. При этом
очаг рака и микрометастазы < 5 мм остаются нераспознанными.
Наиболее перспективным методом визуализации является совмещённая позитронноэмиссионная/компьютерная томография. Этот
метод дает возможность за одно обследование получить информацию об анатомическом строении
и метаболических процессах. Метаболические
процессы (по результатам ПЭТ) здесь могут соотноситься с определенной анатомической локализацией (по данным КТ). Совмещённая позитронноэмиссионная/компьютерная томография имеет
более высокую точность разрешения — до 2 мм, однако также как и ПЭТ подразумевает использование специфичных для опухолевой ткани радиофармпрепаратов.
К современным ультразвуковым высокотехнологичным методам диагностики и стадирования РПЖ
относят эластографию и гистосканнинг.
Эластография — это неинвазивная методика,
используемая при диагностике опухолей, при которой оценивается степень жесткости (эластичность) мягких тканей. В основу методики положена
классическая методика пальпации объемных образований. Опухолевая ткань имеет коэффициент
жесткости до 28 раз превосходящий аналогичный
показатель здоровой ткани. В момент механической компрессии опухоль деформируется меньше,
чем окружающие ткани. При эластографии пальпация осуществляется посредством ультразвуковой
волны и механической компрессии. Программное
обеспечение ультразвукового аппарата обрабатывает принятый отраженный сигнал и воспроизводит
изображение на экране в формате цветного картирования, что позволяет дифференцировать ткани
в зависимости от эластичности. В результате более
плотные структуры тканей отображается оттенками
синего цвета, а легко сжимаемые эластичные участки маркируются красной цветовой шкалой. Результаты эластографии могут помочь в принятии решения о биопсии и выборе участка — «мишени» при
неоднозначных данных ПСА; использование данного метода возможно даже после повторных биопсий
предстательной железы. К недостаткам эластографии относят: высокую зависимость от опыта врача,
производящего исследование, сложность овладения
данным методом диагностики, а также низкая повторяемость результатов.
Гистосканнинг является еще одним новым высокотехнологичным методом ультразвуковой диагностики и стадирования рака предстательной железы.
Осуществляется дифференцировка между опухолевой и здоровой тканью, определение локализации
опухоли при малых ее размерах, невыявляемых с помощью стандартного ТРУЗИ. Чувствительность метода составляет 90 %, специфичность — 72 % [24].
В результате исследования получают информацию
о локализации зон, подозрительных на опухолевые,
что позволяет выполнить прицельную биопсию.
2.7. Номограммы. Большим числом групп исследователей были предложены разнообразные алгоритмы и номограммы для определения местного
распространения РПЖ, вероятности лимфогенного
метастазирования, а также принадлежности пациентов к прогностически неблагоприятной группе.
В основе метода — комплексная оценка результатов
ПРИ, уровня ПСА в плазме крови и степени дифференцировки новообразования. Одним из примеров
может быть индекс CAPRA, позволяющий оценить
вероятность безрецидивной выживаемости больных РПЖ на основании совокупности клинических
и морфологических критериев [25]. Использование
комбинации показателя уровня ПСА, индекса Глисона при биопсии простаты и клинической стадии Т
(номограмма Партина) дает лучшие результаты при
прогнозировании патоморфологической стадии,
чем каждый из параметров по отдельности [26].
2.8. N, M-стадирование. Тазовая лимфаденэктомия — золотой стандарт
определения метастазирования в лимфатические
узлы, N (открытым или лапароскопическим доступом).
М‑стадирование. У 85 % больных, умерших
от РПЖ, отмечают метастатическое поражение скелета [27]. Наличие и распространенность метастазов в кости позволяет определить прогноз в каждом
конкретном случае. Повышенный уровень щелочной фосфатазы, специфичной для костной ткани,
у 70 % может указывать на наличие метастазов в кости [28], однако наиболее чувствительным методом
исследования является остеосцинтиграфия. Помимо костей раковыми клетками могут быть поражены
отдаленные лимфоузлы, легкие, печень, головной
мозг, кожа. В зависимости от локализации отдаленных метастазов для их выявления при мягкотканой
локализации могут быть применены клинический
осмотр, рентгенография грудной клетки, УЗИ, КТ,
МРТ. При уровне ПСА в плазме крови >100 нг/мл
практически у всех больных имеют место отдаленные метастазы РПЖ [29].
III. Причины ошибок при
диагностике и стадировании РПЖ
Среди причин, приводящих к ошибкам при диагностике и стадировании РПЖ можно выделить
субъективные и объективные.
Субъективные:
- Недостаточная квалификация специалистов.
- Неправильная интерпретация данных обследования.
Объективные:
- Отсутствие высоко специфичных методов
диагностики. - Недостаточное использование современных
методов диагностики. - Неиспользование стандартных рекомендаций, предложенных Европейской ассоциацией урологов.
В заключении следует отметить, что в последние
годы предпринимаются попытки совершенствования
методов ранней диагностики и стадирования РПЖ.
Однако существует потребность в создании новых,
более точных методов, позволяющих выявлять клинически значимый РПЖ. К перспективным методам, позволяющим оптимизировать процессы диагностики и стадирования, можно отнести ПЭТ/КТ,
диффузионную МРТ, МР-спектроскопию, динамическую МРТ с повышением контраста. Необходима дальнейшая разработка специфичных для РПЖ
радиофармпрепаратов. Кроме того, важна унификация при интерпретации полученных данных — использование рекомендаций Европейской ассоциации урологов.
Список литературы
- Чиссов В. И., Русаков И. Г. Заболеваемость раком предстательной железы в Российской Федерации // Экспериментальная и клиническая урология. — 2011. — № 2–3. — С. 6–7.
- Quinn M., Babb P. Patterns and trends in prostate cancer incidence,
survival, prevalence and mortality. Part I: international comparisons
// B. J. U. Int. — 2002. — Vol. 90, N 2. — P. 162–173. - Ilic D., O’Connor D., Green S., Wilt T. J. Screening for prostate
cancer: a Cochrane systematic review // Cancer Causes Control.
— 2007. — Vol. 18, N 3. — P. 279–285. - Andriole G. L., Crawford E. D., Grubb R. L. 3rd. et al. Mortality results
from a randomized prostate-cancer screening trial // N. Engl.
J. Med. — 2009. — Vol. 360, N 13. — P. 1310–1319. - Schröder F. H., Hugosson J., Roobol M. J. et al. Screening
and prostate-cancer mortality in a randomized European
study // N. Engl. J. Med. — 2009. — Vol. 360, N 13. —
P. 1320–1328. - Schröder F. H., van der Maas P., Beemsterboer P. et al. Evaluation
of the digital rectal examination as a screening test for prostate
cancer. Rotterdam section of the European Randomized Study of
Screening for Prostate Cancer // J. Natl. Cancer Inst. — 1998. —
Vol. 90, N 23. — P. 1817–1823. - Semjonow A., Brandt B., Oberpenning F. et al. Discordance of
assay methods creates pitfalls for the interpretation of prostatespecific
antigen values // Prostate. — 1996. — Suppl. 7. —
P. 3–16. - Thompson I. M., Pauler D. K., Goodman P. J. et al. Prevalence
of prostate cancer among men with a prostate-specific antigen
level < or = 4.0 ng per milliliter // N. Engl. J. Med. — 2004. —
Vol. 350, N 22. — P. 2239–2246. - Heidenreich A., Bellmunt J., Bolla M. et al. EAU guidelines on
prostate cancer. Part 1: screening, diagnosis, and treatment of
clinically localised disease // Eur. Urol. — 2011. — Vol. 59,
N 1. — P. 61–71. - Carter H. B., Pearson J. D., Metter E. J. et al. Longitudinal evaluation
of prostate-specific antigen levels in men with and without
prostate disease // JAMA. — 1992. — Vol. 267, N 16. —
P. 2215–2220. - Schmid H.-P., McNeal J. E., Stamey T. A. Observations on the
doubling time of prostate cancer. The use of serial prostate-specific
antigen in patients with untreated disease as a measure of increasing cancer volume // Cancer. . 1993. . Vol. 71, N 6. .
P. 2031.2040. - Catalona W. J., Partin A. W., Slawin K. M. et al. Use of the percentage
of free prostate-specific antigen to enhance differentiation of
prostate cancer from benign prostatic disease: a prospective multicentre
clinical trial // JAMA. . 1998. . Vol. 279, N 19. .
P. 1542.1547. - Deras I. L., Aubin S. M., Blase A. et al. PCA3: a molecular urine assay
for predicting prostate biopsy outcome // J. Urol. . 2008. .
Vol. 179, N 4. . P. 1587.1592. - Eichler K., Hempel S., Wilby J. et al. Diagnostic value of systematic
biopsy methods in the investigation of prostate cancer:
a systematic review // J. Urol. . 2006. . Vol. 175, N 5. .
P. 1605.1612. - Donovan J., Hamdy F., Neal D. et al. Prostate Testing for Cancer
and Treatment (ProtecT) feasibility study // Health Technol. Assess.
. 2003. . Vol. 7, N 14. . P. 1.32. - Матвеев Б. П. Клиническая онкоурология. — М.: Вердана,
2003. — 717 с. - Spigelman S. S., McNeal J. E., Freiha F. S., Stamey T. A. Rectal
examination in volume determination of carcinoma of the prostate:
clinical and anatomical correlations // J. Urol. . 1986. .
Vol. 136, N 6. . P. 1228.1230. - Partin A. W., Carter H. B., Chan D. W. et al. Prostate specific antigen
in the staging of localized prostate cancer: influence of tumour
differentiation, tumour volume and benign hyperplasia //
J. Urol. . 1990. . Vol. 143, N 4. . P. 747.752. - Hudson M. A., Bahnson R. R., Catalona W. J. Clinical use of prostate
specific antigen in patients with prostate cancer // J. Urol. .
1989. . Vol. 142, N 4. . P. 1011.1017. - Enlund A., Pedersen K., Boeryd B., Varenhorst E. Transrectal
ultrasonography compared to histopathological assessment for
local staging of prostatic carcinoma // Acta Radiol. . 1990. .
Vol. 31, N 6. . P. 597.600. - Sauvain J. L., Palascak P., Bourscheid D. et al. Value of power
and 3D vascular sonography as a method for diagnosis and staging
of prostate cancer // Eur. Urol. . 2003. . Vol. 44, N 1. .
P. 21.30; discussion 30.31. - 22. Zalesky M., Urban M., Smerhovsky Z. et al. Value of power Doppler
sonography with 3D reconstruction in preoperative diagnostics
of extraprostatic tumor extension in clinically localized prostate
cancer // Int. J. Urol. . 2008. . Vol. 15, N 1. . P. 68.75;
discussion 75. - Fuchsjager M., Shukla-Dave A., Akin O. et al. Prostate cancer imaging
// Acta Radiol. . 2008. . Vol. 49, N 1. . P. 107.120. - Simmons L. A., Autier P., Zat’ura F. et al. Detection, localisation
and characterisation of prostate cancer by prostate HistoScanning
(.) // B. J. U. Int. . 2012. . Vol. 110, N 1. . P. 28.35. - Cooperberg M. R., Freedland S. J., Pasta D. J. et al. Multiinstitutional
validation of the UCSF cancer of the prostate risk assessment
for prediction of recurrence after radical prostatectomy //
Cancer. . 2006. . Vol. 107, N 10. . P. 2384.2391. - Partin A. W., Mangold L. A., Lamm D. M. et al. Contemporary update
of the prostate cancer staging nomograms (Partin Tables)
for the new millennium // Urology. . 2001. . Vol. 58, N 6. .
P. 843.848. - Whitmore W. F. Jr. Natural history and staging of prostate cancer //
Urol. Clin. North Am. . 1984. . Vol. 11, N 2. . P. 205.220. - Wolff J. M., Ittel T. H., Borchers H. et al. Metastatic workup of patients
with prostate cancer employing alkaline phosphatase and
skeletal alkaline phosphatase // Anticancer Res. . 1999. .
Vol. 19, N 4A. . P. 2653.2655. - Rana A., Karamanis K., Lucas M. G., Chisholm G. D. Identification
of metastatic disease by T category, Gleason score and serum PSA
level in patients with carcinoma of the prostate // Br. J. Urol. .
1992. . Vol. 69, N 3. . P. 277.281.