С. Х. Аль-Шукри, С. Ю. Боровец, М. А. Рыбалов
Кафедра урологии Санкт-Петербургского государственного медицинского университета
имени акад. И. П. Павлова
В данном обзоре оцениваются преимущества и недостатки основных методов диагностики и
стадирования рака предстательной железы, приводятся сведения о современных высокотехнологичных методах стадирования и номограммах. Рассматриваются причины ошибок, возникающих
при диагностике и стадировании рака предстательной железы.
Ключевые слова: рак предстательной железы; диагностика; стадирование.
Введение
Повышение эффективности лечения рака предстательной железы (РПЖ) является одной из наиболее актуальных проблем современной урологии.
В мире РПЖ занимает 3–4 место в структуре заболеваемости злокачественными новообразованиями.
В России заболеваемость РПЖ в 2004 году составляла 6,9 %, а в 2009 году — уже 10,7 % [1]. При этом
за последние три десятилетия возросло число мужчин, умерших от этого заболевания [2].
I. МЕТОДЫ ДИАГНОСТИКИ РПЖ
Методы диагностики рпж — включают оценку
результатов пальцевого ректального исследования
(ПРИ), определении уровня ПСА в плазме крови.
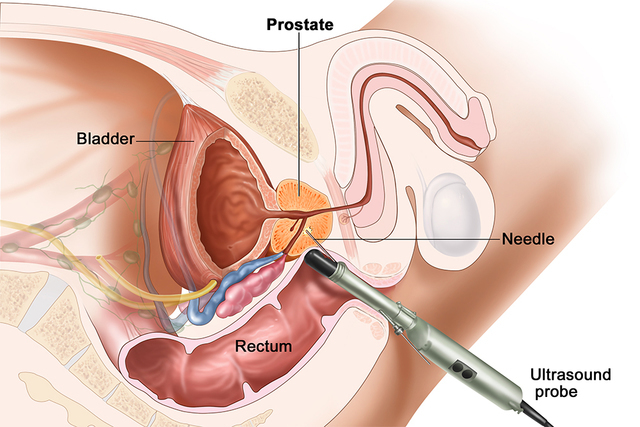
Окончательный диагноз РПЖ может быть установлен только по результатам биопсии предстательной
железы, которую целесообразно выполнять под
ТРУЗ-контролем. При клиническом стадировании
для уточнения границ местного распространения
новообразования предстательной железы и для выявления местных и отдаленных метастазов в дополнение используют различные методы, позволяющие
получить изображение: компьютерную томографию
(КТ), магнитно-резонансную томографию (МРТ),
сцинтиграфию костей скелета и др. Однако результаты этих методов могут быть интерпретированы ошибочно как в пользу гипо, так и гипердиагностики.
Работы многих исследователей посвящены оптимизации скрининга и ранней диагностики РПЖ [3–5].
1.1. ПРИ. До внедрения в широкую клиническую практику ПСА, ПРИ было единственным
методом диагностики РПЖ. Большинство злокачественных новообразований РПЖ располагаются
в периферической зоне простаты и могут быть выявлены с помощью ПРИ, если их объем превышает
0,2 см 3. Положительная прогностическая ценность ПРИ варьирует от 4 % до 11 % у мужчин с уровнем ПСА от 0 до 2,9 нг/мл, и от 33 % до 83 % —
от 3 до 9,9 нг/мл и выше [6]. В связи с тем, что оба
этих метода имеют независимую друг от друга диагностическую ценность, рекомендовано применять
их комбинацию.
1.2. ПСА и его производные. Несмотря на то, что
уровень ПСА в плазме крови повышается при различных заболеваниях предстательной железы —
РПЖ, доброкачественной гиперплазии предстательной железы (ДГПЖ) и простатите, ПСА остается
практически единственным маркером, применяемым в целях ранней диагностики РПЖ. Однако
единых общепринятых международных стандартов
в отношении пороговых значений ПСА, которые
могли бы использоваться для диагностики РПЖ,
не существует [7]. Результаты недавнего исследования по профилактике РПЖ, проведенного в США,
подтвердили, что у многих мужчин РПЖ может
присутствовать, несмотря на низкий уровень ПСА
крови [8] (см. табл. 1).
При использовании более высоких условных
границ уровня ПСА (>4 нг/мл) для принятия решения о целесообразности проведении биопсии простаты повышается и риск пропустить клинически
значимый РПЖ; в тоже время при снижении этого
показателя (< 4 нг/мл) возрастает доля неоправданно выполненных биопсий простаты, когда новообразование отсутствует. До настоящего времени нет
данных литературы, которые позволили бы определить оптимальное пороговое значение ПСА, при
котором необходима биопсия простаты для выявления непальпируемого, но клинически значимого
РПЖ [9].
Таблица 1. Риск РПЖ при низком уровне ПСА в плазме крови
| Уровень ПСА, нг/мл | Риск РПЖ, % |
| 0-0,5 | 6,6 |
| 0,6–1 | 10,1 |
| 1,1–2 | 17,0 |
| 2,1–3 | 23,9 |
| 3,1–4 | 26,9 |
Производные ПСА — скорость нарастания и время удвоения ПСА — были предложены различными
исследователями [10, 11], однако при углубленном
изучении оказалось, что они не представляют большей ценности по сравнению с ПСА, и в настоящее
время не включены в клинические рекомендации
по диагностике РПЖ [9].
В отличие от них, расчет % свободного ПСА
оказался более значимым показателем, используемым преимущественно для выявления РПЖ у больных при значениях ПСА от 4 до 10 нг/мл и отрицательном результате ПРИ. РПЖ выявляют более
чем у половины мужчин с % свободного ПСА < 10,
в то время как при % свободного ПСА > 10 частота
выявляемости РПЖ на превышает 8 % [12].
1.3. PCA3. Относительно новый и интенсивно
исследуемый в настоящее время маркер — PCA3
(простатоспецифический некодирующий мРНК),
который определяют в осадке мочи после массажа простаты. Этот маркер имеет более высокую
чувствительность и специфичность по сравнению с ПСА, не зависит от объема простаты и наличия простатита у больного [13]. Сравнительно
небольшое число опубликованных работ по анализу диагностической ценности этого маркера
не позволяет рекомендовать его для широкого
использования в клинической практике. В связи
с этим в настоящее время этот маркер можно рассматривать как экспериментальный метод диагностики РПЖ.
1.4. ТРУЗИ. Классическая картина гипоэхогенного образования, расположенного в периферической зоне простаты, встречается не всегда, поэтому
ТРУЗИне относят к методам, позволяющим достоверно определять наличие РПЖ. ТРУЗ-контроль
получил широкое распространение при выполнении биопсии простаты.
1.5. Биопсия простаты. Биопсия предстательной железы является достоверным методом верификации диагноза РПЖ. Многими авторами были
предложены различные методики выполнения
этого исследования, отличающиеся по количеству
и участкам расположения биопсийных вколов.
При объёме ПЖ 30–40 см3 необходимо проводить
биопсию не менее чем из 8 точек. С увеличением
количества точек более 12, точность анализа существенно не изменяется [14]. На основании результатов Британского исследования по диагностике и лечению РПЖ была рекомендована биопсия
из 10 точек [15].
II. МЕТОДЫ СТАДИРОВАНИЯ РПЖ
2.1. ПРИ. Принято выделять клиническое стадирование, основанное на данных ПРИ, определении
уровня ПСА, рентгенологических, радиоизотопных
и других клинических методах исследования, а также патологоанатомическое стадирование, которое
становится возможным после морфологического
анализа удаленной предстательной железы, семенных пузырьков и лимфатических узлов. Патологоанатомическое стадирование более точно позволяет
оценить распространение болезни и судить о ее прогнозе. Наиболее важными патологоанатомическими прогностическим факторами после радикальной
простатэктомии являются степень дифференцировки новообразования, позитивный хирургический
край, экстракапсулярное распространение опухоли, ее инвазия в семенные пузырьки и метастазирование в тазовые лимфатические узлы. Сведения
об ошибках патологоанатомического стадирования
не включены в настоящий обзор литературы.
ПРИ позволяет определить не только наличие
РПЖ, но и степень его местного распространения.
Пальпируемая опухоль в простате — это признак,
характерный для низкодифференцированного РПЖ
(степень злокачественности по Gleason — 8–10 баллов). Чувствительность и воспроизводимость
ПРИ весьма низкие, что приводит как к недооценке, так и к переоценке степени распространения
РПЖ. Чувствительность метода при определении
клинической стадии РПЖ не превышает 30 % [16].
Стадия рака простаты правильно диагностируется
с помощью данного исследования менее чем в 50 %
случаев [17].
2.2. ПСА. Более высокий уровень ПСА в плазме крови косвенно указывает на большую степень
распространения РПЖ, но не позволяет достоверно
предсказать ни клиническую, ни патоморфологическую его стадию [18, 19].
2.3. ТРУЗИ позволяет выявить только 60 % опухолей простаты, остальные не распознаются из-за
эхогенности, сходной с таковой у окружающих
здоровых тканях. При этом остаются недиагностированными более 60 % РПЖ на стадии рТ3 [20].
ТРУЗИ в комбинации с цветной допплерографией
позволяет визуализировать проходящие через капсулу кровеносные сосуды, что типично при экстракапсулярном распространении новообразования
[21, 22]. Однако эта методика имеет низкую воспроизводимость, в связи с чем ее относят к категории
вспомогательных.
2.4. Биопсия простаты. По результатам биопсии простаты можно оценить степень местного распространения РПЖ, а также степень злокачественности новообразования в баллах по шкале Gleason.
Процент пораженной ткани — наиболее надежный
прогностический фактор риска инвазии опухоли
в семенные пузырьки и экстракапсулярного распространения новообразования.
2.5. КТ и МРТ недостаточно надежно позволяют
судить о степени распространения РПЖ, чтобы рекомендовать их как обязательные методы обследования. МРТ с эндоректальной катушкой позволяет
более точно определить стадию РПЖ и прорастание
опухоли в семенные пузырьки. Однако на фоне геморроидальных и воспалительных изменений ПЖ
или после ее биопсии интерпретация данных может
быть затруднена [9]. Сочетание контрастной МРТ
и МРТ в Т2‑режиме усиления и применение МРТспектроскопии позволяет лучше верифицировать
опухолевую ткань и диагностировать экстракапсулярное распространение опухоли [23].
Недостатки методов визуализации при РПЖ:
- Ложноотрицательные результаты из-за постбиопсийной крови.
- Артефакты от газа в прямой кишке, перистальтики.
- Ложноположительные очаги.
- Ложноотрицательные результаты ЭМРТ при
РПЖ с инвазией в прямую кишку. - Выявление РПЖ в центральной зоне.
- Невыявляемые очаги рака.
- Высокая зависимость от опыта рентгенолога.
Пути решения: - МРТ до биопсии или через 4 недели после нее.
- Подготовка пациента (микроклизма).
- Динамическое контрастирование.
- МРТ с поверхностной катушкой.
- МР-спектроскопия.
- Субспециализация.
2.6. Высокотехнологичные методы стадирования РПЖ. К новым перспективным методам, позволяющим получить изображение, можно отнести
ПЭТ, при помощи которого диагностируют около
70 % РПЖ на стадии рТ2 и pT3a‑4 [9]. При этом
очаг рака и микрометастазы < 5 мм остаются нераспознанными.
Наиболее перспективным методом визуализации является совмещённая позитронноэмиссионная/компьютерная томография. Этот
метод дает возможность за одно обследование получить информацию об анатомическом строении
и метаболических процессах. Метаболические
процессы (по результатам ПЭТ) здесь могут соотноситься с определенной анатомической локализацией (по данным КТ). Совмещённая позитронноэмиссионная/компьютерная томография имеет
более высокую точность разрешения — до 2 мм, однако также как и ПЭТ подразумевает использование специфичных для опухолевой ткани радиофармпрепаратов.
К современным ультразвуковым высокотехнологичным методам диагностики и стадирования РПЖ
относят эластографию и гистосканнинг.
Эластография — это неинвазивная методика,
используемая при диагностике опухолей, при которой оценивается степень жесткости (эластичность) мягких тканей. В основу методики положена
классическая методика пальпации объемных образований. Опухолевая ткань имеет коэффициент
жесткости до 28 раз превосходящий аналогичный
показатель здоровой ткани. В момент механической компрессии опухоль деформируется меньше,
чем окружающие ткани. При эластографии пальпация осуществляется посредством ультразвуковой
волны и механической компрессии. Программное
обеспечение ультразвукового аппарата обрабатывает принятый отраженный сигнал и воспроизводит
изображение на экране в формате цветного картирования, что позволяет дифференцировать ткани
в зависимости от эластичности. В результате более
плотные структуры тканей отображается оттенками
синего цвета, а легко сжимаемые эластичные участки маркируются красной цветовой шкалой. Результаты эластографии могут помочь в принятии решения о биопсии и выборе участка — «мишени» при
неоднозначных данных ПСА; использование данного метода возможно даже после повторных биопсий
предстательной железы. К недостаткам эластографии относят: высокую зависимость от опыта врача,
производящего исследование, сложность овладения
данным методом диагностики, а также низкая повторяемость результатов.
Гистосканнинг является еще одним новым высокотехнологичным методом ультразвуковой диагностики и стадирования рака предстательной железы.
Осуществляется дифференцировка между опухолевой и здоровой тканью, определение локализации
опухоли при малых ее размерах, невыявляемых с помощью стандартного ТРУЗИ. Чувствительность метода составляет 90 %, специфичность — 72 % [24].
В результате исследования получают информацию
о локализации зон, подозрительных на опухолевые,
что позволяет выполнить прицельную биопсию.
2.7. Номограммы. Большим числом групп исследователей были предложены разнообразные алгоритмы и номограммы для определения местного
распространения РПЖ, вероятности лимфогенного
метастазирования, а также принадлежности пациентов к прогностически неблагоприятной группе.
В основе метода — комплексная оценка результатов
ПРИ, уровня ПСА в плазме крови и степени дифференцировки новообразования. Одним из примеров
может быть индекс CAPRA, позволяющий оценить
вероятность безрецидивной выживаемости больных РПЖ на основании совокупности клинических
и морфологических критериев [25]. Использование
комбинации показателя уровня ПСА, индекса Глисона при биопсии простаты и клинической стадии Т
(номограмма Партина) дает лучшие результаты при
прогнозировании патоморфологической стадии,
чем каждый из параметров по отдельности [26].
2.8. N, M-стадирование. Тазовая лимфаденэктомия — золотой стандарт
определения метастазирования в лимфатические
узлы, N (открытым или лапароскопическим доступом).
М‑стадирование. У 85 % больных, умерших
от РПЖ, отмечают метастатическое поражение скелета [27]. Наличие и распространенность метастазов в кости позволяет определить прогноз в каждом
конкретном случае. Повышенный уровень щелочной фосфатазы, специфичной для костной ткани,
у 70 % может указывать на наличие метастазов в кости [28], однако наиболее чувствительным методом
исследования является остеосцинтиграфия. Помимо костей раковыми клетками могут быть поражены
отдаленные лимфоузлы, легкие, печень, головной
мозг, кожа. В зависимости от локализации отдаленных метастазов для их выявления при мягкотканой
локализации могут быть применены клинический
осмотр, рентгенография грудной клетки, УЗИ, КТ,
МРТ. При уровне ПСА в плазме крови >100 нг/мл
практически у всех больных имеют место отдаленные метастазы РПЖ [29].
III. Причины ошибок при
диагностике и стадировании РПЖ
Среди причин, приводящих к ошибкам при диагностике и стадировании РПЖ можно выделить
субъективные и объективные.
Субъективные:
- Недостаточная квалификация специалистов.
- Неправильная интерпретация данных обследования.
Объективные:
- Отсутствие высоко специфичных методов
диагностики. - Недостаточное использование современных
методов диагностики. - Неиспользование стандартных рекомендаций, предложенных Европейской ассоциацией урологов.
В заключении следует отметить, что в последние
годы предпринимаются попытки совершенствования
методов ранней диагностики и стадирования РПЖ.
Однако существует потребность в создании новых,
более точных методов, позволяющих выявлять клинически значимый РПЖ. К перспективным методам, позволяющим оптимизировать процессы диагностики и стадирования, можно отнести ПЭТ/КТ,
диффузионную МРТ, МР-спектроскопию, динамическую МРТ с повышением контраста. Необходима дальнейшая разработка специфичных для РПЖ
радиофармпрепаратов. Кроме того, важна унификация при интерпретации полученных данных — использование рекомендаций Европейской ассоциации урологов.
Список литературы
- Чиссов В. И., Русаков И. Г. Заболеваемость раком предстательной железы в Российской Федерации // Экспериментальная и клиническая урология. — 2011. — № 2–3. — С. 6–7.
- Quinn M., Babb P. Patterns and trends in prostate cancer incidence,
survival, prevalence and mortality. Part I: international comparisons
// B. J. U. Int. — 2002. — Vol. 90, N 2. — P. 162–173. - Ilic D., O’Connor D., Green S., Wilt T. J. Screening for prostate
cancer: a Cochrane systematic review // Cancer Causes Control.
— 2007. — Vol. 18, N 3. — P. 279–285. - Andriole G. L., Crawford E. D., Grubb R. L. 3rd. et al. Mortality results
from a randomized prostate-cancer screening trial // N. Engl.
J. Med. — 2009. — Vol. 360, N 13. — P. 1310–1319. - Schröder F. H., Hugosson J., Roobol M. J. et al. Screening
and prostate-cancer mortality in a randomized European
study // N. Engl. J. Med. — 2009. — Vol. 360, N 13. —
P. 1320–1328. - Schröder F. H., van der Maas P., Beemsterboer P. et al. Evaluation
of the digital rectal examination as a screening test for prostate
cancer. Rotterdam section of the European Randomized Study of
Screening for Prostate Cancer // J. Natl. Cancer Inst. — 1998. —
Vol. 90, N 23. — P. 1817–1823. - Semjonow A., Brandt B., Oberpenning F. et al. Discordance of
assay methods creates pitfalls for the interpretation of prostatespecific
antigen values // Prostate. — 1996. — Suppl. 7. —
P. 3–16. - Thompson I. M., Pauler D. K., Goodman P. J. et al. Prevalence
of prostate cancer among men with a prostate-specific antigen
level < or = 4.0 ng per milliliter // N. Engl. J. Med. — 2004. —
Vol. 350, N 22. — P. 2239–2246. - Heidenreich A., Bellmunt J., Bolla M. et al. EAU guidelines on
prostate cancer. Part 1: screening, diagnosis, and treatment of
clinically localised disease // Eur. Urol. — 2011. — Vol. 59,
N 1. — P. 61–71. - Carter H. B., Pearson J. D., Metter E. J. et al. Longitudinal evaluation
of prostate-specific antigen levels in men with and without
prostate disease // JAMA. — 1992. — Vol. 267, N 16. —
P. 2215–2220. - Schmid H.-P., McNeal J. E., Stamey T. A. Observations on the
doubling time of prostate cancer. The use of serial prostate-specific
antigen in patients with untreated disease as a measure of increasing cancer volume // Cancer. . 1993. . Vol. 71, N 6. .
P. 2031.2040. - Catalona W. J., Partin A. W., Slawin K. M. et al. Use of the percentage
of free prostate-specific antigen to enhance differentiation of
prostate cancer from benign prostatic disease: a prospective multicentre
clinical trial // JAMA. . 1998. . Vol. 279, N 19. .
P. 1542.1547. - Deras I. L., Aubin S. M., Blase A. et al. PCA3: a molecular urine assay
for predicting prostate biopsy outcome // J. Urol. . 2008. .
Vol. 179, N 4. . P. 1587.1592. - Eichler K., Hempel S., Wilby J. et al. Diagnostic value of systematic
biopsy methods in the investigation of prostate cancer:
a systematic review // J. Urol. . 2006. . Vol. 175, N 5. .
P. 1605.1612. - Donovan J., Hamdy F., Neal D. et al. Prostate Testing for Cancer
and Treatment (ProtecT) feasibility study // Health Technol. Assess.
. 2003. . Vol. 7, N 14. . P. 1.32. - Матвеев Б. П. Клиническая онкоурология. — М.: Вердана,
2003. — 717 с. - Spigelman S. S., McNeal J. E., Freiha F. S., Stamey T. A. Rectal
examination in volume determination of carcinoma of the prostate:
clinical and anatomical correlations // J. Urol. . 1986. .
Vol. 136, N 6. . P. 1228.1230. - Partin A. W., Carter H. B., Chan D. W. et al. Prostate specific antigen
in the staging of localized prostate cancer: influence of tumour
differentiation, tumour volume and benign hyperplasia //
J. Urol. . 1990. . Vol. 143, N 4. . P. 747.752. - Hudson M. A., Bahnson R. R., Catalona W. J. Clinical use of prostate
specific antigen in patients with prostate cancer // J. Urol. .
1989. . Vol. 142, N 4. . P. 1011.1017. - Enlund A., Pedersen K., Boeryd B., Varenhorst E. Transrectal
ultrasonography compared to histopathological assessment for
local staging of prostatic carcinoma // Acta Radiol. . 1990. .
Vol. 31, N 6. . P. 597.600. - Sauvain J. L., Palascak P., Bourscheid D. et al. Value of power
and 3D vascular sonography as a method for diagnosis and staging
of prostate cancer // Eur. Urol. . 2003. . Vol. 44, N 1. .
P. 21.30; discussion 30.31. - 22. Zalesky M., Urban M., Smerhovsky Z. et al. Value of power Doppler
sonography with 3D reconstruction in preoperative diagnostics
of extraprostatic tumor extension in clinically localized prostate
cancer // Int. J. Urol. . 2008. . Vol. 15, N 1. . P. 68.75;
discussion 75. - Fuchsjager M., Shukla-Dave A., Akin O. et al. Prostate cancer imaging
// Acta Radiol. . 2008. . Vol. 49, N 1. . P. 107.120. - Simmons L. A., Autier P., Zat’ura F. et al. Detection, localisation
and characterisation of prostate cancer by prostate HistoScanning
(.) // B. J. U. Int. . 2012. . Vol. 110, N 1. . P. 28.35. - Cooperberg M. R., Freedland S. J., Pasta D. J. et al. Multiinstitutional
validation of the UCSF cancer of the prostate risk assessment
for prediction of recurrence after radical prostatectomy //
Cancer. . 2006. . Vol. 107, N 10. . P. 2384.2391. - Partin A. W., Mangold L. A., Lamm D. M. et al. Contemporary update
of the prostate cancer staging nomograms (Partin Tables)
for the new millennium // Urology. . 2001. . Vol. 58, N 6. .
P. 843.848. - Whitmore W. F. Jr. Natural history and staging of prostate cancer //
Urol. Clin. North Am. . 1984. . Vol. 11, N 2. . P. 205.220. - Wolff J. M., Ittel T. H., Borchers H. et al. Metastatic workup of patients
with prostate cancer employing alkaline phosphatase and
skeletal alkaline phosphatase // Anticancer Res. . 1999. .
Vol. 19, N 4A. . P. 2653.2655. - Rana A., Karamanis K., Lucas M. G., Chisholm G. D. Identification
of metastatic disease by T category, Gleason score and serum PSA
level in patients with carcinoma of the prostate // Br. J. Urol. .
1992. . Vol. 69, N 3. . P. 277.281.
Журнал
Диагностика заболеваний редко обходится без инструментальных и лабораторных исследований. Оценки симптомов недостаточно — нужно узнать, что происходит внутри органов и тканей. Одним из наиболее точных методов обследования является биопсия. Врач производит забор тканевого материала в области предполагаемого патологического процесса с целью его дальнейшего изучения. Микроскопический анализ полученного образца помогает выявить характерные для определенного заболевания изменения. В онкологической практике биопсия считается информативным методом уточнения типа опухоли, ее стадирования.
- Что это за анализ?
- Показания к проведению
- Виды и способы проведения биопсии
- Подготовка
- Может ли биопсия быть ошибочной?
Что это за анализ?
Биопсия — высокоинформативный способ обследования, применяемый в случае необходимости анализа клеток в определенной анатомической области. Забор тканей с их последующим обследованием с помощью микроскопии дает возможность точно оценить клеточный состав. Без такой процедуры сложно обойтись, если врач подозревает наличие доброкачественного или злокачественного новообразования в определенном органе. Это уточняющее исследование, дополняющее результаты других диагностических процедур. Онколог анализирует результаты биопсии, рентгенографии, эндоскопии и иммунологических тестов совместно.
Онкологические заболевания развиваются быстро и угрожают жизни пациента. Нужно как можно раньше выбрать наиболее эффективную схему лечения. Именно с этой целью проводится биопсия. По результатам процедуры врач приходит к выводу, какие травматичные или даже опасные с точки зрения осложнений способы лечения уместны в данном случае. Подбирается тактика оперативного вмешательства, радиотерапии, химиотерапевтического лечения. Все это было бы невозможно без точного определения типа опухоли, ее стадии и распространенности в организме. Нужны цитологические и гистологические тесты.
В качестве примера можно привести злокачественное новообразование прямой кишки, растущее в нижней части органа. В качестве основного метода лечения выполняется иссечение этой анатомической структуры с последующим формированием колостомы для выделения каловых масс. Если диагноз не был полностью подтвержден, подобное вмешательство не проводят. Оно может по ошибке сделать пациента инвалидом.
Показания к проведению
Подобная диагностическая процедура требуется, если врач предполагает о наличии патологического процесса, подтверждение которого невозможно с помощью других способов исследования. В большинстве случаев это онкологические болезни, однако область применения биопсии ими не ограничивается. Например, такое исследование часто назначают гастроэнтерологи для оценки состояния слизистой оболочки органов пищеварительного тракта. Определяется вид воспалительного процесса, подбирается способ его лечения. В гинекологии и эндокринологии этот метод дает возможность определить причину нарушения фертильности, обнаружить ранние признаки воспаления и дисплазии.
Также биопсия необходима для определения особенностей течения и степени тяжести патологического процесса при болезнях печеночной ткани, почек, головного мозга, мышц и других анатомических структур. Это важно для подбора и изменения схемы медикаментозной терапии. По результатам анализа врач определяет прогностические данные.
Виды и способы проведения биопсии
В современной клинической практике чаще всего используют следующие методики выполнения биопсии:
- Мазки, соскобы и бритвенный метод. Зачастую специалисту требуется небольшое количество материала для постановки диагноза. Можно выполнить мазок и получить все необходимые данные при его последующей микроскопии. Например, такой способ часто применяют в гинекологии. Бритвенная биопсия предполагает иссечение тонкого участка кожного покрова с помощью скальпеля или другого инструмента.
- Тонкоигольная пункция. Такая процедура тоже подходит для случаев, когда достаточно получить немного клеток. В область предполагаемого патологического процесса вводится тонкая игла, захватывающая тканевой образец.
- Толстоигольная пункция. Позволяет произвести забор большого образца тканей без иссечения. Ее назначают при злокачественном новообразовании молочной железы, печеночной ткани, предстательной железы. Трепан-биопсия подходит для исследования кожного покрова, костномозговых структур. Используется специальный инструмент в форме цилиндра.
- Аспирационный метод. Это современная техника забора материала, при котором используется вакуумный прибор в форме цилиндра. В качестве механизма применяется отрицательное давление. Прибор присоединяют к игле. Аспирация дает возможность взять несколько образцов в разных участках анатомической структуры.
- Операционная биопсия. Проводится непосредственно во время операции, когда врач иссекает опухолевую ткань. Это высокоинформативное исследование, позволяющее оценить состояние большого количества тканей. Минус такого вида процедуры — определить тип болезни можно только после операции. Плюсом можно считать совмещение лечебной практики с достоверной диагностикой.
- Эндоскопическая биопсия. Проводится во время диагностики внутренних полостных структур, вроде пищеварительного или респираторного тракта. С помощью эндоскопа врач осматривает подозрительные участки тканей и выбирает место забора материала. Плюсом такой техники можно считать повышенную точность результатов исследования.
Способ проведения диагностики выбирают в зависимости от анамнеза пациента.
Подготовка
В большинстве случаев специально готовиться не следует. Достаточно прийти к врачу в день проведения процедуры и подписать необходимые документы. Специалист объяснит, как будет проходить обследование. Расскажет о рисках и возможных неприятных ощущениях. Определенные виды биопсии выполняют под местным обезболиванием. Реже требуется наркоз. Пациент может сам выбирать комфортный для него способ выполнения диагностики. В случае наркоза нужны специальные подготовительные процедуры.
Для биопсии характерны стандартные осложнения, возникающие при других видах вмешательств. Возможно кровоизлияние, инфицирование тканей. Реже возникает травматизация внутренних органов. Такие негативные последствия редки, но врач обязательно уведомляет пациента о рисках.
Может ли биопсия быть ошибочной?
Достоверность исследования зависит от способа его проведения, анамнеза пациента, опыта врача и других факторов. Например, при пункции специалист может получить образец тканей без злокачественных клеток, если игла попала в соседнюю с опухолью область. В этом случае возможен ложноположительный результат. Онкологи учитывают такую вероятность, и всегда назначают уточняющие исследования. Диагноз не ставится только на основе результатов одной процедуры. Всегда проводится комплексная оценка состояния организма.
Медицинский эксперт статьи
Новые публикации
Биопсия простаты при раке предстательной железы
, медицинский редактор
Последняя редакция: 18.10.2021
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
До возникновения метода определения ПСА биопсию предстательной железы выполняли лишь для уточнения диагноза и назначения гормональной терапии в случае пальпаторного обнаружения изменений железы или при метастазах рака простаты.
В настоящее время ранняя диагностика позволяет обнаружить локализованные формы рака простаты и провести радикальное лечение, поэтому от биопсии ожидают дополнительной информации, влияющей на выбор метода лечения.

Виды биопсии предстательной железы
Основной способ выполнения биопсии — множественная пункционная биопсия предстательной железы под контролем трансректального УЗИ иглой 18 G. При проведении сопутствующей антибактериальной терапии риск осложнений невелик. Выполнение биопсии иглой 14 G чревато высоким риском инфекционных осложнений и кровотечения.
Около 18% рака простаты диагностируют при обнаружении пальпируемого образования простаты. При этом в 13 -30% уровень ПСА составляет от 1 до 4 нг/мл. При пальпации узла в железе рекомендовано проведение прицельной биопсии. Чувствительность биопсии, проведённой под контролем дуплексного УЗИ с контрастированием, не уступает чувствительности множественной биопсии. Тем не менее этот метод исследования пока не получил общего признания.
По данным исследований, при содержании ПСА около 4-10 нг/мл рак подтверждают только в 5,5% случаев. При одновременном проведении первичной биопсии этот показатель увеличивается до 20-30. Относительное показание для проведения биопсии — снижение порогового уровня ПСА до 2,5 нг/мл. Во время проведения секстантной биопсии при уровне ПСА 2,5-4 нг/мл обнаружение рака простаты составляет 2-4%, но при расширенной методике биопсии (12-14 вколов) оно увеличивается до 22-27%. Следует отметить, что в 20% случаев обнаруживают латентный рак (объем опухоли менее 0,2 см3). Таким образом, снижение верхней границы нормы ПСА ведёт к обнаружению клинически незначимых опухолей, которые и без лечения не угрожали бы жизни. Для того чтобы установить верхнюю границу нормы ПСА, позволяющую обнаружить непальпируемые, но клинически значимые опухоли, данных пока недостаточно. При определении относительных показаний необходимо учитывать и другие показатели ПСА (прирост, время удвоения и др.). Повышение верхней границы ПСА, при которой необходима биопсия, нерационально, поскольку сохраняется высокая вероятность обнаружения рака простаты. Лишь в возрасте старше 75 лег возможно повышение верхнего порогового значения до 6,5 нг/мл.
Прицельная биопсия предстательной железы необходима лишь при пальпируемой опухоли и уровне ПСА более 10 нг/мл. В целях уточнения диагноза при метастатическом или местнораспространённом процессе достаточно получения 4-6 биоптатов. В остальных случаях рекомендована множественная биопсия.
В последние 15 лет широкое распространение получила методика биопсии, предложенная К.К. Ходжем и соавт. (1989). Суть ее — во взятии биоптатов па середине расстояния между срединной бороздкой и латеральной границей предстательной железы из основания, средней части и верхушек обеих долей, в связи с чем методика получила название сектантной (6-точечной) биопсии. Метод 6-точечной биопсии в дальнейшем был усовершенствован таким образом, чтобы в биоптаты попадали заднебоковые отделы периферической зоны железы, которые недоступны при стандартной технике. Кроме того, с увеличением объёма предстательной железы частота обнаружения рака при использовании сектантной методики уменьшается. Необходимое число образцов ткани требует уточнения. Почти во всех исследованиях увеличение числа биоптатов повышало чувствительность метода (по сравнению с 6-точечной биопсией). Чувствительность биопсии тем выше, чем большее число биоптатов исследовано. В испытаниях на моделях железы установлено, что если объём опухоли составляет 2,5, 5 или 20% объёма железы, то при сектантной биопсии опухоль диагностируют в 36, 44 и 100% случаев. При выполнении биопсии следует учитывать, что в 80% случаев опухоль возникает в периферической зоне. По данным одного из исследований, взятие 13-18 биоптатов увеличивало чувствительность метода на 35%. В нормограммах Viеnnа (2003) отражена зависимость между количеством вколов, возрастом пациента и объемом простаты. При этом точность прогноза составляет 90%.
Зависимость количества биоптатов от возраста пациента и объёма простаты с точностью положительного предсказывающего прогноза 90%
|
Возраст, годы |
Объём простаты, мл |
|||
|
<50 |
50-60 |
70 |
>70 |
|
|
20-29 |
6 |
8 |
8 |
8 |
|
30-39 |
6 |
8 |
10 |
12 |
|
40-49 |
8 |
10 |
12 |
14 |
|
50-59 |
10 |
12 |
14 |
16 |
|
69 |
12 |
14 |
16 |
— |
|
>70 |
14 |
16 |
18 |
— |
Доказано, что при первичной биопсии захватывать переходную зону железы нецелесообразно, поскольку рак в ней встречают очень редко (менее чем в 2% случаев). В настоящее время наиболее распространена 12-точечная биопсия. Огромное значение придают не только количеству вколов, но и наклону иглы.
Заключение биопсии при раке простаты
В гистологическом заключении обязательно должны быть отражены следующие позиции:
- локализация биоптатов; особенно важна при планировании радикальной простатэктомии; распространенность опухоли на одну или обе доли учитывают при выполнении нервосберегающей операции; при поражении верхушки железы этап её мобилизации более сложен; высока вероятность положительного хирургического края при выделении сфинктера уретры;
- ориентация биоптата по отношению к капсуле железы; для уточнения дистальный (ректальный) отрезок окрашивают специальным раствором;
- наличие ПИН;
- объём поражения биоптата и количество положительных вколов;
- дифференцировка опухолевых клеток по Глисону;
- экстракапсулярная экстензия — обнаружение в биоптатах капсулы предстательной железы, прилежащей жировой клетчатки и прорастающей опухолевой ткани, что важно для выбора метода лечения;
- периневральная инвазия, указывающая на распространение опухоли за пределы предстательной железы с вероятностью 96%;
- сосудистая инвазия;
- другие гистологические изменения (воспаление, гиперплазия предстательной железы).
Если вышеперечисленные показатели не отражены в гистологическом заключении, то в нём обязательно следует указать расположение и количество положительных биоптатов, а также степень дифференцировки опухоли по Глисону.

Интерпретация данных биопсии при раке предстательной железы
Интерпретация данных биопсии требует индивидуального подхода. При отрицательном результате первой биопсии необходима повторная биопсия, вероятность обнаружения рака при этом составляет 10-35%. При тяжелой дисплазии вероятность обнаружения рака достигает 50-100%. В этом случае обязательно проведение повторной биопсии в ближайшие 3-6 мес. Доказано, что две биопсии позволяют обнаружить большинство клинически значимых опухолей. Даже после взятия большого количества биоптатов и отрицательном результате первой биопсии повторная биопсия достаточно часто обнаруживает рак. При подозрении на РПЖ ни один из методов диагностики не обеспечивает достаточной чувствительности, позволяющей отказаться от повторной биопсии. Случаи обнаружения единичного очага требуют особого внимания. Клинически незначимый рак (объём опухоли менее 0,5 см3) после радикальной простатэктомии наблюдают в 6-41% наблюдений. В данной ситуации следует комплексно оценить клиническую ситуацию и определить тактику лечения. Наиболее важную роль играют возраст пациента, уровень ПСА, степень дифференцировки опухоли, объём поражения биоптата, клиническая стадия. Наличие в биоптатах простатической интраэпителиальной неоплазии (ПИН) высокой степени (high grade) может свидетельствовать о злокачественном процессе в предстательной железе. Таким больным показана повторная биопсия через 3-12 мес, особенно если первоначально было получено 6 биоптатов. Показания к повторной биопсии — пальпируемое образование в предстательной железе, повышение уровня ПСА и тяжёлая дисплазия при первой биопсии.
К кому обратиться?
Рак предстательной железы: правда и вымысел
11.03.2018
Стоит ли верить всему, что говорят о раке простаты? Развеиваем мифы об этом заболевании
Доля рака предстательной железы составляет 14,4% от всех онкологических заболеваний мужчин, а смертность от этого вида рака находится на уровне 7,6%. Это в достаточной степени изученное заболевание. Вместе с тем существует ряд мифов, которые с некоторой периодичностью циркулируют в обществе. Мы собрали самые распространенные из них и попросили специалистов их прокомментировать, чтобы раз и навсегда разобраться – что из этого заблуждение, а что правда. В материале мы опирались на мнение нескольких экспертов: Антона Барчука, научного сотрудника НИИ Онкологии им. Н.Н. Петрова и Университета Тампере и Вадима Гущина, главы департамента онкологии клиники Mercy, Балтимор, США.
Рак простаты — это болезнь стариков
Это вряд ли можно назвать мифом, ведь болезнь в 6 из 10 диагностируются после 65. Рак редко, но встречается до 40. Средний возраст диагноза – 66 лет. В России в возрасте от 50 до 59 лет показатель смертности от рака предстательной железы не превышает 10 случаев на 100 000 человек, тогда так в возрасте от 70 до 79 она более чем 15 раз выше – 150 на 100 000 мужчин. С другой стороны, нельзя забывать об агрессивных формах рака предстательной железы, которые могут поражать относительно молодых мужчин, поэтому до сих пор проблема лечения рака простаты не может замыкаться на только пожилых мужчинах.
Тут важно отметить другое: в современном мире эволюционирует наше представление о том, кто такой старик. В современном западном обществе 65 лет – это достаточно активный и зрелый возраст. В Америке 65-летний человек ожидаемо проживёт ещё в среднем 18 лет.
Есть характерные симптомы, которые позволяют диагностировать рак простаты
Это миф – характерных симптомов не бывает. Заболевание не всегда вызывает увеличение железы, но когда вызывает – приносит симптомы затруднения мочеиспускания, наличие крови в моче и семени, частое и болезненное мочеиспускание. Симптомы метастатического роста включают боли в костях, отёки ног, потеря веса, плохое самочувствие. Как видно, они не уникальны для болезни. Поэтому, роль врача – оценить каждый из симптомов. Ещё важно знать, что большинство пациентов, столкнувшихся с этими симптомами, не будет страдать раком простаты.
Болезнь развивается медленно и лечить ее не стоит
В первую очередь речь в этом случае идет о наблюдении, анализах, биопсии. Цель этого активного наблюдения – по возможности вовремя диагностировать тот рубеж, за которым лечение рака будет полезнее его отсутствия. Кроме того, в некоторых случаях сложно предсказать, как быстро будет расти опухоль.
Одна из проблем в современной парадигме лечения рака предстательной железы – это гетерогенность (разнородность) самого заболевания. Если мы говорим о раке, который уже диагностирован и подтвержден, то без сомнения отказывать пациенту в лечении просто неэтично, но возникает вопрос о форме этого лечения.
С другой стороны, все чаще врачи встречают небольшие бессимптомные опухоли выявленные только с помощью анализа крови на PSA (простатический специфический антиген). Ответ на вопрос, как поступать в этом случае, в некоторой степени помогло дать недавно опубликованное исследование, в котором больных либо активно лечили, либо активно наблюдали и лечили только при признаках прогрессирования заболевания. Главный вывод был в том, что риск умереть от рака предстательной железы крайне низок в обеих группах.
Активное лечение имеет относительное преимущество над активным наблюдением, но абсолютная выгода крайне и крайне незначительна. Если мы положим на другую сторону весов все нежелательные эффекты лечения – перед нами получается довольно сложное решение, которое, по всей видимости, надо принимать индивидуально с каждым пациентом.
Анализ крови на PSA – это принятый во всем мире метод скрининга рака предстательной железы и помогает диагностировать рак
Скорее миф, но миф, имеющий много сторонников и в научной среде. На данный момент скрининг с помощью PSA не рекомендован ни одной ассоциацией и не проводится организованно ни в одной стране мира. При этом доля урологов и врачей общей практики, которые назначают это обследование без рекомендаций, крайне высока. Нельзя не отметить, что скрининг с помощью PSA снижает смертность от рака, но цена этого снижения – крайне высокая степень гипердиагностики, то есть выявления неагрессивных форм заболевания.
Часто выявляются менее агрессивные формы рака, которые не приводят к проблемам со здоровьем. Однако, сложно сказать пациенту, что у него есть рак простаты, но делать ничего не надо.
Здесь же возникает проблема степени агрессивности методов дальнейшей диагностики и лечения. Ведь речь идет о тяжелой операции, которая имеет, пусть даже низкую, но известную смертность. А сама операция может привести к серьезным для мужчины последствиям: недержанию мочи, нарушению эрекции и тд.
Хирургическое лечение людей, жизни которых заболевание угрожать не сможет – довольно сомнительное решение.
Все эти соображение заставили ведущие онкологические сообщества отказаться на сегодняшний день от теста PSA для массового применения для скрининга рака предстательной железы.
Кроме этого, анализ на PSA может «пропустить» рак. Так в одном крупном исследовании у 15% мужчин с нормальным уровнем PSA при биопсии обнаружили рак предстательной железы. Показатели специфичности и чувствительности для этого теста разняться от исследования к исследованию, но также зависят от концентрации этого биомаркера, которую принимают за пограничную. Еще больше проблем связано с диагностикой рака предстательной железы у мужчин с имеющимися другими заболеваниями простаты, тогда доля ложноположительных тестов может быть еще выше.
PSA не рекомендуется как скрининговый метод для здоровых мужчин. Если он назначается, то врач должен владеть вышеприведенной информацией и уметь рассказать пациенту риски данного невинного теста крови.
Лечение всегда приводит к нежелательным и неприятным последствиям
Лечение рака предстательной железы действительно может привести к потере эрекции, недержанию мочи и проблемам с желудком и кишечником. Частота возникновения и длительность этих расстройств зависит от вида лечения (разные виды операции, облучения, добавочное лечение противогормональных препаратов), от опыта врача, выполняющего лечение, и учреждения, где лечение проводится. Поэтому для пациентов важно напрямую спросить такую статистику, когда речь идёт о выборе типа и места лечения.
Рак простаты передается по наследству
Примерно 5-10% случаев возникновения рака простаты имеют значительную наследственную составляющую. У мужчин, отцу которых был поставлен такой диагноз, вероятность развития болезни повышается в 2 раза. Если рак был у отца и брата риск повышается в 5 раз. Существуют наследственные синдромы, такие как BRCA2 мутации (больше известные у женщин – приводят к раку груди и яичников), которые ассоциированы с повышенной встречаемостью рака простаты. Такие мутации можно выявить (при подозрении) специальным генетическим тестированием.
Вазэктомия может вызвать рак предстательной железы
Пока все же это миф. Результаты исследования, опубликованного в 1993 году исследователями из Гарвардского Университета, предположило такую связь. Однако, более поздняя работа, результаты которой были опубликованы в 2016 году, не нашла связи между вазэктомией и раком предстательной железы. В крупнейшем исследовании, изучавшем влияние вазэктомии на развитие и смерть от рака предстательной железы, принимало участие 363,726 мужчин. В течение 30 лет было зарегистрировано более 66 000 случаев рака предстательной железы и более 7 400 смертей от этого заболевания. Риски как заболеть, так и умереть от рака предстательной железы были одинаковы для мужчин, которым провели вазэктомию и мужчин, которым операция не проводилась.
На риск развития рака простаты влияет половая активность
Несколько исследований в 2000-х годах действительно показали, что частота эякуляции ассоциирована со снижением риска развития рака простаты. Обычно, урологи советуют заниматься сексом 2-3 раза в неделю, в том числе и для возможного снижения риска развития агрессивной формы рака простаты.
Бывает так, что домыслы и мифы настолько плотно входят в нашу жизнь, что порой даже врачи руководствуются этим опытом, проводя анализы и назначая лечение
Здесь важно помнить, что рак – это системное заболевание. Это значит, что одним симптомом или методом лечения тут не обойтись. Кроме этого, не обойтись тут и без регулярного чтения научных исследований о развитии и лечении онкологических заболеваний, ведь именно они позволяют нам бороться с домыслами и принимать верные решения.
Оригинал статьи опубликован на сайте Вести.Медицина.
Биопсия предстательной железы
- Врачи
- Статья обновлена: 18 июня 2020
При подозрении на рак простаты биопсию предстательной железы проводят обязательно всем пациентам. Её результат определяет тактику лечения, а порой и прогноз.
Биопсия предстательной железы — одно из обязательных исследований для окончательной диагностики рака простаты. Проводиться всем больным с подозрением на это заболевание после полного комплекса обследования:
- пальцевое ректальное исследование;
- трансректальное ультразвуковое исследование;
- определение уровня простат-специфического антигена (ПСА).
На основании результатов биопсии предстательной железы решается вопрос о выборе метода лечения каждого конкретного пациента.
Существует несколько методик взятия биопсии предстательной железы. Наиболее распространенной и наименее болезненной является трансректальная биопсия простаты, выполняемая с помощью устройства для биопсии, состоящего из биопсийного пистолета и специальных одноразовых игл.
Перед началом биопсии предстательной железы в прямую кишку через анальное отверстие вводится обезболивающее средство, чаще всего используется гель с лидокаином. Через 5-10 минут после обезболивания в прямую кишку вводится специальный ультразвуковой датчик с насадкой для проведения иглы, с помощью которой будут взяты нитевидные кусочки ткани предстательной железы для её дальнейшего изучения. После введения ректального датчика проводится ультразвуковое исследование простаты для определения точек, из которых будет взята ткань железы. Далее под контролем УЗИ проводится собственно биопсия. Обычно материал для исследования берут из 6-18 точек. Процедура переносится пациентами хорошо, лишь некоторые из них отмечают чувство легкого дискомфорта. После процедуры полученный материал передают в лабораторию для постановки диагноза и определения стадии заболевания.
При биопсии предстательной железы всем пациентам необходимо соблюдать следующие рекомендации:
- на протяжении 7 дней до биопсии нельзя принимать препараты, влияющие на свертываемость крови (аспирин, гепарин, синкумар, фенилин и пр.);
- за 3 дня до биопсии необходимо прекратить прием противовоспалительных препаратов;
- вечером и утром накануне исследования ставится очистительная клизма;
- исследование проводиться натощак;
- в течение суток после биопсии следует ограничить физическую активность;
- на 3-5 дней после биопсии назначается антибактериальная терапия для предотвращения воспаления предстательной железы;
- на следующий день после биопсии необходимо удалить тампон, введенный в прямую кишку врачом для профилактики возможного кровотечения.
Осложнения биопсии предстательной железы:
- гематурия (появление крови в моче);
- гемоспермия (появление крови в эякуляте);
- боли в области промежности и прямой кишки;
- воспаление предстательной железы или обострение хронического простатита;
- воспаление яичка и его придатка (орхоэпидидимит);
- острая задержка мочи;
- кровотечение из прямой кишки.
Источники
- Greenberg SA., Washington SL., Lonergan PE., Cowan JE., Baskin AS., Nguyen HG., Odisho AY., Simko JP., Carroll PR. Residual Benign Prostate Glandular Tissue after Radical Prostatectomy is Not Associated with the Development of Detectable Postoperative Serum PSA. // J Urol — 2021 — Vol — NNULL — p.101097JU0000000000001793; PMID:33905262
- Bosland MC., Nettey OS., Phillips AA., Anunobi CC., Akinloye O., Ekanem IA., Bassey IE., Mehta V., Macias V., van der Kwast TH., Murphy AB. Prevalence of prostate cancer at autopsy in Nigeria-A preliminary report. // Prostate — 2021 — Vol — NNULL — p.; PMID:33905137
- Surasi DSS., Wang X., Bathala TK., Hwang H., Arora S., Westphalen AC., Chang SD., Turkbey B. The impact and collateral damage of COVID-19 on prostate MRI and guided biopsy operations: Society of Abdominal Radiology Prostate Cancer Disease-Focused Panel survey analysis. // Abdom Radiol (NY) — 2021 — Vol — NNULL — p.; PMID:33904992
- da Silva LM., Pereira EM., Salles PG., Godrich R., Ceballos R., Kunz JD., Casson A., Viret J., Chandarlapaty S., Ferreira CG., Ferrari B., Rothrock B., Raciti P., Reuter V., Dogdas B., DeMuth G., Sue J., Kanan C., Grady L., Fuchs TJ., Reis-Filho JS. Independent real-world application of a clinical-grade automated prostate cancer detection system. // J Pathol — 2021 — Vol — NNULL — p.; PMID:33904171
- Han H., Lee HH., Choi K., Moon YJ., Heo JE., Ham WS., Jang WS., Rha KH., Cho NH., Giancotti FG., Choi YD. Prostate epithelial genes define therapy-relevant prostate cancer molecular subtype. // Prostate Cancer Prostatic Dis — 2021 — Vol — NNULL — p.; PMID:33903734
- Mohd Ariffin K., Abd Ghani F., Hussin H., Md Said S., Yunus R., Veerakumarasivam A., Abdullah MA. Hedgehog signalling molecule, SMO is a poor prognostic marker in bladder cancer. // Malays J Pathol — 2021 — Vol43 — N1 — p.49-54; PMID:33903305
- Nabid A., Carrier N., Vigneault E., Van Nguyen T., Vavassis P., Brassard MA., Bahoric B., Archambault R., Vincent F., Bettahar R., Wilke D., Souhami L. OPTIMIZING TREATMENT IN INTERMEDIATE RISK PROSTATE CANCER: SECONDARY ANALYSIS OF A RANDOMIZED PHASE III TRIAL. // Int J Radiat Oncol Biol Phys — 2021 — Vol — NNULL — p.; PMID:33901566
- Chung JW., Kim HT., Ha YS., Lee EH., Chun SY., Lee CH., Byeon KH., Choi SH., Lee JN., Kim BS., Kim TH., Yoo ES., Yoon GS., Baek MC., Kwon TG. Identification of a novel non-invasive biological marker to overcome the shortcomings of PSA in diagnosis and risk stratification for prostate cancer: Initial prospective study of developmental endothelial locus-1 protein. // PLoS One — 2021 — Vol16 — N4 — p.e0250254; PMID:33901217
- Kang HC., Jo N., Bamashmos AS., Ahmed M., Sun J., Ward JF., Choi H. Accuracy of Prostate Magnetic Resonance Imaging: Reader Experience Matters. // Eur Urol Open Sci — 2021 — Vol27 — NNULL — p.53-60; PMID:33899028
- Morel KL., Sheahan AV., Burkhart DL., Baca SC., Boufaied N., Liu Y., Qiu X., Cañadas I., Roehle K., Heckler M., Calagua C., Ye H., Pantelidou C., Galbo P., Panja S., Mitrofanova A., Wilkinson S., Whitlock NC., Trostel SY., Hamid AA., Kibel AS., Barbie DA., Choudhury AD., Pomerantz MM., Sweeney CJ., Long HW., Einstein DJ., Shapiro GI., Dougan SK., Sowalsky AG., He HH., Freedman ML., Balk SP., Loda M., Labbé DP., Olson BM., Ellis L. EZH2 inhibition activates a dsRNA-STING-interferon stress axis that potentiates response to PD-1 checkpoint blockade in prostate cancer. // Nat Cancer — 2021 — Vol2 — N4 — p.444-456; PMID:33899001
Рак предстательной железы (РПЖ) — одно из наиболее распространенных онкологических заболеваний среди мужского населения России и зарубежных стран. По данным Всемирной Организации Здравоохранения РПЖ составляет 14,5% всех злокачественных новообразований [1]. Только в США в 2016 году по прогнозам будет диагностировано 180 890 случаев заболевания РПЖ и 26 120 пациентов умрут от этого заболевания. [2]
В России РПЖ занимает второе место по частоте встречаемости после меланомы кожи и значительно превосходит по распространенности злокачественные новообразования легких и желудка. В структуре онкологической смертности среди мужчин РПЖ стоит на 4 месте и составляет 7,2% всех случаев смерти мужчин от злокачественных новообразований [3].
Важно отметить тот факт, что внедрение скрининговых программ обследования населения и, в частности, популяризация ежегодного контроля уровня сывороточного простатспецифического антигена (ПСА) у мужчин старше 45-50 лет, привело к увеличению выявляемости РПЖ на более ранних стадиях. Сравнение статистических данных по структуре заболеваемости РПЖ в Российской Федерации за 1993 и 2013 гг. демон-
стрирует значительное увеличение доли активно выявленных РПЖ с 2,7% до 25,0%. В 2013 году в среднем в Российской Федерации 49,5% больных имели I-II стадию заболевания (9,3% — I стадию, 40,3 % — II стадию), что на 15,5 % выше, чем в 1993 г.; 31,0% имели III стадию, что на 6 % меньше, чем в 1993 г.; 17,2% — IV стадию против 19,3% в 1993 г. Показатель раково-специфической летальности в течение одного года после установки диагноза снизился с 31,5% до 10,3% [3]. Тем ни менее, количество пациентов с установленным диагнозом РПЖ в России процентном отношении к населению существенно уступает Европейским и Американским показателям, а доля распространенного РПЖ по-прежнему достаточно велика.
Наряду с тем, что радикальная простатэктомия (РПЭ) по-прежнему остается «золотым стандартом» лечения локализованного РПЖ, все большую популярность в последнее десятилетие набирает идея “активного наблюдения” за такими больными. Синонимами «активного наблюдения» являются «отсроченное лечение» и «выжидательная тактика». Следует различать этот вариант лечения и понятие «динамического наблюдения», в рамках которого пациенты преклонного возраста, имеющие тяжелые сопутствующие заболевания или небольшую ожидаемую продолжительность жизни, исходно не являются кандидатами на оперативное вмешательство. Тактика «активного наблюдения» у больных локализованным РПЖ предполагает отказ от проведения радикального лечения (РПЭ и лучевая терапия) и гормональной терапии и наблюдение за пациентами (контроль уровня ПСА, проведение динамической магнитно-резонансной томографии (МРТ), повторных биопсий ПЖ и т.д.) до развития признаков прогрессирования заболевания, при котором начинают активное лечение.
Первой и самой известной публикацией, начавшей дискуссию о возможности «наблюдения» больных РПЖ, стала статья J.I. Epstein и P.C. Walsh, опубликованная в 1993 году, в которой они впервые попытались сформулировать критерии «клинически незначимого рака» [4].
В последующем эта идея была популяризирована в многочисленных публикациях о безопасности и эффективности «активного наблюдения», появившихся в последние годы. К таким работам можно отнести исследование P.C. Albertsen и соавт., которые в 1998 году опубликовали результаты наблюдения за 767 больными в возрасте 55-74 лет, у которых РПЖ диагностировали в 1971-1984 гг. Средний период наблюдения составил 8,6 лет. В подгруппе больных с высоко и умеренно дифференцированными опухолями (2-4 балла и 5 баллов по шкале Глисона) только 4-7% и 6-11% пациентов умерли от прогрессирования РПЖ в течение 15 лет после постановки диагноза. Для пациентов с исходным уровнем злокачественности 3+3=6 этот показатель составил 18-30% в различных возрастных группах [5].
Оправданность тактики активного наблюдения была подтверждена в дальнейшем двумя масштабными исследованиями — PIVOT Trial и SPCG-4 [6,7]. Основываясь на этих публикациях современные рекомендации Европейской Урологической Ассоциации подразумевают возможность проведения «активного наблюдения» у пациентов с локализованным РПЖ при низком риске прогрессии заболевания. В эту группу попадают больные с ожидаемой продолжительностью жизни больше 10 лет, стадией заболевания cT1/2, уровнем общего ПСА менее 10 нг/мл, суммарным баллом по шкале Глисона при биопсии менее 7 и наличие злокачественных изменений не более, чем в двух биопсионных образцах ткани. При этом протяжённость опухолевой ткани в биоптатах не должна превышать 50% [8].
Самой большой сложностью в этой ситуации является то, что основной вес в принятии решения о возможности «активного наблюдения» имеет патоморфологическое заключение, сделанное по результатам мультифокальной тонкоигольной биопсии ПЖ. Именно от его точности, от компетентности патоморфолога и качества выполнения биопсии зависит дальнейшая тактика лечения конкретного пациента. Обнаружены злокачественные изменения в двух, или в трех биоптатах, протяженность опухоли в биоптате 45% или 55% -такие казалось бы незначительные колебания — перемещают пациента из группы с низким риском прогрессии в группу среднего риска. Вопрос о достоверности информации, которую мы получаем в результате обработки данных биопсии ПЖ, неоднократно освещался в литературе. Известно, что точность этих данных далека от абсолютной. Суммарный балл по шкале Глисона может помочь правильно определить стадию заболевания лишь у 31-45% больных [9-11]. Очень часто балл по шкале Глисона подвергается коррекции после выполнения пациентам радикальной простатэктомии. В одной из наших публикаций мы указывали, что такая коррекция была необходима в 54% случаев, причем 2/3 из них в сторону увеличения значения суммарного балла по шкале Глисона [12].
МАТЕРИАЛЫ И МЕТОДЫ
В основу данного исследования положены результаты обследования и лечения 348 пациентов с раком предстательной железы, которым в период с декабря 2014 по декабрь 2015 была выполнена радикальная простатэктомия в клинике урологии МГМСУ им А.И. Евдокимова. Из этой когорты больных была отобрана группа из 25 пациентов, у которых предоперационная диагностика указывала на унилатеральный/унифокальный характер поражения. Всем этим пациентам было предложено проведение «активного наблюдения», но они предпочли оперативное вмешательство. РПЭ с роботической ассистенцией была выполнена 14 пациентам, позадилонным доступом -11. Демографические данные и результаты дооперационного обследования приведены в таблице 1.
Таблица 1. Демографические данные и результаты предоперационных обследований
| Показатель | Среднее значение | Диапазон |
|---|---|---|
| Возраст больных (лет) | 61,72 | СО со h- тг |
| Объем предстательной железы (см3) | 67,3 | 18 — 105 |
| Общий ПСА (нг/мл) | 17 | 2,1 — 29 |
| Протяженность опухолевой ткани в биоптате (%) | 31,43 | 5-100 |
| Показатель | Значение | Количество пациентов (%) |
| Количество позитивных биоптатов из 12 | 1 | 21 (84) |
| 2 | 3 (12) | |
| 5 | 1 (4) | |
| Общий ПСА (нг/мл) | < 10 | 17 (68) |
| окт.20 | 7 (28) | |
| > 20 | 1 (4) | |
| Балл по шкале Глисона | 3+3=6 | 19 (76) |
| 3+4=7 | 3 (12) | |
| 4+3=7 | 2 (8) | |
| 4+4=8 | 1 (4) |
Всем пациентам до операции был определен уровень ПСА в крови, выполнено трансректальное ультразвуковое исследование (ТРУЗИ) ПЖ, пальцевое ректальное исследование (ПРИ) ПЖ и стандартная трансректальная мультифокальная биопсия ПЖ из 12 точек под контролем ТРУЗИ. 18 биопсий были выполнены в ГКБ им. И.С. Спасокукоцкого, остальные 7 — в других лечебных учреждениях. Все гистоморологические исследования и пересмотры препаратов, подготовленные в других медицинских учреждениях, а также послеоперационное гистологическое исследование препаратов удаленных ПЖ проводилось в патоморфологической лаборатории кафедры урологии МГМСУ на базе ГКБ им. И.С. Спасокукоцкого двумя гистоморфологами, сотрудниками кафедры урологии МГМСУ им. А.И. Евдокимова, имеющими одинаковый уровень подготовки и опыт работы, прошедших стажировки в различных центрах США и Израиля.
Стандарты написания гистоморфологических заключений ткани, полученной в ходе тонкоигольной биопсии и после РПЭ, соответствовали рекомендациям обновленного протокола, принятого международным консенсусом уропатологов (ISUP) в 2011 году [14]. Для послеоперационного стадирования заболевания каждый случай РПЖ был оценен и отнесен к определенной стадии в соответствии с классификацией TNM 2010 года.
РЕЗУЛЬТАТЫ
Несмотря на то, что у всех 25 пациентов по данным биопсии имело место унилатеральное, а у 21 (84%) -даже унифокальное поражение, в 23 случаях (92%) после получения результатов патоморфологического исследования препарата удаленной ПЖ было диагностировано наличие патологического процесса в обеих долях ПЖ. У 19 пациентов (76%) клиническая стадия соответствовала T2c, у одного обнаружена экстрапростати-ческая инвазия (стадия T3a), а у трех больных имелась инвазия в семенные пузырьки (стадия T3b). Напрашивается вывод, что унифокальное/уни-латеральное поражение ПЖ в действительности имело место лишь у 8% пациентов. У остальных 23 (92%) пациентов тактика «активного наблюдения» на основании данных биопсии была бы выбрана ошибочно.
Также подверглось корректировке и значение суммы баллов по шкале Глисона: 3+3=6 было определено в 14 случаях (по данным биопсии -19), 3+4=7 — в трех случаях, 4+3=7 — в 6 случаях (по данным биопсии — 2) и 4+5=9 — в двух случаях (по данным биопсии -0). Иными словами, в 32% случаев (у 8 пациентов из 25), произошло изменение показателя суммы баллов по Глисону в сторону её увеличения (табл. 2)
Таблица 2. Распределение пациентов в зависимости от степени злокачественности опухоли по шкале Глисона до и после радикальной простатэктомии
| Суммарный балл по шкале Глисона | По данным биопсии, чел. (%) | По результатам операции, чел. (%) |
|---|---|---|
| 3+3=6 | 19 (76) | 14 (56) |
| 3+4=7 | 3 (12) | 3 (12) |
| 4+3=7 | 2 (8) | 6 (24) |
| 4+4=8 | 1 (4) | — |
| 4+5=9 | — | 2 (8) |
Для иллюстрации рассмотрим более подробно два клинических случая:
Пациент Р., 68 лет, обратился с жалобами на прогрессивное повышение уровня общего ПСА в течение 5 лет (на момент обращения ПСА 10 нг/мл). В анамнезе 4 биопсии больному выполненно в сторонних учреждениях. В первых трех гистологическое заключение -ДГПЖ, в четвертой — аденокарцинома ПЖ. Препараты пересмотрены в нашей патоморфологической лаборатории, подтверждено наличие РПЖ в двух образцах из правой доли, 70 и 90% пораженной ткани в столбиках, 3+4=7 баллов по шкале Глисона. При пальцевом ректальном исследовании выявлено что ПЖ несколько увеличена в размерах, гомогенна, уплотнения не определяются. Пациенту выполнено МРТ органов малого таза с контрастом, в ходе которого очагов подозрительных на РПЖ, признаков распространения злокачественного новообразования (ЗНО) за пределы органа обнаружено не было, семенные пузырьки, регионарные лимфоузлы без особенностей. PiRADS 3. Предполагаемая стадия T2a-bN0M0. Так как ожидаемая продолжительность жизни пациента превышала 10 лет, а так же учитывая хорошее соматическое состояние пациента, были обсуждены различные методы лечения основного заболевания. Пациент настаивал на операции. Была выполнена радикальная робот-ассистированная простатэктомия. При послеоперационном гистологическом исследовании ПЖ с семенными пузырьками: ацинарная аденокарцинома 4+3=7 баллов по шкале Глисона. Поражены обе доли ПЖ. Определяется экстрапро-статическая инвазия (ЭПИ) в области верхушки и нижней части справа, позитивный хирургический край в области верхушки справа. Инвазия РПЖ в правый семенной пузырек. Послеоперационная стадия pT3bN0M0 R+.
Пациент Л., 62 лет, впервые сдал анализ крови на ПСА, отмечено повышение показателя до 7 нг/мл. При ПРИ: предстательная железа несколько увеличена, гомогенна, патологических очагов не определяется. В нашей клинике выполнена стандартная 12-точечная трансректальная биопсия ПЖ под УЗ-на-ведением. В гистологическом материале в одном образце 10% ткани занимает ацинарная аденокарцинома 3+3=6 баллов по шкале Глисона. Пациенту выполнена МРТ органов малого таза с контрастом, в ходе которого очагов подозрительных на РПЖ, признаков распространения ЗНО за пределы органа обнаружено не было, семенные пузырьки, регионарные лимфоузлы без особенностей. PiRADS 2. Предполагаемая стадия T2aN0M0. Так как ожидаемая продолжительность жизни пациента превышала 10 лет, а также учитывая хорошее соматическое состояние пациента, были обсуждены различные методы лечения основного заболевания пациента. Пациент настаивал на операции. Выполнена радикальная робот-ассистированная про-статэктомия. При послеоперационном гистологическом исследовании ПЖ с семенными пузырьками: рост ацинарной аденокарциномы 3+3=6 баллов по Глисону определяется в области верхушки, средней и нижней части с обеих сторон. Признаков ЭПИ не определяется. Семенные пузырьки интактны. Послеоперационная стадия pT2cN0M0.
ОБСУЖДЕНИЕ
Проблемы правильного дооперационного стадирования РПЖ неоднократно поднимались в литературе. Это не всегда было связано с решением вопроса о приемлемости тактики “активного наблюдения”, а скорее приводилось как доказательство несовершенства существующих методов диагностики. РПЖ, очевидно, крайне редко является унифокальным или унилатеральным заболеваниям. К такому выводу пришел J.I. Epstein в обзорной статье, содержащий Medline метаанализ распространенности опухоли внутри ПЖ по данным предоперационной биопсии и послеоперационного исследования. Было доказано, что рТ2а встречается очень не часто, а рТ2Ь — это вообще большая редкость. Абсолютное большинство пациентов имеют стадию рТ2с [15].
В таблице 3 приведены данные о распределении пациентов в зависимости от стадии заболевания в нескольких масштабных исследованиях, в которых пациенты подверглись РПЭ в связи с наличием локализованного РПЖ. Полученные нами данные полностью коррелируют с положением, высказанным J.I. Epstein и соответствуют результатам авторов, приведенных в таблице 3. В среднем, вероятность pT2c у пациентов с локализованным раком предстательной железы, составляет 72,3%.
Таблица 3. Процентное распределение пациентов с локализованным РПЖ в зависимости от стадии заболевания по результатам радикальной простатэктомии
| % pT2a | % pT2b | % pT2c | |
|---|---|---|---|
| J.R. Caso и соавт. [16] | 18 | 6 | 76 |
| G.J. DeCastro и соавт. [17] | 10,8 | 8,4 | 80,8 |
| L.E. Eichelberger, L. Cheng и соавт. [18] | 19,6 | 0 | 80,4 |
| S.K. Hong и соавт. [19] | 23,4 | 0,3 | 76,3 |
| Y. Kordan и соавт. [20] | 24,8 | 2,6 | 72,6 |
Одной из первых работ, в которой авторы выражали сомнение в высокой прогностической значимости биопсии ПЖ для определения клинически незначимых опухолей, была публикация группы бельгийских урологов под руководством Hendrik P. Van Poppel в 1997 г. На примере ретроспективного анализа он доказал, что большинство Т1с опухолей были клинически значимыми, причем 34% из них имели признаки местного распространения за пределы ПЖ (pT3). Протяженность опухоли менее 3 мм в биоптате, по мнению этих авторов, позволяет выявить 18 из 19 клинически незначимых раков и, с другой стороны, “пропускает” 33% рака в переходной и 17% — в периферической зонах [22].
В исследовании M. Noguchi проведен анализ соответствия данных предоперационной мультифокальной биопсии ПЖ результатам послеоперационного гистологического исследования. Интересен тот факт, что до и послеоперационную оценку у всех 450 пациентов проводил один патоморфолог. Результатом этой работы был вывод о крайне часто наблюдающемся несоответствии результатов тонкоигольной биопсии и данных послеоперационного гистологического исследования. Балл по шкале Глисона, установленный на основании предоперационной биопсии, оказался достоверным лишь у 81 из 222 пациентов (36%). Переоценка балла Глисона в сторону увеличения произошла у 102 из 222 больных (46%), а в сторону уменьшения — лишь у 39 (18%). Особенно очевидны различия были при попытке выявлении комбинаторных критериев клинически незначимого РПЖ. Так, корреляция данных биопсии и послеоперационных результатов у пациентов с исходно одним позитивным биоптатом, баллом Глисона не более 6 и объемом опухолевой ткани не более 0,5 см3 составляет около 10% (23 из 222 пациентов). Следует отметить, что выводы нашего исследования во многом совпадают с результатами M. Noguchi. По его данным у 81% (63 из 78) пациентов с одним позитивным биопсийным столбиком имел место клинически значимый РПЖ (после простатэктомии объем опухоли был более 0,5 см3) [23].
К аналогичным выводам пришли и M.K. Terris и соавт. В серии наблюдений у 27 из 124 больных, подвергшихся биопсии, РПЖ был выявлен только в одном биоптате на протяжении не более 3 мм. Лишь у 30% из них после операции было подтверждено наличие клинически незначимого РПЖ. Следует отметить, что по стандартам 1992 года, автор выполнял секстантную биопсию [24].
В 2007 группой авторов во главе с W.J. Catalona были опубликованы результаты исследования, дизайн которого во многом совпадал с нашим. Были проанализированы результаты оперативного лечения 455 пациентов, подходивших под критерии “активного наблюдения”, но выбравших радикальную простатэктомию. У 292 из них злокачественное поражение по результатам биопсии присутствовало не более, чем в двух биопсийных столбиках. У 245 из 292 балл по шкале Глисона был 3+3=6. После операции балл по шкале Глисона, равный 7, был зафиксирован у 78 пациентов (27%), а 25 больных (8%) имели признаки экстрапростатического распространения опухоли. Очевидно, что у этих пациентов тактика «активного наблюдения» была бы “ошибочным выбором”. Авторы пришли к заключению, что примерно у трети пациентов, которым по данным предварительного исследования может быть предложено “активное наблюдение”, такое решение рискует оказаться неправильным [25].
C точки зрения «активного наблюдения», пациент с единичным фокусом РПЖ при биопсии представляется наиболее перспективным, но полученные нами данные, коррелирующие со многими международными исследованиями, приведенными выше, свидетельствуют о высоком риске недооценки распространенности опухолевого поражения в таких случаях. В статье корейских урологов обосновывается утверждение, что чем меньше биопсийных столбиков содержат злокачественные клетки, тем более вероятно расхождение до- и послеоперационного гистологического заключения. Они пришли к выводу, что существенные различия присутствуют в 25% биопсий, причем самым «проблемным» участком, на котором расхождения достигают 38%, является верхушка предстательной железы. При этом обнаружение низкодифференцированного поражения чаще находит подтверждение при выполнении в последующем РПЭ, чем высокодифференцированного [26].
Косвенно об этом свидетельствуют и результаты отсроченного лечения пациентов, которым на основании первичного обследования была выбрана тактика «активного наблюдения». C. Warlick и соавт. в своей статье осветили результаты оперативного лечения 38 пациентов, некоторое время находившихся на “активном наблюдении” в клинике Johns Hopkins. У 23% отсроченная операция выявила так называемый «инкурабельный рак ПЖ» (опухоль невозможно было радикально удалить хирургически), в то время как сразу выполненная операция у других 150 больных обеспечивала снижение этого риска до 16%. Более того, использование прогностических номограмм, разработанных в этом учреждении, показало, что более чем 75% вероятность 10-летней выживаемость без риска прогрессии заболевания имеют все пациенты, оперированные без задержки против 77% больных, которые находились на программе «активного наблюдения» [27].
Следует отметить, что отдаленных результатов “активного наблюдения” пока не так много. Это объясняется двумя причинами -относительной «молодостью» идеи “активного наблюдения” и тем обстоятельством, что около 30% пациентов отказываются от такого лечения в первые 3 года наблюдения, предпочитая его оперативному вмешательству [28]. В таблице 4 мы приводим данные трех масштабных исследований результатов отсроченного оперативного вмешательства на разных сроках наблюдения.
Таблица 4. Результаты «отсроченной» радикальной простатэктомии после различного по продолжительности «активного наблюдения»
| Автор исследования, кол-во пациентов, средняя продолжительность наблюдения | Выживаемость | Наличие метастазов | Процент рТ3 после радикальной простатэктомии, если таковая выполнялась |
|---|---|---|---|
| L. Klotz [29]; N=299, 8 лет | Раково-специфическая — 99,3% | 2/299 | 58% (14/24) |
| C. Parker [30]; N=80, 3,5 года | Раково-специфическая — 100% Общая — 94% | — | 50% (1/2) |
| H.B. Carter [31]; N=405, 2,8 года (от 0,4 до 12,5 лет) | Общая — 98% | 0,50% | 20% (10/49) |
ВЫВОДЫ
В соответствие с полученными нами данными, в 92% случаев локализованного унилатерального/унифокального РПЖ, диагностированного на основании мультифокальной трансректальной биопсии предстательной железы, предоперационная и послеоперационная стадии заболевания различались в сторону увеличения последней, а в 32% случаев отмечалось повышение значения суммы баллов по шкале Глисона. Это доказывает мультифокальную природу развития заболевания при РПЖ и создает определённые трудности при попытке достоверно оценить показания к назначению тактики «активного наблюдения» у этих пациентов. С другой стороны напрашивается вывод, что 12-точечная биопсия ПЖ, являющаяся на сегодняшний день стандартом диагностики РПЖ, скорее всего, не является достаточным инструментом для диагностики унифокального и унилатерального поражения.
Полученные результаты в определенной степени поддерживают сложившуюся в настоящее время практику, когда клиницисты больше склонны к радикальной тактике лечения локализованного РПЖ ввиду высокой вероятности недооценки реальной стадии заболевания на основании всех доступных сегодня методов предварительного обследования. Отсроченное лечение, к которому приходится прибегать при появлении признаков прогрессии заболевания у больных, находящихся на «активном наблюдении», обеспечивает худший результат по сравнению ранним выполнением операции. Такая активная тактика в отношении пациентов с локализованным РПЖ в большинстве случаев согласуется и с желанием пациента «избавиться от РПЖ раз и навсегда». В нашей практике большинство мужчин в возрасте до 65-70 лет настаивают на радикальной операции. Это тем более оправданно, что совершенствование техники выполнения РПЭ, популяризация нервосберегающего варианта операции и, в особенности, применение роботической ассистенции с использованием комплекса daVinci, обеспечивают очень хорошие функциональные и онкологические результаты. Данные мировой статистики свидетельствуют, что около 90% мужчин подвергаются агрессивному лечению, несмотря на тот факт, что только от 15% до 30% случаев РПЖ будут ассоциированы с риском онкологической прогрессии [32].
Необходимы дальнейшие исследования по совершенствованию оптимального алгоритма диагностики РПЖ для более точного стадирования заболевания, в особенности у тех пациентов, которым предполагается проведение «активного наблюдения», «фокальной терапии» и любых видов «отсроченного лечения».
ЛИТЕРАТУРА
1. World Health Organization. GLOBOCAN 2012: estimated cancer incidence, mortality, and prevalence worldwide in 2012 [Internet]. Lyon: International Agency for Research on Cancer; c2015 [2015 Jun 13]. Available from: http://globocan.iarc.fr/ Pages/fact_sheets_population.aspx.
2. Siegel RL, Miller KD, Jemal A. Cancer statistics, 2016. CA Cancer J Clin 2016; 66(1):7-30 doi: 10.3322/caac.21349
3. Петрова Г.В., Каприн А.Д., Старинский В.В, Грецова О.П. Заболеваемость злокачественными новообразованиями населения России. Онкология 2014;(5):5-10.
4. Epstein JI, Carmichael M, Partin AW, Walsh PC. Is tumor volume an independent predictor of progression following radical prostatectomy? A multivariate analysis of 185 clinical stage B adenocarcinomas of the prostate with 5 years of followup. J Urol 1993;149:1478-1481.
5. Albertsen PC, Hanley JA, Gleason DF, Barry MJ. Competing risk analysis of men aged 55 to 74 years at diagnosis managed conservatively for clinically localized prostate cancer. JAMA 1998;280(11):975-80.
6. Wilt TJ, Brawer MK, Jones KM, Barry MJ, Aronson WJ, Fox S, et al. Prostate Cancer Intervention versus Observation Trial (PIVOT) Study Group. Radical prostatectomy versus observation for localized prostate cancer. N Engl J Med 2012; 367(6):203-213. doi: 10.1056/NEJMoa1113162.
7. Bill-Axelson A, Holmberg L, Ruutu M, Garmo H, Stark JR, Busch C, et al. SPCG-4 Investigators. Radical prostatectomy versus watchful waiting in early prostate cancer. N Engl J Med. 2011; 364(18):1708-1717. doi: 10.1056/ NEJMoa1011967.
8. Mottet N, Bellmunt J, Briers E, Bolla M, Cornford P, De Santis M., et.al. EAU-ESTRO-SIOG Guidelines on Prostate Cancer. Part 1: Screening, Diagnosis, and Local Treatment with Curative Intent European Urology, August 2016 Published online: 26 August 2016 Available from: http://www.europeanurology.com/arti-cle/S0302-2838(16)30470-5/abstract/eau-estro-siog-guidelines-on-prostate-can-cer-part-1-screening-diagnosis-and-local-treatment-with-curative-intent
9. Bostwick D G. Gleason grading of prostatic needle biopsies: correlation with grade in 316 matched prostatectomies. Am J Surg Pathol 1994; 18(8): 796-803
10. Cookson M S, Fleshner N E, Soloway SM, Fair WR. Correlation between Gleason score of needle biopsy and radical prostatectomy specimen: accuracy and clinical implications. J Urol 1997;157(2): 559-562
11. Koksal IT, Ozcan F, Kadioglu T C, Esen T, Kiliyaslan I, Tuny M. Discrepancy between Gleason scores of biopsy and radical prostatectomy specimens. Eur Urol 2000; 37(6): 670-674
12. Раснер П.И., Котенко Д.В., Колонтарев К.Б., Пушкарь Д.Ю. Сравнительный анализ функциональных результатов радикальной позадилон-ной и робот-ассистированной простатэктомии у больных локализованным раком простаты. Экспериментальная и клиническая урология 2014;(4):26-30.
13. Stamey TA, McNeal JE, Yemoto CM, Sigal BM, Johnstone IM. Biological determinants of cancer progression in men with prostate cancer. JAMA 1999; 281(15):1395-1400.
14. Samaratunga H, Montironi R, True L, Epstein JI, Griffiths DF, Humphrey PA, et al. Reports on International Society of Urological Pathology (ISUP) Consensus Conference on Handling and Staging of Radical Prostatectomy Specimens [Working group 1: specimen handling] Modern Pathology 2011; 24(11):6-15. doi: 10.1038/modpathol.2010.178.
15. Epstein JI. Prognostic significance of tumor volume in radical prostatectomy and needle biopsy specimens. J Urol 2011; 186(3):790-797. doi: 10.1016/ j.juro.2011.02.2695.
16. Caso JR, Tsivian M, Mouraviev V, Polascik TJ, Moul JW. Pathological T2 subdivisions as a prognostic factor in the biochemical recurrence of prostate cancer. BJUInt 2010; 106(11): 1623-1627. doi: 10.1111/j.1464-410X.2010.09439.x
17. DeCastro GJ, McCann T, Benson MC, McKiernan JM. Pathologic T2 stage subgroups and recurrence-free survival after radical prostatectomy. Urology 2008; 72(6):1214-1218. doi: 10.1016/j.urology.2008.01.054.
18. Eichelberger LE, Cheng L. Does pT2b prostate carcinoma exist? Critical appraisal of the 2002 TNM classification of prostate carcinoma. Cancer 2004; 100(12):2573-2576.
19. Hong SK, Han BK, Chung JS, Park DS, Jeong SJ, Byun SS, Evaluation of pT2 subdivisions in the TNM staging system for prostate cancer. BJU Int 2008; 102(9):1092-1096. doi: 10.1111/j.1464-410X.2008.07897.x.
20. Kordan Y, Chang SS, Salem S, Cookson MS, Clark PE, Davis R, et al. Pathological stage T2 subgroups to predict biochemical recurrence after prostatectomy. J Urol 2009; 182(5):2291-2295. doi: 10.1016/j.juro.2009.07.020
21. van Oort IM1, Witjes JA, Kok DE, Kiemeney LA, Hulsbergen-Van De Kaa CA. The prognostic role of the pathological T2 subclassification for prostate cancer in the 2002 Tumour-Nodes-Metastasis staging system. BJU Int 2008; 102(4):438-441. doi: 10.1111/j.1464-410X.2008.07611.x.
22. Abdelaziz A. Elgamal, Hendrik P. Van Poppel, Wim M. Van De Voorde, Jo A. Van Dopre, Raymond H. Oyen and Luc V. Baert Impalpable invisible stage T1c prostate cancer: characteristics and clinical relevance in 100 radical prostatectomy specimens — a different view. J Urol 1997;157:244-250
23. Noguchi M, Stamey TA, McNeal JE, Yemoto CM. Relationship between systematic biopsies and histological features of 222 radical prostatectomy specimens: lack of prediction of tumor significance for men with nonpalpable prostate cancer J Urol 2001; 166(1):104-109; discussion 109-110.
24. Terris MK, McNeal JE, Stamey T A. Detection of clinically significant prostate cancer by transrectal ultrasound-guided systemic biopsies. J Urol 1992; 148(3):829-832.
25. Griffin CR, Yu X, Loeb S, Desireddi VN, Han M, Graif T, Catalona WJ. Pathological features after radical prostatectomy in potential candidates for active monitoring. J Urology 2007; 178(3 Pt 1):860-863,
26. Kim JW, Park HK, Kim HG, Ham DY, Paick SH, Lho YS, et al. Discordance between location of positive cores in biopsy and location of positive surgical margin following radical prostatectomy. Korean J Urol 2015; 56(10):710-716. doi: 10.4111/kju.2015.56.10.710
27. Warlick C, Trock BJ, Landis P, Epstein JI, Carter HB. Delayed versus immediate surgical intervention and prostate cancer outcome. J Natl Cancer Inst 2006; 98(5):355-357.
28. Bangma CH, van den Bergh RC, Denis L, Roobol MJ. Understanding Active Surveillance. A new treatment option for PSA positive low risk prostate cancer. Central Eur J Urol 2009;62(2):70-73
29. Klotz L. Active surveillance with selective delayed intervention for favorable risk prostate cancer. Urol Oncol 2006; 24(1):46-50
30. Parker C. Watchful waiting, temporarily deferred therapy, or active surveillance? J Clin Oncol 2005; 23(6):1322; author reply 1322-1323.
31. Carter HB, Kettermann A, Warlick C, Metter EJ, Landis P, Walsh PC, et al. Expectant management of prostate cancer with curative intent: an update of the Johns Hopkins experience. J Urol 2007; 178(6): 2359-2364; discussion 2364-2355.
32. Stamey TA, McNeal JE, Yemoto CM, Sigal BM, Johnstone IM. Biological determinants of cancer progression in men with prostate cancer. JAMA 1999; 281(15):1395-1400.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 762.61 кб |
Ключевые слова:
рак предстательной железы, биопсия предстательной железы, стадирование, тактика лечения
Зачем делать биопсию аденомы простаты? Почему мне назначили биопсию аденомы простаты? У меня рак? – все эти вопросы мучают мужчину, которому назначили выполнение биопсии.
Здравствуйте, меня зовут Трофимчук Антон Дмитриевич. Я являюсь специалистом в области биопсии предстательной железы. Выполняю все существующие варианты биопсий простаты на современном уровне. Ранее Вы могли прочитать другие мои статьи, которые помогут Вам разобраться в видах биопсии простаты, подготовки к ней, технике проведения и т.д. Однако есть еще одна тематика, внимание к которой нередко не столь пристальное, нежели к другим аспектам «здоровья» предстательной железы. Речь пойдет о биопсии аденомы простаты. Давайте начинать!
Для начала рассмотрим, что же общего и различного между раком и аденомой простаты.
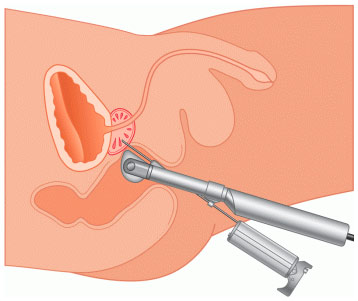
Аденома и рак простаты
Аденома и рак простаты – два заболевания, затрагивающие «здоровье» предстательной железы. Некоторые формы рака простаты, а также рак на ранних стадиях могут проявляться такими же симптомами, как и аденома простаты. Как при аденоме простаты, так и при злокачественной опухоли могут наблюдаться следующие симптомы:
- Затрудненное начало мочеиспускания;
- Необходимость напряжения брюшного пресса для инициации мочеиспускания;
- Учащенное мочеиспускание;
- Учащенное мочеиспускание в ночное время;
- Ослабление струи мочи;
- Прерывание струи мочи и ее капельное истечение;
- Ощущение наполненного мочевого пузыря после мочеиспускания;
- Кровь в моче.
Возникновение этих симптомов связано с тем, что увеличенная железа блокирует отток мочи из мочевого пузыря.
Несмотря на схожесть симптомов, аденома и рак простаты имеют множество различий.
Проведение фьюжн биопсии возможно только на специализированном аппарате, таком как Hitach arietta v70.
Запатентованная технология RVS позволяет сопоставить УЗИ и МРТ в режиме реального времени и осуществить наведение на очаг с точностью до 1 мм.
Аденома простаты – это не рак простаты!
В первую очередь вы должны понимать, что аденома простаты – не рак! Кроме того, аденома простаты не вызывает рак, не является фактором риска озлокачествления или предраковым состоянием. Тем не менее, так как рак и аденома имеют ряд сходных симптомов врачу необходимо провести специальные тесты и исследования с целью выявления точной причины возникших проблем. Кроме того, не стоит забывать и о том, что оба заболевания могут поражать предстательную железу одновременно.
Пальцевое ректальное исследование
Пальцевое ректальное исследование – обязательная процедура, позволяющая мне получить предварительную информацию о состоянии предстательной железы. При аденоме железа увеличена в размере, гладкая на ощупь, эластичной консистенции. Если форма простаты изменена, железа плотная на ощупь, с прощупываемыми узелками по периферии — это может указывать мне наличие ракового процесса. Хотя небезызвестно, что интерпретация результатов этого исследования зачастую субъективно и варьирует в широком диапазоне, в зависимости от опыта специалиста. По данным некоторых исследований вероятность того, что это исследование «поможет» обнаружить рак составляет не более 30-40 %. Тем не менее, пальцевое ректальное исследование является обязательным к проведению при первичном обследовании и рекомендовано всеми известными мировыми урологическими и онкологическими сообществами.
Простат-специфический антиген
Анализ на уровень простат-специфического антигена в крови также позволяет предположить причины возникновения симптомов нарушения мочеиспускания. Отмечу тот факт, что любое заболевание и иные состояния, такие как эякуляция, массаж простаты, наличие камня в мочевом пузыре и т.д. также могут приводить к повышению уровня простат-специфического антигена в большей или меньшей степени.
Большая часть простат-специфического белка образуется в клетках переходной зоны предстательной железы, т.е. зоны, подверженной доброкачественной гиперплазии. В то время как периферическая зона, являющаяся источником рака в большинстве процентов случаев, вырабатывает незначительное количество простат-специфического антигена. Несмотря на то, что объем аденомы может быть значительно больше, чем объем опухоли, раковые клетки вырабатывают в десятки раз больше простат-специфического антигена, чем ткани аденомы.
Значительное повышение уровня простат-специфического антигена (в разы) может свидетельствовать о наличии злокачественного процесса. Например, если уровень ПСА в крови составляет 40 нг/мл, при норме до 5 нг/мл, врач с высокой вероятность может предположить наличие рака. Нередко у мужчины уровень простат-специфического антигена может быть повышен, но результат нельзя точно интерпретировать. Например, уровень ПСА равный 10 нг/мл может свидетельствовать об аденоме простаты, но и не исключать наличие опухолевого процесса. В таких случаях требуются дополнительные исследования.
Если анализы и лабораторно-инструментальные исследования (такие как магнитно-резонансная томография и ультразвуковое исследование простаты) указывают на высокую вероятность рака именно в месте расположения аденомы, то есть в транзиторной зоне – назначается биопсия аденомы простаты. Биопсия – главное исследование, позволяющее подтвердить или исключить рак предстательной железы. При биопсии врач с помощью специальных инструментов получает небольшие фрагменты предстательной железы, которые исследуются под микроскопом.
Что значат результаты биопсии простаты?
После биопсии простаты, фрагменты железы отправляются на исследование, где под микроскопом квалифицированным специалистом, врачом-морфологом делается заключение о наличии атипичных клеток. Более подробно о гистологическом заключении, степени злокачественности рака простаты вы можете прочесть в статье Анализ ткани и результаты биопсии простаты. И лишь на основании сделанного морфологом заключения можно поставить окончательный диагноз и приступить к лечению. Приведенный ниже список вопросов-ответов поможет вам лучше понять медицинский язык врачебного заключения.
1. Что значит, если результаты биопсии гласят «аденоматозная гиперплазия простаты», или «доброкачественная простатическая гиперплазия»? Такие результаты свидетельствуют о доброкачественных изменениях тканей простаты, и отсутствии рака.
2. Если при биопсии простаты не был выявлен рак, могу ли я быть уверен в том, что у меня нет опухоли?
 |
Рисунок. На рисунке изображен процесс получения фрагмента тканей железы. Видно, что биопсиная игла не затрагивает область, в которой есть опухоль. |
К сожалению, в некоторых случаях биопсия простаты может давать ложно-отрицательные результаты. Иногда требуется повторное выполнение биопсии простаты. С целью улучшения первичной диагностики рака простаты и снижения вероятности повторной биопсии существует самый современный вариант биопсии простаты – фьюжн (от англ. Fusion – слияние) биопсия простаты. Вы также можете более подробно ознакомится с информацией про этот вид исследования на нашем сайте
3. Что значит, если в результатах биопсии простаты «хроническое воспаление»?
Как следует из названия эти результаты свидетельствуют о наличии хронического простатита, что никак не связано с раком.
4. Что значат понятия «атрофия» или «аденоз» или «атипическая аденоматозная гиперплазия»?
Это значит, что под микроскопом врач видит нестандартные склеротические для простаты клетки. Но это не является злокачественной опухолью.
5. «Простатическая интраэпителиальная неоплазия» (ПИН) – что это значит?
Это говорит о том, что ткани простаты изменены и клетки не похожи на здоровые клетки. Если результат биопсии гласит о наличии ПИН высокой степени, не переживайте, это не злокачественная опухоль. Если же при биопсии обнаруживается ПИН с атипичными железами, это может быть признаком рака.
6. ASAP (атипичная мелкоацинарная пролиферация) – что это значит?
ASAP — термин, используемый для описания изменений в клетках предстательной железы, видимых под микроскопом, когда неясно, являются ли клетки раковыми. Например, может быть недостаточно измененных клеток, чтобы врач морфолог мог сказать, являются ли они раком. Если у вас есть ASAP, могут потребоваться дополнительные тесты, вплоть до повторной биопсии, чтобы любые дальнейшие изменения клеток были обнаружены на ранней стадии.
Надеюсь, вам понравилась данная статья, и я смог ответить на интересующие и волнующие вас вопросы. В случае, если у вас остались сомнения, вы всегда сможете со мной связаться, и я буду рад их обсудить.

Автор статьи
Трофимчук Антон Дмитриевич
Статьи по данной теме
Промежностная (трансперинеальная) биопсия простаты
Здравствуйте, меня зовут Трофимчук Антон Дмитриевич. Эта статья поможет вам получить исчерпывающую информацию о “промежностной биопсии простаты”. Скорее всего, вы уже читали разную информацию…
Читать полностью
Подготовка к биопсии простаты
Здравствуйте, меня зовут Трофимчук Антон Дмитриевич. На протяжении более чем 12 лет я занимаюсь биопсией предстательной железы. Если вы прочитаете мою статью, то скорее…
Читать полностью
Диета после биопсии простаты
После выполнения биопсии простаты необходимо соблюдать нестрогую диету. Ниже описаны продукты, которые наиболее часто используются в пищу в наших широтах и ограничения по их…
Читать полностью
Трансректальная биопсия простаты
Здравствуйте, меня зовут Трофимчук Антон Дмитриевич. Эта статья поможет вам получить актуальную информацию о самом распространенном виде биопсии предстательной железы – трансректальной биопсии простаты.…
Читать полностью
Где сделать биопсию простаты
Добрый день, дорогие друзья! Меня зовут Трофимчук Антон Дмитриевич. Более 12 лет я занимаюсь биопсией предстательной железы. Если вы читаете эту статью значит вопрос…
Читать полностью
Повторная биопсия простаты
В каких случаях проводится повторная биопсия простаты? Время ожидания результата биопсии предстательной железы составляет около недели. Дальнейшая тактика зависит от заключения гистолога. Результат считается…
Читать полностью
Насколько больно делать биопсию простаты?
Здравствуйте, если вы ещё не читали моих статей о биопсии предстательной железы, то позвольте представиться. Меня зовут Ковченко Григорий Александрович. Более 12 лет я…
Читать полностью
Цена (стоимость) биопсии простаты
Со стоимостью биопсии простаты в нашей клинике вы можете ознакомиться в прайсе. Почему стоимость биопсии простаты так сильно отличается в разных клиниках и почему…
Читать полностью
Повторная биопсия простаты
В каких случаях проводится повторная биопсия простаты? Время ожидания результата биопсии предстательной железы составляет около недели. Дальнейшая тактика зависит от заключения гистолога. Результат считается…
Читать полностью
После биопсии простаты
Здравствуйте, меня зовут Трофимчук Антон Дмитриевич. В этой статье попробую описать в хронологическом порядке что вас ждёт сразу и через некоторое время после биопсии,…
Читать полностью
Анализ ткани и результаты биопсии простаты
Для исследования при трансректальной биопсии простаты мы забираем от 12 до 30 столбиков ткани из разных областей предстательной железы длиной 20 мм и толщиной…
Читать полностью
Секс после биопсии простаты
Противопоказан ли секс после биопсии простаты? После биопсии предстательной железы существует риск развития инфекции мочевыводящих путей. Сама биопсия осуществляется через стенку прямой кишки. Обеспечить…
Читать полностью
Последствия и осложнения после биопсии простаты
Процедура биопсии простаты, как правило, хорошо переносится пациентами. Подробно о Добрый день, дорогие друзья! Меня зовут Трофимчук Антон Дмитриевич. Я провожу фьюжн биопсии простаты…
Читать полностью
Как проводится биопсия простаты
Существует три метода проведения биопсии простаты. Трансректальный – наиболее распространенный метод биопсии простаты. При этом методе биопсия простаты выполняется через прямую кишку. После введения…
Читать полностью
Биопсия простаты
Добрый день, дорогие друзья! Меня зовут Трофимчук Антон Дмитриевич. Биопсией простаты я занимаюсь много лет и накопил достаточно большой опыт в ее выполнении. В…
Читать полностью
Аденома простаты – заболевание, вызывающее массу тревог и волнений. И любое обследование лишь повышает уровень напряжения. Если пациенту назначается биопсия аденомы предстательной железы, это вовсе не означает, что у него обнаружили рак. Биопсия позволяет уточнить, какое именно заболевание стало причиной повышение уровня ПСА.
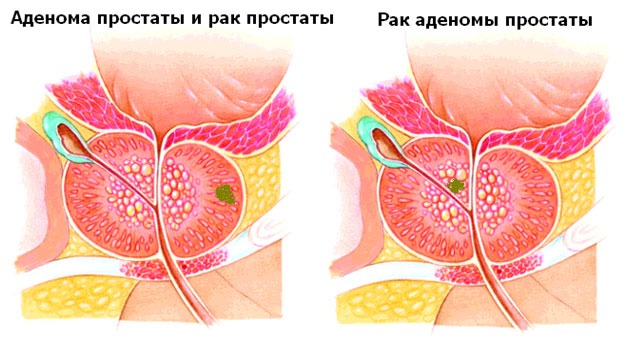
Как аденома (также называемая доброкачественной гиперплазией), так и рак, это проблемы, влияющие на состояние и работоспособность простаты.
Рак предстательной железы имеет немало различных форм, симптомы которых могут проявлять себя также, как и аденома простаты. Кроме того, рак в начальной стадии тоже имеет много сходств с аденомой. Эти симптомы часто сбивают с толку. Потому всегда требуются дополнительные обследования и анализы.
Как аденома простаты, так и рак часто проявляются следующими симптомами:
- Возникновение проблем в процессе мочеиспускания, (также может требоваться напряжение мышц пресса);
- Учащение позывов к мочеиспусканию, в особенности ночью;
- Заметное ослабление струи мочи, прерывания, капельные подтекание мочи;
- Чувство наполненности не исчезает даже после опорожнения мочевого пузыря;
- Гематурия (значительное содержание крови в моче). В 20% случаев это означает развитие злокачественной опухоли (рак простаты). Но при обнаружении гематурии всегда следует так же проводить обследование почек и мочевого пузыря.
При аденоме простаты не обязательно наличие рака предстательной железы!!!
Каждый должен понимать, что аденома простаты и рак – абсолютно разные проблемы. Аденома никогда не является симптомом, причиной появления злокачественной опухоли. Она вообще никак не влияет на процессы, имеющие онкологическую природу.
Но, так как ряд симптомов сходны, урологу нужно получить результаты ряда тестов, которые помогут точно определить, что именно стало причиной возникновения тех, или иных симптомов. Также, следует помнить, что аденома и рак могут присутствовать одновременно. В целом же рак простаты, симптомы которого во многом сходны с аденомой, может сбить человека с толку. Именно поэтому важно провести ряд исследований и тестов.
»»» Мифы о раке предстательной железы
»»» Мифы об аденоме предстательной железы
Пальцевое ректальное исследование при аденоме и раке простаты
Данное обследование помогает урологу узнать, в каком состоянии находится железа. Прощупав простату, врач получает информацию о размерах, гладкости и эластичности. При появлении изменений, уплотнений и узелков, специалист может диагностировать возможность начала раковых процессов.
Простат-специфический антиген
Польза анализа ПСА заключается в том, что таким образом можно уточнить причины появления ряда симптомов. Медицине известно, что такие заболевания как аденома простаты, рак простаты и простатит вызывают повышение ПСА.
В переходной зоне железы формируется основное количество простат-специфического белка. Именно этот участок более всего подвержен возникновению аденомы простаты. Периферическая зона наоборот производит намного меньше ПСА, но является основным источником возникновения злокачественных опухолей. Следует обратить внимание на тот факт, что клетки простаты, поражённые раком, вырабатывают намного больше ПСА, чем ткани простаты с аденомой. Резкое и значительное повышение ПСА свидетельствует если не о появлении рака, то о вероятности процессов, которые могут привести к появлению злокачественных образований. В случае повышения уровня ПСА выше отметки в 40 нг/мл доктор может в большой долей уверенности говорить о раке, НО не стоит забывать, что диагноз рак ставиться только после верификации, т.е. необходимо выполнить биопсию аденомы предстательной железы и получить кусочки ткани, которые отправляются на морфологическое исследование. При ПСА более 10 нг/мл следует также выполнять исследования исключающие наличие метастазов.
Бывают ситуации, при которых сложно определить развитие опухоли. В частности, когда уровень ПСА до 10 нг/мл (норма до 4 нг/мл), врач так же делает предположение о возможности появления злокачественной опухоли и с целью искления злокачественного диагноза требуется выполнение биопсии.
Что означают результаты биопсии аденомы предстательной железы?
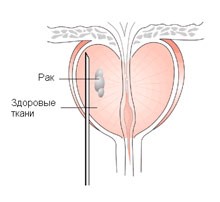
Ткани, взятые при биопсии аденомы предстательной железы для анализа, исследует морфолог. Этот специалист даёт заключение, основываясь на котором уролог может поставить точный диагноз.
Ответы по результатам биопсии аденомы предстательной железы
Далее мы приводим ряд вопросов, касающихся врачебных заключений и ответов на них:
- Вопрос: что означают термины «доброкачественная гиперплазия», и «доброкачественные ткани простаты»?
Ответ: такое заключение означает, что в простате нет злокачественной опухоли.
- Вопрос: можно ли быть уверенным в отсутствии рака простаты, если биопсия аденомы предстательной железы не показала развитие рака?
Ответ: бывают ситуации, когда биопсия даёт неправильный результат. В отдельных случаях, процедуру выполняют повторно.
- Вопрос: что означают понятия «острое воспаление» и «хроническое воспаление»?
Ответ: это всего лишь острый и хронический простатит. И рак простаты к этим заключениям не имеет ни малейшего отношения.
- Вопрос: что означают термины «аденоз», «атрофия», «атипическая аденоматозная гиперплазия»?
Ответ: это означает лишь то, что при биопсии аденомы предстательной железы найдено некоторое количество клеток, которые имеют сходство с раковыми. Но появление этих клеток ещё не означает наличие злокачественной опухоли.
- Вопрос: что такое «Простатическая интраэпителиальная неоплазия» (ПИН)?
Ответ: если вы получили такое заключение, это означает, что в тканях простаты обнаружены изменения, а клетки железы не выглядят, как здоровые.
Дальше есть два варианта:
1. ПИН высокой степени вовсе не означает, что у вас рак;
2. А вот когда биопсия аденомы простаты показывает ПИН с атипичными железами, есть повод для беспокойства. Возможно, это свидетельствует о развитии опухолевых процессов. Но никогда не стоит паниковать раньше времени, в большинстве случаев необходимо выполнить иммуногистохимическое исследование стеклопрепаратов взятых кусочков простаты при биопсии и вовсе не обязательно это будет рак простаты, симптомы которого часто похожи на развитие аденомы.