Туберкулез органов дыхания – одна из самых актуальных проблем здравоохранения в мире и в Российской Федерации. Заболеваемость населения РФ туберкулезом с 1991 г. увеличилась на 150% и в 2002 г. составила 88,1 на 100 тыс. населения. Смертность от туберкулеза увеличилась за этот период почти в 3 раза [1]. Высок процент поздней диагностики туберкулеза легких в лечебных учреждениях общей лечебной сети. В этих случаях только у около 20% больных туберкулезом легких заболевание диагностируют в первые 2–3 недели заболевания, а у остальных 80% – в сроки от 1 до 3 мес. Расхождение диагнозов по туберкулезу у умерших в нетуберкулезных больницах достигает 80% и более. По данным А.Г. Хоменко, особенно часты диагностические ошибки при абациллярных формах туберкулеза. Известно также, что у больных активным туберкулезом органов дыхания микобактерии туберкулеза в мазках мокроты в первые 2–3 недели болезни нередко не обнаруживаются, особенно у больных казеозной пневмонией, и при отсутствии деструктивных изменений в легких [2].
Поскольку основой диагностики туберкулеза служит обнаружение микобактерии туберкулеза (МОТ), приведем сравнительную характеристику методов их обнаружения. При бактериоскопии мазка, окрашенного по Цилю–Нильсену, МБТ могут быть обнаружены при наличии не менее 100.000 –1.000.000 бактериальных клеток в 1 мл патологического материала. Такое значительное количество МБТ встречается при распространенных, преимущественно легочных формах заболевания (диссеминированная, фиброзно–кавернозная, цирротическая). Методы накопления (флотация) повышают выявляемость МБТ по сравнению с обычной микроскопией на 10%. Люминесцентная микроскопия при туберкулезе в настоящее время является эффективным бактериоскопическим методом лабораторной диагностики, широко применяющимся в микробиологических лабораториях Российской Федерации. Чувствительность метода люминесцентной микроскопии 10.000 – 100.000 МБТ в 1 мл материала [8].
Культуральный метод выявления МБТ дает положительные результаты при наличии в исследуемом материале от 20 до 100 жизнеспособных микробных клеток в 1 мл. Однако он трудоемок и длителен в связи с тем, что МБТ являются в основном медленно растущими организмами и рост их колоний наблюдают в течение 2–3 месяцев. Для увеличения результативности культурального метода рекомендуется применять посев материала одновременно на две–три различных питательных среды. Продолжительность роста МБТ ограничивает диагностические возможности клиницистов. МБТ выявляются лишь при 52–65% случаев активного туберкулеза легких, а в клинике внелегочного туберкулеза удельный вес их выявления еще ниже. Значительные трудности представляет обнаружение микобактерий у лиц со скудным их выделением. Среди впервые выявленных больных у одной трети бактериовыделение является однократным. Культуральный метод позволяет проводить определение чувствительности и устойчивости МБТ к противотуберкулезным антибиотикам [8].
За рубежом широкое распространение получила радиометрическая система ВАСТЕС для быстрого обнаружения живых МБТ в жидкой питательной среде. Микобактерии культивируют в жидкой ВАСТЕС–среде, где в качестве источника углерода используется меченая 14С пальмитиновая кислота. При положительных данных бактериоскопического исследования рост МБТ обнаруживали радиометрически на 7–10–й день и на 14–21–й дни при отрицательных данных. К недостаткам этого метода, ограничивающим возможность его широкого применения, относятся: высокая себестоимость исследования; необходимость применения радиоактивных изотопов и специального радиометрического оборудования, сложность работы с изотопной технологией; необходимость дополнительного посева на плотную питательную среду при возникновении проблем с идентификацией или интерпретацией результатов.
Метод ПЦР основан на ферментативной амплификации выбранных специфических участков генома бактерий рода Mycobacterium tuberculosis, их дальнейшей детекции и идентификации. Аналитическая чувствительность метода очень высока и соответствует выявлению 1–10 бактериальных клеток. Чувствительность метода достигает 74–92%, специфичность 92–100%. На эффективность ПЦР–анализа существенным образом влияет метод обработки клинического материала [3]. В ПЦР–диагностике туберкулеза для исследований обычно используют мокроту, промывные воды бронхов, бронхиальные аспираты, плевральную жидкость, мочу, спинномозговую жидкость, кровь, биоптаты лимфоузлов и других тканей.
Если у пациента не удается обнаружить МБТ при стандартном обследовании, проводится дальнейший диагностический поиск, включающий патоморфологическое исследование материала, полученного при биопсии пораженного органа, при котором подтверждением диагноза служит выявление туберкулезной гранулемы с казеозным некрозом, эпителиодными клетками, лимфоцитами, гигантскими многоядерными клетками Пирогова–Лангханса.
Как уже было сказано выше, в настоящее время растет число больных с острыми формами туберкулеза органов дыхания. По данным Челноковой О. (2003г.) , среди впервые выявленных больных туберкулезом органов дыхания число остро прогрессирующих форм составило 35%, у 7% была казеозная пневмония.[7].
Приводим наше наблюдение.
Больная К., 52 лет, поступила в клинику госпитальной терапии ММА имени И.М. Сеченова 01.03.05 с жалобами на выраженную слабость, одышку при минимальной физической нагрузке, разговоре, надсадный приступообразный кашель с выделением желто–зеленой мокроты до 50 мл за сутки, усиливающийся ночью, повышение температуры тела до 38°С, кожный зуд, отсутствие аппетита, похудание на 12 кг за год.
Из анамнеза жизни: Родилась 13 августа 1953 г. в Тамбовской области. В детстве от сверстников в физическом развитии не отставала. Образование высшее – закончила Волгоградский Медицинский институт. Работала врачом–терапевтом. С 1989 года живет в Москве. До 2004 года работала терапевтом–реабилитологом в отделении реабилитации инвалидов центра социального обслуживания. Замужем, имеет 2 сыновей (23 и 16 лет). Вредные привычки отрицает. Менструации с 14 лет, регулярные, необильные, безболезненные. Было 7 беременностей, из них 3 родов, 4 медицинских аборта. Менопауза в 46 лет. Из перенесенных заболеваний: в детстве – частые ангины, ОРВИ, корь, паротит. В 7 лет перенесла туберкулезный бронхоаденит, по поводу чего в течение года принимала противотуберкулезные препараты. В последующем к фтизиатру не обращалась. Аппендэктомия в 20 лет, тонзиллэктомия в 25 лет. Миопия средней степени. Отец умер в 92 года от острого нарушения мозгового кровообращения, мать умерла в 47 лет от рака желудка. Сестра 45 лет – практически здорова. Дети: первый сын трагически погиб, второй сын 23 лет здоров, у третьего сына 16 лет несахарный диабет. Аллергологический анамнез не отягощен.
Из истории заболевания: с 37 летнего возраста пациентка страдала первичным билиарным циррозом. С 1997 г. наблюдается в клинике госпитальной терапии ММА имени И.М. Сеченова, где диагноз первичного билиарного цирроза был подтвержден морфологически. По данным обследования в это время в анализах крови уровень щелочной фосфатазы (ЩФ) и гамма–глутамилтранспептидазы (Г–ГТ) превышал норму в 10 раз, АЛТ и АСТ в 3 раза, также отмечалась анемия (Нв 80–90 г/л), ускорение СОЭ до 50–60 мм/ч. Проводилась терапия урсофальком, сеансы плазмафереза, однако активность заболевания оставалась постоянно высокой: сохранялись синдром цитолиза, холестаза. С 2001 г. выявляется варикозное расширение вен пищевода 2–3 ст., синдром печеночно–клеточной недостаточности. Пациентка продолжала принимать урсофальк, соблюдала диету, чувствовала себя относительно удовлетворительно, кожный зуд был незначительным. Отмечала постепенное снижение массы тела, к концу 2003 года масса тела составляла 58–60 кг.
Резкое ухудшение состояния с декабря 2003 г., когда после переохлаждения появился кашель с гнойной мокротой, эпизод кровохарканья, лихорадка до 38°С. Пациентка была госпитализирована в отделение реанимации и интенсивной терапии (ОРИТ) городской больгницы по месту жительства, где диагностирована двухсторонняя плевропневмония с локализацией инфильтрации в нижней доле слева и верхней и нижней долях справа. Консультирована фтизиатром – туберкулез был отвергнут. Проводилась терапия антибактериальными препаратами, трихополом. Температура тела нормализовалась в течение недели, однако кашель и одышка сохранялись, пациентка похудела на 7 кг. В марте 2004 г. в связи с появлением бронхообструктивного синдрома была госпитализирована в городскую больницу. При исследовании функции внешнего дыхания выявлено снижение показателей жизненной емкости легких, вентиляционные нарушения по обструктивному типу, проба с бронхолитиками отрицательная. Проводилась терапия фликсотидом, вентолином – без существенного эффекта. В апреле вновь отмечаются подъемы температуры тела до 38–39°С, самостоятельно лечилась линкомицином и пефлоксацином в течение 5 дней, температура снизилась до субфебрильных цифр, но одышка и кашель сохранялись на прежнем уровне. Была вновь госпитализирована в городской стационар, где диагносцирован хронический бронхит, проводимая терапия не известна. После выписки сохранялась и нарастала выраженная слабость, кашель с гнойной мокротой, одышка при небольшой нагрузке, субфебрильная температура тела с периодическим повышением до фебрильных цифр, иногда озноб, потливость. В конце июня была госпитализирована в клинику госпитальной терапии им. А.А. Остроумова.
При обследовании было выявлено: в анализах крови: анемия, ускорение СОЭ, снижение альбумина, выраженный синдром холестаза, цитолиза, печеночно–клеточной недостаточности. В мокроте: лейкоциты покрывают все поля зрения. Candida. При компьютерной томографии (КТ) легких: справа во 2 сегменте плотные очаги, в 4 сегменте на фоне ограниченного фиброза – плотные очаги, уплотнение междолевой плевры справа; слева в 3 сегменте участок ограниченного фиброза; в корне правого легкого визувализируется мягкотканный конгломерат, отмечается уменьшение объема и уплотнение легочной ткани 2 и 6 сегментов, просвет 2 бронха не визуализируется, просвет 6 бронха резко сужен и деформирован; конгломерат интимно прилежит к костальной и медиастинальной плевре; субплеврально справа в 6 сегменте – неправильной формы округлое образование 17мм, связанное с конгломератом; жидкости в плевральных полостях не определяется; структуры средостения и корней легких дифференцированы; признаков лимфаденопатии не выявлено. В клинике проводился дифференциальный диагноз между воспалительным процессом в правом легком (возможно, грибковой этиологии), туберкулезом, опухолью правого бронха. Проводилась дезинтоксикационная терапия, урсофальк, цефтриаксон. Однако пациентка отказалась от продолжения обследования и противомикробной терапии и была выписана по собственному желанию. Диагноз оставался неясным.
За последующие 4 месяца отмечалось усиление ночного кашля с выделением слизисто–гнойной мокроты, нарастание одышки (вплоть до одышки при разговоре, в покое), периодически лихорадка до 38–39°С, выраженная общая слабость, отсутствие аппетита, дальнейшее похудание. В начале ноября отметила появление плотного округлого болезненного образования в подчелюстной области слева. Самостоятельно принимала антибиотики без особого эффекта. 25 ноября 2004 г. была госпитализирована в клинику госпитальной терапии им. А.А. Остроумова. Больная поступила в крайне тяжелом состоянии: кахексия, масса тела 38 кг. Кожные покровы бледные, сухие. В подчелюстной области справа пальпируется болезненное округлое образование плотноэластической консистенции, над легкими дыхание ослаблено, в нижних отделах с обеих сторон крепитация, тоны сердца приглушены, ритм правильный, ЧСС 90 в мин, АД 95/60 мм рт.ст., живот мягкий, безболезненный, печень на 1 см выступает из–под края реберной дуги, отеков нет. В связи с нарастанием дыхательной недостаточности 28 ноября пациентка была переведена в ОРИТ ГТК. При обследовании: в анализе крови отмечалась анемия Нв 107 г/л, лейкоцитоз до 24 тыс., относительная лимфопения, ускорение СОЭ до 35 мм/ч, снижение альбумина до 2,7 г/л, холинэстеразы до 1012 МЕ/л (норма 5600–12900), повышение уровня ЩФ 1590 ед/л (норма 98–274), Г–ГТ 323 ед/л (5–61), АСТ 52 ед (0–40), АЛТ 48 ед (0–400, общего билирубина 2,0 мг/дл (0,2–1,0). При компьютерной томографии легких выявлено: в легких в ранее обнаруженном конгломерате в области 2 и 6 сегментов справа определяются полости распада размером 25–28 мм; слева определяется участок консолидации легочной ткани, занимающий практически полностью 8 сегмент и частично 9 и 10; просветы бронхов в данном участке прослеживаются; в области этих изменений в 9 и 10 сегментах определяется снижение воздушности легочной ткани по типу «матового стекла» и усиление легочного рисунка; обширные участки консолидации, снижения воздушности легочной ткани и усиления легочного рисунка определяются преимущественно в язычковых сегментах слева, а также в средней доле, в 3 и 6 сегментах справа; лимфоузлы средостения умеренно увеличены в количестве. Заключение: По сравнению с предыдушими данными наблюдается отрицательная динамика в виде появления обширных участков консолидации и снижения воздушности легочной ткани; формирования полостей в ранее обнаруженных учасках уплотнения легочной ткани. К дифференциально–диагностическому ряду рекомендовано добавить бронхиолит с пневмонией, аспирационную пневмонию, саркоидоз (альвеолярный саркоид), менее вероятно наличие бронхиоло–альвеолярного рака. На ЭКГ: синусовая тахикардия с ЧСС 110 в мин; блокада передней ветви левой ножки пучка Гиса; перегрузка правого предсердия. При УЗИ органов брюшной полости: печень не увеличена, умеренно неоднородная, внутрипеченочные желчные протоки не расширены, воротная вена до 8 мм; желчный пузырь не увеличен, обычной формы, стенки плотные, камней нет; поджелудочная железа не увеличена, умеренно неоднородная, уплотнена; селезенка 116х46 мм; почки расположены низко, нормальных размеров (до 110х48 мм), толщина паренхимы до 12 мм; патологических образований не выявлено; в целом эхогенность паренхимы почек повышена; убедительных данных за наличие лимфатических узлов в брюшной полости не получено.
30 ноября проведена пункция образования подчелюстной области слева, получено 30 мл сливкообразного гноя. В цитограмме картина воспаления, в посеве выявлен рост Staphylococcus aureus 107 (MSSA), Candida 103. Больной проводились повторные санационные фибробронхоскопии (ФБС). При ФБС: просвет трахеи свободный, слизистая бледная, атрофичная, взята биопсия из верхне–долевого бронха слева и справа, браш–биопсия из нижних отделов. В цитограмме бронхиального смыва – клетки пролиферирующего бронхиального эпителия с элементами атипии на фоне воспаления; в посеве выявлен рост Acinetobacter anitratus – 103, чувствительный к левофлоксацину и ципрофлоксацину, Candida – 103. В повторных посевах – рост Candida. Браш–биопсия – клетки бронхиального кубического эпителия, макрофаги, лейкоциты до 20 в п/зр (нейтрофилы, лимфоциты). Биопсия бронха – стенка бронха с явлениями склероза и воспалительной инфильтрации; в прилежащей легочной паренхиме явления неспецифического интерстициального фиброза и слабо выраженная лимфо–гистиоцитарная инфильтрация. В бронхиальном смыве и в жидкости бронхо–альвеолярного лаважа методом ПЦР ДНК микобактерий туберкулеза (МБТ) не обнаружена. В повторных анализах мокроты при микроскопии микобактерии не обнаружены. Однократно в посеве крови выявлен рост E.coli, в связи с чем обсуждался вопрос развития септицемии. Тем не менее в связи с сохраняющимся подозрением на туберкулезную этиологию процесса пациентка неоднократно консультирована фтизиатром. Консультация фтизиатра: «Учитывая длительность заболевания, сохранение инфильтративных изменений в легких с обеих сторон, сохранение полостей деструкции, нельзя исключить специфическую природу заболевания. Рекомендовано: повторное исследование мокроты на микобактерии туберкулеза, повторная рентгенография, компьютерная томография легких в динамике».
Несмотря на ингаляции увлажненного О2, продолжалось нарастание явлений дыхательной недостаточности: состояние больной было тяжелым: отмечалось частое поверхностное дыхание с частотой до 40 и более в мин, угнетение сознания. В связи с этим 29 ноября больная была интубирована и переведена на искусственную вентиляцию легких, требовавшую медикаментозной седации. По мере компенсации состояния к 5 декабря введение седативных препаратов было прекращено. Учитывая компенсацию клинических признаков дыхательной недостаточности, а также положительную рентгенологическую динамику, с 7 декабря проводились попытки перевода больной на самостоятельное дыхание. Однако они оставались безуспешными: при уменьшении количества аппаратных дыханий у больной развивалось тахипноэ до 25–30 в мин и происходило быстрое истощение больной. 10 декабря проведена трахеостомия, и продолжена ИВЛ через трахеостомическую трубку. Течение заболевания осложнилось развитием ДВС–синдрома, проводилась трансфузионная терапия, переливание свежезамороженной плазмы, альбумина. Проводилась массивная антибактериальная терапия со сменой антибактериальных препаратов с учетом результатов посева и определения чувствительности (левофлоксацин + ванкомицин, имипинем, амоксициллин/клавуланат + амикацин), противогрибковая терапия (флуконазол), бронхолитическая, муколитическая, иммунокорригирующая терапия. На фоне проводимой терапии состояние улучшилось, и с 12 декабря ее удалось перевести на самостоятельное дыхание с ингаляцией увлажненного кислорода через трахеостомическую трубку, а с 18 декабря показатели газов крови сохранялись в пределах нормы без ингаляции кислорода. При контрольной компьютерной томографии легких отмечалась некоторая положительная динамика в виде уменьшения консолидации легочной ткани нижней доли левого легкого и формирования полостей в передне–базальных участках с обеих сторон. В результате проведенного обследования с учетом характера течения заболевания диагноз был сформулирован следующим образом: хронический абсцесс средней доли правого легкого с абсцедированием и развитием деструктивной пневмонии обоих легких бактериально–грибковой этиологии. Септицемия. Абсцесс подчелюстной области слева. ДВС–синдром. Дыхательная недостаточность 2–3 ст., продленная ИВЛ. Состояние после трахеостомии от 10.12.2004 г. – хронический слизисто–гнойный бронхит в фазе обострения. Первичный билиарный цирроз, умеренно активный, субкомпенсированный. Портальная гипертензия. Варикозное расширение вен пищевода 2 ст. Печеночно–клеточная недостаточность. Вторичный иммунодефицит. Кахексия. В дальнейшем пациентка была переведена в отделение пульмонологии, где продолжалась антибактериальная (амоксициллин/клавуланат, затем цефепим) и противогрибковая терапия, вводился пентаглобин, гепатопротекторы, свежезамороженная плазма. На фоне проводимой терапии сосотояние несколько улучшилось: нормализовалась температура, уменьшился кашель, пациентка стала передвигаться в пределах палаты. Больная была выписана домой под наблюдение участкового терапевта с рекомендациями продолжить антибактериальную терапию. Но несмотря на это в феврале вновь отмечаются подъемы температуры до 38°С с ознобом, усиление кашля, нарастание одышки и слабости.
В марте 2005 г. пациентка госпитализирована. В повторных анализах мокроты МБТ не обнаруживаются. В отделении проводилась терапия амикацином в течение 2 недель. При микологическом исследовании мокроты выявлен рост Candida albicans и Candida fland в высоком титре, резистентных к флуконазолу и чувствительных только к амфотерицину В. Учитывая деструктивный характер изменений при компьютерной томографии легких, результаты микологического исследования, 14 марта была начата терапия амфотерицином В. Однако в связи с плохой переносимостью, нарастанием гипокалиемии препарат был отменен, продолжена терапия фунгизоном. Продолжалось введение свежезамороженной плазмы, иммуноглобулина, альбумина, гепатопротекторов. В связи с отсутствием динамики в состоянии пациентка заочно была консультирована фтизиатрами: «Туберкулезная природа изменений в легких маловероятна так как: отсутствуют данные за перенесенный туберкулез, остаточные изменения туберкулеза органов дыхания на КТ; повторная микроскопия мокроты и бронхиальных смывов на выявление МБТ при наличии множественных полостей деструкции в обоих легких, исследование мокроты на ДНК МБТ методом ПЦР дали отрицательный результат; лечение антибиотиками широкого спектра в 2004 г. привело к интенсивному улучшению распространенных полисегментарных изменений (инфильтратов) в обоих легких. Целесообразно дополнительно провести исследование мокроты на МБТ методом микроскопии и посева». Течение заболевания осложнилось развитием левостороннего пневмоторакса, проводились пункция и дренирование плевральной полости. В связи с отрицательной динамикой по КТ легких начата антибактериальная терапия ципрофлоксацином и ванкомицином, но в связи с неэффективностью в течение последующих дней получала линезолид. 7 апреля рецидив пневмоторакса. При контрольной КТ: в области 9 сегмента левого легкого наблюдается появление участка инфильтрации легочной ткани размером 40х30х56 мм; также участок инфильтрации 8х16х29 мм определяется слева в 3 сегменте. Воздуха в полости плевры не обнаружено. Пациентка была выписана домой с диагнозом: «Двухсторонняя деструктивная пневмония смешанной этиологии (стафилококковая, кандидозная), тяжелого течения с образование множественных полостей. Рецидивирующий пневмоторакс слева от 27.03.05 и 07.04.04. Диффузный и очаговый пневмофиброз. Вторичная легочная гипертензия. Дыхательная недостаточность 3 стадии. Состояние после трахеостомии от 10.12.04 г. Хронический слизисто–гнойный бронхит в фазе обострения. Первичный билиарный цирроз 3–4 стадии. Печеночно–клеточная недостаточность 2 степени по Чайлд–Пью. Кахексия. Вторичное иммунодефицитное состояние. Энцефалопатия смешанного генеза 2 ст, астено–вегетативный синдром, вестибулопатия».
Однако на следующий день в связи с повторным пневмотораксом была госпитализирована в городскую больницу. Со слов родственников известно, что в стационаре была отменена антибактериальная терапия, назначены системные глюкокортикостероиды, который получала в течение месяца – практически без эффекта. Была выписана домой. 12 июля пациентка скончалась дома. Труп был доставлен в патолого–анатомическое отделение больницы.
Из протокола вскрытия: «В просвете гортани и трахеи гноевидное содержимое. Слизистая оболочка дыхательных путей серо–розовая, без кровоизлияний. Левое легкое воздушной консистенции. На разрезах ткань левого легкого темно–красная, с поверхности разрезов выдавливается пенистая розовая жидкость, из сосудов вытекает жидкая кровь. На поверхности разреза в ткани левого легкого определяются множественные серовато–желтоватые участки без четких границ, творожистой консистенции, размерами до 3х2, 5х2 см, с полостями, заполненными гноем, без четкой капсулы. В верхней доле правого легкого – участок светло–серо–желтого цвета, размерами 6,5х5х3 см, не связанный с крупными бронхами, с нечеткими границами, мягко–эластической консистенции. В остальной ткани правого легкого множественные участки творожистой консистенции, размерами 2,5х5х2 см, светло–серовато–желтоватого цвета, без четких границ, а также полости диаметром до 2 см, заполненные гноем. В обоих легких множественные сливающиеся мелкие зернистые очаги с гноевидным отделяемым. Лимфатические узлы корня легкого уплотнены, размерами до 3,5х2,5х2 см, ткань на разрезах черная, с серовато–желтыми включениями. Пристеночная плевра не утолщена, тонкая, гладкая, блестящая».
Результаты патогистологического исследования: «Легкие – множественные очаги казеозного некроза, часть их без демаркационной зоны. Прилежащие к зоне казеозного некроза альвеолы заполнены фибринозным экссудатом. Часть очагов казеозного некроза со слабо выраженной капсулой, представленной рыхлыми пучками соединительной ткани, диффузно–инфильтрированной лимфоидными элементами. В отдельных участках – эпителиоидные клетки, гигантские клетки инородных тел и Пирогова–Лангханса. Лимфатические узлы корня правого легкого – лимфоидные фолликулы единичные мелкие, без светлых центров. В– и Т–зоны опустошены. Диффузно в препарате лимфоциты. Единичные эпителиоидно–гигантоклеточные гранулемы без явлений казеоза и фиброзирующиеся гранулемы»
Патологоанатомический диагноз: «Основное заболевание: Инфильтративный туберкулез верхней доли правого легкого с кавернизацией. Полисегментарная казеозная пневмония в верхней доле правого легкого. Диссеминация – множественные очаги казеозного некроза в обоих легких. Казеозный некроз лимфатических узлов корня правого легкого. Осложнения: Отек головного мозга. Малокровие органов. Смешанные свертки крови в полостях сердца и крупных сосудах. Дистрофические изменения миокарда, почек. Кахексия. Сопутствующие заболевания: Атерокальциноз аорты. Мелкоузловой цирроз печени. Склероз поджелудочной железы. Остеопороз».
Анализируя данный клинический случай, хочется отметить изначально имевшуюся у врачей настороженность в отношении туберкулеза. Несмотря на повторные отрицательные результаты обнаружения МБТ в мокроте, неспецифическую картину воспаления, полученную при биопсии бронха, и отрицательные результаты ПЦР, сомнения в отношении туберкулезной этиологии процесса оставались до последних дней пребывания больной в стационаре. Особенностью данного случая является отсутствие выделения МБТ даже в той стадии заболевания, когда по данным КТ имелись признаки деструкции легочной ткани. Возможно, это было обусловлено проведением массивной антибактериальной терапии, включавшей препараты, обладающие туберкулостатическим действием (фторхинолоны II поколения и аминогликозиды). Существенным фактором, повлиявшим на ошибку в диагностике было повторное выявление роста бактериальной (золотистый стафилоккк, ацинетобактер) и грибковой флоры в посевах бронхиальных смывов и мокроты. Остается неясным вопрос о сроках развития у больной такой формы туберкулеза, как казеозная пневмония. Кажется маловероятным, что пациентка страдала этой формой туберкулеза в течение всего периода заболевания. Возможно, она развилась уже в терминальной стадии, когда иммунодефицитное состояние усугубило назначение системных глюкокортикостероидов.
По данным Мишина В.Ю., основными причинами диагностических ошибок туберкулеза легких в лечебных учреждениях общей медицинской сети являются: неполно собранный фтизиатрический анамнез, связанный с недостаточной настороженностью в отношении туберкулеза; неправильная оценка и интерпретация клинических проявлений туберкулеза легких в современных эпидемических условиях; неправильная трактовка рентгенологических изменений в легких и отсутствие рентгенологического контроля через 7–10 дней лечения пневмонии; отсутствие или однократное исследование мазков мокроты на микобактерии туберкулеза по Цилю–Нильсену; обзорная бронхоскопия без взятия биопсийного материала; тяжелая сопутствующая патология. Наибольшее число диагностических ошибок отмечается при инфильтративном туберкулезе легких и казеозной пневмонии [4,7].
Казеозная пневмония – это форма вторичного туберкулеза легких, характеризующаяся быстрым развитием и распространением казеозно–некротических изменений в легких в условиях выраженного иммунодефицита и бурного размножения микобактерий. Клинически она проявляется остро прогрессирующим течением с неуклонным усилением интоксикационного, бронхопульмонального синдромов, рентгенологически в легких выявляется поражение 3 и более сегментов, лабораторными признаками иммунодефицита, выраженными метаболическими нарушениями. Госпитализация подавляющего большинства больных казеозной пневмонией (до 86%) в общесоматические стационары определяется наличием «масок» заболевания и тяжелым состоянием больных при обращении за медицинской помощью. Дифференциальный диагноз наиболее часто приходится проводить с сепсисом, гангреной, абсцессом легкого, деструктивной пневмонией [5]. Высокая смертность (60–80%) определяется не только тяжелым, прогрессирующим течением, но и поздним началом противотуберкулезной терапии. При позднем начале она бывает неэффективна вследствие значительного объема поражения легочной ткани и развития выраженных полиорганных нарушений. Неуклонное увеличение объема поражения легочной ткани, которое носит необратимый характер, прогрессивное ухудшение состояния определяют сроки диагностики казеозной пневмонии в течение 1–2 недель как критические. По истечении данного периода в случае отсутствия эффекта от проводимой терапии, отрицательных результатов исследований мокроты на МБТ при сохранении подозрения на казеозную пневмонию целесообразно начинать комплексную противотуберкулезную терапию [6].
В последнее время все чаще врачам терапевтических стационаров приходится сталкиваться с различными формами туберкулеза органов дыхания, протекающими атипично, без бактериовыделения. Настороженность в отношении туберкулеза, тщательный клинико–анамнестический анализ, повторные лабораторные и инструментальные исследования для подтверждения специфической этиологии процесса позволяют своевременно диагностировать туберкулез и направить больного в противотуберкулезный стационар для проведения специфической терапии. С другой стороны, всегда нужно помнить о возможности и необходимости проведения в определенных случаях пробной противотуберкулезной терапии.
Литература:
1. Трифонова А.Ю., Стаханов В.А. Медико–социальные и психологические аспекты заболеваемости населения туберкулезом в современных условиях. // Российский медицинский журнал, №5, 2005 г. с.9–11.
2. Хоменко А.Г. Туберкулез: Руководство для врачей. М., 1998 г.
3. Вишневская Е.Б. Особенности выделения ДНК для ПЦР при туберкулезе внелегочных локализаций. // Проблемы туберкулеза. № 5, 1998 г., с.23–26.
4. Мишин В.Ю., Дейкина О.Н., Назарова Н.В. Дифференциальная диагностика туберкулеза легких и внебольничной пневмонии. // Консилиум медикум, т.6, № 4, 2004 г., с.232.
5. Степанян И.Э. Вопросы диагностики и дифференциальной диагностики туберкулеза органов дыхания в современных условиях. //РМЖ, т.7, №17, 1999г. с.836.
6. Кибрик Б.С., Челнокова О.Г. Проблемы диагностики и лечения казеозной пневмонии. // Пульмонология, т. 13 № 4, 2004 г. с.41–44.
7. Даниляк И.Г. Трудный диагноз болезней органов дыхания. «Русский врач», М., 2005 г. С. 48–70.
8. Козулицына Т.И. Микробиологические исследования./ В руководстве для врачей: Туберкулез органов дыхания. М.,1981 г.– с.136–149.
- Case Report
- Open Access
- Published: 09 June 2020
Infectious Diseases of Poverty
volume 9, Article number: 66 (2020)
Cite this article
-
2749 Accesses
-
8 Citations
-
Metrics details
Abstract
Background
Tuberculosis (TB) is a great mimicker and diagnostic chameleon, and prone to be diagnosed as malignancy. Even though many reports have described the differences between pulmonary TB and lung cancer, the atypical systemic hematogenous disseminated TB (HDTB) is very rare and more confusing in clinical practice.
Case presentation
A 73-year-old man, HIV-negative, was hospitalized to the local county hospital because of chest pain, low-grade fever, asthenia, anorexia and weight loss for the pasting two months. The CT findings of the two lungs showed multiple round or round-like nodules of different sizes, with clear boundaries and partial fusion. The level of serum CA19–9 was significantly higher than normal, and progressively increased. There were multiple enlarged lymph nodes in the neck, mediastinum, abdominal cavity and pelvic cavity. The symptoms were diagnosed as hematogenous spread of gastrointestinal tumor in the local county hospital. However, when transferred to our provincial hospital, through comprehensive dynamic analysis, this patient was diagnosed as atypical systemic HDTB, no cancer at all. Through routine anti-TB therapy for one year, the patient was recovered very well at the follow-up of half year after withdrawal.
Conclusions
In the past, most TB misdiagnosis cases involved in single organ and were finally confirmed through invasive examination. This case enriched clinical experiences in the diagnosis of atypical HDTB. We encouraged clinicians to establish a dynamic thinking for diagnosis and treatment and emphasized the value of biopsy and 18F-FDG-PET in distinguishing TB and cancer.
Background
Tuberculosis (TB) is a huge threat for public health in China, which is within the “high-burden country” list [1]. Even though enormous effort has been taken, treatment and control of TB still face many challenges. Detection and diagnosis of Mycobacterium tuberculosis (MTB) is difficult in most case. What’s worse, TB is a great mimicker and diagnostic chameleon, and prone to be diagnosed as malignancy, and vice-versa, because the radiographic characteristics and clinical symptoms of the two diseases are very similar [2,3,4,5]. Since cancer usually has worse prognosis and costs more medical resources compared with TB, misdiagnosis surely increases much more psychological stress and economical burden to the real TB patients. Furthermore, treatment strategy is totally different between neoplasm and TB. In such case, clinicians are placed into a dilemma to make a definite diagnosis, and are even at risk to become a “misdiagnosis murder” [6]. Thus, it’s pivotal to describe and summarize the nuances between neoplasm and TB through more case reports. Here, we described a very unusual case that a 73-year-old immunocompetent man with hematogenous disseminated TB (HDTB) was misdiagnosed as metastasis with multiple organs involvement.
Case presentation
Lung metastasis
On 7 March, 2018, a 73-year-old man, HIV-negative, was hospitalized to the local county hospital for 2-month chest pain, low-grade fever, asthenia, anorexia and weight loss. The patient had history of type II diabetes mellitus with regular administration of gliclazide, but efficacy was poor. Physical examination revealed body temperature 36.7 °C, pulse rate 96 beats/min, blood pressure 133/83 mmHg, respiratory rate 20/min, oxygen saturation 96% and mildly yellow skin and sclera. Respiratory system, cardiovascular system, neurological system and abdomen were normal. Laboratory examination showed anemia (hemoglobin 114 g/L), abnormal liver function (alanine aminotransferase 57 U/L, aspartate aminotransferase 48 U/L, γ-glutamyl transpeptidase 818 U/L, alkaline phosphatase 671 U/L, total bilirubin 44 μmol/L) and elevated cancer antigen 19-9 (CA19-9, 165 U/ml). The interferon-γ release assay test was negative. The skull computerized tomography (CT) showed lacunar infarction in bilateral basal ganglia. The thorax CT revealed multiple round or round-like nodules with variable sizes scattered throughout both lungs, suggestive of metastatic lung disease (Fig. 1A). Abdominal enhancement CT showed that a mass at the pancreatic head was obviously strengthened in the arterial phase, and the pancreatic duct and intrahepatic bile duct was slightly dilated (Fig. 2). Taken together, all examination results were strongly suspected of lung metastasis, which was originated from the pancreatic head or intestinal origin. However, TB infection could not be excluded completely. The patient denied further biopsy, and chose to accept experimental anti-TB therapy with rifampin and isoniazid. After one month, chest CT showed that lung lesions were not absorbed. Laboratory test showed that CA19-9 sharply increased, up to 1167 U/ml. Sputum smear for acid-fast bacilli (AFB) was negative. The doctors in the local county hospital excluded TB infection and proposed gastrointestinal malignant tumors combined with lung metastasis. The patient family was in deep sorrow and prepared to give up.
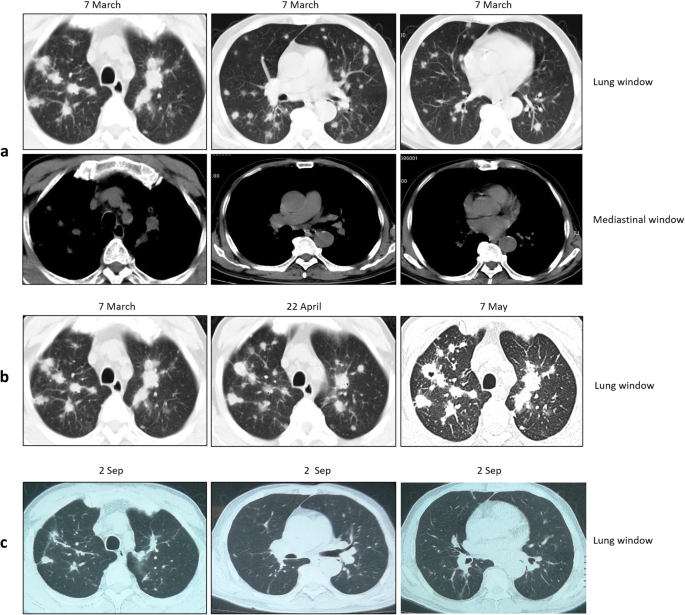
Thorax CT scan at different time points displayed evolution of lesions. a At admission, the thorax CT revealed multiple round or round-like nodules with variable size scattered throughout both lungs. b Development and evolution of lung lesions. The lung CT scan showed that pulmonary nodules gradually evolved with signs of fibrous tissue hyperplasia, such as cords, long burrs and fusion. c After four months of anti-TB treatment, thorax CT scan showed obvious absorbance of the lung lesions
Full size image
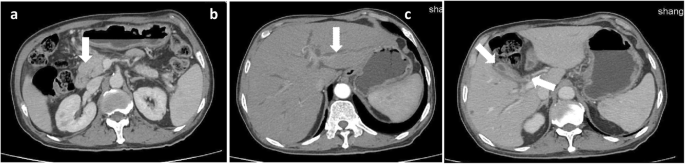
Abdominal enhancement CT suggested lesions in the intestinal tract. a There was a mass at the pancreatic head, indicated by arrow. b Intrahepatic bile duct was dilated, indicated by arrow. c The gallbladder wall (left arrow) and the wall of the upper end of the common bile duct (right arrow) were thicken
Full size image
Hematogenous disseminated TB
On 7 May, 2018, his daughter persuaded the patient to the provincial hospital for further diagnosis. Laboratory examination revealed hyperbilirubinemia (total bilirubin 70 μmol/L), CA19-9 832 U/ml, cancer antigen 125 141 U/ml, neuron-specific enolase 22.98 ng/ml, angiotensin-converting enzyme 178 U/L and serum (1,3)-β-D-glucan 235 pg/ml. 18F-fluorodeoxyglucose positron-emission tomography (18F-FDG-PET) scan showed focal high uptake in the multiple organs, including lung, liver, pancreas, spleen, gallbladder neck (Fig. 3), which suggested benign disease (especially TB). The patient accepted the endoscopic retrograde cholangiopancreatography to relieve hyperbilirubinemia, which was caused by bile duct obstruction. Biopsy from brushed biliary cell indicated no malignant tumor. A CT scan-guided transthoracic needle biopsy of the nodule at the left upper lobe was performed and the histopathology showed coagulative necrosis combining with granulomatous inflammation. AFB staining was positive and Periodic Acid-Schiff staining was negative (Fig. 4). In the meanwhile, qPCR for MTB DNA showed 4900 copy/ml in the sputum. Thus, the diagnosis of TB infection was definite. The patient then accepted anti-TB regimen, including isoniazid (300 mg/once a day [QD]), rifampicin (450 mg/QD), ethambutol (750 mg/QD), pyrazinamide (1500 mg/QD), levofloxacin (600 mg/QD) for three months, followed by isoniazid (300 mg/QD) and rifampicin (450 mg/QD) for another nine months.
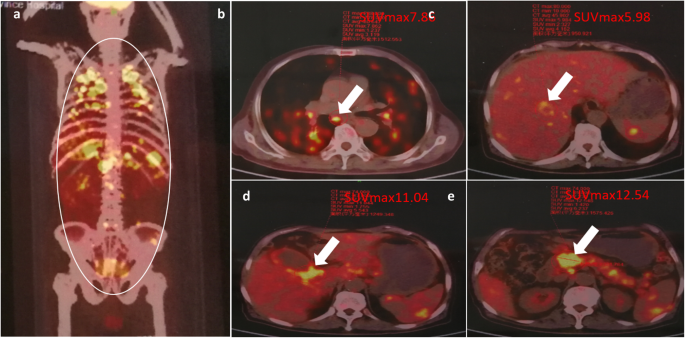
FDG-PET showed high uptake at different foci. a Foci in the whole body were defined by a circle. The yellow bright spots represented high uptake of 18F-FDG by local tissues. The maximum standard uptake value in different organs were shown, including lung (b, 7.86), liver (c, 5.98), gallbladder neck (d, 11.04), pancreatic head mass (e, 12.54)
Full size image
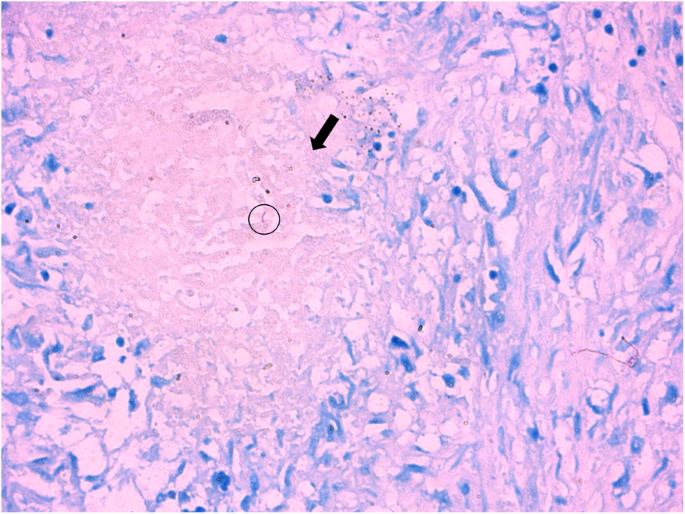
Puncture biopsy of left lung upper lobe revealed coagulative necrosis combined with granulomatous inflammation with hematoxylin-eosin staining (black arrow). Ziehl-Neelsen staining detected acid-fast bacilli (black circle) and Periodic Acid-Schiff staining was negative. Magnification × 200
Full size image
On 2 September, 2018, almost four months after hospitalization to our hospital, the thorax CT revealed that the lung lesions were absorbed significantly (Fig. 1B). After one year of treatment, continuous clinical and radiological improvement was observed, and the drugs were then withdrawn. The patient was asymptomatic at the follow-up of half year after withdrawal.
Discussion
Characteristics of TB misdiagnosis cases
We conducted literature search in NCBI PubMed database with keywords “tuberculosis” and “cancer” or “tumor” from 2016 to 2019. Totally, 23 hits were retrieved about TB misdiagnosis [7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28], including 1 summary analysis and 22 case reports. Half of 22 patients were young adults, with average age under 40. To our interest, none of these 22 patients had underlying diseases at admission except 2 with oncology history, 1 with familial Mediterranean fever, and 1 just subjected to kidney transplantation. It’s noted that 15 (68.2%) of the 22 cases involved in single organ, with lung the most involved organ (54.5%). Of the 22 cases, 19 (86.4%) were confirmed by invasive examination, like biopsy of the lesion. In summary, the clinical manifestations of some TB cases are non-specific, which are most likely misdiagnosed as tumor.
Differences of pulmonary modules between lung metastasis and HDTB
Pulmonary nodules refer to the round intrapulmonary lesions with less than 3 cm in diameter [29]. Multiple nodules in the lung are one of the most common clinical imaging presentations, which appear in a variety of diseases, such as lymphangitis carcinomatosa, silicosis, and bronchioloalveolar carcinoma [30]. In particular, multiple small pulmonary nodules are frequently observed in both lung metastasis and HDTB [31, 32]. Besides, some chronic inflammation and unusual lymphoma involving in the lungs, could also display multiple pulmonary nodules [33]. The imaging manifestations of those diseases are so similar that a definite diagnosis is difficult to make [34]. The differences of nodule characteristics between lung metastasis and HDTB are summarized in Table 1. In our case, lung CT showed multiple round nodules of different size, with clear boundaries and partial fusion. Abdominal CT showed slight dilatation of intrahepatic bile duct and pancreas, enlargement of pancreatic head, multiple low-density foci in spleen.
Full size table
Nonspecificity of CA19-9
CA19-9 level was significantly higher than normal, and progressively increased. It is known that, CA19-9 is synthesized by pancreatic and biliary ductal cells, as well as gastric, colon, endometrial and salivary epithelia. Only small amount of CA19-9 is present in serum [39]. CA19-9 is considered as the marker for pancreatic cancer in clinical practice. However, this indicator has the disadvantage of low specificity [39, 40]. Overexpression of CA19-9 was observed in several benign gastrointestinal disorders, which may be relevant to glycan mediated cell-cell interactions in mucosal immunity [40]. Additionally, higher level of CA19-9 was found in the pancreatic tuberculosis [41, 42]. In our case, sharply increased CA19-9 also played a role of misleading.
Clues to make definite diagnosis
When we looked into these symptoms with comprehensive dynamic analysis, we found that this patient had anemia and his white blood cells was not high, indicating that he was in the course of chronic infection (our clinical experience). There were multiple pulmonary nodules, most of which distributed along with the bronchovascular bundle. Some nodules were not very regular. Pulmonary nodules in the upper lung showed a trend of enlargement, fusion and infiltration. In addition, signs of fibrous hyperplasia such as strips and long burrs appeared in the process of evolution (Fig. 1C). We gradually thought it was more likely to be inflammatory granuloma lesions, instead of malignant tumor. At the other hand, abdominal CT suggested thickening of the gallbladder wall and uniform thickening of the upper-end wall of the common bile duct. Although the head of the pancreas was enlarged, it still had regular shape, clear boundary, and consistent enhancement with the whole pancreas body. All these signs also suggested chronic inflammation. Additionally, in this case, the maximum standard uptake value (SUVmax) of PET CT imaging for pulmonary nodules was 7.86, located between 2.65 and 10.9, which probably indicated benign lesions. The value of PET CT in evaluating the efficacy of TB treatment, especially extrapulmonary TB, has been widely recognized [23]. Unfortunately, given its high cost, it cannot be widely used in China at present. The patient also refused to accept re-examination by PET CT for this reason. Otherwise, the effect of individualized chemotherapy regimen can be better evaluated through the changes in pathological metabolism. Finally, puncture biopsy of lung confirmed pulmonary TB. Through anti-TB treatment, the patient was cure, which in turn supported our diagnosis.
Conclusions
The patient turned out to be atypical systemic HDTB, not cancer at all. Such atypical HDTB was relatively rare in clinical practice. We encouraged clinicians to keep dynamic thinking of the disease in mind and know more special signs of rare diseases.
Availability of data and materials
Data relating to this study are contained and presented in this document. Other materials are available from the corresponding authors on reasonable request.
Abbreviations
- TB:
-
Tuberculosis
- MTB:
-
Mycobacterium tuberculosis
- HDTB:
-
Hematogenous disseminated TB
- CT:
-
Computerized tomography
- AFB:
-
Acid-fast bacilli
- 18F-FDG-PET:
-
18F-fluorodeoxyglucose positron-emission tomography
- QD:
-
Once a day
References
-
World Health Organization. Global tuberculosis report 2019. Geneva: World Health Organization. 2019, Licence: CC BY-NC-SA 3.0 IGO.
-
Fijołek J, Wiatr E, Polubiec-Kownacka M, Błasińska-Przerwa K, Szołkowska M, Szczepulska-Wójcik E, et al. Pulmonary tuberculosis mimicking lung cancer progression after 10 years of cancer remission. Adv Respir Med. 2018;86(2):92–6. https://doi.org/10.5603/ARM.2018.0012.
Article
PubMedGoogle Scholar
-
Ko Y, Mo E-K, Park YB, Kang M-R, Bae JS, Kim Y. Miliary Tuberculosis mimicking brain metastasis from renal cell carcinoma. J Neurocrit Care. 2018;11(1):47–53. https://doi.org/10.18700/jnc.180045.
-
Lang S, Sun J, Wang X, Xiao Y, Wang J, Zhang M, et al. Asymptomatic pulmonary tuberculosis mimicking lung cancer on imaging: a retrospective study. Exp Ther Med. 2017;14(3):2180–8. https://doi.org/10.3892/etm.2017.4737.
Article
PubMed
PubMed CentralGoogle Scholar
-
Singh VK, Chandra S, Kumar S, Pangtey G, Mohan A, Guleria R. A common medical error: lung cancer misdiagnosed as sputum negative tuberculosis. Asian Pac J Cancer Prev. 2009;10(3):335–8. 19640168.
-
Vaghasiya K, Sharma A, Verma R. Misdiagnosis murder: Disguised TB or lung cancer? Pulmon Res Respir Med. 2016;3:e5-6. https://doi.org/10.17140/PRRMOJ-3-e006.
-
Chamberlin K, Orfanos S, Mukherjee A, Moy E, Koganti M, Khan W. A case of disseminated tuberculosis mimicking metastatic cancer. Respir Med Case Rep. 2018;25:239–41. https://doi.org/10.1016/j.rmcr.2018.10.001.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Morikawa K, Misumi S, Fukuda T. A case of pulmonary tuberculosis with multiple nodules mimicking lung metastases. BJR Case Rep. 2019;5(3):20180124. https://doi.org/10.1259/bjrcr.20180124.
Article
PubMed
PubMed CentralGoogle Scholar
-
Kawaratani H, Moriya K, Ishida K, Noguchi R, Namisaki T, Takaya H, et al. Cecal tuberculosis mimicking submucosal tumor. Cecal tuberculosis mimicking submucosal tumor. Intern Med. 2016;55(14):1859–63. https://doi.org/10.2169/internalmedicine.55.5139.
Article
PubMedGoogle Scholar
-
Pintos-Pascual I. Cervix tuberculosis simulating cancer. Cecal tuberculosis mimicking submucosal tumor. Intern Med. 2016;55(14):1859–63. https://doi.org/10.2169/internalmedicine.55.5139.
Article
Google Scholar
-
Ciftci F, Shimbori N, Karnak D. Concurrent central nervous system and endobronchial tuberculosis mimicking a metastatic lung cancer. Clin Respir J. 2017;11(1):98–102. https://doi.org/10.1111/crj.12311.
Article
PubMedGoogle Scholar
-
Ando M, Mukai Y, Ushijima RI, Shioyama Y, Umeki K, Okada F, et al. Disseminated mycobacterium tuberculosis infection masquerading as metastasis after heavy ion radiotherapy for prostate Cancer. Intern Med. 2016;55(22):3387–92. https://doi.org/10.2169/internalmedicine.55.7039.
Article
PubMed
PubMed CentralGoogle Scholar
-
Voit FM, Abdelhafez M, Rothe K, Slotta-Huspenina J, Gaa J, Schmid RM, et al. Disseminated tuberculosis mimicking metastatic gastric cancer-a case report. Z Gastroenterol. 2019;57(12):1487–92. https://doi.org/10.1055/a-1030-4781.
Article
PubMedGoogle Scholar
-
Hajjar W, Ahmed I, Aljetaily S, Al-Obaidan T, Hajjar AW. Endobronchial tuberculosis simulating carcinoid tumor. J Coll Physicians Surg Pak. 2018;28(3):S39-41. https://doi.org/10.29271/jcpsp.2018.03.S39.
-
Di Giovanni SE, Cunha TM, Duarte AL, Alves I. Endometrial tuberculosis simulating an ovarian cancer: a case report. Acta Med Port. 2016;29(6):412–5. https://doi.org/10.20344/amp.7706.
-
Wang H, Qu X, Liu X, Ding L, Yue Y. Female peritoneal tuberculosis with ascites, pelvic mass, or elevated CA 125 mimicking advanced ovarian cancer: A retrospective study of 26 cases. J Coll Physicians Surg Pak. 2019;29(6):588–9. https://doi.org/10.29271/jcpsp.2019.06.588.
-
Gera K, Kishore N. Image diagnosis. Endobronchial tuberculosis masquerading as an Endobronchial tumor with presentation as middle lobe syndrome. Perm J. 2017;21:16–006. https://doi.org/10.7812/TPP/16-006.
Article
PubMedGoogle Scholar
-
Sassalos TM, Rao RC, Demirci H. Ocular tuberculosis masquerading as a tumor. Lancet Infect Dis. 2018;18(8):924. https://doi.org/10.1016/S1473-3099(18)30123-3.
Article
PubMed
PubMed CentralGoogle Scholar
-
Daoudi M, Herrak L, Ftouh ME, Achachi L. [Pseudotumoral bronchopulmonary tuberculosis mimicking cancer in an immunocompetent patient]. Pan Afr Med J. 2019;32:170. doi:https://doi.org/10.11604/pamj.2019.32.170.18129.
-
Moukit M, Fadel FA, Kouach J, Babahabib A, Dehayni M, Rahali DM. Pseudo-tumoral peritoneal tuberculosis mimicking ovarian cancer: an important differential diagnosis to consider. Pan Afr Med J. 2016;25:193. https://doi.org/10.11604/pamj.2016.25.193.10929.
-
Pilaniya V, Gera K, Kunal S, Shah A. Pulmonary tuberculosis masquerading as metastatic lung disease. Eur Respir Rev. 2016;25(139):97–8. https://doi.org/10.1183/16000617.00002315.
Article
PubMedGoogle Scholar
-
Nowakowska-Arendt A, Jagiełło G. Pulmonary tuberculosis mimicking numerous lung metastases—a case study. Med Res J. 2018;3(1):43–6. https://doi.org/10.5603/MRJ.2018.0008.
-
Yates JA, Collis OA, Sueblinvong T, Collis TK. Red snappers and red herrings: pelvic tuberculosis causing elevated CA 125 and mimicking advanced ovarian cancer. A case report and literature review. Hawaii J Med Public Health. 2017;76(8):220–4. 28808611.
PubMed
PubMed CentralGoogle Scholar
-
Schmidt-Lauber C, Jacobi J, Polifka I, Hilgers KF, Wiesener MS. Suspected colonic cancer turns out to be disseminated tuberculosis in a kidney transplant recipient: a case report. Medicine (Baltimore). 2019;98(36):e16995. https://doi.org/10.1097/MD.0000000000016995.
Article
Google Scholar
-
Lan C-C, Wu C-W, Wu Y-K. Systemic tuberculosis mimicking lung Cancer with multiple metastases. Am J Med Sci. 2020;359(3):186–7. https://doi.org/10.1016/j.amjms.2019.09.006.
Article
PubMedGoogle Scholar
-
Rodpenpear N. Tuberculosis of cervix resembling cervical Cancer. J Med Assoc Thail. 2016;99(Suppl 8):S249–52. 29906057.
Google Scholar
-
Vamsi Krishna S, Mallikarjunaswamy B, Issac T, Srinivasalu S. Tuberculosis of knee joint mimicking giant cell tumor-a case report. Indian J Tuberc. 2018;65(3):260–1. https://doi.org/10.1016/j.ijtb.2016.09.021.
Article
PubMedGoogle Scholar
-
Sellami M, Mnejja M, Charfi S, Ghorbel A. Tuberculosis of the tonsil simulating a cancer. Lancet Infect Dis. 2017;17(12):1317. https://doi.org/10.1016/S1473-3099(17)30315-8.
Article
PubMedGoogle Scholar
-
Setio AAA, Traverso A, De Bel T, Berens MS, van den Bogaard C, Cerello P, et al. Validation, comparison, and combination of algorithms for automatic detection of pulmonary nodules in computed tomography images: the LUNA16 challenge. Med Image Anal. 2017;42:1–13. https://doi.org/10.1016/j.media.2017.06.015.
Article
PubMedGoogle Scholar
-
MacMahon H, Naidich DP, Goo JM, Lee KS, Leung ANC, Mayo JR, et al. Guidelines for management of incidental pulmonary nodules detected on CT images: from the Fleischner society 2017. Radiology. 2017;284(1):228–43. https://doi.org/10.1148/radiol.2017161659.
-
Dursun P, Ersoz S, Gultekin M, Aksan G, Yüce K. Ayhan A. Disseminated peritoneal tuberculosis mimicking advanced-stage endodermal sinus tumor: a case report. 2006;16(Suppl 1):303–7. https://doi.org/10.1111/j.1525-1438.2006.00205.x.
Article
Google Scholar
-
Falagas M, Kouranos V, Athanassa Z, Kopterides P. Tuberculosis and malignancy. QJM. 2010;103(7):461–87. https://doi.org/10.1093/qjmed/hcq068.
Article
CAS
PubMedGoogle Scholar
-
Denning DW, Page ID, Chakaya J, Jabeen K, Jude CM, Cornet M, et al. Case definition of chronic pulmonary aspergillosis in resource-constrained settings. Emerg Infect Dis. 2018;24(8):e171312. https://doi.org/10.3201/eid2408.171312.
Article
PubMed CentralGoogle Scholar
-
Onuigbo WI. Some nineteenth century ideas on links between tuberculous and cancerous diseases of the lung. Br J Dis Chest. 1975;69:207–10. https://doi.org/10.1016/0007-0971(75)90081-9.
Article
CAS
PubMedGoogle Scholar
-
Aquino SL. Imaging of metastatic disease to the thorax. Radiol Clin N Am. 2005;43(3):481–95. https://doi.org/10.1016/j.rcl.2005.02.006.
Article
PubMedGoogle Scholar
-
Kawaguchi K, Taniguchi T, Fukui T, Nakamura S, Yokoi K. Radiological findings and surgical outcomes of pulmonary metastases originating from biliary tract carcinoma. Gen Thorac Cardiovasc Surg. 2019;67(11):962–8. https://doi.org/10.1007/s11748-019-01122-6.
Article
PubMedGoogle Scholar
-
Khan F. Review of literature on disseminated tuberculosis with emphasis on the focused diagnostic workup. J Family Community Med. 2019;26(2):83–91. https://doi.org/10.4103/jfcm.JFCM_106_18.
Article
PubMed
PubMed CentralGoogle Scholar
-
Chierakul N, Boonsuk J, Muangman N, Totanarungroj K. Radiographic features for predicting smear-negative pulmonary tuberculosis. J Med Assoc Thail. 2016;99(6):697–701.
Google Scholar
-
Scarà S, Bottoni P, Scatena R. CA 19-9: biochemical and clinical aspects. Adv Exp Med Biol. 2015;867:247–60. https://doi.org/10.1007/978-94-017-7215-0_15.
Article
CAS
PubMedGoogle Scholar
-
Pavai S, Yap S. The clinical significance of elevated levels of serum CA 19-9. Med J Malaysia. 2003;58(5):667–72.
CAS
PubMedGoogle Scholar
-
Bhatia V, Garg PK, Arora VK, Sharma R. Isolated pancreatic tuberculosis mimicking intraductal pancreatic mucinous tumor. Gastrointest Endosc. 2008;68(3):610–1. https://doi.org/10.1016/j.gie.2007.12.022.
Article
PubMedGoogle Scholar
-
Yang Y-J, Li Y-X, Liu X-Q, Yang M, Liu K. Pancreatic tuberculosis mimicking pancreatic carcinoma during anti-tuberculosis therapy: A case report. World J Clin Cases. 2014;2(5):167–169. doi: https://doi.org/10.12998/wjcc.v2.i5.167.
Download references
Acknowledgements
Not applicable.
Funding
This work was supported by Natural Science Foundation of Jiangsu province (Grant No. BK20170133) and social development project of key research and development plan of Jiangsu province (Grant No. BE2018606).
Author information
Authors and Affiliations
-
Department of Tuberculosis, the Second Hospital of Nanjing, Nanjing University of Chinese Medicine, 1-1 Zhongfu Road, Gulou District, Nanjing, Jiangsu Province, 210003, China
Tian-Xing Hang, Gang Fang, Yan Huang & Chun-Mei Hu
-
Clinical Research Center, the Second Hospital of Nanjing, Nanjing University of Chinese Medicine, 1-1 Zhongfu Road, Gulou District, Nanjing, Jiangsu Province, 210003, China
Wei Chen
Authors
- Tian-Xing Hang
You can also search for this author in
PubMed Google Scholar - Gang Fang
You can also search for this author in
PubMed Google Scholar - Yan Huang
You can also search for this author in
PubMed Google Scholar - Chun-Mei Hu
You can also search for this author in
PubMed Google Scholar - Wei Chen
You can also search for this author in
PubMed Google Scholar
Contributions
TXH and GF conducted the literature review and wrote the draft. YH collected clinical data. CMH and WC conceived the study and revised the manuscript. The author(s) read and approved the final manuscript.
Corresponding authors
Correspondence to
Chun-Mei Hu or Wei Chen.
Ethics declarations
Ethics approval and consent to participate
Written consent was exempted by the institutional review boards of the Second Hospital of Nanjing, since no identifying images or other personal information were included.
Consent for publication
All authors have read and approved the manuscript.
Competing interests
The authors declare that they have no competing interests.
Rights and permissions
Open Access This article is licensed under a Creative Commons Attribution 4.0 International License, which permits use, sharing, adaptation, distribution and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons licence, and indicate if changes were made. The images or other third party material in this article are included in the article’s Creative Commons licence, unless indicated otherwise in a credit line to the material. If material is not included in the article’s Creative Commons licence and your intended use is not permitted by statutory regulation or exceeds the permitted use, you will need to obtain permission directly from the copyright holder. To view a copy of this licence, visit http://creativecommons.org/licenses/by/4.0/. The Creative Commons Public Domain Dedication waiver (http://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated in a credit line to the data.
Reprints and Permissions
About this article
Cite this article
Hang, TX., Fang, G., Huang, Y. et al. Misdiagnosis of a multi-organ involvement hematogenous disseminated tuberculosis as metastasis: a case report and literature review.
Infect Dis Poverty 9, 66 (2020). https://doi.org/10.1186/s40249-020-00681-8
Download citation
-
Received: 24 February 2020
-
Accepted: 26 May 2020
-
Published: 09 June 2020
-
DOI: https://doi.org/10.1186/s40249-020-00681-8
Keywords
- Misdiagnosis
- Hematogenous disseminated tuberculosis
- Metastasis
- Pulmonary nodule
- Case Report
- Open Access
- Published: 09 June 2020
Infectious Diseases of Poverty
volume 9, Article number: 66 (2020)
Cite this article
-
2749 Accesses
-
8 Citations
-
Metrics details
Abstract
Background
Tuberculosis (TB) is a great mimicker and diagnostic chameleon, and prone to be diagnosed as malignancy. Even though many reports have described the differences between pulmonary TB and lung cancer, the atypical systemic hematogenous disseminated TB (HDTB) is very rare and more confusing in clinical practice.
Case presentation
A 73-year-old man, HIV-negative, was hospitalized to the local county hospital because of chest pain, low-grade fever, asthenia, anorexia and weight loss for the pasting two months. The CT findings of the two lungs showed multiple round or round-like nodules of different sizes, with clear boundaries and partial fusion. The level of serum CA19–9 was significantly higher than normal, and progressively increased. There were multiple enlarged lymph nodes in the neck, mediastinum, abdominal cavity and pelvic cavity. The symptoms were diagnosed as hematogenous spread of gastrointestinal tumor in the local county hospital. However, when transferred to our provincial hospital, through comprehensive dynamic analysis, this patient was diagnosed as atypical systemic HDTB, no cancer at all. Through routine anti-TB therapy for one year, the patient was recovered very well at the follow-up of half year after withdrawal.
Conclusions
In the past, most TB misdiagnosis cases involved in single organ and were finally confirmed through invasive examination. This case enriched clinical experiences in the diagnosis of atypical HDTB. We encouraged clinicians to establish a dynamic thinking for diagnosis and treatment and emphasized the value of biopsy and 18F-FDG-PET in distinguishing TB and cancer.
Background
Tuberculosis (TB) is a huge threat for public health in China, which is within the “high-burden country” list [1]. Even though enormous effort has been taken, treatment and control of TB still face many challenges. Detection and diagnosis of Mycobacterium tuberculosis (MTB) is difficult in most case. What’s worse, TB is a great mimicker and diagnostic chameleon, and prone to be diagnosed as malignancy, and vice-versa, because the radiographic characteristics and clinical symptoms of the two diseases are very similar [2,3,4,5]. Since cancer usually has worse prognosis and costs more medical resources compared with TB, misdiagnosis surely increases much more psychological stress and economical burden to the real TB patients. Furthermore, treatment strategy is totally different between neoplasm and TB. In such case, clinicians are placed into a dilemma to make a definite diagnosis, and are even at risk to become a “misdiagnosis murder” [6]. Thus, it’s pivotal to describe and summarize the nuances between neoplasm and TB through more case reports. Here, we described a very unusual case that a 73-year-old immunocompetent man with hematogenous disseminated TB (HDTB) was misdiagnosed as metastasis with multiple organs involvement.
Case presentation
Lung metastasis
On 7 March, 2018, a 73-year-old man, HIV-negative, was hospitalized to the local county hospital for 2-month chest pain, low-grade fever, asthenia, anorexia and weight loss. The patient had history of type II diabetes mellitus with regular administration of gliclazide, but efficacy was poor. Physical examination revealed body temperature 36.7 °C, pulse rate 96 beats/min, blood pressure 133/83 mmHg, respiratory rate 20/min, oxygen saturation 96% and mildly yellow skin and sclera. Respiratory system, cardiovascular system, neurological system and abdomen were normal. Laboratory examination showed anemia (hemoglobin 114 g/L), abnormal liver function (alanine aminotransferase 57 U/L, aspartate aminotransferase 48 U/L, γ-glutamyl transpeptidase 818 U/L, alkaline phosphatase 671 U/L, total bilirubin 44 μmol/L) and elevated cancer antigen 19-9 (CA19-9, 165 U/ml). The interferon-γ release assay test was negative. The skull computerized tomography (CT) showed lacunar infarction in bilateral basal ganglia. The thorax CT revealed multiple round or round-like nodules with variable sizes scattered throughout both lungs, suggestive of metastatic lung disease (Fig. 1A). Abdominal enhancement CT showed that a mass at the pancreatic head was obviously strengthened in the arterial phase, and the pancreatic duct and intrahepatic bile duct was slightly dilated (Fig. 2). Taken together, all examination results were strongly suspected of lung metastasis, which was originated from the pancreatic head or intestinal origin. However, TB infection could not be excluded completely. The patient denied further biopsy, and chose to accept experimental anti-TB therapy with rifampin and isoniazid. After one month, chest CT showed that lung lesions were not absorbed. Laboratory test showed that CA19-9 sharply increased, up to 1167 U/ml. Sputum smear for acid-fast bacilli (AFB) was negative. The doctors in the local county hospital excluded TB infection and proposed gastrointestinal malignant tumors combined with lung metastasis. The patient family was in deep sorrow and prepared to give up.

Thorax CT scan at different time points displayed evolution of lesions. a At admission, the thorax CT revealed multiple round or round-like nodules with variable size scattered throughout both lungs. b Development and evolution of lung lesions. The lung CT scan showed that pulmonary nodules gradually evolved with signs of fibrous tissue hyperplasia, such as cords, long burrs and fusion. c After four months of anti-TB treatment, thorax CT scan showed obvious absorbance of the lung lesions
Full size image

Abdominal enhancement CT suggested lesions in the intestinal tract. a There was a mass at the pancreatic head, indicated by arrow. b Intrahepatic bile duct was dilated, indicated by arrow. c The gallbladder wall (left arrow) and the wall of the upper end of the common bile duct (right arrow) were thicken
Full size image
Hematogenous disseminated TB
On 7 May, 2018, his daughter persuaded the patient to the provincial hospital for further diagnosis. Laboratory examination revealed hyperbilirubinemia (total bilirubin 70 μmol/L), CA19-9 832 U/ml, cancer antigen 125 141 U/ml, neuron-specific enolase 22.98 ng/ml, angiotensin-converting enzyme 178 U/L and serum (1,3)-β-D-glucan 235 pg/ml. 18F-fluorodeoxyglucose positron-emission tomography (18F-FDG-PET) scan showed focal high uptake in the multiple organs, including lung, liver, pancreas, spleen, gallbladder neck (Fig. 3), which suggested benign disease (especially TB). The patient accepted the endoscopic retrograde cholangiopancreatography to relieve hyperbilirubinemia, which was caused by bile duct obstruction. Biopsy from brushed biliary cell indicated no malignant tumor. A CT scan-guided transthoracic needle biopsy of the nodule at the left upper lobe was performed and the histopathology showed coagulative necrosis combining with granulomatous inflammation. AFB staining was positive and Periodic Acid-Schiff staining was negative (Fig. 4). In the meanwhile, qPCR for MTB DNA showed 4900 copy/ml in the sputum. Thus, the diagnosis of TB infection was definite. The patient then accepted anti-TB regimen, including isoniazid (300 mg/once a day [QD]), rifampicin (450 mg/QD), ethambutol (750 mg/QD), pyrazinamide (1500 mg/QD), levofloxacin (600 mg/QD) for three months, followed by isoniazid (300 mg/QD) and rifampicin (450 mg/QD) for another nine months.

FDG-PET showed high uptake at different foci. a Foci in the whole body were defined by a circle. The yellow bright spots represented high uptake of 18F-FDG by local tissues. The maximum standard uptake value in different organs were shown, including lung (b, 7.86), liver (c, 5.98), gallbladder neck (d, 11.04), pancreatic head mass (e, 12.54)
Full size image

Puncture biopsy of left lung upper lobe revealed coagulative necrosis combined with granulomatous inflammation with hematoxylin-eosin staining (black arrow). Ziehl-Neelsen staining detected acid-fast bacilli (black circle) and Periodic Acid-Schiff staining was negative. Magnification × 200
Full size image
On 2 September, 2018, almost four months after hospitalization to our hospital, the thorax CT revealed that the lung lesions were absorbed significantly (Fig. 1B). After one year of treatment, continuous clinical and radiological improvement was observed, and the drugs were then withdrawn. The patient was asymptomatic at the follow-up of half year after withdrawal.
Discussion
Characteristics of TB misdiagnosis cases
We conducted literature search in NCBI PubMed database with keywords “tuberculosis” and “cancer” or “tumor” from 2016 to 2019. Totally, 23 hits were retrieved about TB misdiagnosis [7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28], including 1 summary analysis and 22 case reports. Half of 22 patients were young adults, with average age under 40. To our interest, none of these 22 patients had underlying diseases at admission except 2 with oncology history, 1 with familial Mediterranean fever, and 1 just subjected to kidney transplantation. It’s noted that 15 (68.2%) of the 22 cases involved in single organ, with lung the most involved organ (54.5%). Of the 22 cases, 19 (86.4%) were confirmed by invasive examination, like biopsy of the lesion. In summary, the clinical manifestations of some TB cases are non-specific, which are most likely misdiagnosed as tumor.
Differences of pulmonary modules between lung metastasis and HDTB
Pulmonary nodules refer to the round intrapulmonary lesions with less than 3 cm in diameter [29]. Multiple nodules in the lung are one of the most common clinical imaging presentations, which appear in a variety of diseases, such as lymphangitis carcinomatosa, silicosis, and bronchioloalveolar carcinoma [30]. In particular, multiple small pulmonary nodules are frequently observed in both lung metastasis and HDTB [31, 32]. Besides, some chronic inflammation and unusual lymphoma involving in the lungs, could also display multiple pulmonary nodules [33]. The imaging manifestations of those diseases are so similar that a definite diagnosis is difficult to make [34]. The differences of nodule characteristics between lung metastasis and HDTB are summarized in Table 1. In our case, lung CT showed multiple round nodules of different size, with clear boundaries and partial fusion. Abdominal CT showed slight dilatation of intrahepatic bile duct and pancreas, enlargement of pancreatic head, multiple low-density foci in spleen.
Full size table
Nonspecificity of CA19-9
CA19-9 level was significantly higher than normal, and progressively increased. It is known that, CA19-9 is synthesized by pancreatic and biliary ductal cells, as well as gastric, colon, endometrial and salivary epithelia. Only small amount of CA19-9 is present in serum [39]. CA19-9 is considered as the marker for pancreatic cancer in clinical practice. However, this indicator has the disadvantage of low specificity [39, 40]. Overexpression of CA19-9 was observed in several benign gastrointestinal disorders, which may be relevant to glycan mediated cell-cell interactions in mucosal immunity [40]. Additionally, higher level of CA19-9 was found in the pancreatic tuberculosis [41, 42]. In our case, sharply increased CA19-9 also played a role of misleading.
Clues to make definite diagnosis
When we looked into these symptoms with comprehensive dynamic analysis, we found that this patient had anemia and his white blood cells was not high, indicating that he was in the course of chronic infection (our clinical experience). There were multiple pulmonary nodules, most of which distributed along with the bronchovascular bundle. Some nodules were not very regular. Pulmonary nodules in the upper lung showed a trend of enlargement, fusion and infiltration. In addition, signs of fibrous hyperplasia such as strips and long burrs appeared in the process of evolution (Fig. 1C). We gradually thought it was more likely to be inflammatory granuloma lesions, instead of malignant tumor. At the other hand, abdominal CT suggested thickening of the gallbladder wall and uniform thickening of the upper-end wall of the common bile duct. Although the head of the pancreas was enlarged, it still had regular shape, clear boundary, and consistent enhancement with the whole pancreas body. All these signs also suggested chronic inflammation. Additionally, in this case, the maximum standard uptake value (SUVmax) of PET CT imaging for pulmonary nodules was 7.86, located between 2.65 and 10.9, which probably indicated benign lesions. The value of PET CT in evaluating the efficacy of TB treatment, especially extrapulmonary TB, has been widely recognized [23]. Unfortunately, given its high cost, it cannot be widely used in China at present. The patient also refused to accept re-examination by PET CT for this reason. Otherwise, the effect of individualized chemotherapy regimen can be better evaluated through the changes in pathological metabolism. Finally, puncture biopsy of lung confirmed pulmonary TB. Through anti-TB treatment, the patient was cure, which in turn supported our diagnosis.
Conclusions
The patient turned out to be atypical systemic HDTB, not cancer at all. Such atypical HDTB was relatively rare in clinical practice. We encouraged clinicians to keep dynamic thinking of the disease in mind and know more special signs of rare diseases.
Availability of data and materials
Data relating to this study are contained and presented in this document. Other materials are available from the corresponding authors on reasonable request.
Abbreviations
- TB:
-
Tuberculosis
- MTB:
-
Mycobacterium tuberculosis
- HDTB:
-
Hematogenous disseminated TB
- CT:
-
Computerized tomography
- AFB:
-
Acid-fast bacilli
- 18F-FDG-PET:
-
18F-fluorodeoxyglucose positron-emission tomography
- QD:
-
Once a day
References
-
World Health Organization. Global tuberculosis report 2019. Geneva: World Health Organization. 2019, Licence: CC BY-NC-SA 3.0 IGO.
-
Fijołek J, Wiatr E, Polubiec-Kownacka M, Błasińska-Przerwa K, Szołkowska M, Szczepulska-Wójcik E, et al. Pulmonary tuberculosis mimicking lung cancer progression after 10 years of cancer remission. Adv Respir Med. 2018;86(2):92–6. https://doi.org/10.5603/ARM.2018.0012.
Article
PubMedGoogle Scholar
-
Ko Y, Mo E-K, Park YB, Kang M-R, Bae JS, Kim Y. Miliary Tuberculosis mimicking brain metastasis from renal cell carcinoma. J Neurocrit Care. 2018;11(1):47–53. https://doi.org/10.18700/jnc.180045.
-
Lang S, Sun J, Wang X, Xiao Y, Wang J, Zhang M, et al. Asymptomatic pulmonary tuberculosis mimicking lung cancer on imaging: a retrospective study. Exp Ther Med. 2017;14(3):2180–8. https://doi.org/10.3892/etm.2017.4737.
Article
PubMed
PubMed CentralGoogle Scholar
-
Singh VK, Chandra S, Kumar S, Pangtey G, Mohan A, Guleria R. A common medical error: lung cancer misdiagnosed as sputum negative tuberculosis. Asian Pac J Cancer Prev. 2009;10(3):335–8. 19640168.
-
Vaghasiya K, Sharma A, Verma R. Misdiagnosis murder: Disguised TB or lung cancer? Pulmon Res Respir Med. 2016;3:e5-6. https://doi.org/10.17140/PRRMOJ-3-e006.
-
Chamberlin K, Orfanos S, Mukherjee A, Moy E, Koganti M, Khan W. A case of disseminated tuberculosis mimicking metastatic cancer. Respir Med Case Rep. 2018;25:239–41. https://doi.org/10.1016/j.rmcr.2018.10.001.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Morikawa K, Misumi S, Fukuda T. A case of pulmonary tuberculosis with multiple nodules mimicking lung metastases. BJR Case Rep. 2019;5(3):20180124. https://doi.org/10.1259/bjrcr.20180124.
Article
PubMed
PubMed CentralGoogle Scholar
-
Kawaratani H, Moriya K, Ishida K, Noguchi R, Namisaki T, Takaya H, et al. Cecal tuberculosis mimicking submucosal tumor. Cecal tuberculosis mimicking submucosal tumor. Intern Med. 2016;55(14):1859–63. https://doi.org/10.2169/internalmedicine.55.5139.
Article
PubMedGoogle Scholar
-
Pintos-Pascual I. Cervix tuberculosis simulating cancer. Cecal tuberculosis mimicking submucosal tumor. Intern Med. 2016;55(14):1859–63. https://doi.org/10.2169/internalmedicine.55.5139.
Article
Google Scholar
-
Ciftci F, Shimbori N, Karnak D. Concurrent central nervous system and endobronchial tuberculosis mimicking a metastatic lung cancer. Clin Respir J. 2017;11(1):98–102. https://doi.org/10.1111/crj.12311.
Article
PubMedGoogle Scholar
-
Ando M, Mukai Y, Ushijima RI, Shioyama Y, Umeki K, Okada F, et al. Disseminated mycobacterium tuberculosis infection masquerading as metastasis after heavy ion radiotherapy for prostate Cancer. Intern Med. 2016;55(22):3387–92. https://doi.org/10.2169/internalmedicine.55.7039.
Article
PubMed
PubMed CentralGoogle Scholar
-
Voit FM, Abdelhafez M, Rothe K, Slotta-Huspenina J, Gaa J, Schmid RM, et al. Disseminated tuberculosis mimicking metastatic gastric cancer-a case report. Z Gastroenterol. 2019;57(12):1487–92. https://doi.org/10.1055/a-1030-4781.
Article
PubMedGoogle Scholar
-
Hajjar W, Ahmed I, Aljetaily S, Al-Obaidan T, Hajjar AW. Endobronchial tuberculosis simulating carcinoid tumor. J Coll Physicians Surg Pak. 2018;28(3):S39-41. https://doi.org/10.29271/jcpsp.2018.03.S39.
-
Di Giovanni SE, Cunha TM, Duarte AL, Alves I. Endometrial tuberculosis simulating an ovarian cancer: a case report. Acta Med Port. 2016;29(6):412–5. https://doi.org/10.20344/amp.7706.
-
Wang H, Qu X, Liu X, Ding L, Yue Y. Female peritoneal tuberculosis with ascites, pelvic mass, or elevated CA 125 mimicking advanced ovarian cancer: A retrospective study of 26 cases. J Coll Physicians Surg Pak. 2019;29(6):588–9. https://doi.org/10.29271/jcpsp.2019.06.588.
-
Gera K, Kishore N. Image diagnosis. Endobronchial tuberculosis masquerading as an Endobronchial tumor with presentation as middle lobe syndrome. Perm J. 2017;21:16–006. https://doi.org/10.7812/TPP/16-006.
Article
PubMedGoogle Scholar
-
Sassalos TM, Rao RC, Demirci H. Ocular tuberculosis masquerading as a tumor. Lancet Infect Dis. 2018;18(8):924. https://doi.org/10.1016/S1473-3099(18)30123-3.
Article
PubMed
PubMed CentralGoogle Scholar
-
Daoudi M, Herrak L, Ftouh ME, Achachi L. [Pseudotumoral bronchopulmonary tuberculosis mimicking cancer in an immunocompetent patient]. Pan Afr Med J. 2019;32:170. doi:https://doi.org/10.11604/pamj.2019.32.170.18129.
-
Moukit M, Fadel FA, Kouach J, Babahabib A, Dehayni M, Rahali DM. Pseudo-tumoral peritoneal tuberculosis mimicking ovarian cancer: an important differential diagnosis to consider. Pan Afr Med J. 2016;25:193. https://doi.org/10.11604/pamj.2016.25.193.10929.
-
Pilaniya V, Gera K, Kunal S, Shah A. Pulmonary tuberculosis masquerading as metastatic lung disease. Eur Respir Rev. 2016;25(139):97–8. https://doi.org/10.1183/16000617.00002315.
Article
PubMedGoogle Scholar
-
Nowakowska-Arendt A, Jagiełło G. Pulmonary tuberculosis mimicking numerous lung metastases—a case study. Med Res J. 2018;3(1):43–6. https://doi.org/10.5603/MRJ.2018.0008.
-
Yates JA, Collis OA, Sueblinvong T, Collis TK. Red snappers and red herrings: pelvic tuberculosis causing elevated CA 125 and mimicking advanced ovarian cancer. A case report and literature review. Hawaii J Med Public Health. 2017;76(8):220–4. 28808611.
PubMed
PubMed CentralGoogle Scholar
-
Schmidt-Lauber C, Jacobi J, Polifka I, Hilgers KF, Wiesener MS. Suspected colonic cancer turns out to be disseminated tuberculosis in a kidney transplant recipient: a case report. Medicine (Baltimore). 2019;98(36):e16995. https://doi.org/10.1097/MD.0000000000016995.
Article
Google Scholar
-
Lan C-C, Wu C-W, Wu Y-K. Systemic tuberculosis mimicking lung Cancer with multiple metastases. Am J Med Sci. 2020;359(3):186–7. https://doi.org/10.1016/j.amjms.2019.09.006.
Article
PubMedGoogle Scholar
-
Rodpenpear N. Tuberculosis of cervix resembling cervical Cancer. J Med Assoc Thail. 2016;99(Suppl 8):S249–52. 29906057.
Google Scholar
-
Vamsi Krishna S, Mallikarjunaswamy B, Issac T, Srinivasalu S. Tuberculosis of knee joint mimicking giant cell tumor-a case report. Indian J Tuberc. 2018;65(3):260–1. https://doi.org/10.1016/j.ijtb.2016.09.021.
Article
PubMedGoogle Scholar
-
Sellami M, Mnejja M, Charfi S, Ghorbel A. Tuberculosis of the tonsil simulating a cancer. Lancet Infect Dis. 2017;17(12):1317. https://doi.org/10.1016/S1473-3099(17)30315-8.
Article
PubMedGoogle Scholar
-
Setio AAA, Traverso A, De Bel T, Berens MS, van den Bogaard C, Cerello P, et al. Validation, comparison, and combination of algorithms for automatic detection of pulmonary nodules in computed tomography images: the LUNA16 challenge. Med Image Anal. 2017;42:1–13. https://doi.org/10.1016/j.media.2017.06.015.
Article
PubMedGoogle Scholar
-
MacMahon H, Naidich DP, Goo JM, Lee KS, Leung ANC, Mayo JR, et al. Guidelines for management of incidental pulmonary nodules detected on CT images: from the Fleischner society 2017. Radiology. 2017;284(1):228–43. https://doi.org/10.1148/radiol.2017161659.
-
Dursun P, Ersoz S, Gultekin M, Aksan G, Yüce K. Ayhan A. Disseminated peritoneal tuberculosis mimicking advanced-stage endodermal sinus tumor: a case report. 2006;16(Suppl 1):303–7. https://doi.org/10.1111/j.1525-1438.2006.00205.x.
Article
Google Scholar
-
Falagas M, Kouranos V, Athanassa Z, Kopterides P. Tuberculosis and malignancy. QJM. 2010;103(7):461–87. https://doi.org/10.1093/qjmed/hcq068.
Article
CAS
PubMedGoogle Scholar
-
Denning DW, Page ID, Chakaya J, Jabeen K, Jude CM, Cornet M, et al. Case definition of chronic pulmonary aspergillosis in resource-constrained settings. Emerg Infect Dis. 2018;24(8):e171312. https://doi.org/10.3201/eid2408.171312.
Article
PubMed CentralGoogle Scholar
-
Onuigbo WI. Some nineteenth century ideas on links between tuberculous and cancerous diseases of the lung. Br J Dis Chest. 1975;69:207–10. https://doi.org/10.1016/0007-0971(75)90081-9.
Article
CAS
PubMedGoogle Scholar
-
Aquino SL. Imaging of metastatic disease to the thorax. Radiol Clin N Am. 2005;43(3):481–95. https://doi.org/10.1016/j.rcl.2005.02.006.
Article
PubMedGoogle Scholar
-
Kawaguchi K, Taniguchi T, Fukui T, Nakamura S, Yokoi K. Radiological findings and surgical outcomes of pulmonary metastases originating from biliary tract carcinoma. Gen Thorac Cardiovasc Surg. 2019;67(11):962–8. https://doi.org/10.1007/s11748-019-01122-6.
Article
PubMedGoogle Scholar
-
Khan F. Review of literature on disseminated tuberculosis with emphasis on the focused diagnostic workup. J Family Community Med. 2019;26(2):83–91. https://doi.org/10.4103/jfcm.JFCM_106_18.
Article
PubMed
PubMed CentralGoogle Scholar
-
Chierakul N, Boonsuk J, Muangman N, Totanarungroj K. Radiographic features for predicting smear-negative pulmonary tuberculosis. J Med Assoc Thail. 2016;99(6):697–701.
Google Scholar
-
Scarà S, Bottoni P, Scatena R. CA 19-9: biochemical and clinical aspects. Adv Exp Med Biol. 2015;867:247–60. https://doi.org/10.1007/978-94-017-7215-0_15.
Article
CAS
PubMedGoogle Scholar
-
Pavai S, Yap S. The clinical significance of elevated levels of serum CA 19-9. Med J Malaysia. 2003;58(5):667–72.
CAS
PubMedGoogle Scholar
-
Bhatia V, Garg PK, Arora VK, Sharma R. Isolated pancreatic tuberculosis mimicking intraductal pancreatic mucinous tumor. Gastrointest Endosc. 2008;68(3):610–1. https://doi.org/10.1016/j.gie.2007.12.022.
Article
PubMedGoogle Scholar
-
Yang Y-J, Li Y-X, Liu X-Q, Yang M, Liu K. Pancreatic tuberculosis mimicking pancreatic carcinoma during anti-tuberculosis therapy: A case report. World J Clin Cases. 2014;2(5):167–169. doi: https://doi.org/10.12998/wjcc.v2.i5.167.
Download references
Acknowledgements
Not applicable.
Funding
This work was supported by Natural Science Foundation of Jiangsu province (Grant No. BK20170133) and social development project of key research and development plan of Jiangsu province (Grant No. BE2018606).
Author information
Authors and Affiliations
-
Department of Tuberculosis, the Second Hospital of Nanjing, Nanjing University of Chinese Medicine, 1-1 Zhongfu Road, Gulou District, Nanjing, Jiangsu Province, 210003, China
Tian-Xing Hang, Gang Fang, Yan Huang & Chun-Mei Hu
-
Clinical Research Center, the Second Hospital of Nanjing, Nanjing University of Chinese Medicine, 1-1 Zhongfu Road, Gulou District, Nanjing, Jiangsu Province, 210003, China
Wei Chen
Authors
- Tian-Xing Hang
You can also search for this author in
PubMed Google Scholar - Gang Fang
You can also search for this author in
PubMed Google Scholar - Yan Huang
You can also search for this author in
PubMed Google Scholar - Chun-Mei Hu
You can also search for this author in
PubMed Google Scholar - Wei Chen
You can also search for this author in
PubMed Google Scholar
Contributions
TXH and GF conducted the literature review and wrote the draft. YH collected clinical data. CMH and WC conceived the study and revised the manuscript. The author(s) read and approved the final manuscript.
Corresponding authors
Correspondence to
Chun-Mei Hu or Wei Chen.
Ethics declarations
Ethics approval and consent to participate
Written consent was exempted by the institutional review boards of the Second Hospital of Nanjing, since no identifying images or other personal information were included.
Consent for publication
All authors have read and approved the manuscript.
Competing interests
The authors declare that they have no competing interests.
Rights and permissions
Open Access This article is licensed under a Creative Commons Attribution 4.0 International License, which permits use, sharing, adaptation, distribution and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons licence, and indicate if changes were made. The images or other third party material in this article are included in the article’s Creative Commons licence, unless indicated otherwise in a credit line to the material. If material is not included in the article’s Creative Commons licence and your intended use is not permitted by statutory regulation or exceeds the permitted use, you will need to obtain permission directly from the copyright holder. To view a copy of this licence, visit http://creativecommons.org/licenses/by/4.0/. The Creative Commons Public Domain Dedication waiver (http://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated in a credit line to the data.
Reprints and Permissions
About this article
Cite this article
Hang, TX., Fang, G., Huang, Y. et al. Misdiagnosis of a multi-organ involvement hematogenous disseminated tuberculosis as metastasis: a case report and literature review.
Infect Dis Poverty 9, 66 (2020). https://doi.org/10.1186/s40249-020-00681-8
Download citation
-
Received: 24 February 2020
-
Accepted: 26 May 2020
-
Published: 09 June 2020
-
DOI: https://doi.org/10.1186/s40249-020-00681-8
Keywords
- Misdiagnosis
- Hematogenous disseminated tuberculosis
- Metastasis
- Pulmonary nodule
Пневмония – это воспалительное заболевание легких, которое может иметь бактериальное, вирусное или грибковое происхождение. Для подбора адекватного лечения необходимо правильно и своевременно установить диагноз.
В некоторых случаях симптомы пневмонии могут совпадать с другими заболеваниями органов дыхания, однако методы их лечения будут отличаться. В этом случае врачу необходимо провести дифференциальную диагностику для уточнения диагноза. Для получения качественного обследования рекомендуется обратиться в Юсуповскую больницу.
Таблица возбудителей
Дифференциальная диагностика пневмонии позволяет точно поставить диагноз для назначения необходимой терапии. При подборе препаратов обязательно учитывается причина развития заболевания. Ниже представлена таблица с основными возбудителями воспаления легких и как они проявляются:
|
Тип возбудителя |
Клиническая картина |
|
Пневмококки |
· острое начало; · повышение температуры тела до 38-40°С; · кашель с мокротой желтого цвета. |
|
Микоплазмы |
· постепенное начало; · першение в горле; · насморк; · анемия; · несильный кашель; · субфебрильная температура тела. |
|
Стафилококк |
· выраженный интоксикационный синдром; · одышка; · кашель; · боль в грудной клетке; · повышение температуры тела до 38-40°С; · тяжелое течение. |
|
Вирусы |
· ринит; · фарингит; · частый кашель с хрипами; · увеличение лимфатических узлов; · колебание температуры тела в течение суток. |
|
Грибки |
· кашель; · легочные кровотечения; · слабость; · мышечная боль; · колебание температуры тела. |
Дифференциальная диагностика внебольничной пневмонии
Внебольничная пневмония — заболевание, которое возникло вне лечебного учреждения (синоним: амбулаторная, домашняя). Является очень серьезной патологией легких и может закончиться летальным исходом. Поэтому важно начать лечение как можно раньше. От правильно установленного диагноза будет зависеть эффективность лечения.
Дифференциальная диагностика направлена на сравнение заболеваний по определенным критериям (симптоматика, результаты исследований) и исключение неподходящих заболеваний для получения единственно верного диагноза. При пневмонии дифференциальная диагностика поможет исключить следующие болезни:
- туберкулез;
- бронхит;
- рак.
Они имеют схожую клиническую картину в начале развития заболевания.
Дифференциальная диагностика пневмонии и туберкулеза
Наиболее часто ошибки в диагностике совершают при сравнении пневмонии и туберкулеза. Важно отличать эти два заболевания, поскольку терапевтические схемы их лечения значительно разнятся. Те методы терапии, которые дают результат при пневмонии, не будут эффективны при туберкулезе. Также большинство методов физиотерапии при пневмонии нельзя использовать при туберкулезе. Это связано с риском усугубить состояние.
Дифференциальная диагностика туберкулеза легких и пневмонии в Юсуповской больнице проводится с использованием новейшей аппаратуры европейских и американских производителей. Современные рентгенологические, бактериологические и лабораторные методы исследования позволяют врачам клиники быстро установить точный диагноз и назначить адекватную терапию.
|
Критерий |
Туберкулез |
Пневмония |
|
Общая интоксикация организма |
Выраженная |
Выраженная |
|
Температура тела |
Выше 38°С |
Выше 38°С |
|
Сухой кашель с болевыми ощущениями |
Присутствует |
Присутствует |
|
Наличие мокроты |
Присутствует, может появляться кровь |
Присутствует |
|
Бледность кожных покровов |
Присутствует |
Присутствует |
|
Туберкулиновая проба |
Всегда положительна |
В большинстве случаев отрицательна (очень редко показывает положительный результат, что и дает основание для неправильного диагноза) |
|
Эффективность антибиотикотерапии |
Отсутствует |
Присутствует |
|
Результаты рентгенограммы |
Инфильтративные тени неоднородны, присутствуют очаги отсева |
Четкие локальные инфильтративные тени |
|
Результаты бактериологического исследования |
Микобактерии туберкулеза |
Неспецифическая флора |
Инфильтративным туберкулезом чаще болеют люди, имеющие контакт с больным или пребывающие в группе риска. Причиной пневмонии является переохлаждение, фарингит, заболевание придаточных пазух носа, трахеобронхит. Воспаление легких начинается остро, для туберкулеза характерно подострое начало. При туберкулезе интоксикация умеренная, воспаление легких протекает с выраженным интоксикационным синдромом.
При инфильтративном туберкулезе температура тела субфебрильная, реже фебрильная, с чередованием высоких и нормальных цифр. Пневмония проявляется высокой температурой постоянного характера. Кашель при туберкулезе неинтенсивный и нечастый, с выделением слизисто-гнойной мокроты. Признаком пневмонии является интенсивный кашель, преимущественно с гнойной мокротой.
В общем анализе крови у пациентов с туберкулезом определяют умеренное повышение количества лейкоцитов и скорости оседания эритроцитов, нередко лимфопению и моноцитоз. При пневмонии отмечается выраженный лейкоцитоз и значительно повышенная скорость оседания эритроцитов. В мокроте больных туберкулезом находят микобактерии туберкулеза, при пневмонии – грамположительные или грамотрицательные микроорганизмы. На рентгенограммах больных туберкулезом рентгенологи определяют сегментарное или полисегментарное затемнение неоднородного характера. Оно располагается преимущественно в 1-2 и 6 сегментах легкого. В зоне поражения или корней легкого определяются кальцинаты. При пневмонии однородное затемнение локализуется в базальных сегментах средней и нижней доли легкого.
Клинико-рентгенологические проявления пневмонии и инфильтративного туберкулеза легких и пневмонии имеют определенные особенности, но они носят косвенный характер. Для того чтобы установить точный диагноз, врачи Юсуповской больницы проводят бактериологическое исследование, позволяющее идентифицировать возбудителя инфекционного заболевания. Во время диагностической бронхоскопии производят биопсию и отправляют материал на гистологическое исследование. Компьютерная томография также позволяет провести дифференциальную диагностику пневмонии и туберкулеза легких.
Клинико-рентгенологическая картина при туберкулезе легких и пневмонии будет выглядеть следующим образом:
|
Морфологические проявления |
Рентгенологические симптомы |
Клиническая форма туберкулеза легких |
|
Бронхолобулярное экссудативное воспаление |
Неоднородная тень, которая состоит из сливающихся мелких или крупных в один или несколько соединений, в центре которых выявляется полость распада |
Инфильтративный туберкулез, ограниченный 1–2 сегментами легких |
|
Сливное бронхолобулярное экссудативное воспаление |
Неправильной или округлой формы неоднородная тень, слабой интенсивности, с нечеткими контурами или же обширная неоднородная тень с наличием одиночных или множественных полостей распада |
Инфильтративный туберкулез, ограниченный 1–2 долями легких |
|
Лобарный творожистый некроз |
Обширное интенсивное затемнение, которое распространяется более чем на одну долю легкого с наличием одиночных или множественных полостей распада |
Казеозная пневмония |
Причины ошибок дифференциальной диагностики
В 30% случаев первично установленный диагноз пневмонии не подтверждают при дальнейшем обследовании пациентов. 20% пациентам туберкулез диагностируют в течение первых 2-3 недель заболевания. У 80% дифференциальная диагностика туберкулеза и пневмонии проводится 1-3 месяца.
Основными причинами диагностических ошибок являются:
- плохо собранный фтизиатрический анамнез;
- неправильная оценка и интерпретация клинических проявлений туберкулеза легких в современных условиях;
- некорректная трактовка рентгенологических изменений в легких;
- отсутствие рентгенологического контроля через 7–10 дней лечения пневмонии;
- отсутствие или однократное исследование мазков мокроты на микобактерии туберкулеза;
- выполнение обзорной бронхоскопии без взятия биопсийного материала;
- тяжелые сопутствующие заболевания.
Наиболее часто врачи допускают диагностические ошибки при казеозной пневмонии и инфильтративном туберкулезе легких.
Дифференциальная диагностика пневмонии и обструктивного бронхита
Обе патологии чаще всего начинаются с острых респираторных заболеваний. При обструктивном бронхите и при пневмонии основным симптомом является кашель с выделением мокроты. Однако пневмония обычно протекает тяжелей: у больного имеется выраженная интоксикация, высокая температура тела. В некоторых случаях пневмония у курящего пациента будет иметь одинаковую клиническую картину с хроническим бронхитом курильщика. При обструктивном бронхите температура может повышаться в течение 2-3 дней и далее не превышает субфебрильные показатели. Во время проведения дифференциального диагноза учитывают природу происхождения заболевания: у пневмонии – преимущественно бактериальная, у обструктивного бронхита – легочная.
|
Критерий |
Обструктивный бронхит |
Пневмония |
|
Общая интоксикация организма |
Нет или умеренная |
Выраженная |
|
Температура тела |
В пределах от 37 до 38°С |
Выше 38°С |
|
Одышка |
Присутствует |
Присутствует |
|
Сухие свистящие хрипы |
Присутствуют |
Отсутствуют |
|
Влажные хрипы |
Отсутствуют |
Присутствуют |
|
Результаты рентгенограммы |
Усиление легочного рисунка |
Четкие локальные инфильтративные тени |
Дифференциальная диагностика пневмонии и рака легких
Начальные проявления воспаления легких и развития онкологического процесса не отличаются. При подозрении на пневмонию пациенту назначают курс антибиотиков. Если через неделю они не показывают результат, пациента отправляют на обследование для подтверждения или исключения злокачественного новообразования. Дифференциальный анализ проводят на ранней стадии рака, так как в дальнейшем будут проявляться характерные симптомы. При метастазировании и прорастании опухоли в плевральные ткани заболевание имеет ярко выраженную клиническую картину. Появляются сильные боли при кашле, в мокроте присутствует кровь. Возникают боли в суставах.
|
Критерий |
Рак легких |
Пневмония |
|
Общая интоксикация организма |
Нет или умеренная |
Выраженная |
|
Температура тела |
Нет или субфебрильная |
Выше 38°С |
|
Сухой кашель с болевыми ощущениями |
Присутствует |
Присутствует |
|
Наличие мокроты |
Присутствует, может появляться кровь |
Присутствует |
|
Бледность кожных покровов |
Присутствует |
Присутствует |
|
Эффективность антибиотикотерапии |
Отсутствует |
Присутствует |
|
Результаты рентгенограммы |
Очаговая тень |
Четкие локальные инфильтративные тени |
|
Результаты бактериологического исследования |
Аномальные клетки |
Неспецифическая флора |
Лечение пневмонии
В Юсуповской больнице выполняют своевременную и точную постановку диагноза. В клинике проводят все необходимые диагностические мероприятия для выявления пневмонии: осмотр терапевта, лабораторные исследования, рентгенографию. Качественная диагностика позволяет определить тип пневмонии, что важно при назначении терапии.
Воспаление легких лечат медикаментозно с помощью антибактериальной терапии. Выбор препарата будет зависеть от возбудителя заболевания. Дополнительно используют препараты для симптоматического лечения. К ним относятся жаропонижающие, болеутоляющие, отхаркивающие средства. После получения первых положительных результатов лечения и стабилизации нормальной температуры назначают специальные массажи и дыхательную гимнастику. Больной пневмонией должен соблюдать постельный режим, хорошо питаться, принимать витамины, пить достаточное количество жидкости.
Юсуповская больница предлагает своим пациентам стационарное лечение с комфортными палатами. Пациенту оказывают круглосуточное медицинское обслуживание опытные врачи-терапевты, пульмонологи и квалифицированный младший персонал. В палатах есть все необходимые предметы гигиены, специальная система вентиляции обеспечивает очищение воздуха в каждом помещении больницы. Пациентам предоставляют сбалансированное питание, которое подбирает диетолог, учитывая пожелания пациента.
Все сложные для дифференциальной диагностики случаи пневмонии обсуждаются на заседании экспертного совета. Запишитесь на прием к врачу по телефону Юсуповской больницы, где работают кандидаты и доктора медицинских наук, врачи высшей категории, являющиеся ведущими специалистами в области диагностики заболеваний легких.
Быстрая навигация
Как диагностировать туберкулез: Туберкулез — это бактериальная инфекция, вызванная Mycobacterium tuberculosis. Первичная диагностика туберкулеза потребует проведения рентгена легких и последующей консультации у фтизиатра. В качестве дополнительного обследования врач может назначить КТ легких, УЗИ, анализы крови и мокроты, биопсию.
Какой врач лечит туберкулез: При симптомах туберкулеза следует сначала обратиться к врачу фтизиатру.
Туберкулез — это бактериальная инфекция, которая распространяется воздушно-капельным путем при кашле или чихании инфицированного человека. В основном он поражает легкие, но может поражать любую часть тела, включая живот, железы, кости и нервную систему.
Причины туберкулеза
Туберкулез, поражающий легкие, является наиболее заразным типом, но обычно он распространяется только после длительного контакта с больным. У большинства здоровых людей естественная защита организма от инфекций и болезней убивает бактерии, и заболевание не развивается, или предотвращает их распространение в организме. Если иммунной системе не удается убить или сдержать инфекцию, она может распространиться в легкие или другие части тела, и развивается активный туберкулез с клиническими проявлениями. В некоторых случаях бактерии заражают организм, но не вызывают никаких симптомов – это называется латентный туберкулез. До 10% людей с латентным туберкулезом в конечном итоге заболевают активной формой болезни через несколько лет после первоначального заражения. Хотя туберкулез передается так же, как простуда или грипп, он не настолько заразен. Человеку придется проводить длительные периоды (несколько часов) в тесном контакте с инфицированным, чтобы самому заразиться инфекцией. Например, туберкулез обычно передается между членами семьи, живущими в одном доме. Не все больные туберкулезом заразны — пациенты с внелегочной формой заболевания не распространяют инфекцию и не опасны для окружающих.
Группы риска по туберкулезу
Любой человек может заразиться туберкулезом, но наибольшему риску подвержены люди:
- которые живут, приехали или провели время в стране или районе с высоким уровнем заболеваемости;
- находящиеся в длительном тесном контакте с инфицированным человеком;
- с состоянием, ослабляющим иммунную систему, например, диабетом, ВИЧ-инфекцией;
- проходящие лечение, ослабляющее иммунную систему, такое как химиотерапия; очень молодого или пожилого возраста;
- с плохим состоянием здоровья или с плохим питанием;
- злоупотребляющие алкоголем или наркотиками
- находился в местах лишения свободы.
ВИЧ и туберкулез
Пациенты, живущие с ВИЧ, подвергаются более высокому риску заражения инфекцией и смерти от туберкулеза. Латентный туберкулез при отсутствии лечения с большей вероятностью перейдет в активную форму у больного ВИЧ. Пациентам с ВИЧ рекомендуются следующие шаги, чтобы снизить риск заражения инфекцией туберкулеза:
- периодические обследования на туберкулез
- терапия от ВИЧ в соответствии с рекомендациями медицинских работников
- избегать контактов с больными туберкулезом
- отказ от табакокурения
- сбалансированная диета, богатая питательными веществами. Помогает снизить риск осложнений от ВИЧ и улучшить усвоение лекарств
- регулярные физические упражнения для укрепления здоровья иммунной системы.
Симптомы туберкулеза легкого
Симптомы туберкулеза различаются в зависимости от того, какая область тела поражена. Заболевание обычно развивается медленно, и может пройти несколько недель, прежде чем пациент заметит у себя какие-либо симптомы. Иногда они могут проявиться только через несколько месяцев или даже лет после первоначального заражения.
Общие симптомы туберкулеза
- отсутствие аппетита и похудание;
- высокая температура;
- ночное потоотделение;
- крайняя усталость или утомляемость.
Однако эти признаки могут иметь множество различных причин и не всегда являются признаком туберкулеза.
Туберкулез легких
В большинстве случаев туберкулеза поражаются легкие, что может вызвать:
- постоянный кашель продолжительностью более 3 недель, обычно с выделением мокроты, которая может быть с примесью крови;
- одышка, которая постепенно ухудшается.
Внелегочный туберкулез
Реже туберкулезные инфекции развиваются в областях за пределами легких, таких как лимфатические узлы, кости и суставы, пищеварительная система, мочевой пузырь и репродуктивная система, а также головной мозг и нервная система. Симптомы могут включать:
- постоянно воспаленные, опухшие и болезненные железы;
- боль в животе;
- боль и потеря движения в пораженной кости или суставе;
- постоянная головная боль;
- судороги.
Диагностика туберкулеза
Для диагностики туберкулеза используются несколько тестов в зависимости от типа подозреваемого заболевания.
Легочный туберкулез
Диагностика легочного туберкулеза может быть трудной и обычно требует проведения нескольких анализов. Пациенту может быть назначен рентген грудной клетки или КТ легких, чтобы выявить изменения внешнего вида легких, указывающие на туберкулез, а также будут взяты образцы мокроты для исследования ее на наличие возбудителя инфекции. Эти тесты важны для выбора наиболее эффективного лечения больного.
Внелегочный туберкулез
Для подтверждения внелегочного туберкулеза можно использовать несколько тестов, которые включают:
- КТ, МРТ или УЗИ пораженной части тела;
- эндоскопические методы исследования – фиброгастродуоденоскопия, лапароскопия;
- анализы мочи и крови;
- биопсия — небольшой образец ткани или жидкости берется из пораженной области и исследуется на наличие микобактерий;
- люмбальная пункция, при которой небольшой образец спинномозговой жидкости берется из основания позвоночника и исследуется на предмет распространения бактерий на нервную систему.
Диагностика на латентный туберкулез
В некоторых случаях человеку может потребоваться пройти тест на латентный туберкулез, например, это может потребоваться, если он находился в тесном контакте с кем-то, у кого была установлена активная легочная форма заболевания, или если он недавно был в стране с высоким уровнем туберкулеза. Проба Манту — широко используемый тест на латентный туберкулез. Она заключается в введении небольшого количества вещества под названием туберкулин в кожу предплечья. Его также называют туберкулиновой кожной пробой (ТКП). Если у пациента латентная туберкулезная инфекция, кожа будет чувствительна к туберкулину, и на месте инъекции появится твердая красная шишка, обычно в течение 48–72 часов после проведения теста. Если у человека очень сильная кожная реакция, ему потребуется рентген грудной клетки, чтобы подтвердить наличие активного туберкулеза. Если у него нет скрытой инфекции, кожа не отреагирует на пробу Манту. Однако, поскольку для развития туберкулеза может потребоваться много времени, возможно, придется пройти повторное обследование на более позднем этапе. Если пациенту сделали прививку БЦЖ, у него может быть легкая кожная реакция на пробу Манту, и это не обязательно означает, что у него латентный туберкулез.
Анализ высвобождения гамма-интерферона
Анализ высвобождения гамма-интерферона (IGRA) — это анализ крови на туберкулез, который становится все более доступным. Он может использоваться для диагностики латентного туберкулеза:
- если у пациента положительная проба Манту;
- если он ранее делал вакцинацию БЦЖ — проба Манту может быть ненадежной в этих случаях;
- как часть скрининга на туберкулез, если он только что прибыл из страны, где туберкулез распространен;
- если пациент собирается пройти курс лечения, который подавит его иммунную систему; если он медицинский работник.
Лечение туберкулеза
Хотя туберкулез является серьезным заболеванием, которое может привести к летальному исходу, если его не лечить, смерть при проведении терапии крайне редка. Лечение туберкулеза обычно предполагает прием антибиотиков в течение нескольких месяцев, причем большинство пациентов для этого в госпитализации не нуждаются.
Легочный туберкулез
Больному с активной формой легочного туберкулеза будет назначен как минимум 6-месячный курс комбинации антибиотиков. Обычные схемы лечения включают:
- 2 антибиотика (изониазид и рифампицин) на 6 месяцев;
- 2 дополнительных антибиотика (пиразинамид и этамбутол) в течение первых 2 месяцев 6-месячного периода лечения.
Может пройти несколько недель, прежде чем пациент почувствует себя лучше. Точное время будет зависеть от общего состояния здоровья и степени тяжести туберкулеза. После 2-недельного приема антибиотиков большинство больных перестают быть заразными и отмечают положительную динамику. Тем не менее, важно продолжать прием лекарств точно в соответствии с предписаниями и пройти весь курс антибиотикотерапии. Если прекратить прием антибиотиков до завершения курса или пропустить прием дозы, туберкулезная инфекция может стать устойчивой к антибиотикам. Это потенциально опасно, потому она потребует более агрессивного, длительного и, возможно, более токсичного способа лечения.
Лечение внелегочного туберкулеза
Внелегочный туберкулез можно лечить с помощью той же комбинации антибиотиков, что и легочную форму. Если у больного туберкулез в таких областях, как мозг или перикард – околосердечная сумка, ему сначала могут прописать кортикостероид (преднизолон) в течение нескольких недель одновременно с антибиотиками. Это поможет уменьшить отек в пораженных участках. Как и при легочном туберкулезе, важно принимать лекарства точно в соответствии с предписаниями и пройти весь курс лечения.
Лечение туберкулеза с множественной лекарственной устойчивостью
Хотя в настоящее время это редкость, но все же есть штаммы туберкулеза, устойчивые к 2 или более антибиотикам. Это известно как туберкулез с множественной лекарственной устойчивостью. Он требует гораздо более длительного курса лечения антибиотиками — от 9 до 24 месяцев в зависимости от формы. Туберкулез с множественной лекарственной устойчивостью обычно имеет менее благоприятные исходы, чем классическая форма заболевания.
Лечение латентного туберкулеза
Если у пациента выявлен латентный туберкулез в возрасте 65 лет и младше, обычно рекомендуется лечение. Однако антибиотики, используемые для лечения туберкулеза, могут вызывать повреждение печени у пожилых людей, поэтому для каждого больного используется индивидуальная тактика. В некоторых случаях тестирование и лечение латентного туберкулеза может быть рекомендовано пациентам, которым требуется лечение, ослабляющее их иммунную систему, такое как долгосрочные стероидные препараты, химиотерапия или биологические ингибиторы. Лечение латентного туберкулеза обычно включает:
- либо прием комбинации рифампицина и изониазида в течение 3 месяцев;
- либо изониазид самостоятельно в течение 6 месяцев.
Латентный туберкулез не лечится, если считается, что он устойчив к лекарствам. В этом случае пациент может регулярно наблюдаться, чтобы убедиться, что инфекция не активизируется.
Побочные эффекты лечения
Изониазид может вызывать повреждение нервов (периферическая невропатия). Поэтому пациентам, проходящим курс лечения туберкулеза, назначают добавки с витамином B6 (пиридоксин), чтобы снизить этот риск. В редких случаях антибиотики могут вызвать серьезное повреждение глаз. Рифампицин может снизить эффективность некоторых видов контрацепции, например, комбинированных противозачаточных таблеток, поэтому при приеме рифампицина следует использовать альтернативный метод контрацепции.
Вакцинация от туберкулеза
Вакцина БЦЖ обеспечивает защиту от туберкулеза и рекомендована Всемирной организацией здравоохранения младенцам, детям и взрослым в возрасте до 35 лет, которые считаются подверженными риску заражения туберкулезом. Вакцина БЦЖ обычно не вводится лицам старше 35 лет, поскольку нет никаких доказательств того, что она работает для людей этой возрастной группы. В группы риска входят:
- дети, проживающие в районах с высоким уровнем заболеваемости туберкулезом; люди с близкими родственниками из стран с высоким уровнем заболеваемости туберкулезом;
- люди, которые собираются жить и работать с местным населением более 3 месяцев в районе с высоким уровнем заболеваемости туберкулезом.
Если человек является медицинским работником и контактирует с пациентами или клиническими образцами, ему также следует сделать прививку от туберкулеза независимо от возраста, если: он не был ранее вакцинирован, и результаты кожной пробы Манту или анализа крови на выделение гамма-интерферона отрицательны.
Профилактика туберкулеза
Обычно пациенту с туберкулезом не нужно изолироваться на время лечения, но важно принять некоторые основные меры предосторожности, чтобы остановить распространение инфекции на семью и друзей. Больному следует:
- держаться подальше от работы, школы, пока он не перестанет быть заразным для окружающих;
- всегда прикрывать рот при кашле, чихании или смехе;
- аккуратно утилизировать использованные салфетки в герметичном пластиковом пакете;
- по возможности открывать окна, чтобы обеспечить приток свежего воздуха в тех местах, где он проводит время; не спать в одной комнате с другими людьми.
Лучшие специалисты в Санкт-Петербурге с рейтингом 4.5+
Ананьев Семен Михайлович
Специализация: Фтизиатр
Врачебный стаж: с 2010 года
Где ведет прием: Клиника Скандинавия
Кулакова Наталья Валерьевна
Специализация: Фтизиатр
Врачебный стаж: с 1998 года
Где ведет прием: Немецкая семейная клиника, Клиника Скандинавия
Литература
- Борисов С.Е. Диагностика туберкулеза: возможности и пределы // В сб.: Туберкулез сегодня: проблемы и перспективы. М. — 2000 — с. 92-97.
- Cardona PJ. Reactivation or reinfection in adult tuberculosis: Is that the question? Int J Mycobacteriol. 2016 Dec;5(4):400-407. doi: 10.1016/j.ijmyco.2016.09.017. Epub 2016 Oct 27. PMID: 27931680.
- Гинцбург A.JI. Генодиагностика инфекционных заболеваний // Журн. микробиол., эпидемиол. и иммунобиол. -1998. № 3. — с. 8695.
- Литвинов В.И., Гергерт В.Я., Мороз A.M. Иммунология туберкулеза // Вестник РАМН. 1999. — № 7. — с. 8-11.
- Koch A, Mizrahi V. Mycobacterium tuberculosis. Trends Microbiol. 2018 Jun;26(6):555-556. doi: 10.1016/j.tim.2018.02.012. Epub 2018 Mar 23. PMID: 29580884.
- Сон И.М. Заболеваемость туберкулезом // Реферативный сборник «Туберкулез». 1997. — № 6. — с. 1-14.
- Черноусова JI.H., Ларионова Е.Е., Севастьянова Э.В. Роль ПЦР-анализа в комплексных бактериологических исследованиях во фтизиатрии // Проблемы туберкулеза. 2001. — № 3. — с. 58-60.
- Cardona PJ. Pathogenesis of tuberculosis and other mycobacteriosis. Enferm Infecc Microbiol Clin (Engl Ed). 2018 Jan;36(1):38-46. English, Spanish. doi: 10.1016/j.eimc.2017.10.015. Epub 2017 Dec 2. PMID: 29198784.
Последние статьи о диагностике
Тест на пиковую скорость потока
Тест на пиковую скорость потока — это простое измерение того, насколько быстро человек может выдохнуть воздух из легких. Его часто используют для диагностики и мониторинга астмы.
Трансплантация легкого
Трансплантация легкого — это операция по удалению и замене больного легкого здоровым легким от донора. Донором обычно является умерший человек, но в редких случаях часть легкого может быть взята у живого донора. Трансплантация легких проводится нечасто, в основном это связано с отсутствием доступных доноров, поскольку спрос на пересадку намного превышает доступное предложение пожертвованных легких. Это означает, что пересадка органа будет проведена только в том случае, если есть относительно высокие шансы на ее успех. Например, трансплантация легких не будет рекомендована онкологическим больным, потому что рак может вернуться в донорские легкие. Если пациент курит, его также не будут рассматривать для трансплантации легких.
Гранулематоз с полиангиитом (гранулематоз Вегенера)
Как диагностировать гранулематоз с полиангиитом: Гранулематоз с полиангиитом (гранулематоз Вегенера или ГПА) — редкое аутоиммунное заболевание, при котором кровеносные сосуды воспаляются. В основном оно поражает уши, нос, носовые пазухи, почки и легкие. Заболеть этим недугом может любой человек, в том числе ребенок, но чаще всего он встречается у пожилых людей. Точная причина возникновения гранулематоза Вегенера пока неизвестна.
Что покажет КТ легких с контрастом и без
Компьютерная томография лёгких — это неинвазивный метод обследования, который проводят в рамках КТ органов грудной клетки. Цель данного сканирования — максимально визуализировать лёгкие, бронхи, плевру, нижнюю часть трахеи, ткани средостения, нижнюю часть пищевода.